轻度胃肠炎伴婴幼儿良性惊厥发病机制的研究进展
2019-03-16美丽,图雅
美 丽,图 雅
(1.内蒙古医科大学研究生学院,呼和浩特 010020; 2.内蒙古自治区妇幼保健院小儿神经内科,呼和浩特 010020)
轻度胃肠炎伴婴幼儿良性惊厥(benign infantile convulsions associated with mild gastroenteritis,BICE)是指轻度胃肠炎婴幼儿发生的无热惊厥,该病起初以欧洲国家和日本报道居多,我国对BICE的认识较晚。Komori等[1]提出BICE的诊断条例,目前国内外均参照该诊断标准:①轻度胃肠炎病程中发生的无热惊厥;②多数患儿既往体健,无惊厥相关基础疾病;③惊厥次数为1次或多次,典型病例为成簇性惊厥发作;④排除热性惊厥等其他常见惊厥性疾病;⑤发作间期脑电图检查多数无异常;⑥粪便可检测出致病源,血清电解质、血糖、脑脊液常规检查在正常值范围内;⑦多数患儿预后良好。近年来,我国BICE的发病率呈上升趋势,充分认识BICE的发病机制,及时正确预防和控制反复惊厥的发生非常关键[2-3]。现对BICE的病原、炎症反应、分子遗传学、离子通道等方面的致病机制予以综述,以期为BICE的临床预防和诊治提供指导。
1 病原体直接感染中枢神经系统
了解BICE致病源对其发病机制的研究至关重要。目前,轮状病毒、诺如病毒、肠道腺病毒、柯萨奇病毒、星状病毒等常见肠道病毒感染引起的胃肠炎均可发生惊厥,导致BICE的发生;空肠弯曲菌、志贺菌属、沙门菌属等细菌感染也可导致BICE[3-4]。近年来,以病毒感染相关性BICE报道居多[3-5]。既往认为,人轮状病毒感染是最主要的致病源,但随着轮状病毒疫苗的普及,诺如病毒感染或逐渐成为BICE的主要致病源[6]。Chen等[7]发现,诺如病毒感染引起的胃肠炎比轮状病毒感染引起的胃肠炎更易发生惊厥,诺如病毒感染对患儿中枢神经的损害可能更大。轮状病毒致病期间通常寄生于小儿肠道,但也可引起肠道外感染,小儿轮状病毒性脑炎临床症状相对较轻,多数预后多良好。Hongou等[8]在轮状病毒胃肠炎伴发无热惊厥患儿脑脊髓液中可检测到轮状病毒结构性蛋白4、轮状病毒结构性蛋白7和抗轮状病毒IgG的存在,并指出轮状病毒G2亚型可能更易引起惊厥发作。Abe等[9]在轮状病毒感染的BICE患儿脑脊液、咽拭子、尿液、粪便中同时检测出具有相同结构蛋白区的轮状病毒RNA,认为轮状病毒从外周血通过血脑屏障进入中枢,导致病毒性脑炎或轮状病毒同时感染肠道和中枢神经系统,从而引发惊厥。由此认为,BICE的发生是病原体直接感染中枢神经系统所致,故提出病毒性脑炎学说,杜丽君[10]的研究发现,部分BICE患儿脑电波有脑炎相关弥漫性异常,认为BICE不能完全排除脑炎,但由于条件限制并未同时检测患儿脑脊液病毒及抗原、抗体等相关检查来明确是否发生了病毒性脑炎。
目前多数学者对脑炎学说提出质疑,根据脑脊液和血液中神经元特异性烯醇化酶的浓度可代表神经细胞的损伤程度,路新国[11]研究发现,BICE脑脊液病毒阳性患儿脑脊液中神经元特异性烯醇化酶的水平与脑脊液病毒阴性患儿无明显差异,认为两组患儿中枢神经系统损伤程度一致,病毒存在于中枢神经系统并不引发局部炎症,并否定了脑炎学说。也有学者认为,BICE患儿脑脊液的致病机制与热性惊厥相似,患儿惊厥导致血脑屏障通透性增高,惊厥发生在前,病毒进入中枢神经在后,再次否定了脑炎学说[12]。BICE患儿除惊厥外,其余临床表现均不符合脑炎临床特征,目前未见轮状病毒外其他病原导致脑炎的相关报道,病原体在BICE发病中的具体机制仍有待深入研究。
2 感染导致的细胞免疫功能紊乱及炎性因子改变
辅助性T细胞(helper T cell,Th)分为Th1细胞和Th2细胞两种,主要表面标志为CD4,受抗原刺激后Th细胞增殖分化,分泌的细胞因子参与机体免疫调节过程介导免疫应答。Th1细胞产生白细胞介素(interleukin,IL)2、肿瘤坏死因子α、γ干扰素等;Th2细胞产生IL-6、IL-10等;正常机体Th1细胞和Th2细胞的功能处于动态平衡,感染引发机体免疫功能失调,可导致体内一系列与免疫相关的临床表现或疾病。
小儿胃肠炎的发生与机体免疫功能异常相关,胃肠炎病程中发生惊厥的患儿体内免疫功能失调或较无惊厥患儿更强烈,过量炎性因子释放和免疫平衡失调可造成神经系统损害,提高神经元的兴奋性[13-14]。邹小杰等[13]发现,BICE组病程急性期和恢复期外周血IL-10表达水平均明显高于对照组(健康体检儿童),BICE组恢复期外周血IL-10、IL-6水平低于急性期;还认为,胃肠炎初期体内促炎因子分泌升高导致神经组织损伤,IL-10大量分泌保护和修复神经组织损伤,最终过度分泌的IL-10反而抑制促炎因子及其他细胞因子(如IL-6、肿瘤坏死因子α等)的释放,导致机体免疫环境失去平衡,加重患儿免疫损伤和脑损伤;惊厥组患儿恢复期IL-10表达水平低于急性期,提示随着病情好转免疫失衡逐渐恢复正常。
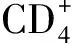
3 一氧化氮堆积学说
一氧化氮(nitric oxide,NO)参与体内神经突触传递过程,体内NO升高可提高机体惊厥率。一氧化氮合酶(nitric oxide synthase,NOS)是NO合成的关键酶,维持正常体内NO水平主要通过NOS的调节来完成。研究发现BICE患儿体内NOS活性增强,导致患儿血液和脑脊液中NO异常堆积,升高程度显著高于普通胃肠炎及热性惊厥、脑炎、脑膜炎等,机体炎性环境也有助于NO反应性增高[16]。石凯丽等[17]认为,NO可影响BICE患儿脑内钙离子浓度,激活NOS,使NO产生增多,进而使细胞内钙浓度升高,升高的钙离子导致惊厥的产生和传播,同时细胞内钙浓度升高使中枢神经系统兴奋性氨基酸谷氨酸盐释放增加,最终导致惊厥发生。体内内源性硫化氢可降低机体惊厥易感性、抑制NO/NOS体系的表达、调节γ氨基丁酸B受体功能等,对惊厥所致脑损伤有保护作用[18]。张远达等[19]发现,BICE患儿内源性硫化氢生成减少,对NOS的活性抑制减少,导致NO合成增多。NO在BICE惊厥机制中扮演重要角色,多种途径使胃肠炎患儿体内NO过度生成,最终引发惊厥,由此推测,合理应用NOS抑制剂、氮氧化物拮抗剂对BICE引起的惊厥有一定治疗作用[11]。
4 肠道益生菌群数量减少及肠黏膜屏障能力降低
人体内肠道益生菌处于一定的平衡状态,一旦失去平衡(如菌种间比例发生大幅变化等)将会导致相应疾病。体内肠道益生菌可通过“菌群-肠-脑轴”参与肠道和中枢神经系统的双向调节,肠道益生菌产生的NO及硫化氢等产物可能影响患儿血脑屏障功能[20]。BICE患儿体内NO浓度过高,NO自身及其代谢产物也会损害肠道屏障功能,导致各类益生菌群数量降低。感染引起的肠道益生菌群数量降低及肠黏膜屏障能力下降可能与胃肠炎患儿发生惊厥有一定联系。杜自强等[21]对BICE、急性轻度胃肠炎、健康体检儿童3组患儿的粪便大肠埃希菌、肠球菌、乳酸杆菌、双歧杆菌的数量差异进行统计学分析发现,BIEC组患儿的菌群数量最低,正常儿童的菌群数量最高,提示BICE患儿肠道黏膜屏障功能受到严重损害。卢乐声等[22]通过BICE患儿的粪便菌群培养及测定NO等肠黏膜屏障指标证明,BICE患儿存在肠道内益生菌数量减少和肠黏膜屏障功能下降,适当补充肠道菌群可以改善BICE患儿病情。
5 婴幼儿惊厥阈值学说及遗传易感性
婴幼儿大脑皮质发育不全、神经髓鞘对兴奋冲动的绝缘作用差、血脑屏障功能发育不完善、额叶发育落后等神经系统解剖生理特点均降低婴幼儿惊厥阈值,婴幼儿反复惊厥也可增加其对惊厥的易感性。BICE发病年龄多在6个月至3岁,其惊厥可能是与婴幼儿大脑惊厥阈值低有关的“反应性惊厥”。吴惧等[23]认为,BICE惊厥与热性惊厥有共同的发病性质,与婴幼儿大脑皮质发育未完善和血脑屏障功能差有关。遗传因素在婴幼儿良性惊厥性疾病发病原因中占重要地位,惊厥性疾病常有家族聚集性。BICE患儿发生惊厥与遗传因素也有很大关系,Verrotti等[24]报道,BICE患儿的一级与二级亲属癫痫患病率可高达16.4%。Okumura等[25]研究发现,姐弟、单卵双胞胎在胃肠炎病程中均发生无热惊厥,且同一对双胞胎惊厥发作时间和发作形式基本一致,脑电图均表现为右枕区的局灶性阵发性放电迅速扩散到所有区域,可见BICE发病与潜在遗传因素相关,但具体遗传方式和机制仍不明确。
6 基因突变、离子及离子通道异常
富含脯氨酸的跨膜蛋白2基因是小儿热性惊厥、癫痫等多种儿童惊厥性疾病的致病基因,可编码体内数百种氨基酸。富含脯氨酸的跨膜蛋白2基因突变可导致神经元突触功能失调和神经元过度兴奋,使机体惊厥易感性增加[26]。Okumura等[27]报道,富含脯氨酸的跨膜蛋白2基因突变在婴幼儿良性惊厥性疾病患者中常见,其中包括BICE患儿。然而,Weng等[28]针对BICE患儿进行基因突变检测并未发现富含脯氨酸的跨膜蛋白2基因异常。Ishii等[29]也认为,富含脯氨酸的跨膜蛋白2基因突变可能与BICE患儿发生惊厥无关。已有研究证实,钠离子通道相关基因突变可提高小儿惊厥易患性,钠离子通道α1亚单位基因是人类癫痫最常见的突变基因,影响动作电位去极化,导致不同类型的惊厥发生;而限制神经元钠离子通道药物卡马西平控制BICE惊厥的效果较好,由此可见,胃肠炎患儿发生惊厥可能与机体钠离子通道相关基因突变有关,基因突变与BICE惊厥间的具体关系有待进一步探索明确[29-30]。婴幼儿时期神经系统的发育对各种营养物质和微量元素的需求量较大,胃肠炎时血清电解质相对缺乏,电解质紊乱可增加惊厥易感性;BICE患儿血清锌、钠、钙离子水平虽在正常值范围,但较无惊厥胃肠炎患儿低;腹泻病程长,导致血清锌离子浓度降低,可能导致惊厥的发生;患儿血清钠离子浓度偏低可能影响患儿惊厥持续时间;小儿钙通道活性或钙动员可引发大脑异常放电导致惊厥[31-33]。Yeom等[34]发现,胃肠炎伴惊厥发作组血清钙离子水平低于普通胃肠炎组。综上所述,胃肠炎患儿血清离子水平偏低可能与患儿惊厥发作有一定关联。
7 归类于婴幼儿癫痫
良性婴儿癫痫是临床常见的儿童癫痫类型,呈自限性,多数预后好,部分患儿预后较差,可出现一定程度的认知障碍、语言发育落后等,其惊厥发作与BICE有共同之处,均以集丛性惊厥发作为特点,发作类型多为局灶性发作继发全面性发作。根据BICE患儿脑电图及临床惊厥发作的特点,认为BICE是小儿良性婴儿癫痫的一种特殊类型。Komori等[1]观察发现,BICE患儿的惊厥可从部分性发作变为全身性发作,也可从全身性发作变为部分性发作。Imai等[35]检测发现,同一BICE患儿3次发作期脑电图分别起源于右枕、左枕和右顶枕部继而全身泛化,临床表现为惊厥部分性发作继发全面性惊厥发作,认为BICE是小儿良性婴儿癫痫的一种表现形式,但目前国际抗癫痫联盟癫痫分类中仍未见BICE。
8 小 结
BICE患儿发生惊厥的可能机制为病原体感染使体内致惊厥物质增多、免疫调控功能紊乱以及基因突变、遗传易感等多种因素共同作用的结果。BICE有导致婴幼儿永久性脑损伤的风险[36]。BICE临床诊断并不困难,但目前对控制该病急性期惊厥尚无统一最佳方案和治疗药物,临床医师对BICE的理解认识仍不足,充分认识BICE发生惊厥的具体机制,从根本上解决其治疗问题非常必要。近年来对BICE的研究确实取得了一些突破,但仍缺少相关大样本前瞻性研究,临床仍未见BICE的规范化治疗方案,相关研究成果在BICE治疗中仍未得到广泛推广和应用。
