咖啡酸的化学改性及产物抗氧化性的研究
2019-03-09宋京九
王 东,赵 雪,宋京九,祝 钧
(北京工商大学 理学院,北京 100048)
咖啡酸(CA)又名水解咖啡鞣酸、3,4-二羟基肉桂酸[1]。咖啡酸作为天然存在的酚酸类化合物,是次生植物代谢产物,并且几乎在所有植物中都存 在[2,3]。咖啡酸又是天然的抗氧化剂,不但可以影响食物的色泽、稳定性、风味、营养价值,而且在化妆品和医药领域也有广泛的应用[4-6]。氧化是电子从一个原子向另一个原子的转移,是有氧生命新陈代谢的重要组成部分,当机体内电子发生转移时,就会产生自由基[7]。常见的有氧自由基、羟基自由基等,活性氧自由基有高度反应性,攻击蛋白质、脂质、DNA、酶,诱导引发细胞、组织的损伤,使得生物机体遭到破坏[8]。Son等[9]研究了咖啡酸的抗氧化性,认为使得咖啡酸具有良好的抗氧化性的原因是其分子结构中邻苯二酚环中的邻二羟基官能团。咖啡酸易溶于乙醇和热水,微溶于冷水[10],在常见溶剂体系中的溶解度很低、配伍性差,且来源天然的咖啡酸衍生物有效性差等原因,限制了其应用[11,12]。Yoo等[13]在1-(3-二甲基氨基丙基)-3-乙基碳二亚胺盐酸盐(EDC)、1-羟基苯并三唑(HOBt)的作用下,合成一系列咖啡酰胺化合物,发现它们对DPPH自由基、超氧阴离子有很好的清除作用,对脂质过氧化有很好的抑制作用。Aladedunye等[14]合成了12种高收率的二氢咖啡酰胺化合物,采用清除DPPH自由基实验评价其抗氧化活性。发现这些新化合物比α-生育酚和丁基化羟基甲苯(BHT)具有显著清除自由基的作用。因此,通过合成咖啡酸酰胺类化合物,既可以保持其生物活性,又可以扩大其应用 范围。
笔者以咖啡酸和氨基酸乙酯盐酸盐为原料通过HOBt/EDC法合成4种咖啡酸氨基酸类衍生物,运用核磁共振氢谱(1H NMR)和高效液相色谱-质谱 (HPLC-MS)表征确定4种化合物的结构。通过体外清除DPPH自由基、羟基自由基试验、红细胞溶血试验来表征目标产物的抗氧化活性及刺激性,以期为咖啡酰氨基酸衍生物作为新化妆品原料的应用提供理论 指导。
1 实验部分
1. 1 主要试剂与仪器
咖啡酸、甘氨酸乙酯盐酸盐、丙氨酸乙酯盐酸盐、L-丝氨酸乙酯盐酸盐、L-苏氨酸乙酯盐酸盐、HOBt、EDC,北京伊诺凯科技有限公司。醋酸、七水合硫酸亚铁、乙酸乙酯、二甲基甲酰胺(DMF)、三乙胺、邻二氮菲、1,1-二苯基-2-三硝基苯肼(DPPH)、菲洛嗪、抗坏血酸(Vc),均为分析纯,北京化玻站生物分析技术有限公司;新鲜兔血,北京海淀区兴隆实验动物养殖厂;十二烷基硫酸钠(SDS),美国Amresco Biotechnology Grade。
OSB-2100旋转蒸发仪,上海爱朗仪器有限公司;XK-88微型加热磁力搅拌器,扬州市邗江公道玻璃仪器厂;SHZ-Ⅲ循环水真空泵,上海亚荣生化仪器厂;TE212-L电子天平,赛多利斯科学仪器(北京)有限公司;核磁共振仪,瑞士Bruker;Xevo G2 Q-TOF质谱仪,美国Waters;Infinite M200 PRO酶标仪,瑞士Tecan;台式离心机,德国Eppendorf Centrifuge 5810 R。
1. 2 咖啡酰氨基酸酯衍生物的合成[11]
本研究主要采用甘氨酸乙酯盐酸盐、丙氨酸乙酯盐酸盐、L-丝氨酸乙酯盐酸盐和L-苏氨酸乙酯盐酸盐在EDC脱水剂的作用下分别与咖啡酸进行反应,生成相应的咖啡酰氨基酸乙酯,具体结构式见下。
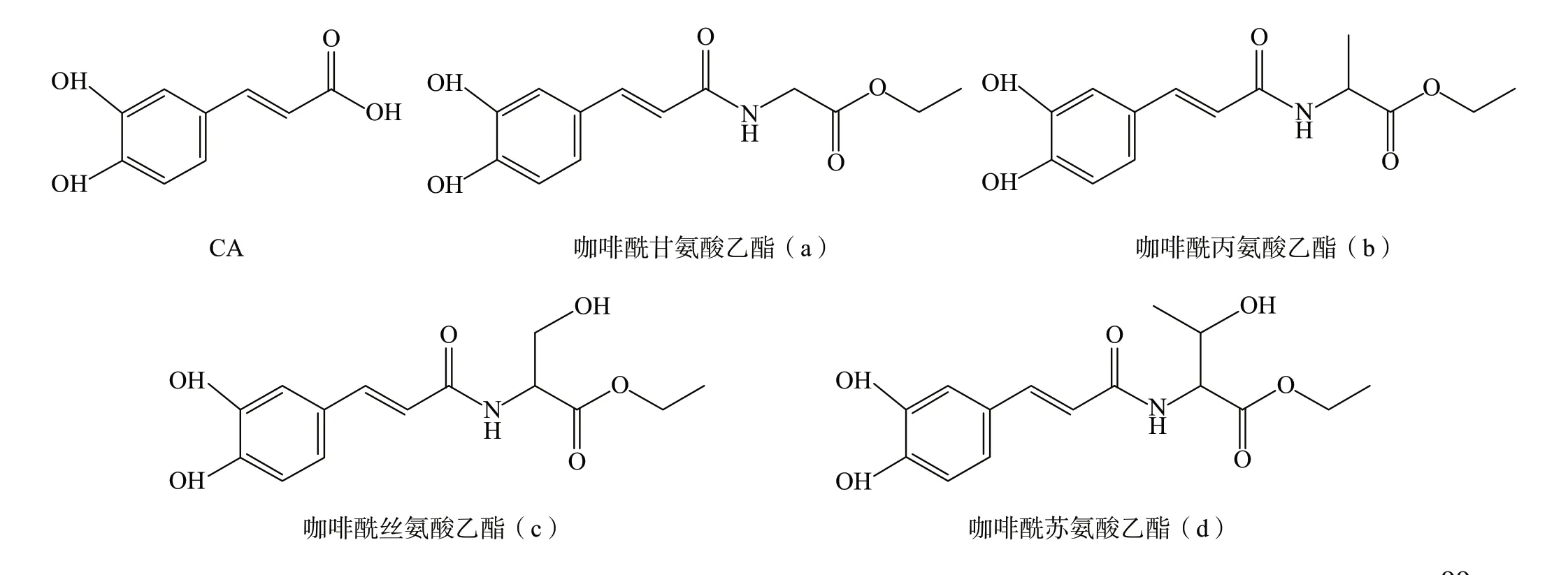
实验产物均以咖啡酸(8.25 mmol)与相应的氨基酸盐酸盐(8.25 mmol)为原料合成。以咖啡酰甘氨酸乙酯的合成为例。向置于冰水浴中的圆底烧瓶中加入已溶解在DMF(25 mL)中的咖啡酸(1.5 g,8.25 mmol)、l-羟基苯并三唑(1.15 g,8.5 mmol)和甘氨酸乙酯盐酸盐(1.15 g,8.25 mmol),慢慢滴加三乙胺(3.45 mL,24.75 mmol),反应10 min后,加入EDC (1.6 g,8.35 mmol),自然升温到25 ℃,反应18 h。用薄层层析法(TLC)检测是否反应完全。若没有完全,继续反应,直至反应完全。将反应物倒入200 mL水中,分别用乙酸乙酯(4×100 mL)萃取和饱和食盐水(2×100 mL)冲洗,有机相用无水硫酸钠干燥过夜、过滤、硅胶柱色谱柱分离(洗脱剂为乙酸乙酯和石油醚,体积比为1∶2),减压蒸去溶剂,得到稠状膏体,真空干燥得到浅黄色固体。
1. 3 咖啡酰氨基酸酯衍生物的结构鉴定
1. 3. 1 咖啡酰氨基酸酯衍生物TLC鉴定
对经过色谱柱纯化后的各化合物溶液进行薄层色谱分析。薄层层析硅胶板GF254(50 mm×200 mm),展开剂为乙酸乙酯和石油醚(体积比为1∶2)。对照物质为咖啡酸(7.5 g/L),检测是否为单一斑点。
1. 3. 2 咖啡酰氨基酸酯衍生物1H NMR表征
各称取5 mg咖啡酰氨基酸乙酯衍生物,分别溶解于0.5 mL的氘代二甲基亚砜(DMSO-d6)或氘代丙酮(C3D6O)中,配制成10 g/L的样品溶液置于核磁共振管中。仪器运行条件:AV400 MHz。通过氢谱的数据分析目标产物中氢的类型及数量。
1. 3. 3 咖啡酰氨基酸酯衍生物HPLC-MS表征
样品的配制:取1 mg咖啡酰氨基酸酯衍生物溶解在1 mL的质谱级乙腈中,配制成1 g/L的溶液,稀释成质量浓度为1 μg/L的待测液。液相色谱条件:流动相为乙腈和水。质谱条件:ESI离子源,ESI+;扫描范围 m/z 50~500;电喷雾电压4 500 V。
1. 4 清除DPPH自由基试验
参考文献[15]中的方法测定了样品清除DPPH自由基能力:各待测组分均用无水乙醇溶解,配制成一系列浓度,将不同浓度的样品溶液(1 mL)与1 mL DPPH (2×10-4mol/L)的乙醇溶液混合,对混合物进行剧烈摇动,在黑暗中停留30 min,在517 nm处测定吸光度,以Vc作为阳性对照。样品对DPPH自由基的清除能力以IC50(DPPH自由基抑制率达50%所需的物质浓度)表示。DPPH自由基抑制率按下式计算。
DPPH自由基抑制率=[(Ab+Ac-Aa)/Ab]×100%
式中,Aa为样品组(1 mL待测液与1 mL DPPH溶液混合)吸光度,Ab为对照组(1 mL待测物溶剂与1 mL DPPH溶液混合)吸光度,Ac为空白组(1 mL待测液与1 mL无水乙醇混合)吸光度。
1. 5 清除羟基自由基试验
用文献[16]的方法测定样品对羟基自由基的清除能力,用DMSO溶液将待测物配制成不同浓度的溶液。取磷酸盐缓冲液(0.2 mol/L,pH=7.4)、菲啰啉的乙醇溶液(0.75 mmol/L)、FeSO4水溶液(0.75 mmol/L)、样品溶液各1 mL加入试管中,再加入1 mL H2O2水溶液(H2O2体积分数0.01%),混匀。反应混合物在37 ℃下孵育1 h,在536 nm处测定混合物的吸光度值,以Vc作为阳性对照。用IC50(抑制率达50%所需的样品浓度)表示样品的清除羟基自由基的能力。羟基自由基抑制率计算公式如下。
羟基自由基抑制率=[(Ac-Ab)/(Aa-Ab)]×100%
式中,Aa为对照组(用1 mL水代替1 mL H2O2)吸光度,Ab为空白组(用1 mL水代替1 mL待测液)吸光度,Ac为样品组吸光度。
1. 6 红细胞溶血试验
红细胞(red blood cell,RBC)溶血试验是根据原料对血红细胞细胞膜的刺激,导致其破裂后血红蛋白漏出,分光光度法测定化学物质作用后的红细胞悬液的吸光度,可以计算出溶血率。在相同RBC浓度和样品浓度下,吸光度越大,说明细胞溶血率越高,表明样品的刺激性越强。预先配制pH=7.4的磷酸盐缓冲液(添加葡萄糖1.8 g/L)及抗凝剂柠檬酸缓冲液(20 g/L柠檬酸三钠C6H5Na3O7·2H2O,8 g/L柠檬酸C6H8O7)。样品均用磷酸盐缓冲液稀释配制浓度均为1 mmol/L(咖啡酸衍生物均溶解于DMSO)。以SDS (1.3 g/L)作为阳性对照。新鲜血液(已用柠檬酸抗凝剂处理)用磷酸盐缓冲液稀释后,经离心除杂,配制体积分数为2%的红细胞悬液,摇晃均匀。各样品溶液与RBC悬液按V(样品)∶V(RBC)= 3∶1添加于离心管中,混匀,用去离子水和PBS分别替代样品按相同体积比添加,作为完全溶血和阴性对照,然后于室温下摇床孵育1 h。取出受试物/RBC混合液置于离心机中,反应物于10 000 r/min速度下离心1 min,终止孵育。于540 nm处测定其吸光度值(每个浓度测定3个平行,结果取平均值)。溶血率计算公式如下。
红细胞溶血率=[(A样品-A阴性)/(A完全溶血-A阴性)]×100%
式中,A阴性为PBS缓冲溶液作用于红细胞悬液后测定的吸光度值,A完全溶血为去离子水作用于红细胞悬液后测定的吸光度值,A样品为样品作用于红细胞悬液后测定的吸光度值。
1. 7 数据分析
所有数据源于3次重复试验。采用线性拟合计算IC50值。
2 结果与讨论
2. 1 咖啡酸酰氨基酸乙酯的结构表征
化合物a,b,c和d的结构经1H NMR 和HPLC-MS表征,确定其结构及分子量,与预期目标产物结果一致,表征结果如下:
a:产率:60%;黄色固体;熔点:167~170 ℃;1H NMR (400 MHz,DMSO-d6):9.39 (s,1H,OH),9.15 (s,1H,OH),8.40 (s,1H,NH),7.26 (d,J=15.6 Hz,1H,HC=C),6.97 (s,1H,ArH),6.86 (d,J=8.2 Hz,1H,ArH),6.75(d,J=8.1 Hz,1H,ArH),6.40(d,J=15.7 Hz,1H,C=CH),4.10(q,J=7.1 Hz,2H,CH2),3.90(d,J=5.9 Hz,2H,OCH2),1.20(t,J= 7.1 Hz,3H,CH3);ESI+-MS (m/z):266.063 5( [M+H]+)。
b:产率:73%;黄色固体;熔点:122~126 ℃;1H NMR (400 MHz,DMSO-d6):9.39 (s,1H,OH),9.16 (s,1H,OH),8.38 (d,J=6.7 Hz,1H,NH),7.25 (d,J=15.6 Hz,1H,HC=C),6.95 (s,1H,ArH),6.84 (d,J=7.9 Hz,1H,ArH),6.75 (d,J=8.0 Hz,1H,ArH),6.38 (d,J=15.7 Hz,1H,C=CH),4.40~4.24 (m,1H,CH),4.09 (dd,J=14.0,7.0 Hz,2H,OCH2),1.31(d,J=7.3 Hz,3H,CH3),1.19 (t,J=7.1 Hz,3H,CH3);ESI+-MS (m/z):280.046 8 ([M+H]+)。
c:产率:66%;浅黄色固体;熔点:124~126 ℃;1H NMR (400 MHz,C3D6O):8.19 (s,1H,OH),7.98(s,1H,OH),7.42 (s,1H,NH),7.13 (d,2H,HC=C),6.98 (d,J=15.6 Hz,1H,ArH),6.66 (d,J=15.6 Hz,1H,ArH),6.81 (d,J=37.4 Hz,1H,ArH),4.66 (s,1H,OH),4.17 (t,J=10.4 Hz,1H,CH),3.97 (d,J=10.8 Hz,2H,OCH2),2.97 (dd,J=136.7,101.0 Hz,2H,OCH2),1.47~1.07(m,3H,CH3);ESI+-MS(m/z):296.037 ([M+H]+)。
d:产率:76%;黄色固体;熔点:79~81 ℃;1H NMR (400 MHz,C3D6O):8.17(s,1H,OH),8.04(s,1H,OH),7.31(s,1H,NH),7.02(d,J=40.9 Hz,2H,HC=C),6.86(d,J=8.1 Hz,1H,ArH),6.61(d,J=15.6 Hz,1H,ArH),6.72(d,J=8.1Hz,1H,ArH),4.45(d,J=6.1 Hz,1H,OH),4.22(s,1H,CH),4.02(q,J=7.1 Hz,2H,OCH2),3.92(d,J=7.1 Hz,1H,CH),2.90~2.56(m,3H,CH3),1.27~0.69(m,3H,CH3);ESI+-MS(m/z):309.31([M+H]+)。
2. 2 DPPH自由基清除能力的比较
IC50值越小,表明其对DPPH自由基清除能力越强,反之,则越弱。咖啡酰氨基酸酯衍生物清除DPPH自由基的IC50值见表1,各数值间差异显著(P<0.05)。咖啡酰氨基酸酯衍生物清除DPPH自由基能力由强到弱的顺序为:c>d>a>CA>b>VC。可知咖啡酰氨基酸酯衍生物清除DPPH自由基的能力明显高于常用抗氧化剂Vc(阳性对照)。而且咖啡酸与不同氨基酸成酰胺后清除自由基活性强弱明显不同,表明侧链氨基酸基团对于咖啡酰胺类衍生物的抗氧化性影响显著,氨基酸基团对清除活性影响强弱顺序为:丝氨酸>苏氨酸>甘氨酸>丙氨酸。4种合成的咖啡酸衍生物中咖啡酰丝氨酸乙酯清除DPPH自由基能力最强,其IC50值为13.5 µmol/L。
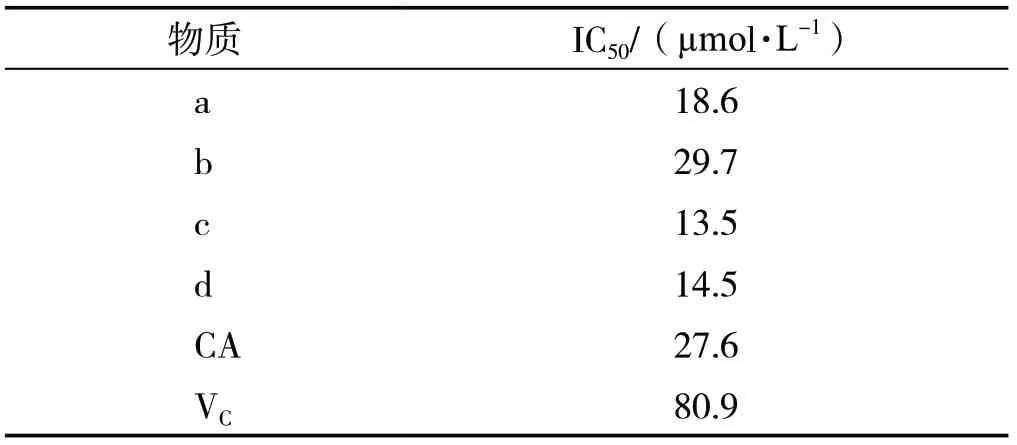
表 1 不同合成产物对DPPH自由基的清除效应Tab. 1 Sc avenging effects of different synthetic products on DPPH free radicals
2. 3 羟基自由基清除能力的比较
不同咖啡酰氨基酸酯衍生物作用于羟基自由基后IC50值如表2所示,各数值间具有显著性差异(P<0.05)。它们对羟基自由基的清除能力由强到弱的顺序为:b>c>d>CA>a>VC。可知咖啡酸及其酰胺类衍生物对于羟基自由基的清除能力均强于常用抗氧化剂VC(阳性对照)。不同咖啡酰氨基酸酯衍生物清除羟基自由基能力的不同,反应出其抗氧化的强弱与化合物的侧链氨基酸基团有关。4种合成的咖啡酸衍生物中咖啡酰丙氨酸乙酯清除羟基自由基能力最强,其IC50值为0.214 mmol/L。
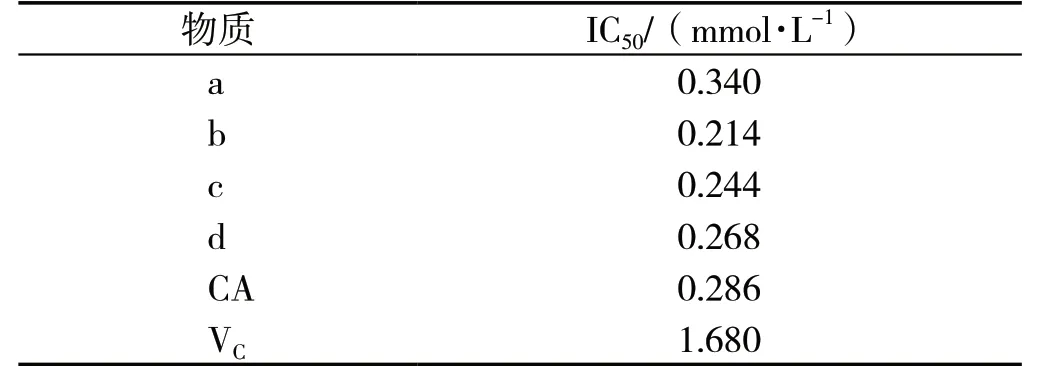
表 2 不同合成产物对羟基自由基的清除效应Tab. 2 Scavenging effects of different synthetic products on OH radicals
2. 4 红细胞溶血率
前期研究发现配制样品浓度越大,对应的RBC溶血率越高,说明样品浓度越大,对红细胞膜的刺激性越强。样品溶血率值如表3所示,反应样品浓度为1 mmol/L(SDS质量浓度为1.3 g/L)时对红细胞膜的刺激性大小,样品溶血率由大到小排序为:SDS(74%)> CA(2.39%)>a(2.38%)>b(1.07%)>DMSO(0.89%)、d(-0.38%)、c(-0.85%)。由溶血率大小推知,咖啡酸与氨基酸乙酯盐酸盐成酰胺后刺激性明显降低。
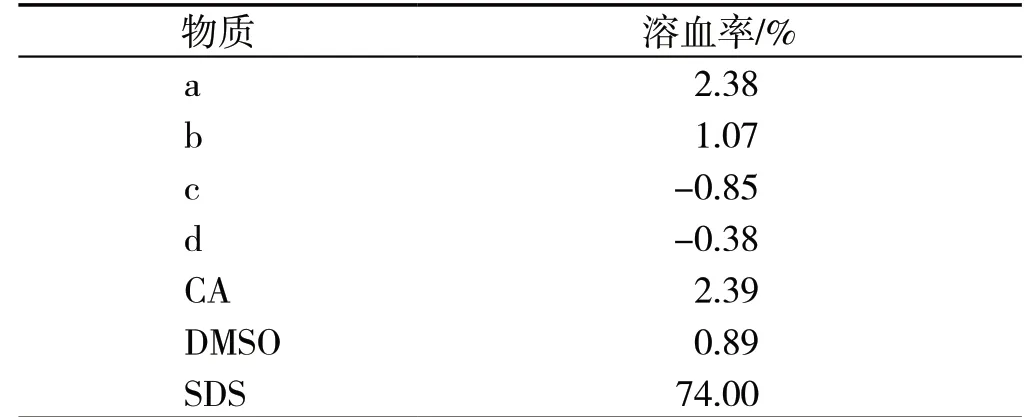
表 3 不同合成产物溶血率Tab. 3 Effects of different compounds on hemolysis ratio
3 结论
合成了咖啡酰甘氨酸乙酯、咖啡酰丙氨酸乙酯、咖啡酰丝氨酸乙酯、咖啡酰苏氨酸乙酯,且后三种咖啡酰氨基酸乙酯未见文献报道。实验结果显示4种咖啡酸酰胺类衍生物溶解性无明显增加,但功效性均有提高,都呈现了较好的抑制DPPH自由基、羟基自由基活性的效果,且咖啡酰丝氨酸乙酯清除DPPH自由基能力最强,其IC50值为13.5 µmol/L;咖啡酰丙氨酸乙酯清除羟基自由基能力最强,其IC50值为0.214 mmol/L。不同咖啡酰氨基酸酯衍生物对DPPH、羟基自由基抑制作用活性排序差异性可能是由于不同功效评价实验体系反应机理不同导致的偏差,4种合成产物抗氧化性存在差异,这主要是由于氨基酸的结构不同而导致的差异性。4种咖啡酸酰胺类衍生物相对于咖啡酸单体对红细胞膜的刺激性更弱,表明改性后的咖啡酸具有更高的安全性。
