系统评价与Meta分析的内涵及价值
2019-03-08靳英辉吴世文拜争刚曾宪涛
靳英辉, 吴世文, 拜争刚, 曾宪涛
(1. 武汉大学中南医院循证与转化医学中心·武汉大学循证与转化医学中心·武汉大学第二临床学院循证医学与临床流行病学教研室,武汉 430071; 2. 武汉大学新闻与传播学院广电系·武汉大学媒体发展研究中心,武汉 430072;3. 南京理工大学公共事务学院社会学系·南京理工大学循证社会科学与健康研究中心,南京 210098)
系统评价(systematic review)与Meta分析(Meta-analysis)发展至今天,已成为研究者及实践者均需关注的方法。特别是近年来其结果带来的对现有证据颠覆性的观点,每每引起轩然大波。如2017年12月,JAMA刊出的Meta分析表明补钙和维生素D不能降低50岁以上社区人群骨折风险[1];2018年3月,JAMACardiol刊出的Meta分析表明服用ω-3脂肪酸与致死性或非致死性冠心病或任何重要的血管事件无显著关系[2]。事物的发展及对事物的认知是不断深化的,伴随着系统评价与Meta分析的广泛传播,亦产生了一些误解。因此,正确理解其内涵及价值,对有效使用系统评价与Meta分析、避免其局限性具有重要意义。
1 系统评价与Meta分析的发展
1.1 Meta分析的发展
Meta分析亦被译为荟萃分析、元分析、统分分析等。据资料可查源自于法国分析学家皮埃尔-西蒙·德·拉普拉斯(Pierre-Simon de Laplace)和德国著名数学家约翰·卡尔·弗里德里希·高斯(Johann Karl Friedrich Gauss)发明的合并效应量的方法;Meta分析的具体应用最早可追溯至英国皇家天文学家乔治·比德尔·艾里爵士(George Biddell Ariy),他在1861年出版的针对天文学家的专著中阐释了Meta分析的方法[3]。在医学领域,著名的统计学家卡尔·皮尔逊(Karl Pearson)于1904年应用该方法将接种肠热病疫苗与生存率之间的相关系数进行了合并。他认为“由于受发生概率错误大小的影响,很多分组资料均太小,不足以获得结论性的结论”,这一合并的理由至今仍为进行Meta分析的重要理由[4-5]。
Meta分析于1930年开始广泛在社会科学领域应用;且Meta分析这一术语由美国教学心理、社会学家吉恩·格拉斯(Gene V. Glass)于1976年命名并定义为“The statistical analysis of large collection of analysis results from individual studies for the purpose of integrating the findings”[6-7]。此后,尽管对Meta分析的定义争议不断,许多方法学家均对其进行定义,但均倾向于“Meta分析是对以往的研究结果进行系统定量综合的统计学方法”这一核心要义。1985年,美国社会教育学家拉里·弗农·郝奇斯(Larry Vernon Hedges)和美国教育统计学家英格拉姆·奥尔金(Ingram Olkin)共同出版了第一本专行介绍Meta分析的著作[8]。1991年,生态学领域的首项Meta分析发表[9]。1995年,首篇介绍生态学与进化学领域的Meta分析正式发表[10]。2013年,首部介绍生态学与进化学领域的Meta分析制作手册正式出版,该书提供了在生态学和进化学中进行Meta分析的第一个全面性的指南,也与其他领域相关,如异质性是预期的、合并了在不同领域中使用的不同方法的明确考虑[11]。
如今,Meta分析在心理、经济、生态、管理、地理、教育、犯罪、工程、进化生物学等领域得到广泛应用,医学领域仅仅是当前应用Meta分析最为活跃的领域之一。2018年3月,美国Stony Brook University生态与进化学系杰西卡·古雷维奇(Jessica Gurevitch)等在Nature正刊撰写综述介绍了Meta分析,认为“Meta分析作为一种重要的工具,通过量化已知的识别未知的东西来促进科学的快速发展”[12]。
1.2 系统评价的发展
系统评价亦被译为系统综述,起源于研究合成(research synthesis)。这一术语是英国著名的流行病学家及内科医生阿奇·科克伦(Archie Cochrane)于1979年提出的[7,13]。在临床实践中,他注意到已发表的7项随机对照试验的结果显示对早产孕妇采用氢化泼尼松治疗可降低早产儿死亡率30%至50%,然而大多数产科医师却不知晓这一疗法有效,导致约1%的早产儿因未应用该治疗而死亡。因此,科克伦提出“医学各专业应将所有相关的随机对照试验收集起来进行系统评价,并随着新的试验结果的出现不断更新,以得出更为科学可靠的结论,从而为临床实践提供可靠的证据”。实际上,在1972年他就主张“医学干预应建立在经过严格评价的、基于随机对照试验汇总分析的证据基础上”[14],这一主张最终发展成了开展系统评价必要性的理论基础。
随后,美国医师辛西娅·穆罗(Cynthia D. Mulrow)在分析了1985—1986年间发表在JAMA、NEJM、AnnInternMed和ArchInternMed这4种著名医学期刊上的综述后指出[15]: 医学综述应致力于解决一个具体的问题,应行有效检索、应制定明确的纳入/排除标准、应标准化评价过程与方法、应客观全面整合结果,只有建立在系统且全面收集、评价和整合后的结论才可信;此外,综述作者还应指出当前综述的局限性及提出日后改进的建议。穆罗医师的这一观点奠定了制作系统评价的方法学基础。
1989年,英国产科医师伊恩·杰弗里·查默斯爵士(Iain Geoffrey Chalmers)带领团队系统性的评价了低价格、短疗程的类固醇药物治疗有早产倾向孕妇的随机对照试验结果,评价结果显示类固醇药物可显著降低婴儿死于早产并发症的风险[16]。该研究被称之为“一项震惊整个医学界的研究”;同时也标志着现代意义上的Cochrane系统评价(Cochrane systematic review, CSR)的雏形初步形成。2018年10月,英国循证医学方法学家迈克·克拉克(Mike Clarke)撰文介绍了系统评价及Systematic Reviews杂志,包括了对系统评价的历史、现在及未来的反思[17]。
2 系统评价与Meta分析的定义及关系
2.1 两者的定义
为减少机遇而逐渐发展成熟的Meta分析和为降低偏倚而不断完善的科学综述于20世纪90年代最终在医学领域融合,诞生了“Systematic Reviews”这种全新证据生产方法。1993年7月在伦敦召开的会议上,英国Cochrane中心的方法学家与BMJ杂志的编辑们正式提出“Systematic Reviews”这一术语,并大力进行推广,如今开展系统评价的理念和方法已获广泛接受[7]。系统评价可以是定性的(qualitative systematic review),即未采用Meta分析;也可以是定量的(quantitative systematic review),即包含了Meta分析。
在西班牙内科医师及流行病学家米克尔·波尔塔(Miquel Porta)主编的第5版A Dictionary of Epidemiology中,对Meta分析的定义有3大要点[18]: ①它是一种统计分析方法,针对独立的研究结果进行;②它需考察研究结果间差异的来源,当结果具有足够的相似性时方可使用该方法进行定量合成;③Meta分析具有定性成分和定量成分。因此,可看出Meta分析是将≥2项相同研究主题研究的结果进行定量的综合分析,这一过程包括问题的提出、纳入及排除标准的制定、相关研究文献的全面检索、基本信息的描述、相关数据的提取和定量统计分析等。然而,Cochrane协作网(https://www.cochrane.org/evidence)定义的要点为: (1) 如果单个研究的结果被组合起来产生一个整体的统计数据,这通常被称为Meta分析;(2) 许多Cochrane系统评价通过从多个试验中收集数据来衡量受益和危害,并将它们组合起来产生一个平均结果,目的是提供更精确的干预效果评估和减少不确定性;(3) 并非所有的Cochrane系统评价数据库(Cochrane Databases of Systematic Review, CDSR)中的系统评价均包括Meta分析。
上述的第5版词典对系统评价定义的亦有3大要点[18]: (1) 它运用限制偏倚的策略严格评价与综合针对某一具体问题的所有相关研究;(2) Meta分析不一定是系统评价的必须部分;(3) 它与Meta分析的不同之处在于其不包括对结果的定量总结。因此可见,系统评价是基于某一具体问题,全面收集全球所有未或已发表的相关研究,筛选出符合纳入标准的研究并使用临床流行病学的原则和方法对其进行严格的评价,然后再行定性或/和定量(Meta分析)合成,从而得出更为可靠地结论。而Cochrane协作网对其的定义的三大要点为: (1) 系统评价是识别、评估和综合所有符合预先设定的合格标准的实验性证据,以回答一个特定的研究问题;(2) 进行系统评价的研究人员使用明确的、系统的方法,以减少偏见的观点来选择,以产生更可靠的结果来为决策提供信息;(3) CSR是发表在CDSR上有关卫生保健和卫生政策研究的系统评价。
2.2 系统评价与Meta分析的关系
从上述内容来看,系统评价与Meta分析既同而不和、又和而不同。今天Meta分析仍可以独立使用,但必须遵循一定的报告格式。两者之间有4点需要注意: (1) Meta分析可应用于诸多领域,而系统评价几乎只限于医学领域;(2) Meta分析可作为系统评价的一部分,但也可单用;(3) 医学领域中,广义的系统评价包括Meta分析;(4) Meta分析≠系统评价。
两者的关系如下: (1) 制作系统评价时并非必须要行Meta分析;(2) 纳入的研究是否具有足够的相似性是是否行Meta分析的主要根据;(3) 制作Meta分析时也并非一定要将其做成系统评价;(4) 对多项同质性好的研究进行了Meta分析的系统评价可称之为定量系统评价;(5) 若纳入研究因同质性不足而无法行Meta分析(即未行Meta分析)、仅行了描述性分析的系统评价称为定量系统评价;(6) 未行Meta分析的系统评价应属于吉恩·格拉斯研究分层的第二层次、单纯的Meta分析则应属于第三层次[19]。用图形来表示,则两者关系如图1。
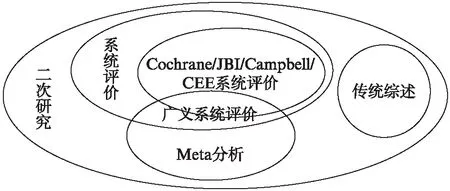
图1 系统评价/Meta分析与传统综述的关系Fig.1 Relationship between systematic review/meta-analysis and narrative reviewCEE: The Collaboration for Environmental Evidence;JBI: Joanna Briggs Institute
2.3 系统评价与传统综述的区别
传统的文献综述,即叙述性的文献综述(narrative review)。系统评价与Meta分析不同于传统综述。2001年,英国学者Petticrew对两者做了清晰的比较[20],见表1;图1也展示了两者的区别。
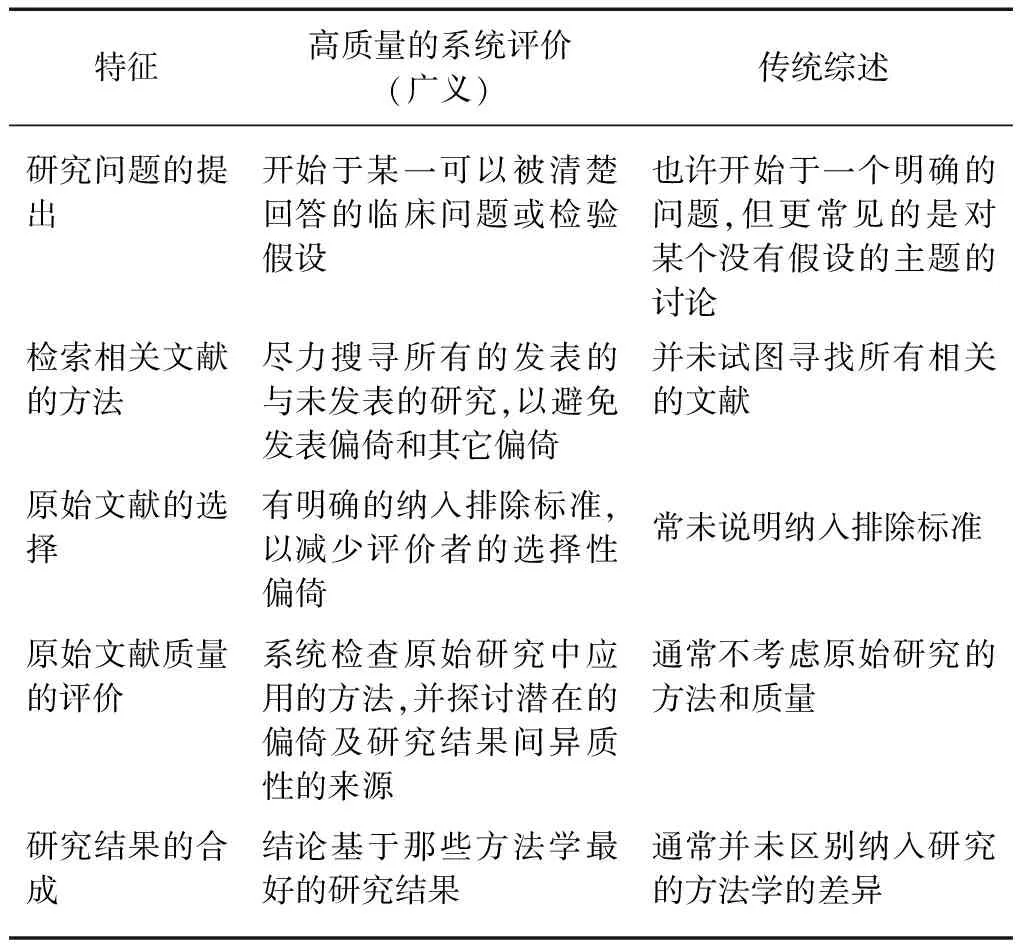
表1 传统综述与系统评价的区别
早在1995年,伊恩·查默斯爵士等指出系统评价/Meta分析与传统综述相比较,具有以下优点[21]: (1) 使用明确的方法学及流程以最大程度限制在纳入及排除研究的过程中出现偏倚;(2) 经过正式比较不同研究的结果,能得出概括性与一致性的结果;(3) 可明确异质性产生的原因、对特定亚组产生新的假设;(4) 进行Meta分析能增加全部结果的精确性;(5) 得出的结论更为可信及精确;(6) 大部分信息能迅速被研究者、卫生服务人员及政策制定者采用;(7) 缩短了研究发现到有效诊治策略实施之间的时间差。
3 系统评价与Meta分析的价值
3.1 增加客观性、解决分歧及引出新见解
为何要行系统评价与Meta分析呢?以医学研究为例,这样的情况很常见: 甲药与乙药干预某一疾病的效果孰优孰劣、抑或是等效,一般会有多项相关研究发表。然而,这些研究的结果至少存在下述两种情况: (1) 相互矛盾的结果,即有的结果具有统计学上的差异、有的则无,此时就需要量化不同研究结果间的变异程度并考虑结果的意义;(2) 结果是一致的,即均有统计学上差异或均无,此时仍需尽可能估算出准确无误的效应量、及探讨一致性研究结果的稳健性程度。显然,系统评价与Meta分析能达成这些目标。
当前公认系统评价与Meta分析有以下9个方面的优点[6-8,21-24]: (1) 对同一主题多项研究的结果间一致性进行评价;(2) 对同一主题多项研究的结果行定性/定量合成;(3) 有效寻找新的或需进一步研究的研究问题,特别适于研究的选题;(4) 当解答目标问题受制于某些条件(如研究对象或时间的制约)时,系统评价与Meta分析是一种较佳的解决方法;(5) 能从方法学的角度评价现阶段某个主题的研究设计;(6) 发现某些单项研究未能阐明的问题、可得出对该问题更为全面的认识,亦可解决专家间意见不一不致的局面;(7) Meta分析扩大了样本量、可增加统计效能和估计效应值的精确度,增强结果的可靠性与客观性;(8) Meta分析的结果有时会出现一些研究者事先想不到的结果,从而引出新见解;(9) 使证据的使用更加方便。
如图2所示,该图展示了PKRP与TURP治疗良性前列腺增生症后的电切综合征(TURS)的发生情况[25]。若未开展Meta分析,会认为两者在TURS的发生率是没有区别的;但经过Meta分析之后,发现了意想不到的结果,即PKRP的TURS发生率显著低于TURP,也就证明PKRP在这个结局上更安全。因此,与传统的描述性的综述相比,设计合理、制作严谨的系统评价与Meta分析能对所有证据进行更为全面、客观的评价,能对结局指标及其效应量进行更准确、客观的评估,并能很好的解释不同研究的结果间的异质性。
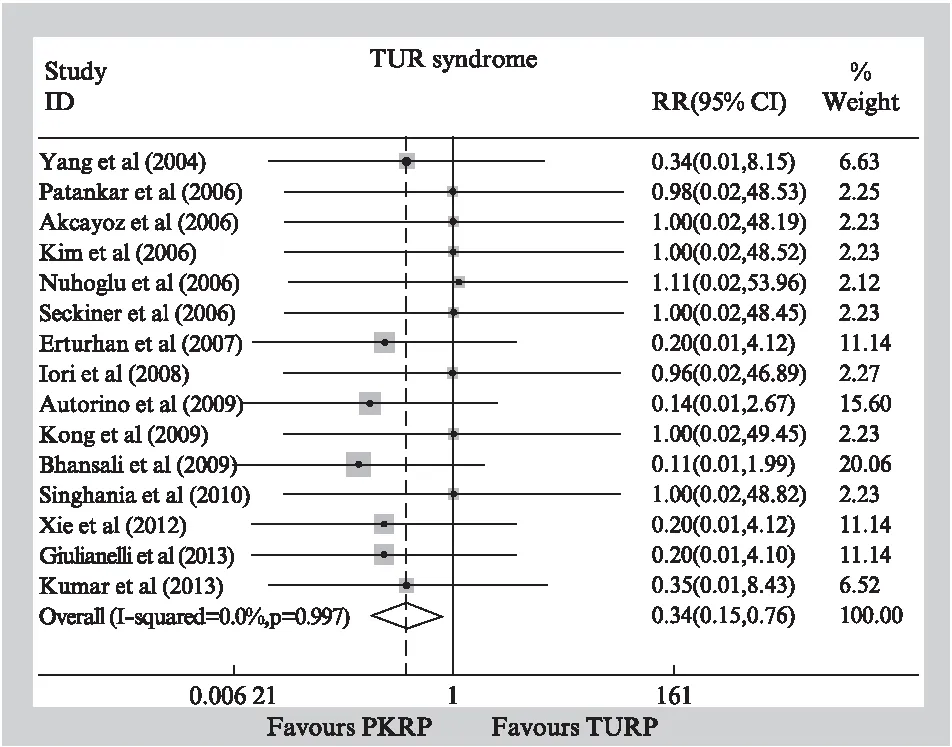
图2 示例: Meta分析产生意想不到的发现[25]Fig.2 Example: Emerging unexpected finding from meta-analysis
3.2 提升研究价值、降低浪费
重复研究导致的研究资源浪费是一个较为普遍性且严重的问题。2016年,BMJ发表文章指出“所有新的研究都应以现有证据的系统评价/Meta分析为前提”,目的是“Reducing Waste, Increasing Value”。该文同时用图展示了如何使用系统评价与Meta分析[26]。而且开展临床研究的选题思路来源,其中之一就是来源于前期的系统评价与Meta分析的结果,近年来国内许多临床研究团队发表高水平的学术论文的研究选题及设计优化即是如此[27-29]。
3.3 为指南提供证据
临床实践指南(Clinical Practice Guideline, CPG)是开展实践的重要参考。目前,得到广泛认可的最为规范的定义主要是有美国医学研究所(Institute of Medicine, IOM)提出的定义和世界卫生组织(World Health Organization, WHO)提出的定义。
1990年,IOM提出了临床实践指南的定义: 针对特定的临床情况,系统制定出的帮助临床医生和患者做出恰当处理的指导性意见[30]。2011年,IOM对指南对定义进行了更新: “CPG是针对患者特定的临床问题,基于系统评价形成的证据,并对各种备选干预方式进行全面的利弊平衡分析后提出的最优化指导意见”[31]。并明确指出循证临床实践指南(Evidence-Based Clinical Practice Guideline, E-CPG)的六大特征: (1) 必须基于当前所有证据(重点考虑最新的系统评价与Meta分析)形成的系统性评价;(2) 必须是多学科协作;(3) 必须考虑患者的意愿价值偏好;(4) 制定的过程要透明,最大程度的控制可能存在的偏倚,避免利益冲突;(5) 要明确患者临床问题的结局指标和备选干预方案之间的逻辑关系,有明确的证据质量分级和推荐强度;(6) 新的证据出现时,应当及时更新指南。这个定义提出后,进一步明确了循证临床实践指南的定义和特点,得到许多国家学者的认可与推崇。
2012年,WHO对制订研发的指南提出了明确的定义: “WHO指南是指任何包含了有关卫生干预推荐意见的文件,这些干预设计临床、公共卫生或卫生政策。推荐意见告诉指南使用者“应该做什么”,指导人们在影响卫生保健和资源利用的不同干预之间做出选择[32]。WHO指南需要遵循两大原则: 推荐意见基于对现有证据的全面客观的评价;形成推荐意见的流程清晰明确。
因此,制定/修订指南的重要步骤就是规划系统评价/Meta分析,并基于此使用证据分级标准进行分级。以WHO指南制定的流程为例,依次顺序是[32]: (1) 成立WHO指导小组;(2) 列出优先主题;(3) 检索文献获得相关数据及现有系统评价;(4) 核实是否有其他指南;(5) 制定指南范围方案;(6) 形成可能的推荐意见;(7) 初步构建PICO问题;(8) 按要求进行评审与修订。可以看出,系统评价是重要的环节。
4 系统评价/Meta分析与循证医学的关系
循证医学的定义明确指出了任何一项决策都必须包括三大要素: 当前最佳的研究证据、医生的临床经验和患者的意愿[33];这亦是循证医学的三要素。可以看出: (1) 证据只是三要素之一;(2) 经过系统化评价的证据是最佳的证据;(3) 系统评价与Meta分析属于系统化评价的证据。再者,系统评价与Meta分析只是循证医学证据来源的重要方法之一,并非全部方法。
当前国内最大的误解就是将循证医学与系统评价/Meta分析相等同。实际上早在1996年循证医学的先驱大卫·萨科特(David L. Sackett)等就特别提出不要一提及循证医学就将其和随机对照试验/Meta分析联系在一起[34]。武汉大学循证与转化医学中心曾宪涛博士认为廓清循证医学与系统评价/Meta分析与的关系只需把握两点: (1) 证据只是证明有用,有用不等于对我有价值、更不等于我会选择;(2) 证据不等于决策,只是决策三要素之一。他亦举了一个例子以助理解[33]: 假设一对夫妇中丈夫患了前列腺癌且怀疑伴骨转移,当前证据表明PET-CT是诊断骨转移的最佳手段。那么有以下6种情况: (1) 该夫妇为贫困人群,一次检查的费用对其来说是昂贵的,尽管主治医师推荐PET-CT,但他们应该会选择普通的CT;(2) 该夫妇经济条件很好,主治医师推荐PET-CT,但他们依据所掌握的知识坚持认为PET-CT的辐射量很大而拒绝,要求使用普通的CT;(3) 该夫妇经济条件很好,且要求使用PET-CT,但被告知所在地区的医院没有PET-CT设备,只能选择普通的CT;(4) 该夫妇经济条件很好,在武汉大学中南医院住院,经主治医师推荐后,愿意选择PET-CT进行检查;(5) 该夫妇经济条件很好,愿意选择PET-CT且所在地区的医院有PET-CT设备,其主治医师认为普通的CT即可解决,但他们坚持要使用PET-CT进行检查,最后主治医师遵从了他们的意愿;(6) 该夫妇经济条件很好,愿意选择PET-CT且所在地区的医院有PET-CT设备,但其主治医师认为普通的CT即可解决,最终他们决定听从医生的建议选择了普通的CT检查。此即“有用≠对我有价值≠我会选择”。
再者,决策还受到国家或当地政策法规、风俗习惯及文化的影响。例如超声检查是鉴别胎儿性别的最佳证据,可用来进行选择性妊娠,但因国家政策法规不允许等而无法实施,这也是“证据≠决策”的体现。
5 结 语
系统评价与Meta分析因为需要而产生,因不完善而持续优化。身处学术时代与信息爆炸时代的我们,应该去掌握这门方法;冗余的、过载的信息不仅造成了信息的混杂,而且带给了信息处理的负担。从新闻传播学的角度考察,系统评价与Meta分析通过整合信息,能够通过明确“此时此刻”医学专业共同体的共识,为专业的医学报道提供确切的信息,纾解新闻信息中对不确定的医学知识或健康信息的争议,从而推动医学报道不断提升科学性与前沿性。这在今天信息爆炸的语境中显得尤为重要。近年来,循证健康新闻报道的出现,以及对相关工具包的开发可谓是有益的尝试。其次,系统评价与Meta分析通过整合信息、明晰结论、发现新趋势,为确定的信息报道提供了重要的支撑。关照健康教育与公共卫生运动,系统评价与Meta分析所做的工作以及取得的研究成果能够用于健康促进,推动公众不断提升其健康素养。再者,在学术研究层面,系统评价与Meta分析可用于开展健康传播话题的研究,例如控烟宣传效果研究、癌症信息认知及其影响因素研究等,用整合的数据推动健康话题的聚合研究。尽管系统评价与Meta分析仍有许多值得研究的地方[35],但我们有理由相信,系统评价与Meta分析将持续服务于各学科的发展。
