蒿属植物降糖活性成分及提取方法研究进展
2019-03-01肖建琪李达张杰黄雪峰冯锋
肖建琪,李达,张杰,2,黄雪峰*,冯锋,2,3**
(1. 中国药科大学天然药物化学教研室, 江苏 南京210009;2. 中国药科大学生物材料重点实验室, 江苏 南京 210009;3. 江苏食品药品职业技术学院, 江苏 淮安 223003)
随着我国国力的不断提升,人民生活水平和生活质量逐年提高,糖尿病患病人数也越来越多。糖尿病会引发多种并发症,如心脑血管类疾病等。目前对于糖尿病的治疗,尚停留于“治标不治本”,仍无药物可以彻底治愈糖尿病,只是用药物来维持症状不致加剧[1]。糖尿病是一种由于胰岛细胞分泌异常引起的一种以高血糖为特征的慢性病[2]。中医学将糖尿病归于“消渴”的范畴,是一种虚实结合的复杂疾病[3]。由于相对西药而言,中药来源广泛、价格低廉、毒副作用可能较小,中医药治疗糖尿病在我国已经得到越来越多的认可。
蒿属植物在我国广泛分布,是包含数量最多的菊科植物之一[4],由于此属植物具有独特的香气,因此常可以用作食品原料[5-7]。该属植物中的艾叶、茵陈蒿、奇蒿、滨蒿等为常用中药,并为中国药典收载品种,因此研究该属植物具有深远的意义。
随着现代分离分析技术以及药理活性评价手段的不断提高,蒿属植物在降血糖方面的研究取得了一定进展,本文对蒿属植物降糖主要活性成分、降糖作用机制、提取方法和质量分析等多方面进行归纳总结,旨在为蒿属植物降糖活性的深入研究和开发利用提供参考。
1 多糖
随着现代科技的不断进步,植物多糖的作用广为人知,菊科植物中的多糖类成分降血糖活性也逐渐受到重视[8-9]。但对于其中蒿属植物中的多糖类化合物,截至目前仅报道了艾叶多糖的降血糖活性。
1.1 艾叶多糖的降血糖作用机制研究
尹美珍等[10]为筛选蒿属植物艾叶的降血糖活性部分,采用80%乙醇回流提取、去离子水提取方法和乙醇沉淀法,从艾叶的水提液中获得艾叶多糖粗品,用去离子水配制3种不同浓度的艾叶多糖溶液,并用链脲佐菌素造2型糖尿病模型,测定血糖胰岛素含量和肝糖原水平。结果显示:艾叶多糖不仅能明显降低糖尿病小鼠的血糖,还能改善糖耐量,且其高剂量组的降血糖效果更好,由实验结果可知艾叶多糖是艾叶降糖的活性成分。其作用机制是增加糖尿病小鼠的肝糖原,从而调节其血糖浓度,起到降低血糖作用。
1.2 多糖的提取与纯化
1.2.1 多糖的提取胡岗等[11]利用水浴回流的方法提取艾叶中的多糖类化合物,首先用无水乙醇在80℃的条件下回流提取1.5 h,浓缩得到浸膏后,用去离子水在同等条件下回流提取3次,提取后仍然过滤浓缩,并反复应用水洗醇析,最后用Saveg法去除蛋白等杂质,得到艾叶多糖粗提物。
甘昌盛等[12]采用水提的方法提取艾叶多糖,用正交实验法,探索料液比、浸泡时间和提取时间对艾叶多糖提取率的影响。结果发现,对其影响最大的是料液比,其次是浸泡时间,影响最小的是提取时间,最佳提取工艺是:料液比为1 : 20、浸泡和提取时间分别为5和4.5 h。
罗旋等[13]采用超声波法提取艾叶多糖,提取温度为95 ℃,提取时间为2 h,提取之前超声作用30 min,其中料液比为1 : 20,其余步骤与胡岗等[11]的步骤类似。
李华生等[14]采用加压同步萃取法,通过单因素影响实验和正交实验对各种因素进行了比较,发现加压对艾叶多糖的提取率影响显著,且发现艾叶多糖的最佳提取工艺条件为:溶剂体积分数为50%、固液比l : 30(g : mL)、萃取压力0.9 MPa、萃取时间40 min、萃取温度120℃。在此条件下,多糖的提取率为6.82%。
1.2.2 艾叶多糖的纯化沈霞[15]用多种方法进行脱色对比,发现最佳脱色方法是ADS-7静态吸附法,基于单因素试验的响应面法对艾叶多糖的ADS-7静态吸附法工艺进行了优化,获得其最佳工艺条件为:温度40 ℃,吸附3 h,在此条件下,多糖得率为0.25%。
1.3 艾叶多糖的结构表征
艾叶多糖的结构一般含有支链且结构相对比较复杂,相对分子质量也大,故对其分析较困难。在进行结构表征时,需先使用酸水解法等将多糖分解成相对分子质量较小的多糖或寡糖,才可进行色谱光谱联用分析以确定其单糖组成、糖苷键的类型和位置。纯度测定也是多糖分析的基本项目之一[15],经纯度确定的艾叶纯化多糖,可进行药理或体内实验。
1.4 艾叶多糖的含量测定
艾叶多糖的含量测定方法有硫酸-蒽酮法和硫酸-苯酚法[15],其中硫酸-苯酚法测定方法中所用的苯酚需要重蒸,实验操作不安全,故常用硫酸-蒽酮法来测定艾叶多糖的含量。艾叶多糖的分析流程见表1。

表 1 艾叶多糖的分析流程Table 1 Analytical procedures of polysaccharides from Artemisia argyi Levl. et Vant.
2 黄酮类化合物
黄酮类化合物在多种植物中广泛存在,是一类重要的天然有机化合物,也是中药中一类含量较高的有效成分,据统计,艾叶的药理活性主要有:治疗和预防心血管疾病的发生、抗肝脏毒性、抗炎、抗菌、抗病毒及解痉等[16]。
目前已经报道的蒿属中有降糖活性的黄酮类化合物包括香茅醇(1)、异鼠李素(2)、槲皮素(3)、金丝桃苷(4)、异鼠李素-3-O-葡萄糖苷(5)、异鼠李素-3-O-生物碱(6)、蒙花苷(7)、木犀草素(8)、芹菜素(9)、异泽兰黄素(10)、素柚皮素(11)和合金欢(12)[17-19]。

2.1 黄酮类化合物的降血糖作用机制
2.1.1 延缓葡萄糖吸收糖尿病是一种以高血糖为特征的慢性疾病,2型糖尿病的常见治疗手段是降低餐后血糖值。现代药理学研究发现,艾叶中的黄酮类化合物对α-葡萄糖苷酶、α-淀粉酶等糖苷酶具有一定的抑制活性[20]。α-葡萄糖苷酶抑制剂是近年来的研究热点,其是通过抑制小肠上皮刷状缘上的葡萄糖苷酶的活性,抑制多糖、双糖等向葡萄糖转化,减少小肠对葡萄糖的吸收从而降低血糖[21]。
Anaya-Eugenio等[19]为了研究蒿属植物茵陈蒿中的降血糖活性成分,对有机提取物、浸渍物和精油3个提取部位进行了葡萄糖耐量和淀粉糖耐量的小鼠体内实验,结果显示其中浸渍物提取部位是3个部分中活性最好的,进一步对其中的有效成分进行了分离,得到了异泽兰黄素和棕矢车菊素等5个化合物,通过体外α-葡萄糖苷酶的活性抑制实验,进一步验证了这些化合物的降血糖活性。
2.1.2 改善胰岛素抵抗胰岛素抵抗(insulin resistance,IR)是指胰岛素从分泌到发挥效应的过程中,在受体前、受体和受体后任何一处缺陷均造成的一种现象,IR是许多代谢类疾病如糖尿病、冠心病等[20]的诱因。Santana等[22]发现黄酮类化合物有降血糖活性,其作用机制是:在胰岛素敏感性组织中通过各种细胞内信号途径来调节碳水化合物的消化、胰岛素分泌和葡萄糖摄取,从而呈现良好的降糖和改善IR的作用。
2.2 黄酮的提取与纯化
陈瑶等[23]利用酶法辅助的方法提取得到泥蒿中的总黄酮部分,并利用单因素分析的方法对其中的4个变量进行了分析,包括纤维素酶的质量分数(A)、溶剂乙醇的体积分数(B)、料液比(C)和提取温度(D),由实验结果可知,其最佳提取工艺为:A=3%、B=40%、C=1 : 10、D=50 ℃,在此工艺下可得到4.12%的总黄酮。
卫星星等[24]用艾叶进行实验,用索氏提取法对艾叶进行提取,以艾叶中总黄酮的含量为指标,用单因素分析的方法对提取溶剂、提取时间、提取温度和料液比进行了摸索,结果显示其最佳提取条件为:提取溶剂为70%乙醇,提取时间为3 h,温度为80 ℃,料液比为1 : 35(g : mL),在此条件下总黄酮提取率达3.85%。以上结果证明:用索氏提取法对艾叶进行总黄酮的提取是一种操作简便、低成本的方法,值得开发和利用。
另据报道,总黄酮还可以用大孔树脂吸附方法[25]、超声波辅助提取法[26]等获得。
2.3 总黄酮的含量测定
总黄酮的含量测定方法常见的有紫外-可见分光光度法[27],目前药典中所用的也是此种方法。
2.4 黄酮的分离纯化方法
蒿属植物中黄酮类化合物的分离纯化方法有:柱色谱法、薄层色谱法[28]、高效液相法(HPLC)、大孔树脂吸附法[29]。
3 绿原酸类化合物
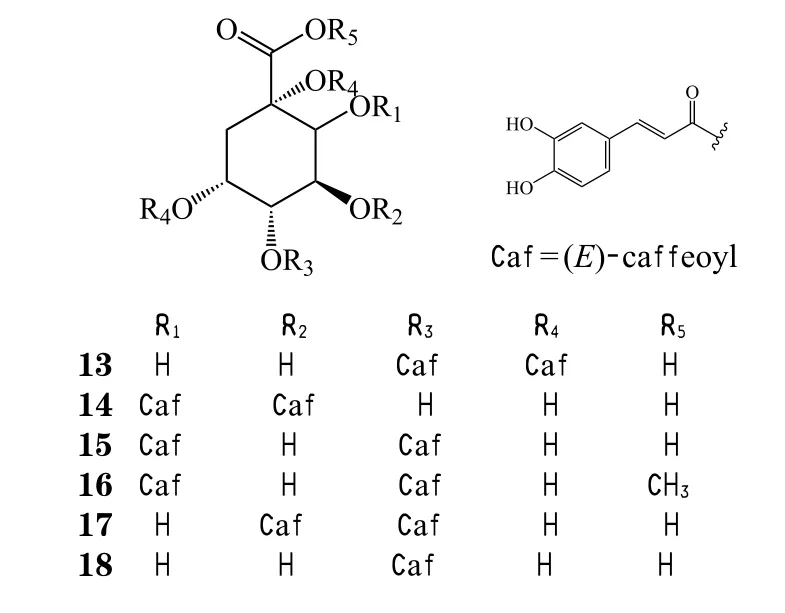
绿原酸(chlorogenic acids)又名咖啡鞣酸,属于酚类化合物,主要存在于菊科蒿属植物中[30],是植物细胞在有氧呼吸过程中经磷酸戊糖途径(hexose monophosphate,HMS)的中间产物合成的一种苯丙素类物质。绿原酸是一种重要的生物活性物质,具有抑菌、抗氧化等多种药理活性[31-32]。目前已报道的蒿属植物中有降糖活性的绿原酸类化合物有1,5-二咖啡酰奎宁酸(13)、3,4-二咖啡酰奎宁酸(14)、3,5-二咖啡酰奎宁酸(15)、3,5-二咖啡酰奎宁酸甲酯(16)、4,5-二咖啡酰奎宁酸(17)和3-咖啡酰奎宁酸(18)[17]。
3.1 绿原酸的降血糖作用机制
Islam等[17]为了探明12种蒿属植物的降血糖成分,对其进行了甲醇提取,并对甲醇提取物进行了α-葡萄糖苷酶抑制实验和蛋白酪氨酸磷酸酶1B(protein tyrosine phosphatase 1B,PTP1B)抑制实验,发现茵陈显示出最强的抑制活性。随后,他们对茵陈全草进行了甲醇提取,用二氯甲烷、乙酸乙酯和正丁醇依次萃取,得到4个萃取部位,并进行了α-葡萄糖苷酶抑制实验和PTP1B抑制实验,结果显示除了水部位外,其他萃取部位均有抑制活性,于是对这些部位进行了分离提取,共得到25个化合物,分别是10个香豆素类化合物、8个黄酮类化合物、6个咖啡酰奎宁酸类化合物和1个色原酮。对这些单体化合物进行了上述抑制实验,结果显示:1,5-二咖啡酰奎宁酸、3,4-二咖啡酰奎宁酸和3,5-二咖啡酰奎尼酸甲酯等3种绿原酸类化合物对α-葡萄糖苷酶的抑制活性[IC50分别为(146.06±0.07)、(128.07±5.45)、(80.95±4.10)μmoL · L-1]均优于阳性对照药阿卡波糖 [IC50=(187.34±3.31)μmoL · L-1],结果表明绿原酸类化合物通过抑制小肠中α-葡萄糖苷酶的活性,从而延缓了葡萄糖的转化,使葡萄糖含量降低。
3.2 绿原酸类化合物的提取与纯化
绿原酸类化合物的提取有多种方法,传统的提取方法有:水提法、醇提法、乙酸乙酯提取法、超声波辅助提取法、水提醇沉法、壳聚糖絮凝剂吸附法、大孔树脂吸附法等;新型的提取方法有:超声微波双辅助、分子印迹法、高速逆流法、膜分离技术、酶解法等[32-33]。其中,水提醇沉法应用最广泛,在提取茵陈时,使用70%的乙醇所得绿原酸的含量最高;在工业中多用壳聚糖絮凝剂吸附法,原因是壳聚糖易降解、安全环保;与传统的分离纯化方法相比,新型的方法具有操作简便、重现性高、分离快速、价格低廉等显著优点。
4 其他成分
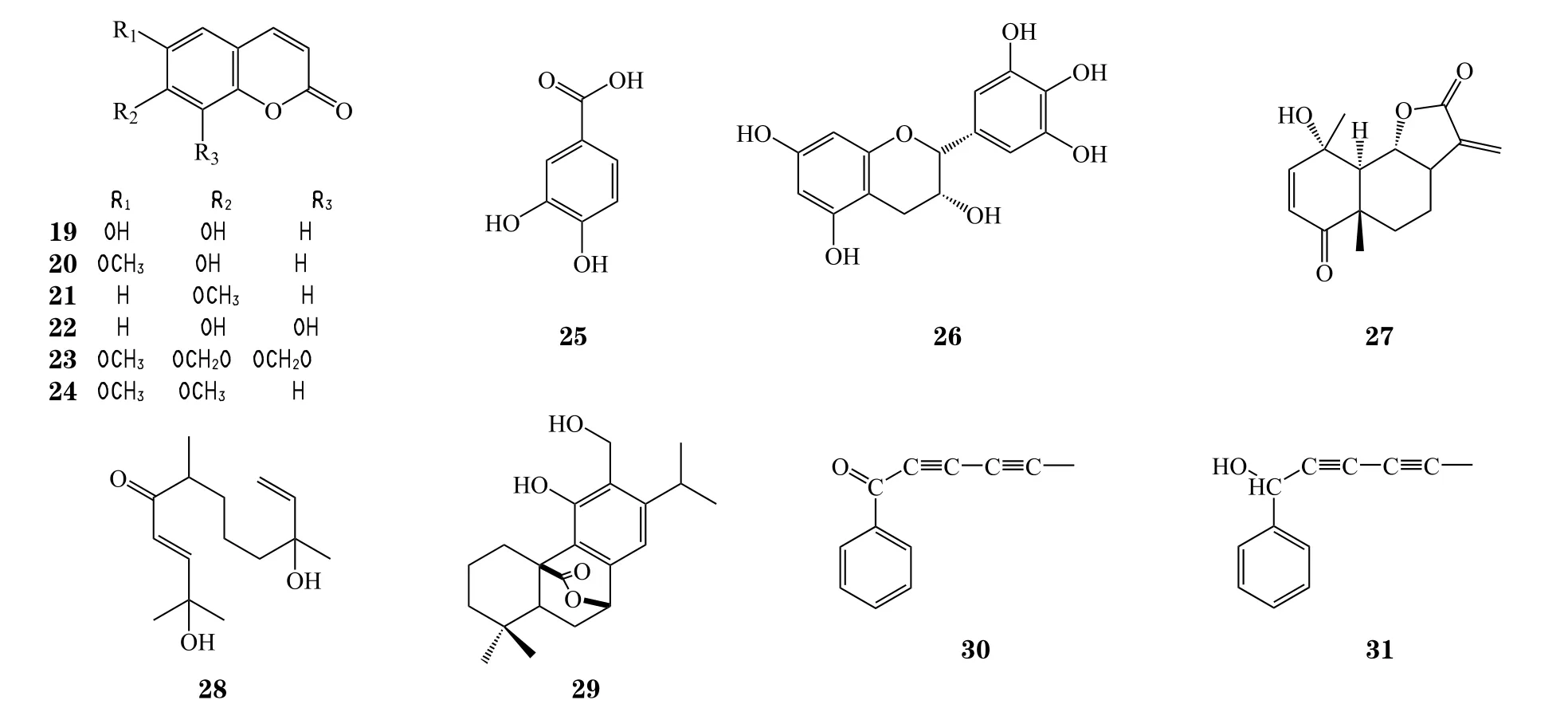
除了上述化学成分外,蒿属植物中还存在一些其他具有降血糖活性的化学成分,如香豆素类化合物:东莨菪内酯(19)[17]、伞形花内酯(20)[17]、7-甲氧基香豆素(21)[17]、瑞香素(22)[17]、6-甲氧基青蒿素C(23)[17]和滨蒿内酯(24)[34];酚类化合物:原儿茶酸(25)[35]、原儿茶素(26)[35]、青蒿素(27)[19]、salvinine(28)[19]和鼠尾草酚(29)[36];其他类成分:茵陈青霉素(30)[37]、茵陈蒿素(31)[37]。这些化合物的降血糖机制都是通过抑制小肠中α-葡萄糖苷酶的活性,从而延缓了葡萄糖的转化,使葡萄糖含量降低,起到了降血糖的作用。
5 结语
目前,糖尿病已成为最受全球关注的病症之一,鉴于高血糖是糖尿病的主要特征且是引起心血管疾病的重要因素,因此有必要开发价廉、高效、低毒的降血糖新药。蒿属植物在我国分布广泛,资源易得,故蒿属植物来源的新型天然降血糖药物具有巨大的开发潜力。本文主要综述了蒿属植物中具有降血糖活性的多糖类、黄酮类、绿原酸类等化学成分,以及它们的相关降血糖活性机制。其中降血糖机制主要包括:1)通过增加肝糖原和改善糖耐量;2)抑制α-葡萄糖苷酶的活性,进而减少对葡萄糖的吸收;3)调节AMPK信号通路,改善IR。然而,国内外学者对蒿属植物的降血糖机制研究尚不够彻底、系统,故有必要对蒿属植物中活性成分的降血糖机制进行深入研究,以进一步阐明其药效物质基础,为寻找新的天然降血糖成分提供科学依据,且这一研究也将具有广阔的应用前景。
