超声评价2型糖尿病患者内脏脂肪与皮下脂肪的特点
2019-02-28徐向东朱小虎
徐向东 朱小虎 黄 杨 刘 兰
1 成都医学院临床医学院,四川省成都市 610500; 2 成都医学院第一附属医院超声科; 3 成都军区机关医院内二科
2型糖尿病(Diabetes mellitus type 2,T2DM)是以糖、脂代谢紊乱为主要临床特征的慢性代谢性疾病,严重威胁着我国中老年人的生命健康,是心脑血管疾病的重要危险因素[1]。近年研究发现,脂肪组织不仅能储存能量,而且还具有分泌功能,尤其是内脏脂肪,可分泌TNF-α、IL-6、MCP-1、瘦素等细胞因子,这些因子与炎症、动脉粥样硬化、代谢紊乱的发生和发展密切相关[2]。而心外膜脂肪组织(Epicardial adipose tissue,EAT)属特殊的内脏脂肪组织,被研究者称为内脏脂肪的标志,是心肌及大血管表面与浆膜性心包脏层之间的脂肪组织,主要分布于心脏房室沟、室间沟及心室周围[3]。本研究旨在分析T2DM患者与正常人群内脏脂肪与皮下脂肪的特点,为T2DM患者心血管疾病的防治提供相关理论基础。
1 对象与方法
1.1 研究对象 选择我院2017年1月—2018年7月的T2DM住院患者120例为T2DM组,其中男57例,女63例;年龄49~79岁,平均年龄(64.43±7.26)岁。以同期120例健康体检者为对照组,其中男59例,女61例;年龄48~77岁,平均年龄(63.39±7.02)岁。T2DM组纳入标准:(1)T2DM诊断标准依据中华医学会《中国2型糖尿病防治指南(2013年版)》;(2)排除其他先天性及后天性慢性疾病,如肿瘤,严重肝、肾、肺部疾病及高血压、冠心病、先天性心脏病、器质性心脏瓣膜病等心脏疾病。对照组纳入标准:研究期间于本院体检人群,经相关医学检查排除各类先天性及后天性慢性疾病。两组性别、年龄比较差异无统计学意义(P>0.05)。
1.2 仪器和方法
1.2.1 仪器:采用GE-Logic vivid E9、Mindray-Resona 7超声诊断仪,探头选用M5Sc心脏探头、频率3~5MHz,C5腹部探头,频率2~5MHz及9L高频探头、频率7~10MHz。
1.2.2 人体测量及实验室检查:对两组对象进行病史采集,测量身高、体重,计算体重指数(BMI);空腹抽取静脉血,测定血糖、糖化血红蛋白(HbA1c)、血脂[包括甘油三酯(TG)、总胆固醇(TC)、低密度脂蛋白胆固醇(LDL-C)、高密度脂蛋白胆固醇(HDL-C)]。
1.2.3 脂肪厚度测量:(1)EAT测量:受检者左侧卧位,探头置于胸骨左侧,于左室长轴切面显示右室前壁EAT。测量时要求取样线垂直于右室前壁,利用M型超声于收缩末期测量心外膜与心包脏层间的脂肪厚度[4]。(2)腹腔脂肪测量:受检者仰卧位,探头置于脐上缘,测量腹直肌内侧缘至腹主动脉前壁的距离[5]。需空腹以排除肠气干扰,检查时需屏住呼吸,以排除呼吸和腹壁紧张度的影响。(3)肝前脂肪测量:受检者仰卧位,沿腹正中线、剑突到脐方向进行纵向扫查,在腹正中线上测量腹白线内缘至肝左叶前缘的最大距离[6]。(4)皮下脂肪测量:受检者仰卧位,探头置于脐上缘,测量腹直肌内侧缘至皮肤内缘的垂直距离[5]。以上所有脂肪测量须3次并取平均值。

2 结果
2.1 两组脂肪组织厚度及物理、生化指标检查结果比较 T2DM组EAT厚度较对照组厚,差异具有统计学意义(P<0.05);而两组间腹腔脂肪、肝前脂肪及皮下脂肪厚度比较差异无统计学意义(P>0.05)。两组间空腹血糖、HbA1c、BMI、TG、TC、LDL-C及HDL-C比较差异有统计学意义(P<0.05)。见表1。

表1 两组相关变量的比较
2.2 相关性分析 EAT厚度与HbA1c、TG、TC及LDL-C存在正相关性(P<0.05),与HDL-C存在负相关性(P<0.05);腹腔脂肪厚度与BMI、TG、LDL-C存在相关性(P<0.05);肝前脂肪厚度与TG、LDL-C存在相关性(P<0.05);皮下脂肪厚度仅与BMI存在相关性(P<0.05);四种脂肪组织厚度与年龄均无明显相关性(P>0.05)。见表2。
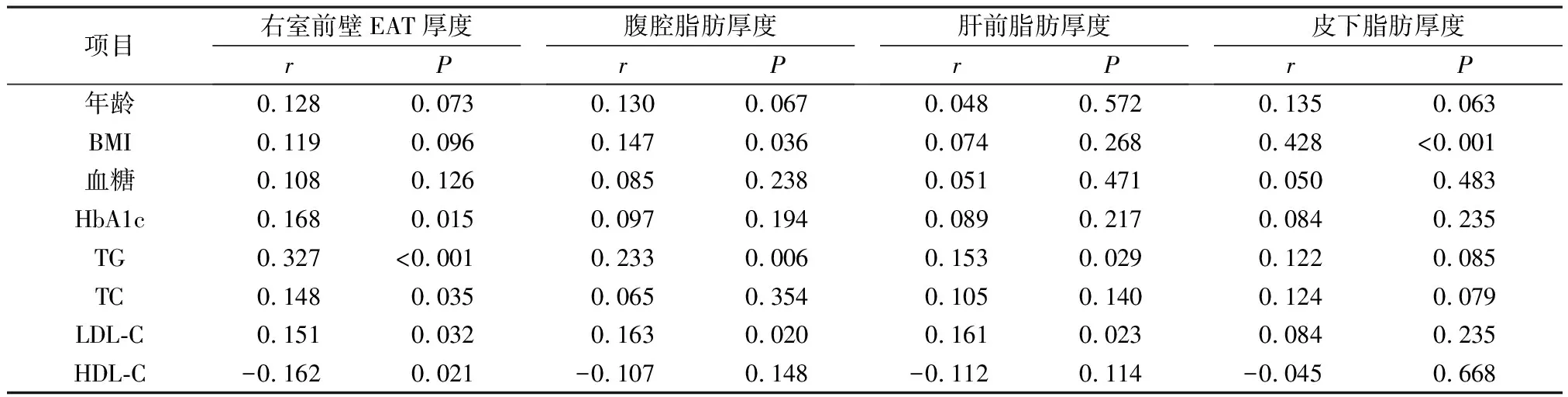
表2 各部位脂肪厚度与基本资料、物理及生化指标的相关性
2.3 EAT的Logistic多元回归分析 对与EAT存在相关性的相关变量进行Logistic多元回归分析,结果显示HbA1c、TG是 EAT增加的独立危险因素,而HDL-C升高是保护性因素,TC及LDL-C对回归分析无统计意义。见表3。
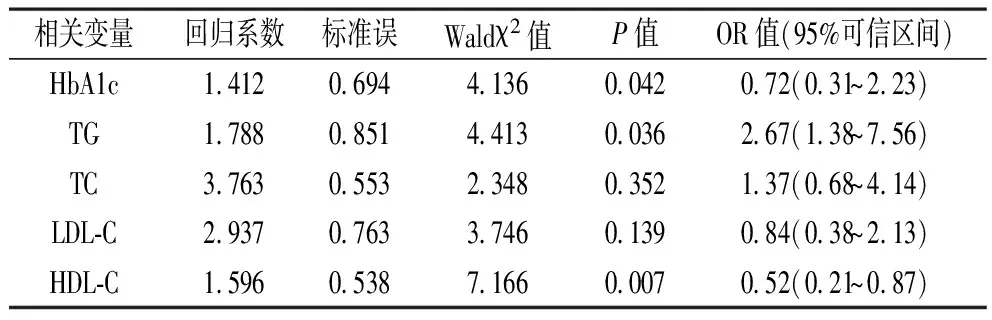
表3 EAT的Logistic多元回归分析
3 讨论
T2DM是心血管事件的独立危险因素,合并向心性肥胖和血脂异常时,具有更高的心血管疾病和糖尿病相关并发症风险[7]。本研究结果发现T2DM患者的EAT厚度高于对照组,而腹腔脂肪、肝前脂肪及皮下脂肪厚度较对照组无明显增厚。与祁荣兴等[8]研究的结果提示2型糖尿病患者心外脂肪厚度较正常人群增加相符合。两组中非EAT脂肪厚度比较无明显差异,这可能与T2DM患者脂肪分布具有明显的向心性特点有关[9];而且EAT是沉积在心脏周围特别是围绕在冠状动脉周围的脂肪组织,其本质是一种特殊的内脏脂肪,EAT和T2DM的发生及进展也存在联系,如EAT分泌的抵抗素是一种肽激素,是肥胖、胰岛素抵抗及炎性反应的重要链接;分泌的脂联素是一种胰岛素增敏激素,能改善胰岛素抗性和动脉硬化症,在临床中表现出抗糖尿病、抗动脉粥样和炎症的能力,但研究发现T2DM患者心外膜脂肪中脂联素水平显著减低[10];另一原因可能是肝周及腹腔脂肪范围较广,本研究仅测量了肝前脂肪及腹主动脉前的腹腔脂肪厚度,不能较好地评价肝周及腹腔脂肪总量的变化,因此存在一定局限性。EAT由冠脉分支供血,与冠脉、心肌之间无筋膜,即不存在解剖屏障,因此其分泌的生物活性物质可直接作用于动脉和心肌,促进患者心血管事件的发生[11]。利用EAT厚度判断患者发生心血管疾病的危险是否有帮助,目前仍无公认的基于超声的EAT厚度阈值,但Meenakshi等[12]研究发现EAT厚度>4.4mm即是心血管疾病的独立危险因子,而且这一危险程度随EAT厚度的增加而提高,当EAT厚度超过6.9mm时其危险程度更大。
相关性分析结果显示研究的各类内脏脂肪厚度与血脂异常均存在一定相关性,但EAT与各项血脂均存在相关性,表明EAT与血脂异常的联系可能更为密切。在EAT的Logistic多元回归分析中得出HbA1c、TG是EAT增加的独立危险因素,而HDL-C升高是保护性因素,这在临床上有助于对T2DM并发症的控制,做到早期发现、早期治疗。
内脏脂肪是沉积在胸腹腔内脏器或大血管周围的脂肪组织,众所周知,即使体重相同的人,其体内脂肪总量及脂肪分布均是不同的。目前对人体脂肪定量评价的方法较多,最简单的是人体直接测量法,如BMI、腰围、腰臀比等,这些指标虽测量快速、简单无创,但不能表现皮下及腹部内脏脂肪数量,对内脏脂肪尤其是EAT的评测准确性差。CT及MRI可对内脏脂肪进行精确测量,特别是MRI被认为是评估EAT的“金标准”,可将心脏分为一系列切面,追踪每个切面的EAT,经过图像整合,较精准计算EAT体积[13],但因辐射、费用高及检查时间长,它们无法作为常规筛选工具。EAT沉积较局限,超声心动图对EAT的检测结果与CT及MRI结果具有良好的相关性[12],且超声心动图更简便、安全、费用低、重复性好,因此超声心动图检测EAT厚度可作为反映内脏脂肪厚度的较好指标。
综上所述,本研究发现T2DM患者EAT厚度较正常人群增厚,EAT与T2DM相关糖脂代谢危险因素存在相关性,且优于肝前脂肪、腹腔脂肪及皮下脂肪;超声心动图能较准确评估EAT厚度,且无创、便捷、廉价,较肝周、腹腔脂肪更利于观测。因此利用超声检测的EAT厚度可为T2DM患者心血管疾病的防治提供相关理论基础,使T2DM人群在心血管疾病等并发症的评估和预防中获益。
