丹参多酚酸盐对大鼠心肌缺血再灌注后心肌细胞凋亡的抑制作用及机制研究
2019-02-27
中药丹参味苦、微寒,具有活血通络、祛瘀止痛、凉血消痈、清心除烦之功效,常用于心血管系统疾病的预防与治疗[1]。丹参多酚酸是丹参的有效成分之一。王强等[2]研究发现丹参多酚酸能够通过降低氧化应激损伤、抑制神经细胞凋亡而对实验性脑缺血再灌注损伤大鼠模型具有一定的神经保护作用,但关于丹参多酚酸对心肌组织缺血再灌注后细胞凋亡的影响文献报道尚不多见。本实验拟通过复制心肌缺血再灌注大鼠模型,研究丹参多酚酸盐对心肌缺血再灌注后细胞凋亡的影响,并探讨其可能的作用机制。
1 材料与方法
1.1 实验动物、药物与试剂 实验用大鼠(品系SD大鼠,清洁级,雄性,鼠龄8周龄,220~260 g)购自河北省实验动物中心[SCXK(冀)2013-1-003]。丹参多酚酸盐购自上海绿谷制药有限公司(规格:每瓶50 mg)。2,3,5-氯化三苯基四氮唑(TTC)购自美国Sigma公司;苏木素-伊红(HE)试剂盒、缺口末端标记(TUNEL)试剂盒购自南京建成生物工程研究所;Bcl-2、Bax、激活型Caspase-3多克隆抗体购自上海碧云天生物技术有限公司。
1.2 实验方法
1.2.1 动物分组、模型制备与给药 设假手术组、模型组、丹参多酚酸盐各剂量组(分别予10 mg/kg、20 mg/kg、40 mg/kg),每组20只。通过夹闭左冠状动脉前降支复制心肌缺血再灌注大鼠模型,心电图示ST段抬高或T波高耸为心肌缺血,夹闭30 min后松开动脉夹,ST段或T波恢复表示再灌注成功[3];假手术组大鼠除不夹闭左冠状动脉前降支外,其余操作同模型组。丹参多酚酸盐各剂量组腹腔注射给药治疗,每日1次,疗程7 d。
1.2.2 心肌梗死面积测定 取心脏组织后放置于-20 ℃冰箱20 min,切片,置2% TTC溶液(恒温37 ℃)避光孵育15 min,灰白色为梗死区,通过医学成像软件计算梗死面积。
1.2.3 心肌组织病变及细胞凋亡的观察 制备心肌组织蜡块并切片,经脱蜡水化后,通过HE染色及倒置光学显微镜观察进行组织病理学检查,通过TUNEL染色观察细胞凋亡状况。凋亡指数(AI)计算:每张切片选取不重叠的6个视野计数细胞总数和凋亡细胞数,计算AI,AI(%)=(阳性细胞数/细胞总数)×100%,各组分别计算平均值。
1.2.4 蛋白质免疫印迹(western blotting)法检测凋亡相关蛋白表达 取心肌组织并研磨匀浆,经4℃、12 000 r/min离心20 min处理后取沉淀,行80 ℃高温蛋白变性后进行电泳、转膜、春红溶液染色,脱脂奶粉封闭2 h,一抗Bcl-2、Bax、激活型Caspase-3、β-actin(1∶500)4 ℃过夜;洗膜,二抗(1∶100)室温摇床孵育1 h后经增强化学发光法(ECL)显色。根据条带灰度值,以β-actin为内参半定量分析凋亡相关蛋白表达。
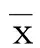
2 结 果
2.1 各组心电图监测结果比较 与假手术组比较,模型组及丹参多酚酸盐各剂量组大鼠术后左心室前壁呈灰白色并渐变为发绀症状,心电图示ST段抬高或T波高耸,提示造模成功。丹参多酚酸盐各剂量组心电波形均明显改善,其中丹参多酚酸盐40 mg/kg组波形接近正常。详见图1。

A:假手术组;B:模型组;C:丹参多酚酸盐10 mg/kg组;D:丹参多酚酸盐20 mg/kg组;E:丹参多酚酸盐40 mg/kg组
2.2 各组心肌组织梗死面积比较 与假手术组比较,模型组大鼠心肌组织梗死面积明显升高(P<0.05);丹参多酚酸盐20mg/kg组、40mg/kg组大鼠心肌组织
梗死面积较模型组显著降低(P<0.05或P<0.01);丹参多酚酸盐10 mg/kg组梗死面积与模型组比较,差异无统计学意义(P>0.05)。详见表1。
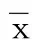
表1 各组大鼠心肌组织梗死面积比较(±s) %
模型组与假手术组比较,1)P<0.05;各剂量组与模型组比较,2)P<0.05,3)P<0.01
2.3 各组心肌组织病变情况比较 假手术组大鼠心肌组织未见明显异常;模型组大鼠心肌组织出现肌原纤维断裂、排列紊乱,细胞空泡变性,细胞质着色不均,胞核深染等病理性改变;丹参多酚酸盐各剂量组大鼠心肌组织病变较模型组呈现不同程度改善,以丹参多酚酸盐40mg/kg组效果最为显著。详见图2。

A:假手术组;B:模型组;C:丹参多酚酸盐10 mg/kg组;D:丹参多酚酸盐20 mg/kg组;E:丹参多酚酸盐40 mg/kg组
2.4 各组心肌细胞凋亡情况比较 模型组心肌细胞凋亡数量较假手术组明显增多;丹参多酚酸盐各剂量组心肌细胞凋亡数量明显减少,以丹参多酚酸盐40 mg/kg组最为显著。模型组大鼠心肌细胞AI较假手术组显著升高(P<0.01);丹参多酚酸盐20 mg/kg组、40 mg/kg组AI较模型组显著降低(P<0.05或P<0.01);丹参多酚酸盐10 mg/kg组AI与模型组比较,差异无统计学意义(P>0.05)。详见表2、图3。
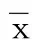
表2 各组大鼠心肌细胞AI比较(±s) %
模型组与假手术组比较,1)P<0.01;各剂量组与模型组比较,2)P<0.05,3)P<0.01

A:假手术组;B:模型组;C:丹参多酚酸盐10 mg/kg组;D:丹参多酚酸盐20 mg/kg组;E:丹参多酚酸盐40 mg/kg组
2.5 各组大鼠心肌组织Bcl-2、Bax、激活型Caspase-3蛋白表达检测结果比较 模型组大鼠心肌组织Bcl-2、Bax蛋白、激活型Caspase-3蛋白较假手术组显著上调表达(P<0.05或P<0.01),Bcl-2/Bax比值较假手术组显著降低(P<0.01)。与模型组比较,丹参多酚酸盐20 mg/kg组、40 mg/kg组能显著上调抑凋亡蛋白Bcl-2表达,且显著下调促凋亡蛋白Bax表达(P<0.05或P<0.01),提高Bcl-2/Bax值(P<0.01),显著下调促凋亡蛋白激活型Caspase-3蛋白表达(P<0.05或P<0.01)。详见表3、图4。
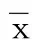
表3 各组大鼠心肌组织Bcl-2、Bax、激活型Caspase-3蛋白表达(±s)
模型组与假手术组比较,1)P<0.05,2)P<0.01;各剂量组与模型组比较,3)P<0.05,4)P<0.01
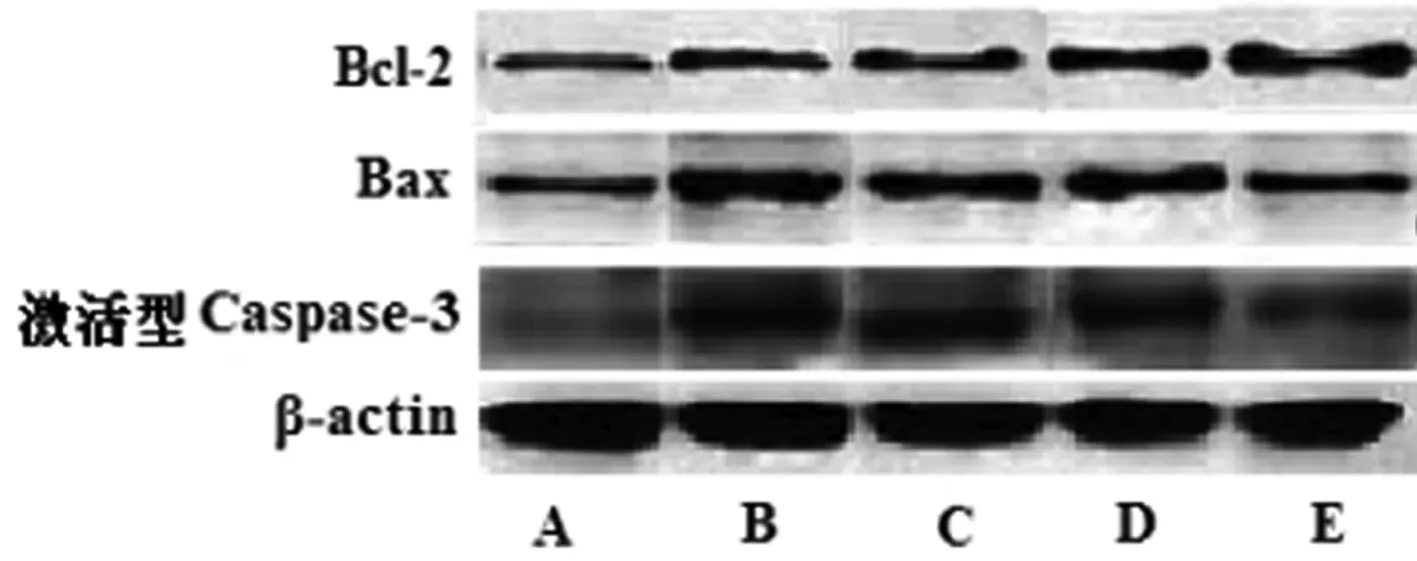
A:假手术组;B:模型组;C:丹参多酚酸盐10 mg/kg组;D:丹参多酚酸盐20 mg/kg组;E:丹参多酚酸盐40 mg/kg组
3 讨 论
冠状动脉粥样硬化性心脏病及其继发性急性心肌梗死(acute myocardial infarction,AMI)发病率随着高血压、高血脂等基础疾病发病率的上升而逐年升高,已经发展成为不容忽视的健康问题。目前,药物或手术溶栓仍是临床上应对AMI的首选方案,但溶栓后血管再通所引发的血流再灌注损伤却成为影响预后的主要因素。血流再灌注损伤的形成机制极为复杂,其中明确的有氧化应激、炎症、心肌细胞凋亡等[4-8]。
结扎左冠状动脉前降支是实验室常用的制备心肌缺血再灌注动物模型的方法,造模过程中进行心电图实时监测,ST段抬高或T波高耸为心肌缺血典型表现,该造模方法操作简单、成功率与重复率双高[9]。本研究发现模型组大鼠术后左心室前壁呈灰白、发绀症状,心电图示ST段抬高或T波高耸,提示造模成功。既往研究发现丹参多酚酸具有抗凋亡、抗氧化、抗炎等多种药理学作用[2,10-11]。心肌缺血再灌注大鼠经丹参多酚酸盐治疗能够有效改善心电图,抑制心肌组织病变,减小梗死面积,提示丹参多酚酸盐具有抑制心肌缺血再灌注损伤的作用。
促凋亡蛋白激活型Caspase-3、Bax和抑凋亡蛋白Bcl-2在细胞凋亡过程中发挥着重要的调控作用[12],其中Bcl-2和Bax同属Bcl-2基因家族。Bcl-2通过抑制细胞色素C释放、调节细胞内钙浓度而表现出抑凋亡作用[13];Bax通过破坏线粒体膜渗透性、激活促凋亡蛋白激活型Caspase-3而表现出促凋亡作用[14];同源的Bax和Bcl-2能够聚合形成同源二聚体而彼此抑制对方的活性,因此Bax、Bcl-2的相对含量更能反映二者在细胞凋亡过程中所起到的调控作用[15]。本研究发现,心肌缺血再灌注大鼠经丹参多酚酸盐治疗能明显上调抑凋亡蛋白Bcl-2表达,下调促凋亡蛋白Bax和激活型Caspase-3表达,提高Bax/Bcl-2值,这可能是丹参多酚酸盐抑制心肌缺血再灌注大鼠心肌细胞凋亡的重要分子机制之一。
丹参多酚酸盐对心肌缺血再灌注大鼠心肌细胞凋亡具有抑制作用,可能与其调节凋亡相关蛋白Bcl-2、Bax、激活型Caspase-3表达有关。
