紫外-可见分光光度法在定量监测2,3,5-三碘苯甲酸缓释中的应用
2019-02-21刘来俊徐海燕王富军
刘来俊,徐海燕,赵 帆,王富军,王 璐
(1.东华大学 纺织学院,上海 201620;2.东华大学 纺织面料技术教育部重点实验室,上海 201620)
聚对二氧环己酮(PPDO)是一种半晶质的脂肪族聚酯醚,其分子主链中含有酯键,完全降解时间在 6~12 月之间,降解产物为水和二氧化碳,对人体没有毒害[1-2]。此外,PPDO 大分子链中含有独特的醚键,使其具有强度高、柔韧性好、刚度小等优点,是理想的医用生物降解材料[3]。目前,PPDO 单丝已成功运用于医用可吸收缝合线[4],同时在血管支架[5]、组织工程支架[6]、下腔静脉滤器[7]、食道管支架[8]、气管支架[9]等方面也有广泛的应用前景;但 PPDO 中仅含有 C、H、O 元素,没有高电子云密度的元素(如卤素或金属元素),几乎不吸收电磁光谱,无法在手术中或术后通过 X 光成像技术检测,因此,需赋予 PPDO 单丝显影性能,以满足其在手术时定位及手术后监测的需求。
2,3,5-三碘苯甲酸(TIBA)是一种油性物质,几乎不溶于水,能溶于碱性溶液(NaOH、 KOH等)和一些有机溶剂(乙醇、二甲基亚砜等)。其分子中含有碘原子,且单位摩尔的TIBA中碘原子的含量较高,具有很强的显影效果,是很多商用显影剂的主要成分[10-11]。与同为油性物质的PPDO 通过熔融共混挤出的方式可一体化得到PPDO显影纤维,并且其显影性能取决于共混材料中 TIBA 含量的多少。而PPDO 是可降解的聚合物材料,一旦用于体内,其显影特性会随着PPDO 的降解和TIBA 的溶出而降低,因此通过体外模拟来研究 PPDO显影纤维中 TIBA 的释放规律,建立体外降解与显影效果之间的联系是极其重要的。TIBA的热分解温度与PPDO较为接近,因而无法采用热重分析(TGA)的方式来分析释放量。此外,TIBA密度较小,不易分离,常规的称量法不仅在操作上存在一定的难度,并且在测量上也会有较大的误差。
紫外-可见分光光度计具有灵敏度高、准确度好、易于操作等优点,广泛应用于无机和有机物的定性和定量检测[12]。基于此,本文采用分光光度法测量PPDO显影纤维降解液中TIBA的含量,研究了PPDO显影纤维在不同降解周期内TIBA的释放规律。
1 实验部分
1.1 实验仪器与试剂
DHY4/12型微型锥共混仪(上海德弘橡塑机械有限公司);TU-1901型双光束紫外-可见分光光度计(北京普析通用仪器有限责任公司);CHP-80Q型二氧化碳培养箱(上海三发科学仪器有限公司);1000~10 000 μL 移液枪(德国普兰德公司);FA2004型精密电子天平(上海良平仪器仪表有限公司)。
无水乙醇(分析纯,国药集团化学试剂有限公司),中性的磷酸缓冲溶液PBS(成分包括NaCl 137 mmol/L,KCl 2.7 mmol/L,Na2HPO410 mmol/L,KH2PO42 mmol/L),其pH值为7.2±0.2;2,3,5-磺苯甲酸(TIBA,纯度大于98%,南京奥多福尼生物科技有限公司);聚对二氧环乙酮(PPDO,实验室自制)。
1.2 显影纤维的制备
将干燥后的PPDO和TIBA按照质量比为90∶10在微型双锥共混仪中进行共混,经过加热和螺杆的剪切作用,使2种组分混合均匀。本实验采用130 ℃的共混温度,共混时间为30 min,转速为20~ 30 r/min,制备PPDO/TIBA共混物。共混结束后,材料通过直径为1 mm的挤出口挤出。采用手动牵伸,拉伸成长丝,常温冷却固化。
1.3 降解液的测试方法
1.3.1TIBA标准曲线的绘制
利用紫外-可见分光光度法可以准确分析降解液中析出的微量TIBA,前提是TIBA要能够均匀、稳定地分散在稀溶液中,但TIBA是油溶性物质,不溶于水,也不溶解于PBS缓冲溶液。由于生物材料的降解一般采用的是PBS磷酸缓冲溶液,而随着PPDO显影纤维的降解,释放的TIBA不易在降解液中得到较好的溶解和分散,因而,不能直接通过测试降解液的吸光度值来获知显影剂TIBA的释放量。通过前期探索,并考虑到TIBA能够完全溶解于乙醇溶液,乙醇与水能够以任意比例互溶,本文配制了3种比例的PBS和乙醇共混溶液,分别制备梯度含量的TIBA溶液,通过测定溶液的吸光度值,绘制吸光度与TIBA质量浓度散点曲线,并进行线性回归拟合。
对相同质量浓度的TIBA乙醇溶液和TIBA-PBS乙醇溶液进行光谱扫描发现,2种溶液均在232 nm附近出现峰值,这表明TIBA的特征峰值在232 nm左右,PBS溶液中的溶质Na2HPO4、KH2PO4、NaCl和KCl对TIBA的吸收峰基本没有影响。
称取0.1 g TIBA粉末加入到50 mL无水乙醇中,超声溶解5 min。用移液枪分别吸取体积为0.5、1.0、1.5、2.0、2.5、3.0、3.5 mL的TIBA无水乙醇溶液,向其中加入PBS缓冲溶液,使得体系中PBS缓冲溶液与无水乙醇的体积比分别为1∶3、1∶1和3∶1,不同PBS与乙醇体积比的溶液分别记为R1、R2和R3。每种比例下,配制成质量浓度分别为5、10、15、20、25、30、35 mg/L的待测溶液。取上述待测溶液约3 mL于比色皿中,采用紫外-可见分光光度计进行光谱扫描和光度测量,每种试样测量3次以保证实验的准确性。
1.3.2标准液稳定性的测定
为研究TIBA在体积比为3∶1的PBS和乙醇共混溶液中的稳定性,将TIBA质量浓度分别为5、10、15、20、25、30、35 mg/L的溶液静置于37 ℃培养箱中,以模拟体外降解的环境。8 d后测试溶液的吸光度值,以判断其稳定性。
1.3.3TIBA体外累积释放率的测定
降解实验前,用去离子水清洗样品,在40 ℃真空干燥箱干燥24 h至恒态质量,取干燥后试样 3根,分别用精密电子天平称量并记录每根纤维的质量。将试样放置于离心管中,加入pH值为7.2±0.2的PBS溶液10 mL,密封后置于(37±1) ℃恒温培养箱中进行体外释放实验。图1示出为降解液的收集流程图。在1、3、6、10、16、22、30 d收集10 mL降解液,向离心管中加入4 mL无水乙醇,用于溶解黏附在离心管内壁以及纤维表面的TIBA,最后再向离心管中加入2 mL磷酸缓冲溶液,这样收集到的溶液中PBS与无水乙醇的体积比为3∶1。每次提取后,向离心管中补充10 mL相同pH值的PBS溶液。将提取后的溶液中加入PBS和无水乙醇体积比为 3∶1的共混液进行一定倍率的稀释,充分搅拌以保证均匀混合。取上述溶液3 mL于比色皿中,用紫外可见分光光度计测试吸光度,每种浓度含量的溶液测定3次,以保证测定结果有效。结合TIBA质量浓度与吸光度标准曲线,利用下式计算TIBA的累积释放率:
式中:Q为TIBA在n个时间节点的累积释放率,%;Xn为n个时间节点的稀释倍率;Cn为n个时间节点的释放浓度,mg/L;V为体积,L;mc为共混纤维中TIBA的计算质量,mg。
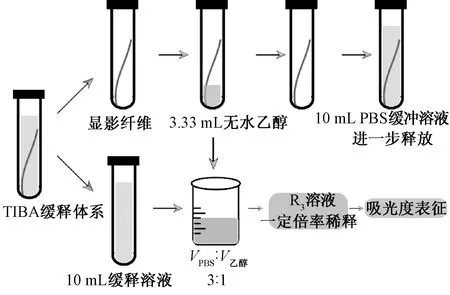
图1 降解液收集流程示意图Fig.1 Schematic diagram of degradation fluid collection process
2 结果与讨论
2.1 不同PBS/乙醇共混比下TIBA回归曲线
图2~4分别示出TIBA在R1、R2和R3标准液的光谱图和质量浓度-吸光度拟合曲线。
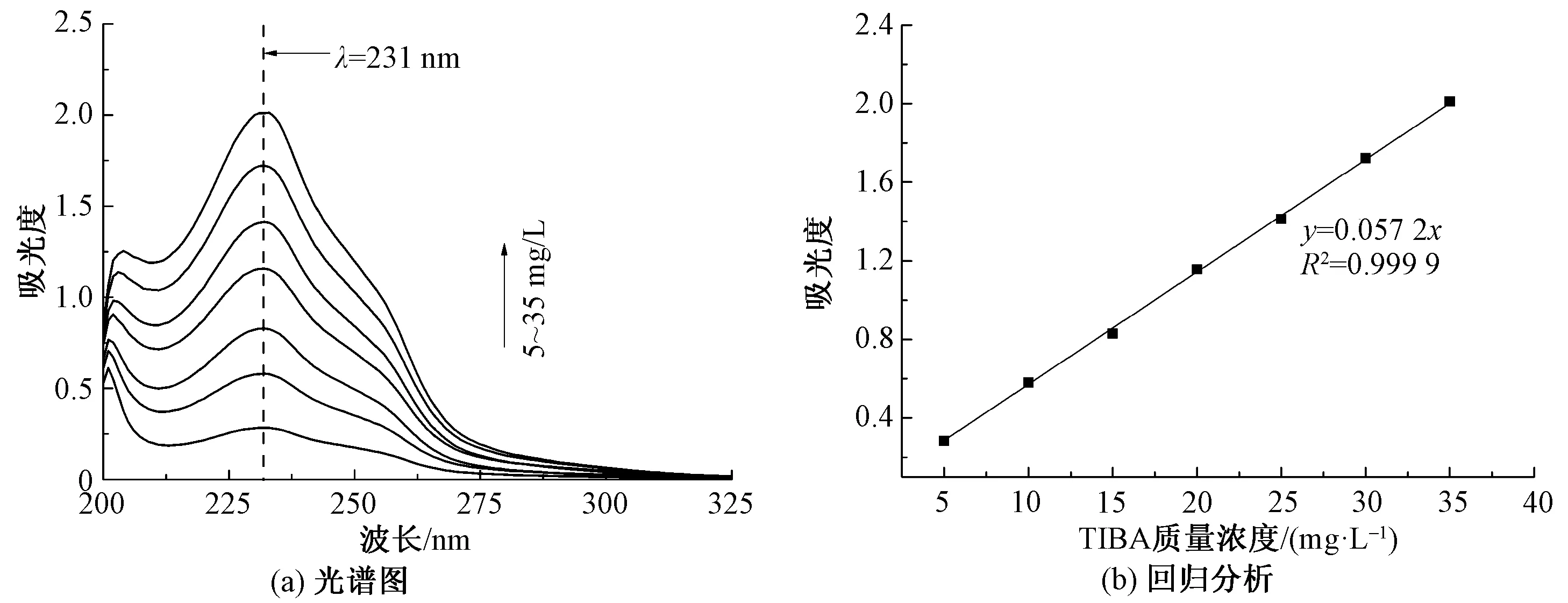
图2 TIBA在R1溶液中的光谱图和回归分析Fig.2 Spectrum (a) and regression analysis (b) of TIBA in solution R1
以TIBA的质量浓度为自变量,吸光度值为因变量进行线性拟合,得到TIBA溶液浓度和吸光度之间的线性拟合函数关系。结果表明:TIBA的R1标准液在波长为231 nm处测得最大吸收峰,回归方程为y=0.057 2x;TIBA的R2标准液在波长为232 nm处测得最大吸收峰,回归方程为y=0.0612x;TIBA的R3标准液在波长为232 nm处测得最大吸收峰,回归方程为y=0.0583x。回归直线的线性范围在[0,35 mg/L],3种共混比例的溶液的拟合度均达到了0.999,接近1,说明这3种共混比例的溶液其质量浓度-吸光度线性回归关系十分明显,即在上述3种共混比下,其拟合曲线均可用于估算降解液中TIBA的含量。考虑到乙醇的用量,后续实验采用PBS和乙醇的体积比为3∶1。
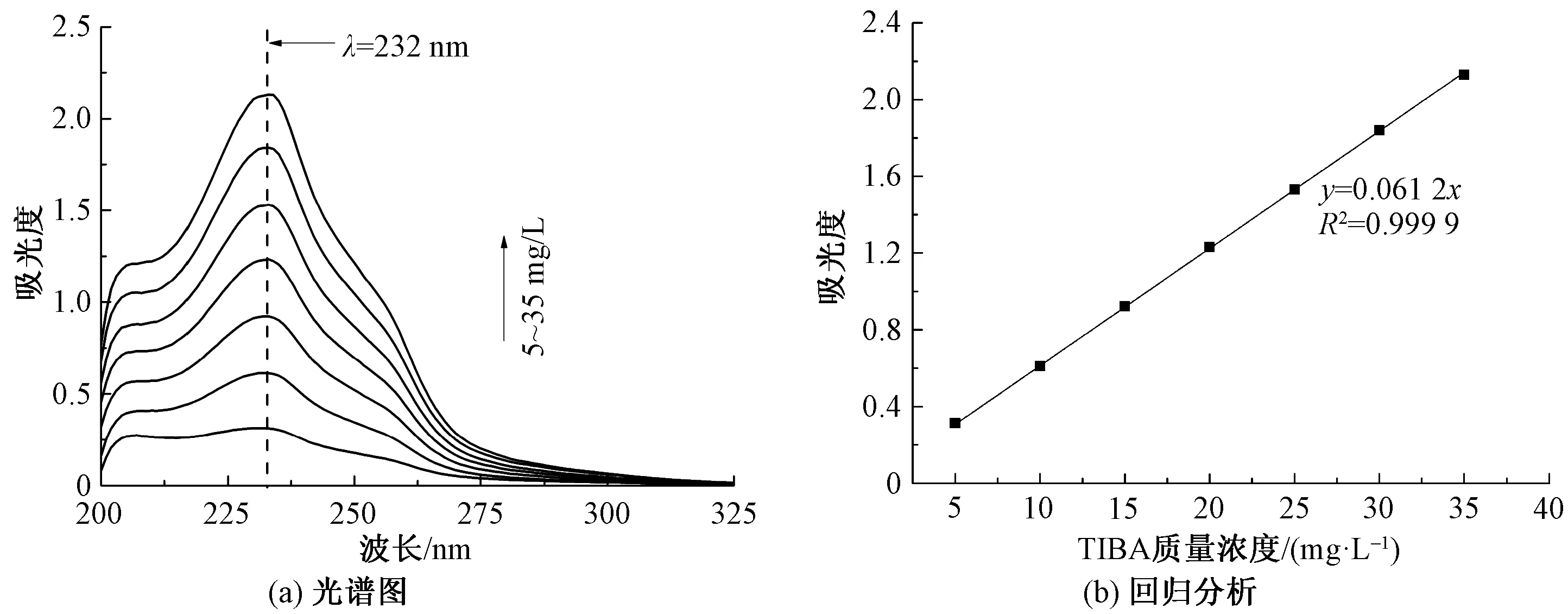
图3 TIBA在R2溶液中的光谱图和回归分析Fig.3 Spectrum(a) and regression analysis(b) of TIBA in solution R2
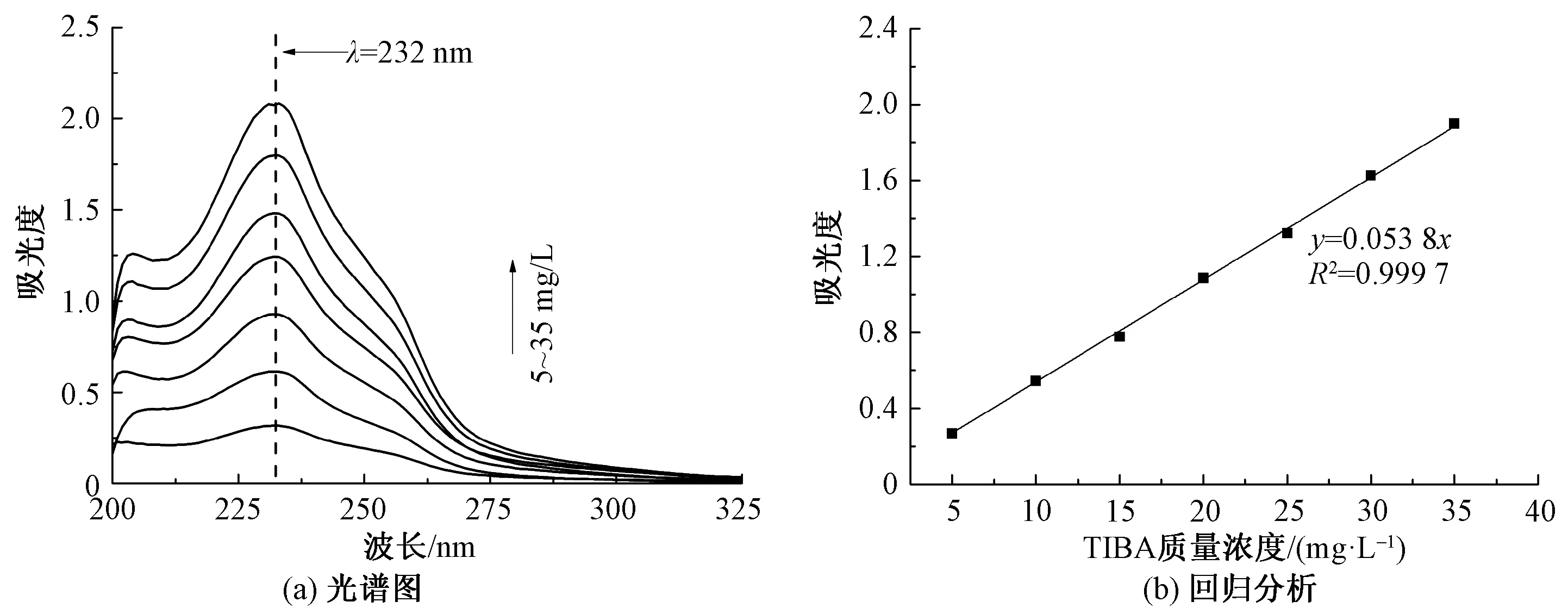
图4 TIBA在R3溶液中的光谱图和回归分析Fig.4 Spectrum(a) and regression analysis(b) of TIBA in solution R3
图5示出为8 d后标准液R3的光谱图和回归分析。其中回归分析中的散点为吸光度的实测值,直线为标准状态下的回归方程y=0.058 9x。结果表明,静置8 d后,共混溶液依然在波长为232 nm处测得最大吸收峰。测试值与回归方程y=0.058 9x相比,低质量浓度区域5、10、15、20、25 mg/L偏差较小,而在高质量浓度区域30、35 mg/L处存在一定程度的偏差,这可能是由于共混液在保存过程中,存在少量溶剂挥发逸散的现象,导致测试值的吸光度值增加,与回归曲线的结果存在少量偏差。通过线性拟合得出的散点与回归方程y=0.058 9x的偏差为0.988 6,即R2为0.998 6,接近于1,偏差较小,可认为TIBA的浓度和吸光度值依然遵循最初的回归曲线。实验设计的最长换液周期为8 d,能够保证析出的TIBA在共混液中保持稳定,因此可用最初的回归方程y=0.053 8x计算TIBA的浓度。
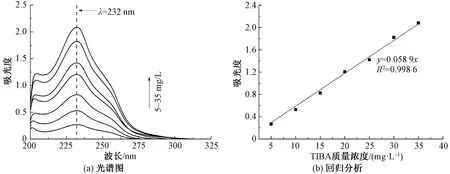
图5 8 d后TIBA在R3溶液中的光谱图和回归分析Fig.5 Spectrum (a) and regression analysis(b) of TIBA in solution R3 after 8 days
2.2 TIBA累积释放率测试结果分析
TIBA与大多数药物一样,属于小分子物质,PPDO属于可降解的高分子材料。PPDO与TIBA复合的材料体系与很多药物缓控释体系类似,TIBA从PPDO基质中释放可以参考药物释放的模型[13]。为更加直观地描述TIBA在磷酸缓冲溶液的体外模拟环境中的释放情况,建立TIBA的释放行为与显影效果的关系,借助表1所示的药物释放常规模型进行TIBA的累积释放率-降解周期拟合,以进一步探究显影剂TIBA中的释放规律[14-16]。根据TIBA累积释放率和时间的关系拟合各个函数模型。R2表示判定系数,R2的值越接近于1,则表示拟合程度越高。一般而言,拟合曲线与实测曲线的特征一致,则拟合程度越高,且各个参数的物理意义明确,则是比较理想的函数模型[17]。

表1 药物释放常规模型Tab.1 Common drug release kinetics
注:Mt为时间节点为t的药物累积释放量;M0为初始的药物上载量;Mt/M0为时间节点t的药物累计释放率;k为释放动力学常数。
通过测量不同降解周期的降解液吸光度值,按照回归方程y=0.053 8x计算TIBA的质量浓度,然后根据公式计算出TIBA的累积释放率,如图6所示。可以看出,标准液R3中的3个试样(S1、S2、S3)的TIBA累计释放规律较为相似,现以S2试样为例进行说明。表2示出S1、S2和S3中TIBA的累积释放率的拟合参数。
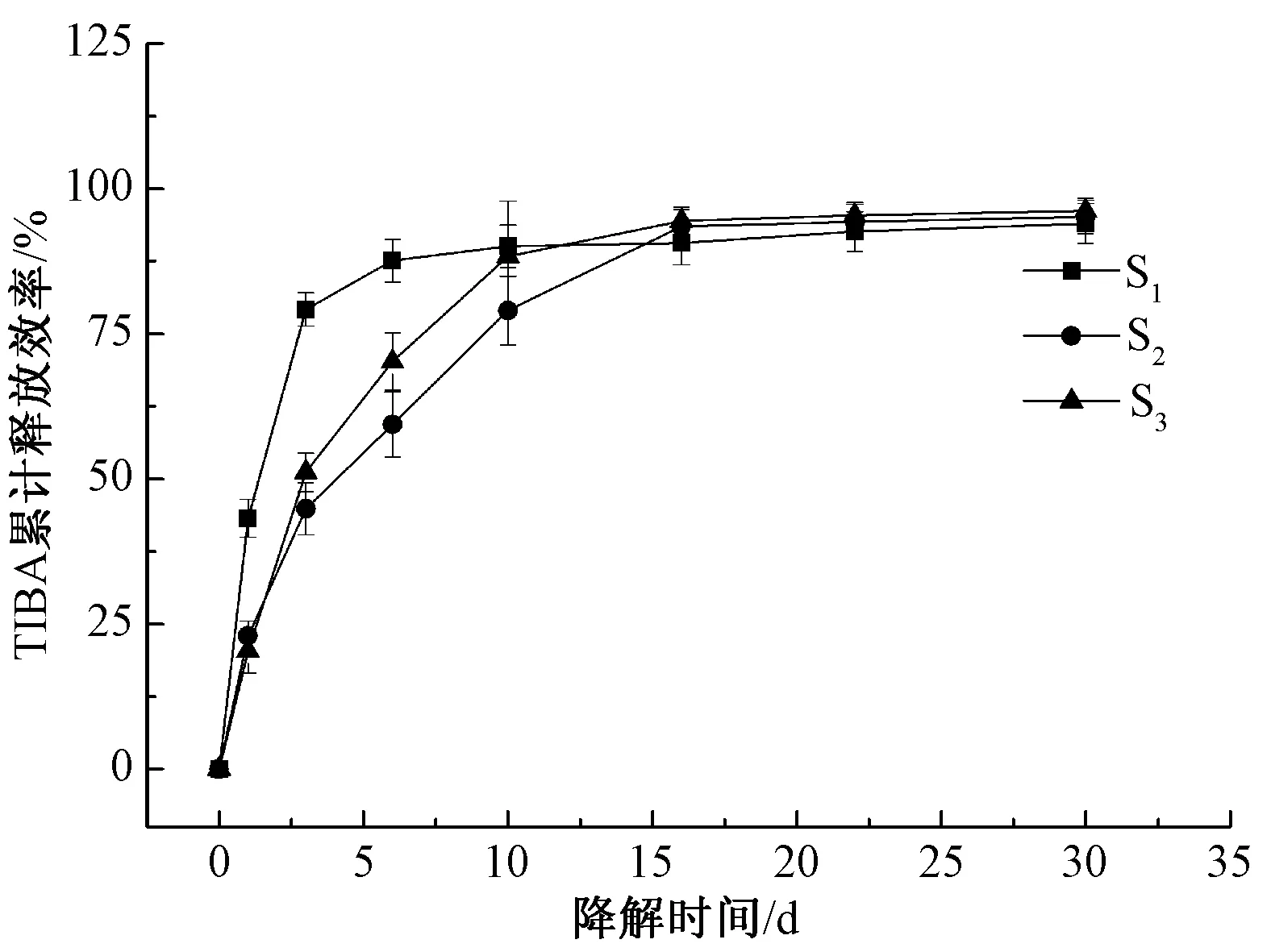
图6 S1、S2和S3 中TIBA的累积释放率Fig.6 Cumulative release ratio of TIBA in S1、S2 and S3
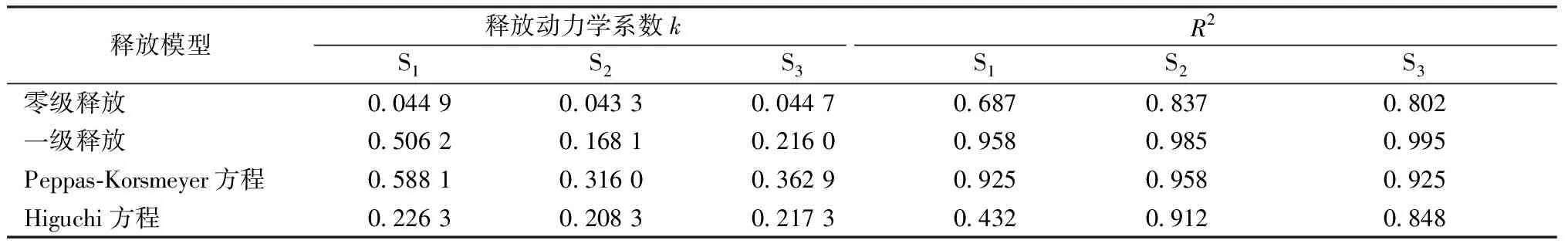
表2 S1、S2和S3中TIBA缓释拟合参数Tab.2 TIBA release fitting parameters in S1、S2 and S3
注:Peppas-Korsmeyer方程中S1,S2和S3的释放动力学系数分别为0.157 2,0.352 7,0.318 5。
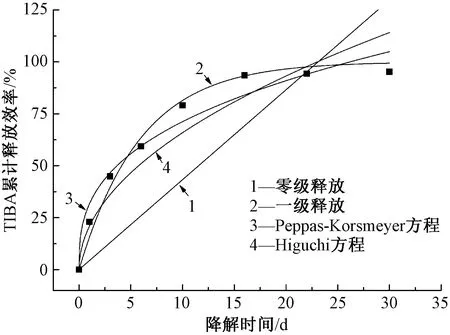
图7 S2中TIBA的累积释放率-时间拟合结果Fig.7 Cumulative release rate-time fitting results of TIBA in S2
S2采用4种释放模型拟合时,R2值分别为0.837、0.985、0.958和0.912,其中一级释放模型的R2值最接近于1。图7示出4种模型的拟合曲线。可以看出,一级释放模型的拟合效果最好,因此认为,一级释放是S2的主要拟合模型。观察图7中的拟合曲线可知,PPDO显影纤维中TIBA的释放主要分为2个阶段,初期的快速释放和后期的缓慢释放,这主要是与共混样品为纤维形态相关。样品为纤维形状,其外周与PBS缓冲溶液的接触面积较大,不断受到溶液的侵蚀,其中的TIBA和PPDO的无定型区易受PBS溶液的侵蚀,从纤维当中释放出来。
3 结 论
1)在PBS缓冲溶液与无水乙醇的体积比分别为1∶3,1∶1和3∶1的3种共混溶液中,以TIBA的质量浓度为自变量、吸光度值为因变量进行线性拟合,均能得到回归关系明显的线性方程,故3个拟合曲线均可用于估算降解液中TIBA的含量。
2)共混液在37 ℃的环境中静置8 d,仍能保证析出TIBA在共混液中保持稳定,并确定最长换液周期为8 d。
3)采用4种药物释放常规模型对TIBA的累计释放量进行拟合发现,其符合一级释放模型。
FZXB
