基于整合药理学的黄芪-三七药对干预ARDS的分子机制研究*
2019-02-16梁旭李雁李昕
梁 旭 李 雁 李 昕
(北京中医药大学东直门医院,北京 100700)
急性呼吸窘迫综合征(ARDS)是临床常见的急危重症,是由多种病因如感染、创伤等导致的以进行性呼吸困难、顽固性低氧血症和肺组织水肿为主要特征的临床综合征[1]。ARDS的治疗目前以保护性机械通气、限制性液体管理等支持治疗和控制原发病为主,临床上多采用糖皮质激素、一氧化氮吸入、肺表面活性物质及对症治疗,但均无可靠的循证医学证据。药物等如β2受体激动剂、他汀类药物和角质形成细胞生长因子虽在动物实验中取得了一定疗效,但并未获得满意的临床效果,且可能出现较严重的临床副作用[2-4]。Meta分析研究表明,中西医结合治疗ARDS在降低病死率等方面优势明显,中药复方具有多靶点治疗疾病的特点,相比单一的阻滞剂可能具有更好的临床优势,对ARDS的防治具有广阔的应用前景[5]。
根据临床表现,ARDS可归属于中医 “暴喘”“肺衰”等范畴。中医学认为肺气虚损,毒瘀互阻,进而导致肺气衰败是ARDS的关键病机[6]。目前,关于中医药治疗ARDS的报道甚少,课题组在前期工作中采用国家级名老中医杜怀棠教授经验方——益气化瘀解毒方,以扶正祛邪为原则,从益气、化瘀、解毒等方面对ARDS模型大鼠进行预防治疗,结果发现益气化瘀解毒方可显著减轻肺组织损伤程度,并可减低炎症因子及关键炎症蛋白的表达水平,但具体的作用机制尚未完全阐明[7-9]。
整合药理学平台(TCMIP,http://www.tcmip.cn/)是整合了中药成分、中药材、中药方剂、疾病/症状靶标等数据的中医药资源信息开源数据库平台,通过建立“中药方剂-化学成分-作用靶标-疾病靶标”的多维网络关联,构建“中药-成分-靶标-通路”复杂网络,为中药复方的作用机制研究提供了新思路[10]。本研究基于整合药理学原理,对课题组前期有效方益气化瘀解毒方中的益气化瘀药对——“黄芪-三七”进行研究,构建其干预ARDS作用机制的分子网络,为深入研究该复方治疗ARDS的机理和进一步阐述ARDS的发病机制提供科学依据。
1 数据来源与方法
1.1 “黄芪-三七”化学成分收集 TCMIP中药材数据库依据《中国药典》(2015年版),收录了400余味常用中药材信息[10]。在其中药信息设定界面对“黄芪”“三七”进行检索并收集其所有化学成分,建立“黄芪-三七”药对化学成分信息数据库。
1.2 ARDS疾病候选靶标收集 在整合药理学平台疾病靶标信息数据检索界面,以急性呼吸窘迫综合征的英文缩写“ARDS”作为关键词进行检索,可收集到疾病靶标数据库中目前已知的ARDS治疗靶点,作为“黄芪-三七”药对的候选治疗靶标。
1.3 靶标预测 TCMIP平台利用Open Babel软件对中药成分进行二维结构相似性检索,通过在中药靶标预测界面选取相似性分数≥0.8的所有药物靶标作为“黄芪-三七”药对的潜在作用靶标,建立药物候选靶标信息数据库[11]。
1.4 蛋白质-蛋白质相互作用信息(PPI) TCMIP整合了 HAPPI、InAct、HPRD、Reactome、OPHID、MINT,PDZ Base,DIP等数据库中蛋白质-蛋白质相互作用信息。通过该平台的PPI数据库,可获得“黄芪-三七”药对作用的潜在靶标与ARDS疾病靶标之间的PPI。
1.5 网络构建与分析 通过网络分析,计算“黄芪-三七”药对潜在靶标与治疗ARDS的疾病靶标之间的PPI信息网络特征值,以节点连接度(degree)的2倍中位数为卡值,选取中药靶标-疾病靶标互作网络的核心节点;在此基础上,以节点连接度、节点紧密度和节点介度的中位数为卡值,选取同时满足3个卡值的节点为“黄芪-三七”药对潜在靶标-ARDS疾病靶标相互作用网络的关键节点[12]。通过基因功能和通路的富集分析,挖掘分析“黄芪-三七”药对治疗ARDS关键网络靶标及其对应的活性成分,并构建 “中药-核心成分-关键靶标-主要通路”的可视化网络图,进一步明确中药干预疾病的作用机制。
1.6 关键靶标分析及通路富集 TCMIP整合基因本体数据库 GO(http://www.gene ontology.org/)和 KEGG通路数据库(http://www.kegg.jp)资源,可直接提取靶标基因或蛋白质的分子功能、细胞内定位及其所参与的生物学反应和通路,对“黄芪-三七”药对干预ARDS的关键作用靶标进行基因功能分析和通路富集分析,并将GO和KEGG计算分析的结果以P值降序的方式排列显示。
2 结 果
2.1 “黄芪-三七”药对化学成分靶标预测及分析 通过TCMIP数据库共收集得到黄芪化合物成分29个,主要为黄芪皂苷类和黄芪多糖类;三七化合物成分95个,主要为三七皂苷、人参皂苷、西洋参皂苷和氨基酸类。研究表明,黄芪甲苷Ⅳ抑制脂多糖(LPS)处理的小鼠中的NF-κB激活和炎性基因表达[13];黄芪多糖通过阻断NF-κB活化抑制TNF-α处理的人血管内皮细胞中ICAM-1和VCAM-1的表达[14];三七中的人参皂苷Rb1可通过减少ICAM-1和ICAM-1基因的表达,改善肺微血管内皮细胞间连接,减轻肺损伤[15]。针对上述成分,共预测出黄芪的潜在作用靶标1 273个,三七的潜在作用靶标626个,经相似性分数≥0.8筛选后,得到黄芪预测靶标185个,三七预测靶标86个,二者共有的靶标71个,提示黄芪和三七在共性靶标之间存在潜在的叠加作用。
对“黄芪-三七”药对候选靶标进行基因分析,取P值排名前20得到候选靶标具有的基因功能信息见表1,可见其功能涉及钠离子通道复合体、突触后膜电位的调节、细胞线粒体功能、电压门控钠通道活性、离子跨膜转运调控、动作电位下的膜去极化、神经元动作电位、心肌细胞膜去极化的调节、肉碱代谢过程、痛觉感觉等条目。对“黄芪-三七”候选靶标进行通路富集分析,取P值排名前20得到候选靶标参与的通路信息见表2,可见涉及通路主要有循环系统、神经系统、PPAR信号通路、内分泌系统、过氧化物酶体、脂质代谢、心肌细胞肾上腺素能信号转导、辅助因子和维生素的代谢、脂肪酸代谢、甘油磷脂代谢、半乳糖代谢、α-亚麻酸代谢等。

表1 “黄芪-三七”药对候选靶标具有的功能信息
2.2 “黄芪-三七”药对治疗ARDS的核心靶标网络通过TCMIP的PPI相互作用数据库,构建 “黄芪-三七”药对的潜在靶标与疾病靶标相互作用网络。根据条件筛选出关键靶标655个,根据degree排序仅显示排名前100的靶点,得到“黄芪-三七”治疗ARDS的候选靶标网络,见图1。图中节点的大小与degree成正比关系,其中已知治疗ARDS的直接靶标78个,潜在药物靶标3个,共同靶标2个。根据比较网络中每条边的介度值,发现TSC1、NSDHL、PIK3R1等靶标的节点介度值更大,在网络中发挥的作用也更大。

表2 “黄芪-三七”药对候选靶标参与的通路信息

图1 “黄芪-三七”药对干预ARDS的候选靶标网络
以上关键靶标中,部分已知疾病靶标如:前列腺素G/H合成酶2(PTGS2)主要与炎症反应的调节、一氧化氮生物合成过程的正调节、NF-κB进入细胞核的正向调节、对肿瘤坏死因子的反应、炎症细胞迁移的正调节、血管内皮生长因子生成的正调控、血小板衍生生长因子产生的正调节、细胞对流体剪切应力的反应、细胞对缺氧的反应、细胞周期的负向调控;丝氨酸/苏氨酸-蛋白激酶A-Raf(ARAF)功能涉及ATP结合、蛋白激酶活性、受体信号传导蛋白质活性、金属离子结合等;丝氨酸/苏氨酸蛋白磷酸酶PP1-γ催化亚基(PPP1CC)与有丝分裂细胞周期、转化生长因子β受体信号通路、小GTP酶介导的信号转导、蛋白质去磷酸化、细胞分裂、三酰甘油分解代谢过程相关。潜在药物靶标:钠/钾转运ATP酶亚基α-1(ATP1A1)功能主要与ATP结合、磷酸酶活性、钠钾离子结合相关;过氧化物酶体肉毒碱O-辛酰基转移酶 (CROT)功能主要涉及脂肪酸β-氧化、细胞脂质代谢过程、辅酶A代谢过程产生前体代谢物和能量等;肉碱O-棕榈酰转移酶1(CPT1A),主要与细胞脂质代谢、蛋白质同源寡聚化、脂肪酸β-氧化、上皮细胞分化等功能相关。共同靶标2个:葡萄糖激酶(GCK),功能主要涉及ATP结合及葡萄糖的结合;丝氨酸/苏氨酸蛋白激酶D1(YWHAE),功能主要与离子通道结合、蛋白质活性、MHCⅡ类蛋白质复合物结合、酶结合、RNA结合、ATP结合、蛋白激酶C活性等相关。
ARDS的发病机制较为复杂,其肺损伤过程涉及多个病理环节的不同分子作用过程。上述靶标涉及诸多生理病理分子机制,主要与炎症反应的调节、血管内皮生长因子调节、蛋白质相互作用及代谢、细胞生长和死亡、信号因子的正负调节等相关,这不仅说明了ARDS的发病机制复杂,同时说明“黄芪-三七”药对干预ARDS的作用主要是通过对炎症反应-血管内皮功能-细胞生长及死亡的多靶点、网络状的综合调控而实现。
2.3 “黄芪-三七”药对治疗ARDS关键靶标的GO基因功能分析 “黄芪-三七”药物靶标与疾病靶标基因功能主要涉及细胞质代谢、蛋白质结合、细胞核核质、血小板活化、ATP结合、蛋白质磷酸化、转录模板DNA的正向调控、蛋白丝氨酸/苏氨酸激酶活性、RNA聚合酶Ⅱ启动子转录的正向调控、蛋白激酶结合及活性、有丝分裂细胞周期的G2/M转换、凋亡过程的负调控、肽基丝氨酸磷酸化等,见表3。
2.4 “黄芪-三七”药对治疗ARDS的KEGG通路富集分析 根据P值排序仅显示排名前20的KEGG通路,见表4。通路富集分析结果显示,“黄芪-三七”药对治疗ARDS的主要作用通路有细胞生长与死亡、ErbB信号通路、FoxO信号转导通路、神经营养因子信号转导通路、细胞间通讯、癌症信号通路、细胞周期、内分泌系统、胰腺癌、传染性疾病、甲状腺激素信号通路、前列腺癌、HTLV-Ⅰ感染等。
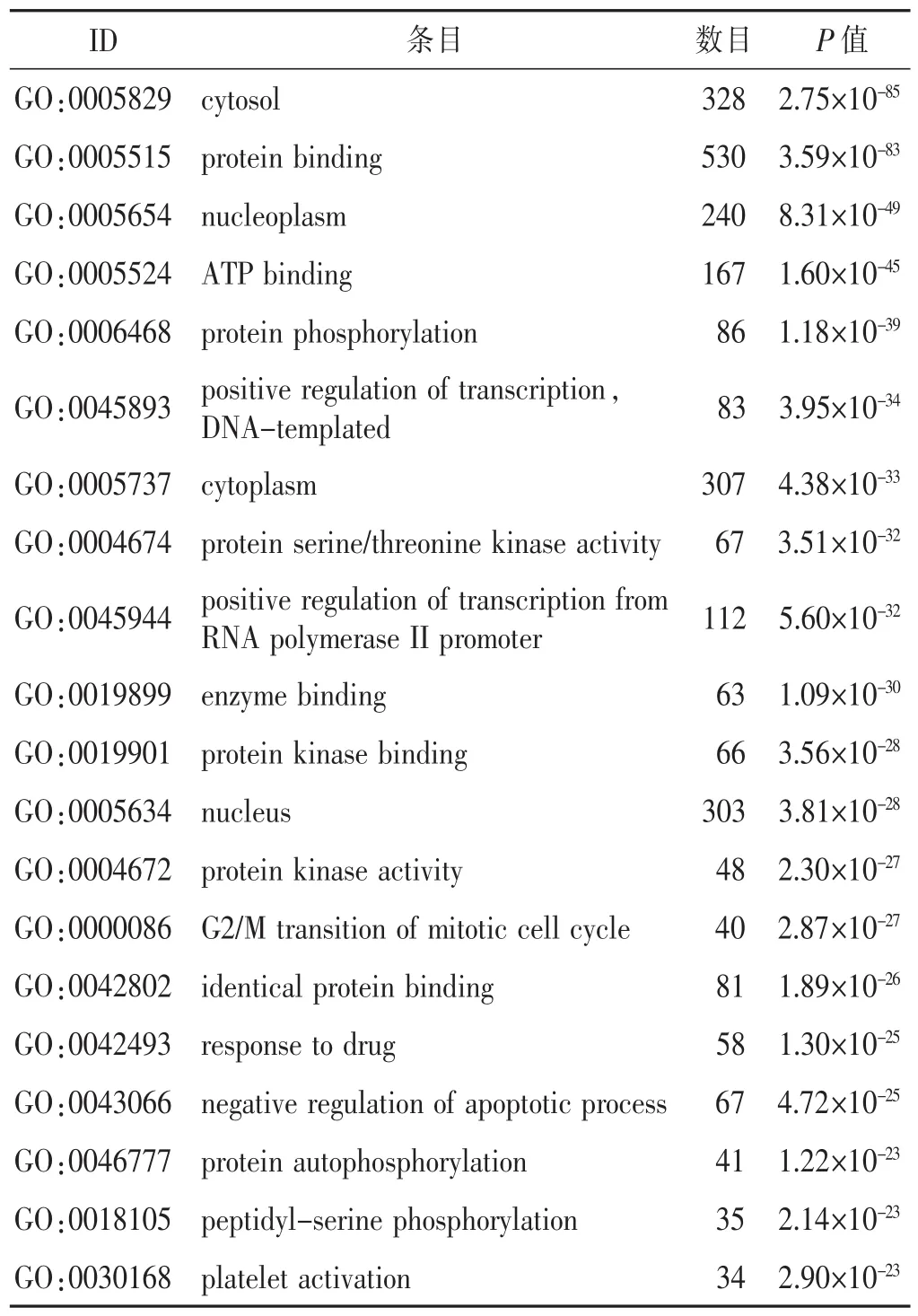
表3 “黄芪-三七”药对治疗ARDS关键靶标基因信息功能分析

表4 “黄芪-三七”药对治疗ARDS关键靶标通路信息
2.5 “黄芪-三七”药对治疗ARDS的“中药-成分-靶标-通路”多维网络分析 如图2。通过TCMIP数据库分析可以看出,“黄芪-三七”药对治疗ARDS作用主要与52个化学成分相关联,其中黄芪成分17个,三七成分34个,共有成分1个。黄芪成分以黄芪皂苷和黄芪苷为主,如黄芪皂苷Ⅰ、Ⅱ、Ⅲ、Ⅳ、Ⅴ、Ⅵ、Ⅶ等;三七主要成分以三七皂苷为主, 如三七皂苷 A、B、C、D、E、F、G、H、R1、R4,人参皂苷 Rc、Rg1,西洋参皂苷Ⅰ、Ⅲ、Ⅳ等。共有成分为十六烷酸(棕榈酸)。

图2 “黄芪-三七”药对干预ARDS“中药-成分-靶标-通路”多维网络分析
其中,黄芪皂苷、三七皂苷、人参皂苷均已通过实验证实具备减轻急性肺损伤(ALI)的药理作用。张吉等发现黄芪甲苷可能通过抑制GRP78和CHOP蛋白表达调控内质网应激状态,改善急性肺损伤状态[16];赵建军等观察到黄芪甲苷能上调LPS致ALI大鼠肺水通道蛋白5的表达从而减轻LPS致ALI大鼠肺炎症损伤反应[17];徐旭等发现黄芪皂苷可显著延长电刺激大鼠颈总动脉形成血栓的时间,并能抑制血小板聚集,提高前列环素和一氧化氮(NO)水平,降低血栓素A2/前列环素比例,从而抗血栓形成[18];刘永琦、李金田等发现黄芪皂苷调节Th1/Th2型细胞因子的平衡及TNF-α含量可能是其抗肺纤维化的机理之一[19];陈宇清等发现,三七总皂苷可以明显降低ALI大鼠的血清和BALF中的TNF-α、IL-6及-IL-10水平,有助于减缓或阻止ALI向ARDS发展[20]。人参皂苷具有扩张血管、改善微循环、抑制血小板的聚集,促进血管内皮细胞功能的恢复,调节血管活性物质,抗氧化、改善微循环、清除氧自由基、诱导细胞凋亡、抗组织损伤、抗肿瘤等药理作用[21]。巩秀丽研究发现,人参皂苷液可减缓ALI大鼠的呼吸窘迫程度,改善肺通气和减轻肺水肿,通过抑制大鼠肺组织中 SP-A蛋白和SP-B蛋白含量的降低来治疗 ALI[22]。
“黄芪-三七”药对作用于ARDS的相关通路主要有MAPK信号通路、PI3K-Akt信号通路、ErbB信号通路、FoxO信号转导通路、细胞生长及死亡、非小细胞型肺癌、细胞循环、细胞通讯、内分泌系统、神经营养因子信号通路、感染性疾病、HTLV-1感染、结直肠癌、胰腺癌、甲状腺激素信号通路、雌激素信号通路等。
其中丝裂原活化蛋白激酶(MAPK)信号通路与各种细胞功能相关,包括细胞增殖,分化和迁移[23]。正常表达的MAPK相关蛋白分子包括细胞外信号相关激酶 (ERK)、Jun 氨基末端激酶 (JK1/2/3)、p38 蛋白和ERK5,IL-8可通过MAPK和PI3K信号通路诱发细胞趋化作用所需的黏附分子如整合蛋白MAC-1的表达。MAPK通路及PI3K通路亦可通过G蛋白等分子相联通[24]。
磷脂酰肌醇3′-激酶(PI3K)-Akt信号传导通路可被多种类型的细胞刺激或毒性损伤激活,主要与细胞转录、翻译、增殖、生长和存活等相关,参与细胞凋亡、蛋白质合成与代谢等细胞周期过程[25]。
ErbB受体酪氨酸激酶(RTK)家族将细胞外生长因子配体与细胞内信号通路结合,调节多种生物反应,包括增殖、分化、细胞运动和存活[26]。RTK家族成员之一表皮生长因子受体(EGFR,也称为ErbB-1或HER1),可诱导受体同源二聚体和异二聚体的形成以及内在激酶结构域的激活,进而诱导各种信号传导途径[27]。MAPK途径是所有ErbB受体下游的共同靶标,同时PI3K途径可被大多数ErbB直接或间接激活。
FoxO信号转导通路参与调节细胞生理过程中特定基因的表达,包括细胞凋亡,细胞周期控制,葡萄糖代谢,抗氧化应激等[28]。FoxO蛋白的中心调节机制与胰岛素、生长因子及PI3K下游的丝氨酸-苏氨酸激酶Akt/蛋白激酶 B(Akt/PKB)的磷酸化相关[29]。
以上信号通路之间通过ERK、Akt等关键蛋白相互联系沟通,形成了ARDS发病过程中的复杂分子通路,通过对 “中药-成分-靶标-通路”多维网络分析,发现“黄芪-三七”药对成分在干预ARDS病程进展中发挥了重要作用,其调控炎症反应、抗细胞凋亡及保护肺血管内皮细胞的分子机制与课题组前期实验结果具有很高的吻合度[7-9]。
3 结 论
网络药理学注重整体性和动态性的特点,与中药复方注重多组分配伍、多靶点干预及系统调控的思想不谋而合[30]。TCMIP结合大数据和模型计算,应用人工智能、数据挖掘、网络科学构建了智能化和网络化平台,为中药复方及经方药对的研究提供了新思路和新方法。
益气化瘀解毒方在防治ARDS的前期动物实验中作用明显,“黄芪-三七”作为益气化瘀核心药对作用突出,本研究通过网络药理学研究技术,发现“黄芪-三七”药对主要活性成分可针对多个靶点、多条通路发挥干预ARDS的作用,其作用可能与 TSC1、NSDHL、PIK3R1等关键靶标及MAPK信号通路、PI3K-Akt信号通路、ErbB信号通路、FoxO信号转导通路等有关,这些靶点及通路与文献报道的急性肺损伤的发病机制及课题组的前期研究成果多有吻合。本研究是基于网络药理学原理的综合数据分析,具体机制及物质基础还将通过实验加以验证,望本研究能够为复方核心药对的进一步研究及ARDS的临床治疗提供参考。本研究表明,“黄芪-三七”药对可通过多靶点、多途径干预ARDS,为其进一步的药效物质基础分析和防治作用机制研究提供了依据。
