基于知识图谱的国内外真实世界研究演进与比较*
2019-02-15李立伟徐梦丹姜顺军喻鹏久
李立伟 徐梦丹 魏 理 姜顺军 喻鹏久
真实世界研究(real-world study,RWS)也叫比较效果研究,起源于实用性临床试验(practical trial),是一种新兴的研究理念[1]。随着信息技术的不断进步,在政产学研医共同需求的驱动下,RWS得到快速的发展,并逐渐成为药品上市后评价研究的重要方式之一。2016年12月7日,美国国会批准通过《21世纪治愈法案》(21st Century Cure Act,21CCA),从政策面肯定了RWS的价值与意义;欧洲卫生技术评估(health technology assessment,HTA)机构,如英国、法国、德国等HTA机构,已广泛认可真实世界证据(real-world evidence,RWE)在确定新药价值方面的重要性[2],政策激励为RWS的成熟奠定了良好的基础。国内学者对中国期刊全文数据库中2001年~2016年收录的137篇真实世界临床应用的文献进行计量学分析,得出近些年国内相关研究正快速发展的结论[3]。本文在进一步扩展文献分析范围和时间跨度的基础上,综合比较2000年1月至今国内外RWS领域演进及知识基础,以期为国内RWS研究提供借鉴和参考。
1 研究方法与数据来源
1.1 研究方法
科学知识图谱以科学知识计量为研究对象,是表征科学知识发展进程和结构关系的一种图像[4]。本文运用CiteSpace知识图谱绘制工具[5-6],通过综述国内外RWS领域经典文献的主要内容,定性分析RWS的知识基础;通过绘制关键词聚类图谱、引证文献图谱、合作作者图谱以及关键词分布时序图谱等,定量分析国内外RWS研究热点和前沿趋势。
1.2 数据来源
本文基于Web of Science(WOS)核心合集数据库和中国期刊全文数据库,经人工阅读标题与摘要,排除报纸、征文通知、会议通知及与研究无关的文献后,中国期刊全文数据库共获得288篇,WOS数据库获得1 072篇相关文献。见表1。

表1 数据来源
2 研究热点分析
2.1 国际RWS领域热点分析
关键词是一篇文章中最能体现主题特征和核心内容的短语或词组,一个研究领域在一定时期内关键词的集合,可以揭示该领域在特定时期的总体内容特征和发展脉络[7]。在CiteSpace生成的知识图谱中,具有紫色外框的年轮状同心圆通常被认为是研究方向发生转变或引起大量学者关注的“突现”节点,需重点分析[8]。从知识领域的角度看,频次和中心度较高的关键词,为该时期内被研究者普遍关注的问题,也就是该时期的研究热点。综合考虑关键词出现的频次、中心度和突现性,筛选出排名前20的关键词,见表2和图1。
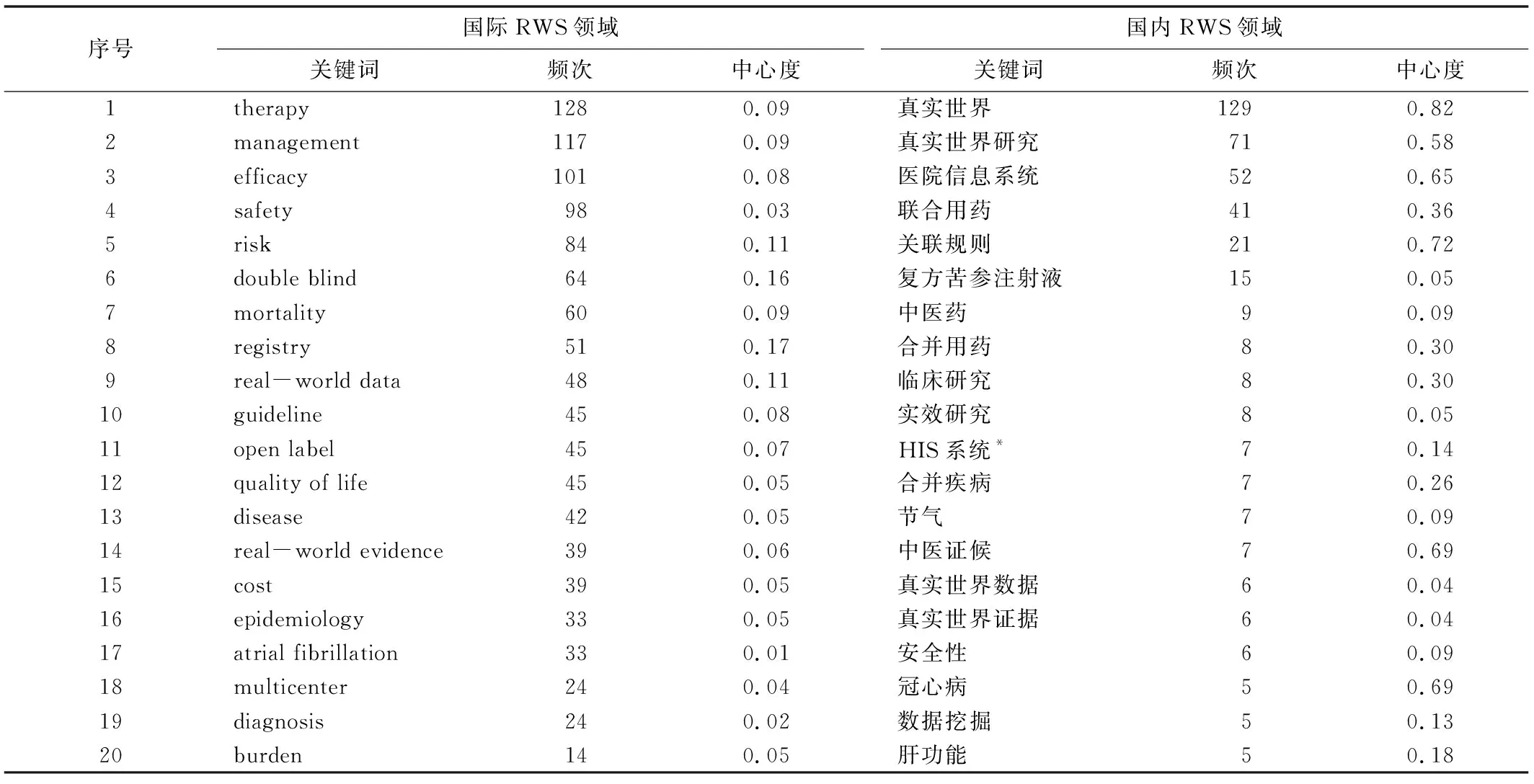
表2 国内外RWS领域高频关键词信息
*注:HIS系统是指医院信息管理系统

图1 国际RWS领域研究热点与关键词知识图谱
结合表2和图1可以看出,国际RWS领域高频关键词主要集中于医药领域的“therapy”、 “management”、“efficacy”、“safety”、“risk”等关键词。热点之间通过多个细分领域相互联系,形成一个多中心的复杂网络。具体来说,国际RWS领域在研究内容方面可概括为以下几个热点:(1)疾病治疗与管理:得益于医疗信息技术的快速发展,全世界范围内特别是西方发达国家现已建立较为完善的各级医疗数据库。与之相适应的研究也逐渐增多,包括疾病发病率、死亡率、影响因素、风险因素、疾病基础诊疗模式、最新诊疗进展、数据库管理、不同治疗措施下患者预后及临床结局研究等。(2)安全性研究:医疗产品上市前研究规模有限,一些罕见的或需长时间观察的不良反应多难以发现;真实世界中联合用药、超说明书用药的安全性问题也难以证实。基于医疗机构、卫生部门、医药企业对医疗产品上市后安全性的刚性需求,药物/医疗器械真实世界安全性评价成为当下研究热点,包括药品新适应症、超剂量用药、联合用药、药品/医疗器械长期用药的安全性评估以及罕见不良事件发生率等细分领域研究。(3)有效性研究: 根据研究对象的不同,真实世界有效性研究包括单一药品或医疗器械的疗效观察、不同药品间比较有效性评价以及药品在RWS与随机对照试验研究的临床有效性比较等。(4)经济学及社会学研究:近些年,医药企业在新药研发与申报时需进一步考虑药物经济性和社会承受性问题,相关研究作为药物定价、医保报销的重要凭证而引起重视,研究包括疾病成本分析、疾病药物经济学负担、成本效果分析、成本效益分析、患者生活质量评价等多个细分领域研究。
2.2 国内RWS研究热点分析
由表2和图2可知,国内RWS领域研究以“真实世界”为中心,围绕“医院信息系统”、“联合用药”、“关联规则”、“中医证侯”等关键词展开,主要为中医药相关研究。根据研究是否使用真实世界数据(real-world data, RWD)具体可概括为以下几个方面:(1)RWS应用分析:相关研究包括对RWS定义、内涵、研究设计的解读,RWS在药物上市后安全性、有效性应用等多方面的解释性分析。(2)中医药上市后评价:相关研究包括药
品疗效评价、联合用药、安全性等细分领域研究。(3)疾病临床特征分析:主要研究包括合并用药、合并疾病、中医证候、节气、疾病风险因素管理等。

图2 国内RWS领域研究热点与关键词知识图谱
3 知识基础研究
3.1 国际RWS领域知识基础
知识基础由一个领域研究前沿的引文所构成,通过对知识基础的分析有助于我们进一步了解该研究前沿的本质[6,9]。本文根据引文频数的高低,确定了6篇国际RWS领域代表性研究文献,见表3和图3。

表3 国际RWS领域高引文频数文献
注:*为RWS领域引用频次

图3 国际RWS领域知识基础图谱
Patel等[10]、Granger等[11]与Connolly等[12]在一项与华法林比较的心房纤颤临床双盲研究中,分别证实Rivaroxaban,Apixaban和Dabigatran在预防缺血性脑卒中和全身血管栓塞性疾病发生方面具有良好的疗效和安全性;Afdhal[13]通过临床试验,证实Ledipasvir联合Sofosbuvir每日一次,连续用药12周~24周对HCV基因Ⅰ型感染患者具有显著的治疗作用;Zinman等[14]评价了Empagliflozin在合并高危心血管疾病的2型糖尿病中应用的安全性;Sherman等[15]从数据利用的角度给出RWE的定义:即“RWE可看作是一种将各类医疗保健信息纳入评价的研究方式”,并指出RWE与传统临床研究不是方法学的差异,而是证据的数据来源上的差异。
3.2 国内RWS领域知识基础
根据引文频数和文献突现性,确定6篇国内RWS领域经典文献,见表4和图4。国内经典文献的主要内容有:刘保延[16]提出“从临床中来到临床中去一体化中医临床科研范式”;庄严等[17]在RWS数据库设计方面进行了探讨;杨薇等[18]提出利用医院HIS系统临床数据和数据挖掘分析技术进行中药上市后安全性评价的科研思路;王连心等[19]采用巢式病例对照研究的分析方法,实证分析了参麦注射液过敏反应的可疑因素;谢雁鸣等[20]从理论分析的角度,提出RWS在中药上市后安全性、有效性评价等方面具有重要的作用;黎元元等[21]实证分析了灯盏细辛注射液临床应用的人群特征和合并用药情况。

表4 国内RWS领域高引文频数文献
注:*为RWS领域引用频次

图4 国内RWS领域合作作者图谱
4 前沿趋势分析
4.1 国际RWS领域前沿趋势
RWS由来已久,当时由于数据收集、处理等技术层面的限制,并未得到广泛的应用。国际上较为典型的大规模的RWS设计要始于1999年马萨诸塞大学医学院发起的急性冠脉事件全球注册研究(global registry of acute coronary events,GRACE)以及Fox[22]和Cazzoletti等[23]根据全球哮喘防治建议指南,在1999年~2002年针对欧洲呼吸疾病健康调查开展的随访性研究。2005年~2007年,RWS主要基于注册登记数据,开展疾病风险因素调查和临床结局分析,同时期药物真实世界有效性得到关注;2008年~2012年,“therapy”、“management”、“safety”等关键词突现,RWS进一步扩展到药物或医疗器械安全性、疾病管理、患者生活质量评价等新的研究领域。2013年~2016年,随着美国卫生信息化战略规划及精准医疗计划的阶段性完成,美国掀起RWS浪潮,RWS进入快速发展期,RWD在临床应用中的重要价值得到重视,有关RWD的应用研究显著增多。进入2016年,随着21CCA的正式颁布,“real-world evidence”成为突现词,RWS正式进入以“RWE”为核心的“新循证”时代。未来基于大病例数据库的医疗产品风险效益研究以及疾病预防、风险预警等大数据应用研究有望成为新的研究热点。见图5。
4.2 国内RWS领域前沿趋势
我国早在1984年便开展了冠心病介入治疗的注册登记研究[24],但直到2002年霍勇[25]“伴随循证医学走入真实世界——GRACE研究给我们的提示”一文中才正式提出循证医学与真实世界结合推动临床研究发展的论断。2010年~2011年,“数据挖掘”、“关联规则”等关键词突现,大数据分析技术在RWS领域的应用研究成为热点;2012年~2015年,随着我国多个品种的中药注射剂上市后真实世界安全性评价研究的完成,“医院信息系统”、“联合用药”、“中医证侯”等关键词突现,中医药临床评价成为该时期研究热点;2016年~2018年,受美国关于药品新适应症审批制度改革的影响,“疗效评价”、“安全性”、“真实世界数据”、“RWE”等成为新的研究热点。见图6。

图5 国际RWS领域热点趋势时序图知识图谱
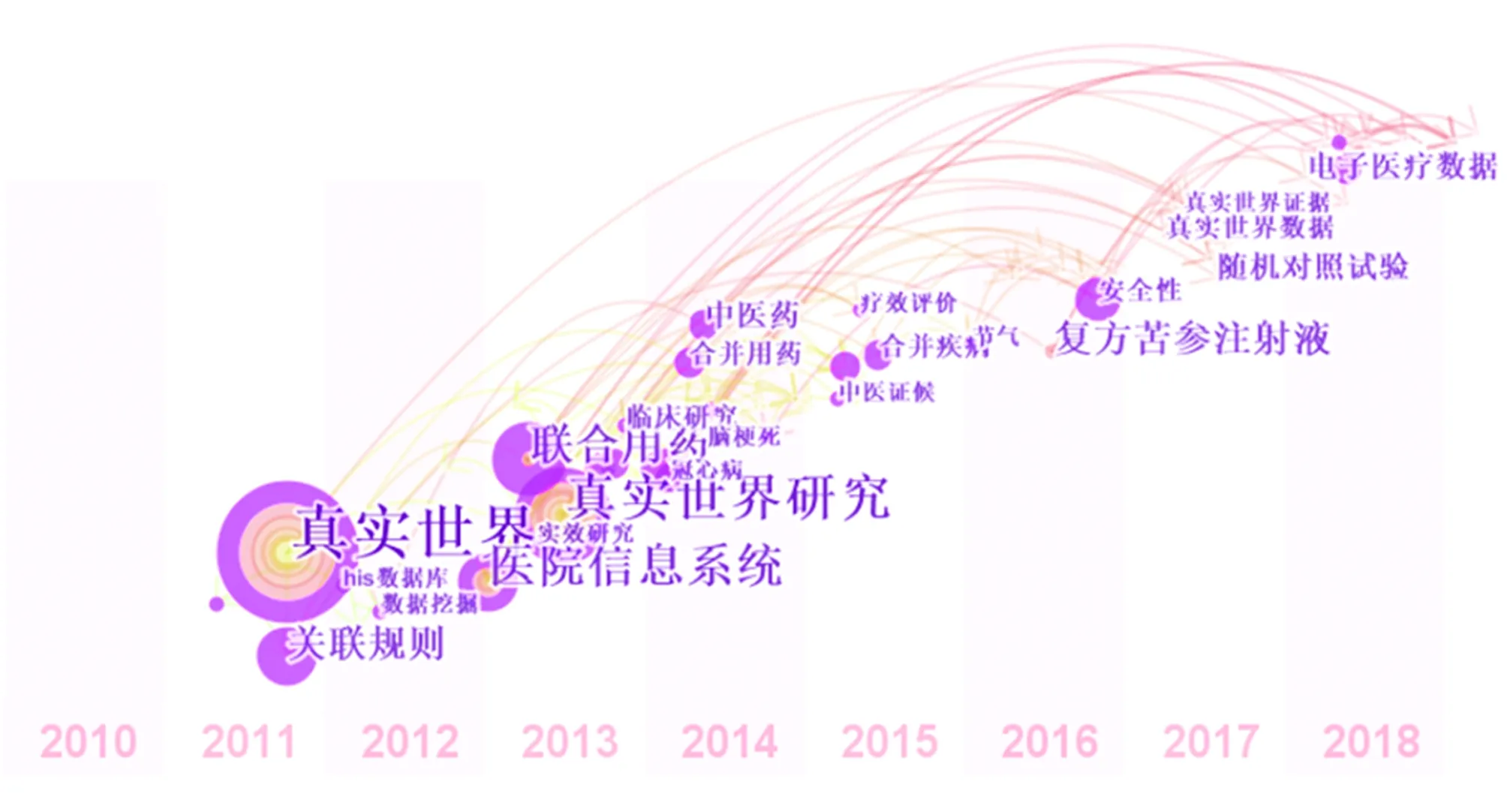
图6 国内RWS领域热点趋势时序图知识图谱
5 讨论与分析
在传统临床研究费用大幅增长,而医疗卫生决策证据并未相应增加的大背景下,随着世界范围内医学事业的快速发展、信息技术的不断进步,RWS成为医疗卫生领域持续关注的焦点[15,26]。
从研究热点来看,国际RWS领域研究热点覆盖面广,细分领域的研究较多,以应用性研究为主的研究体系正日趋完善;国内RWS热点较为单一,主要集中在对真实世界概念分析和中医药临床用药分析等方面。与国际研究相比,国内药品上市后的经济学和社会学评价研究尚未形成热点,有关药物有效性的研究也多停留于理论分析层面,已开展RWS的医药品种也较为匮乏。
从知识基础来看,国际RWS领域知识基础主要为药品上市前大型随机对照试验临床研究和RWE指南等;国内RWS领域知识基础以中医药研究的试验方案和数据库设计、上市后安全性研究等为主。与国际研究相比,国内RWS领域研究较多关注于基础层面设计,而决策参考层面的RWE应用研究还有待深入。
从热点趋势来看,国际RWS在明确的政策刺激和较为完善的医疗信息建设下,正形成以RWE挖掘为主导的研究模式;国内RWS研究近些年发展迅猛,随着我国 “建设符合国际标准的审评体系”的不断深入,加快RWD在药品上市后再评价方面的应用研究有望成为主旋律。与国外相比,我国在RWD的应用方面是远远不足和相对落后的,这可能与国内医院信息系统数据分散、异质性高、应用环境相对封闭紧密有关。
基于以上分析,为促进我国RWS更快更好的发展,提出以下建议:(1)应加快国内真实世界大数据平台建设,如建立大规模的分布式研究网络(类似于美国食品药品监督管理局发起的“迷你哨点研究”)和可分析型病例报告表(case report form, CRF)数据库等,促进医疗数据的有效应用,为RWS奠定基础;(2)欧美等国家已在政策面普遍认可RWS的价值[2,15],我国在2017年6月被人用药品注册技术要求国际协调会议(International Council for Harmonization,ICH)接纳为ICH监督会员(regulatory member),正致力于建立明确、统一的符合国际标准的审评技术体系。 在这种形势下,国家医药卫生部门也应在政策层面对RWS在药物安全性、经济性评价中的应用给予支持和引导,如加快完善RWS相关评价标准的制订,为RWS发展排除障碍;(3)政、产、学、研、医在RWS中应充分利用自身优势,精准定位,寻找各自利益诉求的结合点,形成合力、协同发展,为RWS注入不竭动力。
