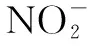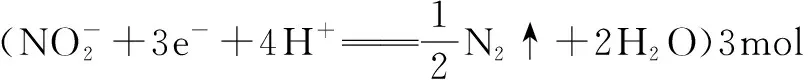电解质溶液中粒子的定向运动问题探析
2019-02-15刘宇
刘 宇
(四川省泸县二中 646106)
电池的内电路由电解质或者熔融电解质充当,在放电过程中,电解质体系中由于粒子在电极上放电,导致电极区域的离子浓度发生变化,为平衡区域电荷守恒,电解质溶液中的粒子通过定向运动解决问题.
一、粒子运动的定性分析
例1 一种新型燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-.下列对该燃料电池说法正确的是( ).
A.在熔融电解质中,O2-由负极移向正极
B.电池的总反应是:2C4H10+13O2→8CO2+10H2O
C.通入空气的一极是正极,电极反应为:O2+2H2O+4e-=4OH-
D.通入丁烷的一极是负极,电极反应为:C4H10+13O2-+26e-=4CO2+5H2O
答案 B

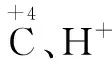
例2 碱性硼化钒(VB2)一空气电池工作时反应为:4VB2+11O2=4B2O3+2V2O5.用该电池为电源,选用情性电极电解硫酸铜溶液,实验装置如图1所示.下列说法正确的是( ).
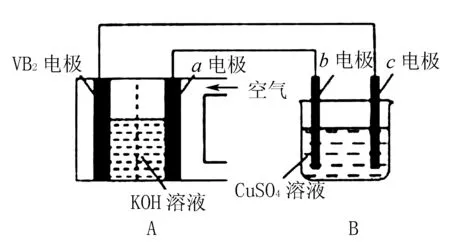
图1
A.VB2电极的电极反应式为:

B.外电路中电子由c电极流向VB2电极
C.电解过程中SO42-向b电极移动
D.电解过程中,b电极表面有红色物质析出
答案 C

方法技巧电极反应也属于化学反应,因此在书写时需要关注电解质溶液环境,本题原电池电解质溶液为碱性,因此生成的H+还能发生后续反应被消耗;电极反应过程会使电解质溶液区域电荷不守恒导致粒子的定向运动,但粒子运动不是为了在电极放电.
例3 据报道,以硼氢化合物NaBH4(硼元素的化合价为+3价)和H2O2作原料的燃料电池,负极材料采用Pt/C,正极材料采用MnO2,可用作空军通信卫星电源,其工作原理如图2所示.下列说法正确的是( ).
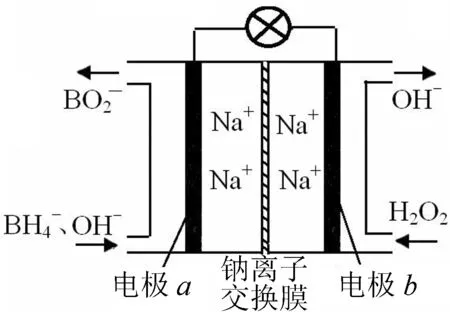
图2
A.电池放电时Na+从a极区移向b极区
B.每消耗3 mol H2O2,转移的电子为3 mol
C.电极a采用MnO2,MnO2既作电极材料又有催化作用
答案:A
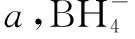
能力提升电极放电导致区域电荷不守恒,可通过粒子的定向运动平衡电荷,本题电极a阴离子减少,可通过Na+移向b极区,或者OH-移向a极区平衡电荷,但是在钠离子交换膜使用下,只能Na+选择性的作定向运动.
二、粒子运动的定量分析


B.放电时,交换膜右侧溶液中有大量白色沉淀生成
C.若用NaCl溶液代替盐酸,则电池总反应随之改变
D.当电路中转移0.01 mol e-时,交换膜左侧溶液中约减少0.02 mol离子
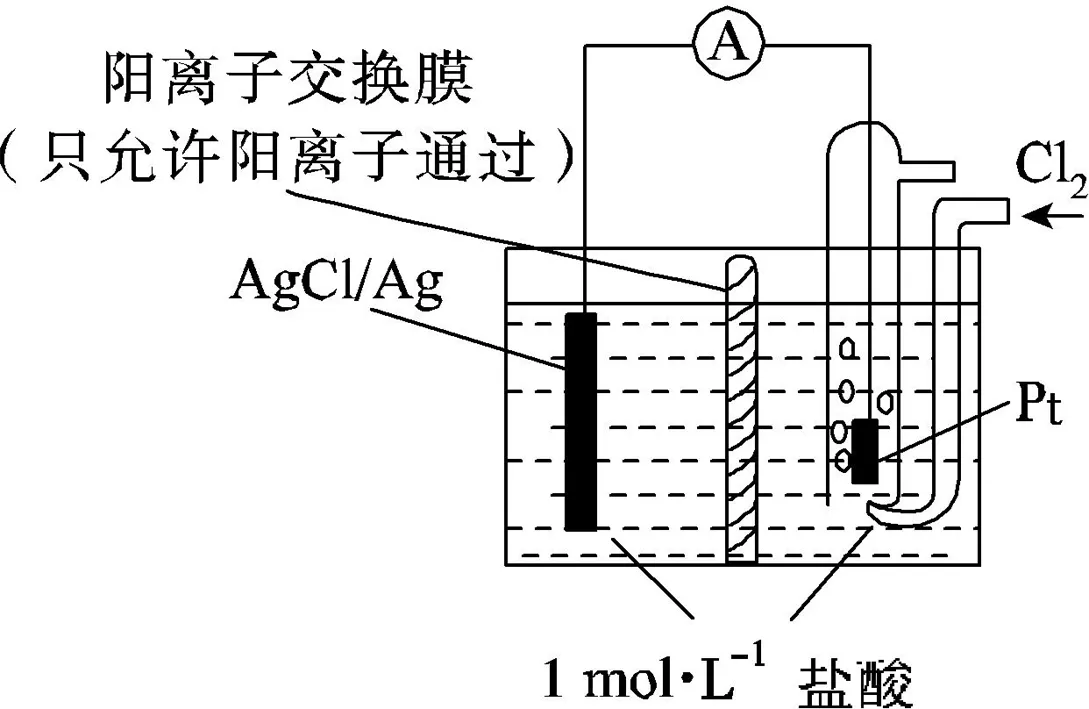
图3
答案:D

误区警示在电解质溶液中,由于电极反应的发生,可能使得电极区域的离子浓度发生变化,放电后溶液中的阴阳离子分别进行定向运动以维持区域的电中性原理,在隔膜情况下,限定了阴离子(或阳离子),甚至特定离子通过隔膜,因此放电实质反应能接触到的离子发生变化,连带反应发生变化.
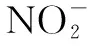
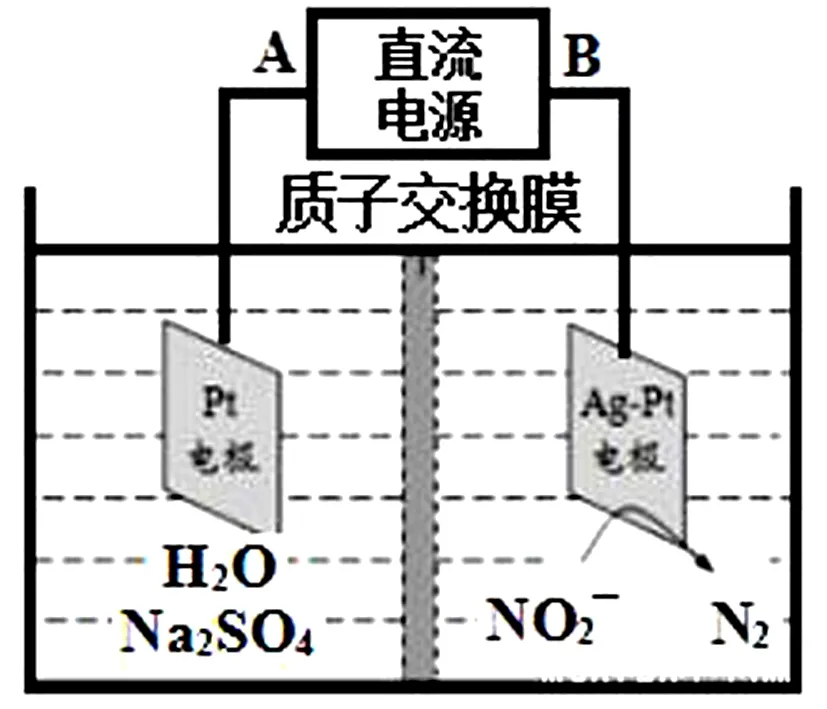
图4
①电源的正极是____(填A或B),阴极反应式为____.
②若电解过程中转移了3 mol电子,则膜两侧电解液的质量变化差|Δm左|-|Δm右|为____g.
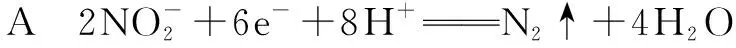
②16