吡唑并嘧啶衍生物对微生物的影响
2019-02-15饶国武
许 芬,饶国武
(浙江工业大学药学院,浙江 杭州 310014)
0 前言
化学家在二十世纪50年代中期研究了作为嘌呤类似物的吡唑并嘧啶,据报道它具有各种生物活性。1955年,化学家Howard E.Skipper等人首次探索了吡唑并嘧啶类化合物的抗肿瘤活性[1],并深入研究了吡唑并嘧啶类化合物,引起了各国化学家的广泛兴趣。据文献[2-3],吡唑并嘧啶具有良好的物理性质,光学和生理活性以及高反应性,并能与各种试剂发生化学反应,因此具有广阔的前景。
寄生虫(parasite)是指具有致病性的低等真核生物,可作为病原体,也可作为媒介传播疾病。寄生虫特征为在宿主或寄主(host)体内或附着于体外以获取维持其生存、发育或者繁殖所需的营养或者庇护的一切生物。许多小动物以寄生的方式生存,依附在比它们更大的动物身上。
寄生虫可以改变寄主的行为,以达到自身更好地繁殖生存的目的。人类若受到一些寄生在脑部的寄生虫,如终生寄生在脑部的弓形虫(Toxoplasmosis),其反应能力会降低。
病菌是引起人类疾病的细菌和病毒,统称为病原菌或致病菌(pathogenic bacterium)。细菌在人体内寄生,增殖并引起疾病的特性称为细菌的致病性或病原性(pathogenicity)。致病性是细菌种的特征之一,具有质的概念,如鼠疫细菌引起鼠疫,结核杆菌引起结核。致病性强弱程度以毒力(virulence)表示,是量的概念。
革兰氏阳性和革兰氏阴性病原体,例如金黄色葡萄球菌(Staphylococcus aureus)、酿脓葡萄球菌(Staphylococcus pyogenes)、鼠伤寒沙门氏菌和大肠杆菌引起食物中毒,风湿热,沙门氏菌病,腹泻等许多传染病。这些在全球都是严重的健康问题。全球有百万人受到感染,每年因这些细菌感染死亡达到15万人[4]。
在抗生素使用前的时代,轻微的伤害和常见的感染可能会导致危及生命的疾病。20世纪最伟大的成就之一是抗生素的发现,它显著改善了生活质量,彻底改变了现代医学[5-7]。
1 吡唑并嘧啶衍生物的抗菌作用
细菌对传统抗生素如青霉素和四环素的耐药性迅速增加,这促使人们继续寻找具有新型抗菌活性的新型化合物。吡唑并嘧啶是一类重要的化合物,吸引了化学家的注意,因为化学治疗药物,如抗菌药物,抗病毒药物和细胞毒性药物的性质都有很好的文献记载。吡唑并嘧啶和相关杂环在药物化学中具有广泛的重要药效团和特殊结构。据文献调查显示,吡唑并嘧啶衍生物具有多种药理活性,如CNS抑制剂,精神安定剂,结核抑制剂,抗高血压药,镇痛剂和抗菌活性。吡唑并[1,5-a]嘧啶构架是[5-6]稠合双环杂环,除了用于各种药理学研究外,已经成为多用途骨架,从它们对多种疾病靶标的效用来看,吡唑并[1,5-a]嘧啶在制备各种药物和生物活性分子方面显示出巨大的合成价值[8]。
1.1 吡唑并[1,5-a]嘧啶的抗菌活性
吡唑并[1,5-a]嘧啶作为嘌呤类似物,其重要性在化学和药理学中都有体现。另一方面,磺酰胺类化合物具有多种生物活性。这促使研究者探索含有磺酰氨基的吡唑并[1,5-a]嘧啶的合成,以筛查其抗菌活性。通过实验表明,大多数这类化合物存在革兰氏阳性菌和革兰氏阴性菌的抗菌活性[9]。
通过琼脂扩散法测定合成化合物1(其合成方法见Scheme 1)的抗微生物活性评价化合物对大肠杆菌(MTCC443)、枯草芽孢杆菌(MTCC441)、金黄色葡萄球菌(MTCC96)和伤寒沙门氏菌的抗菌活性。用抗生素青霉素(25μg/mL)作为抗菌药物和制霉菌素(25μg/mL)作为抗真菌药物的参比药物,使用二甲基亚砜(1%,DMSO)作为无化合物的对照[8]得到实验数据。
1.2 吡唑并[3,4-d]嘧啶类抗菌活性
在使FOL7185作为模板来设计用于用BtIspD和BtIspE测试的许多吡唑并嘧啶类似物时,尽管FOL7185在抑制区测定中对B.thailandensis和铜绿假单胞菌没有显示出可测量的生长抑制,但其许多类似物确实显示出生长抑制。化合物2(其合成方法见Scheme 2)抑制B.thailandensis浓度为0.1 mM (这与卡那霉素相当)。 该化合物还显示出对铜绿假单胞菌多重耐药菌株的可测量的效力,因此证明了跨物种抑制作用和作为广谱抗生素活性的起点的潜力。在STDNMR研究中,化合物2显示与BtIspE的活性位点的显著相互作用,表明这些类似物可以通过破坏类异戊二烯生物合成来抑制细菌生长[7]。
使用纸片扩散法测试化合物3,4和5(Figure 1)对金黄色葡萄球菌ATCC 6538,表皮葡萄球菌ATCC 12228,大肠杆菌 ATCC 8739,绿脓假单胞菌ATCC 1539,以及它们对白色念珠菌ATCC 10231的抗真菌活性,发现化合物3,4和5对抗金黄色葡萄球菌ATCC 6538(分别为MIC:185;78;和 156μg/Ml)和化合物 5对白色念珠菌ATCC 10231 (MIC:312.5 μg/mL)(使用微量稀释法测定这些化合物的最小抑制浓度)[10]。
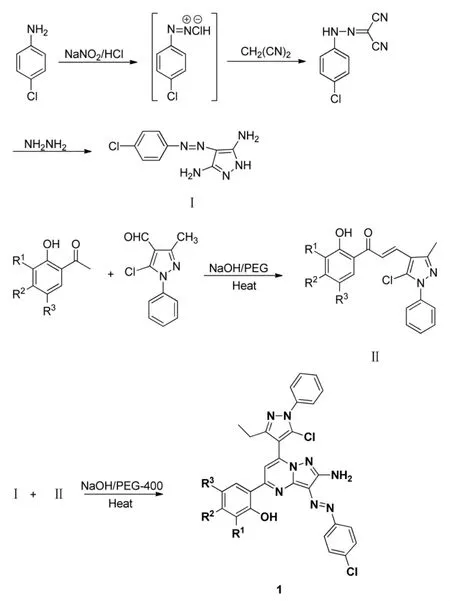
Scheme1 具有抗菌活性的吡唑并[1,5-a]嘧啶衍生物的合成
2 吡唑并嘧啶衍生物抗寄生虫活性
吡唑并嘧啶是嘌呤类似物,其像嘌呤一样被致病性血蝇代谢(该代谢序列在人类或其他哺乳动物中不存在)。别嘌呤醇是由吡唑并嘧啶碱基经历核糖磷酸化为核糖核苷酸产生,该核糖核苷酸可以保持原样或被氨基化成氨基类似物进一步转化成氨基吡唑并嘧啶核糖核苷三磷酸,后者被并入RNA中。该代谢序列已经在利什曼原虫属和锥虫属中得到证明[11]。
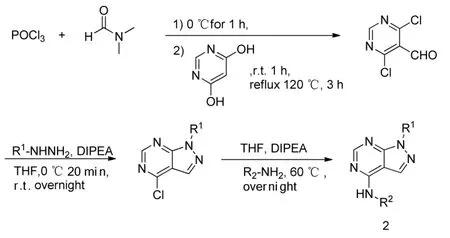
Scheme2 具有抗菌活性的吡唑并[3,4-d]嘧啶衍生物的合成
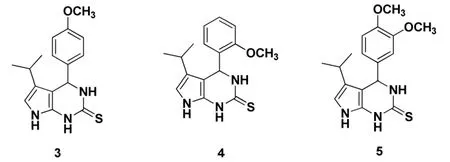
Figure1 具有抗金黄色葡萄球菌和白念珠菌的吡唑并嘧啶衍生物
2.1 某些吡唑并[1,5-a]嘧啶的抗滴虫活性
关于吡唑并[1,5-a]嘧啶的生物学性质的调查研究促使人们探索开发含有稠合硝基吡咯环的抗寄生虫化合物。例如,3-硝基吡唑并 [1,5-a]嘧啶衍生物6(其合成方法见Scheme 3),其中R1为H或C2H5且R2为H或COOC2H5COOH。 然而,研究这些新化合物3-硝基-4,6-二取代吡唑并[1,5-a]嘧啶酮(7, 8, 9 和 10, Figure 2)的所有衍生物的活性结果显示其并非完全缺乏对除滴虫以外的细菌、真菌和寄生虫的活性[12]。
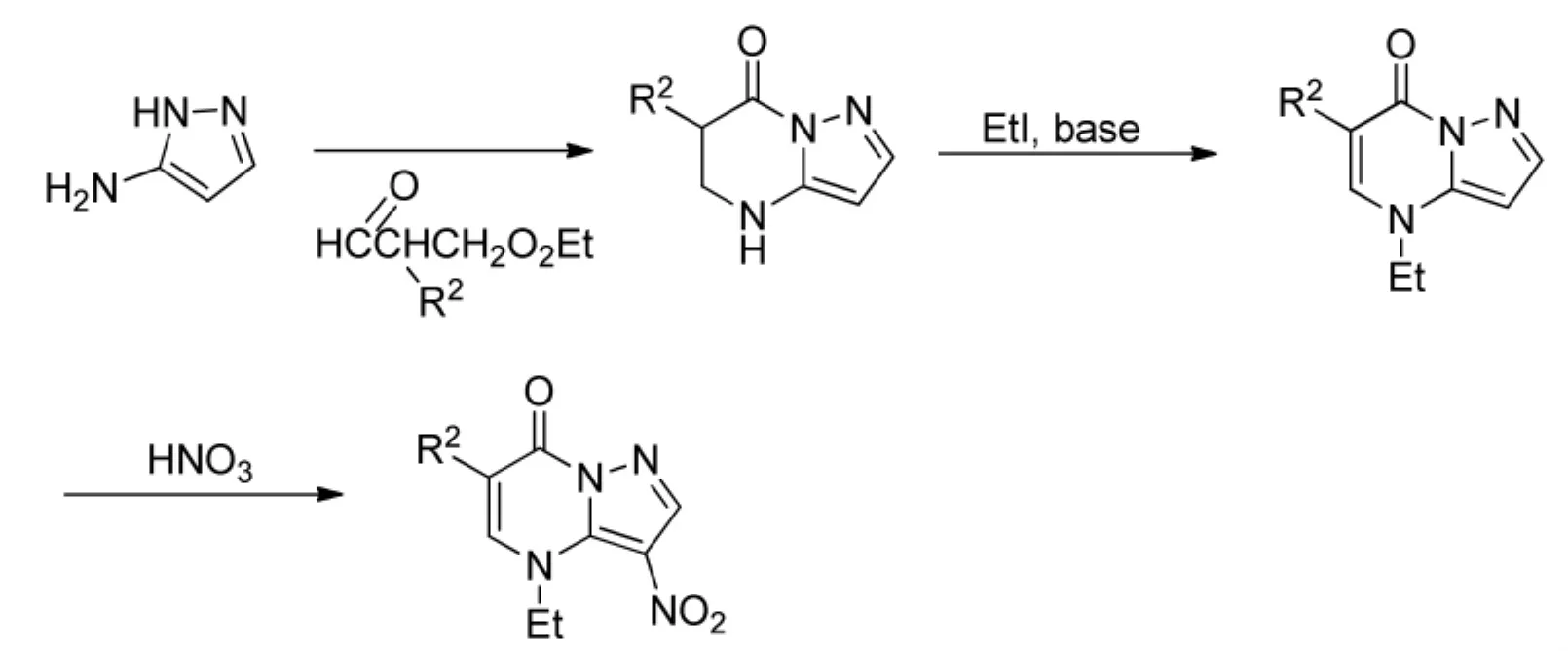
Scheme3 具有抗滴虫活性的吡唑并[1,5-a]嘧啶衍生物的合成
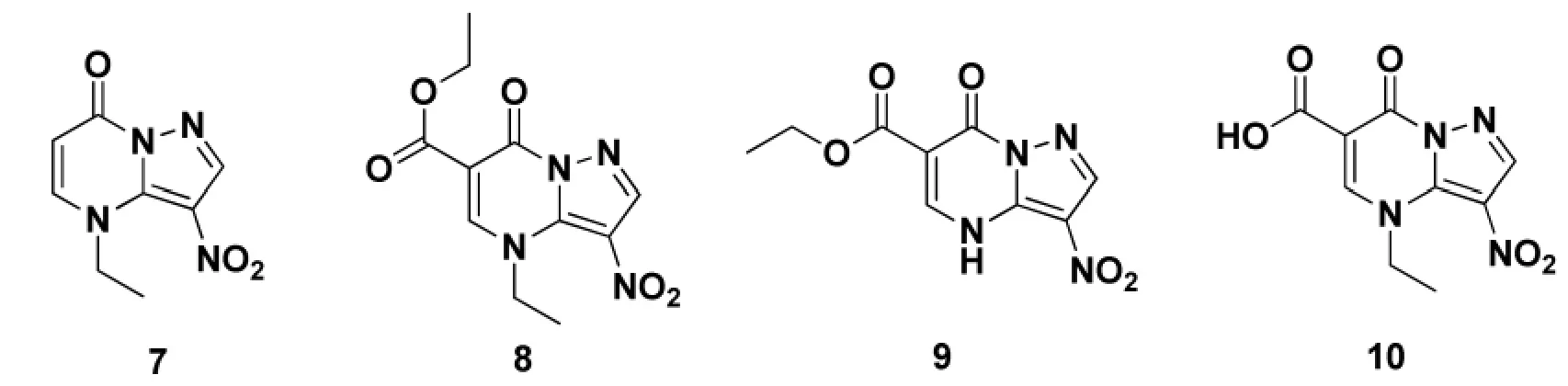
Figure2 3-硝基-4,6-二取代吡唑并[1,5-a]嘧啶酮
2.2 别嘌呤醇对克氏锥虫的影响
别嘌呤醇(4-羟基吡唑并[3,4-d]嘧啶)是体外抗克氏锥虫的有效药物。 这种寄生虫寄生的重要形式,就如同人类恰加斯病的发病机制,是血流和细胞内形式。用放射性标记的别嘌呤醇和通过高效液相色谱法分析该化合物的代谢产物的实验表明,血管和细胞内形式的克氏锥虫均以与体外对于epimastig-otes所显示的相同的方式代谢别嘌呤醇。通过感染动物和感染了克氏锥虫的组织培养系统分离出的有机体证明了致病形式的吡唑并嘧啶的代谢途径。 用别嘌呤醇治疗感染组织培养物及根除感染的调查意味着别嘌呤醇可能对克氏锥虫感染的化疗有用,这一假设已在一项动物研究中得到证实[13]。
2.3 抗利什曼虫和锥虫属
吡唑并嘧啶碱别嘌呤醇被磷酸核糖基转移酶活化为核糖核酸,将核糖核苷酸胺化成4-氨基吡唑并嘧啶核糖核苷酸,随后磷酸化成三磷酸酯形式并掺入RNA中。吡唑并嘧啶核糖核苷霉素B和别嘌呤醇核糖核苷通过核苷磷酸转移酶活化,如上所述将得到的核糖核苷酸胺化并掺入RNA中。 这些代谢特征不仅发生在昆虫载体中,而且发生在人的致病细胞内。 在利什曼原虫和锥虫属中存在的嘌呤的酶学和代谢的差异为化疗开发提供了极好的机会[14]。
哺乳动物细胞从头合成嘌呤,此外还具有连接嘌呤碱基和核苷的能力,以用于核酸和辅酶的合成。 利什曼原虫和锥虫属物种缺乏从头合成嘌呤,但可利用嘌呤掺入的主动补救机制。这些差异和人类与原生动物之间嘌呤补救途径中酶的特异性相关的吡唑并嘧啶代谢方面的差异使人们对这些生物的生物化学有了更全面的理解,并且可能发现由这些生物引起的疾病的药化学治疗形式的一些实际应用物[11]。
2.4 吡唑并[3,4-d]嘧啶核糖核苷作为抗球虫药
4-(烷硫基)-1H-吡唑并[3,4-d]嘧啶的核糖核苷已被证明是有用的抗球虫剂。 在研究中,不饱和4-烯丙基硫代和4-丁烯硫基衍生物 (11和12,Figure 3)显示出比它们的饱和同系物在体内对柔嫩艾美耳球虫更具活性。
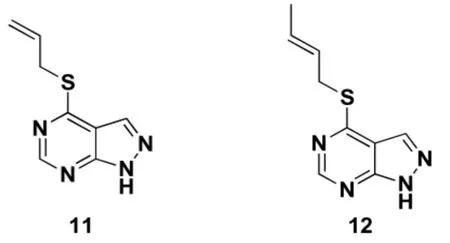
Figure3 具有抗球虫活性的吡唑并[3,4-d]嘧啶衍生物
研究表明,1H-吡唑[3,4-d]嘧啶的核糖核苷能够抑制雏鸡中柔嫩艾美耳球虫的发育。 结果表明,烷基硫代衍生物在用4-烷基硫代化合物的研究中优于烷基氨基衍生物,显然,4-取代基的烷基链中的不饱和键增强了其体内活性。由于发现饱和的同源物,因此该研究已扩展至包括4-(芳基烯基)硫基和 4-(芳基炔基)硫基类似物[15]。
2.5 抗隐孢子虫属和刚地弓形虫
原生动物隐孢子虫和弓形虫是无处不在的寄生虫,感染人类和家养动物,是一种引起人类主要健康问题C.parvum的寄生虫 (因为它是通过水传播疾病的)。C.parvum感染会导致衰弱性腹泻,这可能增加免疫功能低下患者的生命危险。 最近的研究致力于将发展中国家的儿童腹泻病的发病率控制在15%~20%左右[16-18]。
原生动物隐孢子虫和弓形虫是两种寄生虫,均含有一组钙依赖性蛋白激酶(CDPK),这些激酶在植物和纤毛虫中发现,但不存在于人类或真菌中。所以,一系列在 C.parvum(CpCDPK1)和T.gondii(TgCDPK1)中靶向 CDPK1 的有效抑制剂便产生了。这些抑制剂对CpCDPK1和TgCDPK1的选择性高于哺乳动物SRC和ABL。此外,它们能够在C.parvum入侵HCT-8宿主细胞的早期阶段发生作用,这与它们对侵入人成纤维细胞的弓形虫的作用相似。
实际上,Shokat及其同事已经表明,含有丙氨酸或甘氨酸残基的突变哺乳动物激酶对吡唑并嘧啶类抑制剂特别敏感,所述吡唑并嘧啶抑制剂(化合物 13~15,Figure 4)[19-21]能够有效地抑制TgCDPK1的催化活性并阻断刚毛虫侵入人成纤维细胞。在C.parvum (CpCDPK1)中也发现了TgCDPK1的同源物,但其在寄生虫侵袭中的作用尚未阐明。
3 总结
吡唑并嘧啶衍生物作为嘌呤的类似物,其具有多种生物活性,其中最主要的为抗癌和本文所述的对微生物的影响。以吡唑并嘧啶环为母环的许多化合物均能抗微生物生长或影响其代谢的过程,无论是抗菌还是抗寄生虫,都为灭除外物入侵,保护机体健康做出了贡献。
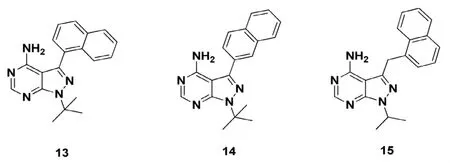
Figure4 具有抗隐孢子虫属和刚地弓形虫的吡唑并嘧啶衍生物
