远志皂苷元对内皮祖细胞移植治疗急性心肌梗死模型大鼠心功能的影响
2019-02-15靳文学乔秀兰
靳文学 乔秀兰
(重庆市中医院 1心血管科,重庆 400021;2针灸科)
急性心肌梗死(AMI)是全球发病率较高的一种疾病,外科手术和介入治疗是AMI目前主要临床传统疗法,此两种疗法均旨在重新建立血供,但对损伤的心肌组织和细胞并无修复效果。内皮祖细胞(EPCs)是与血管新生有关的骨髓干细胞亚群〔1〕,国内外诸多研究已经表明,EPCs在重建血供〔2〕、促进缺血性组织血管新生〔3〕,向心肌细胞和内皮细胞等细胞的分化〔4,5〕、缓解内皮功能障碍的肺动脉高压〔6〕及肿瘤防治等方面有卓越表现。在AMI治疗方面,EPCs移植也表现出了令人满意的疗效,EPCs移植可促进血管重建,改善心脏功能;向毛细血管内皮细胞分化,促进心肌梗死的恢复,改善心脏功能〔7~9〕。远志是我国传统的药材,其主要的活性组分有皂苷类、黄酮类、寡糖酯和生物碱等。远志皂苷元是其药理作用的主要活性成分之一,其在抗氧化、抑制炎症、抗衰老及抗细胞毒性方面疗效卓著〔10〕。在AMI进程中,心肌缺血再灌注会加剧内质网应激,引发心肌细胞凋亡,加重心肌梗死危害〔11〕,李子希等〔12〕研究表明,远志皂苷元可通过缓解内质网应激保护心肌。此外,远志皂苷元可促进血管内皮细胞增殖和活化,抑制内皮细胞的凋亡〔13~16〕。据此推测,远志皂苷元可提高EPCs移植的作用效果,然而目前远志皂苷元对EPCs移植治疗心肌梗死大鼠影响的研究尚为空白。本文旨在探讨远志皂苷元干预和EPCs移植联合治疗对AMI大鼠心功能的影响。
1 材料与方法
1.1实验动物 80只体重300~350 g健康SD大鼠(2.5月龄左右,雄性)由重庆医科大学提供,室温25℃,湿度50%~80%,SPF环境下自由饮水和采食,许可证号:SCXK(渝)2012-0001。
1.2主要材料 实验所用显微镜均由上海仪圆光学提供,二氨基联苯胺(DAB)购自北京化学试剂集团有限公司;胰蛋白酶购自美国Sigma公司;磷酸盐缓冲液(PBS)由Hyclone提供;细胞培养箱购自Heraeus Sepatech 公司。外周血内皮祖细胞由华中科技大学同济医学院附属协和医院提供。EBM-2培养基、胎牛血清均购自Hyclone;Trizol试剂盒购自Invitrogen;聚氰基丙烯酸正丁酯(BCA)蛋白浓度试剂盒(增强型)、5×十二烷基磺酸钠(SDS)蛋白上样缓冲液、20×三乙醇胺缓冲盐水(TBS)缓冲液等购自南京建成生物。SP-DiI染料购自北京大清生物技术有限公司;血管内皮生长因子(VEGF)抗体购于北京百迈客生物科技有限公司,β-actin抗体购于艾康生物技术(杭州)有限公司。生理盐水从上海交通大学医学院附属仁济医院购进。超净工作台提供自艺斯高上海贸易有限公司。荧光染色溶液的配制:将2.5 g SP-Dil染料用1 L的二甲基酰胺(DMF)溶解。远志皂苷元购自上海诚凛生物科技有限公司。
1.3建立大鼠模型及实验分组 取80只SD雄性大鼠建立AMI模型:麻醉大鼠,气管插管进行机械通气并密切监测心电变化。对所有实验大鼠开胸,辨认并结扎左冠状动脉前降支近段,以结扎冠状动脉后心肌颜色变暗、心脏变大、左室前壁局部心肌运动明显减弱及心电图ST段抬高为标准判定AMI模型建立成功与否。判定后缝合大鼠胸部切口后将之放回笼中饲养,将实验大鼠平均随机分为四组:AMI对照组(组Ⅰ)、远志皂苷元治疗组(组Ⅱ)、EPCs移植组(组Ⅲ)、EPCs移植联合远志皂苷元治疗组(组Ⅳ),各20只。
1.4体外复苏并培养扩增大鼠外周血EPCs 将冻存原代EPCs置于60℃恒温水浴箱,30 s内进行EPCs快速复苏。融化之后迅疾转入EP管并加入EBM-2培养基,重复小心吹打细胞使其均匀分布,随后离心弃上清液。将复苏后的细胞用EBM-2完全培养基调整为1×106/ml的密度。进行培养待EPCs汇合度达80%以上时,胰蛋白酶溶液消化2~3 min后终止消化;离心弃上清重悬细胞。调整细胞密度至1×106/ml培养7 d。离心弃上清,将EPC细胞密度调整为8×105/ml,加入5 μl CM-Dil标记细胞;随后置于培养箱中标记孵化25~30 min后离心弃上清PBS重悬,重复标记两次,显微镜下观察细胞标记的情况。镜下可见EPCs标记显现出鲜艳的橘红色,且颜色均匀,备用。实验大鼠建模1 h之后,进行EPCs移植和远志皂苷元干预治疗。将100 μl CM-Dil标记好的EPCs细胞悬液分5点分别注射到组Ⅲ及组Ⅳ心肌梗死区域的边缘,尾静脉注射100 μl生理盐水;将100 μl生理盐水分5点分别注射组Ⅱ大鼠心肌梗死区边缘,组Ⅱ和组Ⅳ尾静脉注射3 mg/ml远志皂苷元溶剂;分别于组Ⅰ心肌梗死区域边缘和尾静脉注射与上述EPCs混悬液和远志皂苷元试剂相同体积的生理盐水;连续治疗3 d。
1.5超声心动图检测大鼠心功能改变及毛细血管密度 EPCs移植后3 w及6 w,分别从各个实验组选取5只大鼠进行心功能变化测定。采用超声诊断仪记录3个心动周期左室收缩末期内径(LVDs)、左室舒张末期内径(LVDd)、左室前壁舒张末期厚度(LVAWd)、左室舒张末期容积(EDV)、收缩末期容积(ESV)并计算左室射血分数(LVEF)的平均值。于移植后3 w和6 w,处死大鼠迅速打开其胸腔,剥离出大鼠心肌梗死组织将之分为3份:1份置于液氮中备用;1份石蜡组织制片备用免疫组化染色;1份冰冻组织切片备用苏木精-伊红染(HE)染色。对心肌梗死组织进行石蜡包埋组织切片,CD34免疫组化染色并于显微镜下计数平均毛细血管密度。
1.6逆转录聚合酶链反应及酶联免疫吸附测定梗死周边区VEGF基因及蛋白的表达 研磨匀浆大鼠心肌梗死组织并提取组织的总RNA,通过Primer Primer5.0软件设计引物,VEGF引物序列上游:5′-AGAAGGAGGAGGGCAGAATCA-3′;下游:5′-CAAATGCTTTCTCCGCTCTGA-3′,目的片段长度326 bp;参照物β-actin引物序列上游:5′-ACTCCTGCTTGCTGATCCACATC-3′;下游5′-AGCGGGAAATCGTGCGTGCGTGAC-3′,片段长度为471 bp。反应后琼脂糖凝胶电泳并成像仪摄片,用Image proplus6.0图像分析软件测算电泳条带的OD值,进而计算其相对表达量。取大鼠心肌梗死区域组织匀浆液,4 000 r/min离心取组织上清液,用ELISA试剂盒(购自南京建成生物有限公司)测定VEGF含量。根据免疫显色反应的当量关系可知实验大鼠心肌梗死组织的VEGF水平。
1.7荧光显微镜观察心肌内移植内皮祖细胞EPCs 干预治疗3 w和6 w之后制作大鼠心肌梗死组织冰冻切片并进行4′,6-二脒基-2苯基吲哚染色。干燥后,显微镜下观察时,随机选取每张冷冻切片的3个视野并且对之进行拍照记录;假设每张照片的总亮度为1,每张照片选取一个光亮度点,利用ACDsee5.0软件确定其坐标值。随机选取5个视野,计数CM-Dil阳性细胞数及细胞总数,计算标记率。标记率=视野内阳性细胞总数/视野内细胞总数×100%。
1.8大鼠心肌修复情况 取出大鼠心肌梗死组织,10%甲醛固定组织;梯度酒精脱水,逐渐脱去组织块中的水分。再将组织块置于既溶于酒精,又溶于石蜡的透明剂二甲苯中透明,以二甲苯替换出组织块的中酒精,随后进行浸蜡包埋。将包埋好的蜡块固定于切片机上,切成5~8 μm薄片。将薄片烫平,再贴到载玻片上,45℃恒温烘干。脱蜡后,进行HE染色。染色后的切片经纯酒精脱水,再经二甲苯使切片透明。将已透明的切片滴上加拿大树胶,盖上盖玻片封固。待树胶干燥后,荧光显微镜下观察各组心肌梗死组织的病理学变化。于治疗后3 w和6 w,选取各个实验组5只大鼠麻醉处死,立即取出大鼠的心脏于液氮冻存30 min。随后取长轴垂直方向1~2 mm切片,以2,3,5-三苏基氨化四氮唑(TTC)染色法计算心肌梗死面积〔17〕。
1.9统计学方法 应用SPSS13.0统计软件进行t检验、方差分析。
2 结 果
2.1EPCs形态观察 冷冻保存的EPCs复苏后重悬于新鲜的EPCs细胞培养液中,多数细胞生长良好。培养5~6 d发现细胞明显增殖即可传代,移植后2 w细胞呈平形排列或漩涡状集落生长,排列紧密;传代后的细胞传至第3代细胞生长迅速,纯度高、 形态单一(图1)。选取第3代细胞进入实验。
2.2大鼠心功能改变检测结果 在细胞移植和药物干预3 w及6 w后,与组Ⅰ相比,组Ⅱ、Ⅲ、Ⅳ心功能和左室收缩舒张功能明显改善(P<0.05);组Ⅳ较组Ⅱ、Ⅲ显著提高了大鼠的心脏功能和左心室的舒缩能力(P<0.05)。见表1。
图1 第3代 EPCs的形态(×200)
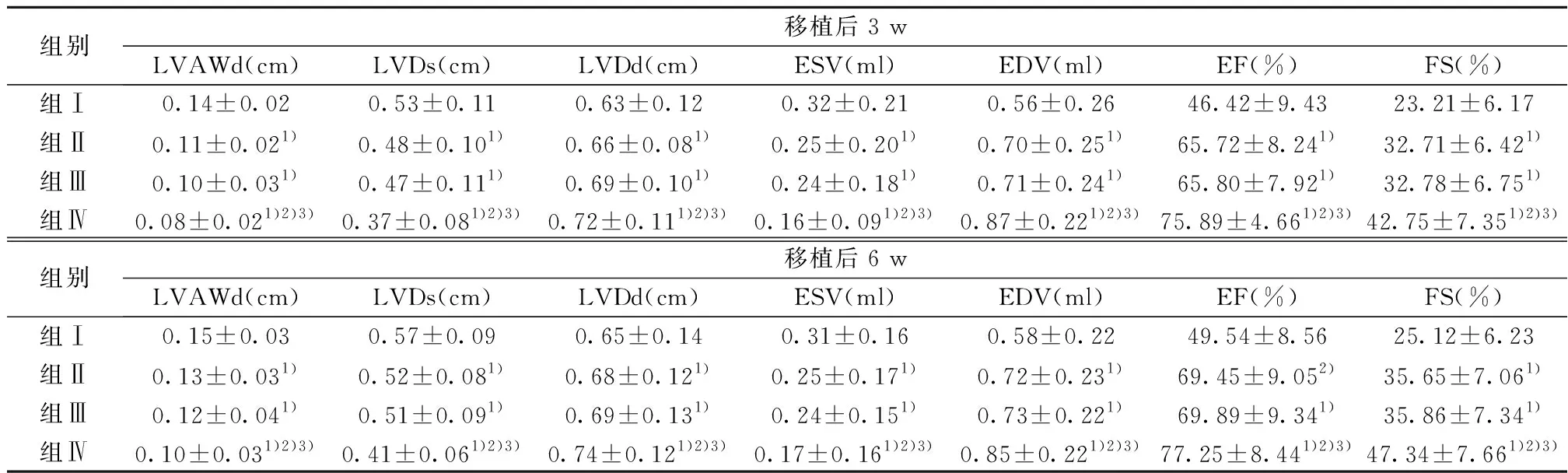
组别移植后3 wLVAWd(cm)LVDs(cm)LVDd(cm)ESV(ml)EDV(ml)EF(%)FS(%)组Ⅰ0.14±0.020.53±0.110.63±0.120.32±0.210.56±0.2646.42±9.4323.21±6.17组Ⅱ0.11±0.021)0.48±0.101)0.66±0.081)0.25±0.201)0.70±0.251)65.72±8.241)32.71±6.421)组Ⅲ0.10±0.031)0.47±0.111)0.69±0.101)0.24±0.181)0.71±0.241)65.80±7.921)32.78±6.751)组Ⅳ0.08±0.021)2)3)0.37±0.081)2)3)0.72±0.111)2)3)0.16±0.091)2)3)0.87±0.221)2)3)75.89±4.661)2)3)42.75±7.351)2)3)组别移植后6 wLVAWd(cm)LVDs(cm)LVDd(cm)ESV(ml)EDV(ml)EF(%)FS(%)组Ⅰ0.15±0.030.57±0.090.65±0.140.31±0.160.58±0.2249.54±8.5625.12±6.23组Ⅱ0.13±0.031)0.52±0.081)0.68±0.121)0.25±0.171)0.72±0.231)69.45±9.052)35.65±7.061)组Ⅲ0.12±0.041)0.51±0.091)0.69±0.131)0.24±0.151)0.73±0.221)69.89±9.341)35.86±7.341)组Ⅳ0.10±0.031)2)3)0.41±0.061)2)3)0.74±0.121)2)3)0.17±0.161)2)3)0.85±0.221)2)3)77.25±8.441)2)3)47.34±7.661)2)3)
与组Ⅰ比较:1)P<0.05;与组Ⅱ比较:2)P<0.05;与组Ⅲ比较:3)P<0.05,下表同
2.3毛细血管密度的测定 与组Ⅰ相比,治疗3 w后组Ⅱ、Ⅲ、Ⅳ均显著增加了心肌梗死组织中的新生毛细血管密度,组Ⅳ较组Ⅲ明显增高(P<0.05)。治疗6 w后,各组新生毛细血管密度均较治疗3 w后显著增加,而组Ⅱ、Ⅲ、Ⅳ均显著高于组Ⅰ(P<0.05),组Ⅳ效果最佳。见表2。
2.4VEGF基因和蛋白的表达 与组Ⅰ相比,治疗3 w后组Ⅱ、Ⅲ、Ⅳ心肌梗死组织中VEGF mRNA和蛋白相对表达水平均显著提高(P<0.05),组Ⅳ显著高于其他组(P<0.05)。在治疗6 w后,各组心肌梗死组织中VEGF mRNA和蛋白相对表达水平较治疗3 w明显提高;组Ⅱ、Ⅲ VEGF mRNA和蛋白表达水平显著高于组Ⅰ(P<0.05),而组Ⅳ明显高于组Ⅱ、Ⅲ(P<0.05)。见表2和图2。

表2 各组新生毛细血管密度、心肌梗死组织VEGF mRNA和蛋白表达水平及心肌梗死面积
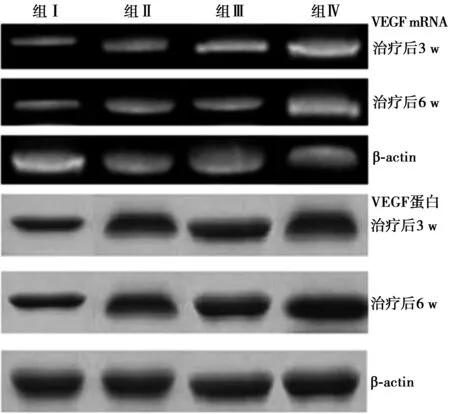
图2 各组VEGF mRNA和蛋白表达
2.5CM-Dil标记阳性EPCs 治疗3和6 w后,组Ⅱ和组Ⅰ未见CM-Dil标记阳性EPCs;组Ⅳ与组Ⅲ可观察到较多的CM-Dil标记阳性EPCs,组ⅣCM-Dil阳性EPCs明显多于组Ⅲ。见图3。
2.6心肌修复情况 在干预治疗3 w之后,组Ⅰ心肌组织发生了明显的组织病理学变化,如心肌梗死区域内肌纤维溶解、心肌肌组织发生断裂,心肌细胞排列紊乱;治疗各组心肌梗死组织形态学病变明显缓解,心肌组织区域正常,心肌细胞排列较为整齐,有明显的新生毛细血管存在;其中组Ⅳ心肌梗死状况明显好转,新生毛细血管最多,心肌细胞排列整齐度最佳(图4)。治疗3 w和6 w后,与组Ⅰ相比,组Ⅱ、Ⅲ、Ⅳ的心肌梗死区域梗死面积显著降低,组Ⅳ低于其他各组。见表2。

图4 各组心肌修复情况(×200)
3 讨 论
在心肌缺血早期,往往出现心肌肥大和心肌胶原瘢痕,随之即发生心功能障碍,心肌舒缩能力下降和心肌坏死。EPCs是主要存在于机体骨髓中的干细胞亚群。在机体发生某种病理状况时,骨髓中的EPCs被动员进入外周血循环系统,开始向病理组织迁移。与其他干细胞特性相似,EPCs具有向组织缺血或者内皮损伤部位归巢的特性,并最终黏附、结合在受损血管部位。在EPCs迁移归巢过程中,VEGF等细胞因子发挥着重要作用。Miglionico等〔18〕通过对冠心病患者设置EPCs捕捉支架,取得了令人满意的治疗效果;这证明EPCs在心肌缺血性梗死部位的集聚对心肌梗死恢复具有重要作用。
国内外诸多研究已经表明,体外移植EPCs可显著提高心肌梗死动物的心脏功能,促进新生血管的形成〔19,20〕。其主要机制可能是:(1)EPCs分化为血管内皮细胞并直接形成新的血管,重新构建血液供应;(2)旁分泌VEGF等,保护心肌梗死部位的损伤细胞;(3)EPCs还可与宿主的细胞相互融合,增强缺血区域的心肌细胞功能。然而,Yao等〔21〕研究显示,体外移植的EPCs在宿主体内存活时间有限,因此这限制了EPCs移植效果。Schuh等〔22〕和Sen等〔23〕通过适当辅助性支持EPCs的移植,提高了EPCs的心肌梗死治疗效果,改善了心肌梗死后的心脏功能。远志皂苷元可促进血管内皮细胞的增殖并抑制内皮细胞的凋亡,据此推测其对于EPCs移植可能具有较好的辅助性支持效果。本研究结果显示,EPCs体外移植后,远志皂苷元明显提高了EPCs移植效率,增加了EPCs在心肌梗死组织的含量。这提示远志皂苷元还可通过提高EPCs在心肌梗死部位的存活率提高心肌梗死的治疗效果。VEGF在正常人心肌中含量较低,但在冠状动脉疾病中则表达水平急剧升高;只是VEGF的受体表达水平也随之提高,进而提高了内皮细胞增殖,放大了VEGF生物学效应〔24〕。VEGF可以促进血管内皮细胞的增殖,促进心肌血管的形成,增加血供〔24~26〕。此系因体外移植的EPCs及其分化而成的内皮细胞分泌增加所致。
综上,远志皂苷元干预提高了EPCs的移植效率,增加了EPCs在心肌梗死组织中的存留,进而促进心肌梗死恢复。远志皂苷元干预和EPCs移植的联合治疗提高了EPCs移植效率和治疗效果,其主要通过促进心脏功能恢复、缓解心肌组织病变、提高新生血管密度和VEGF的表达水平。远志皂苷元的干预对EPCs移植起到了明显的辅助支持作用,并为该细胞移植治疗心肌梗死开辟新的途径和思路,但其机制尚需要进一步探讨。
