Fe3O4/纤维素磁性纳米材料对亚甲基蓝的吸附性能研究
2019-02-13赖金花刘凯杨聪陶玉婷吴迪刘贤响
赖金花,刘凯,杨聪,陶玉婷,吴迪,刘贤响
(湖南师范大学 化学化工学院 石化新材料与资源精细利用国家地方联合工程实验室,湖南 长沙 410081)
磁性纳米复合物(MNCs)具有磁性强、比表面积大等特点,作为吸附剂用于废水的净化逐渐得到了国内外学者的高度关注[1-7]。MNCs 吸附剂是通过在磁性纳米颗粒(MNPs)的表面修饰或包裹聚合物[8]、表面活性剂[9]、贵金属[10]和无机氧化物[11]等得到的。
Fe3O4是一种典型的磁性纳米粒子,因磁效应和表面效应等特殊的性质,在生物医学、重金属离子的吸附等领域发挥着重要作用,应用前景十分广阔。添加高分子聚合物对 Fe3O4纳米颗粒进行负载,可以获得能在水中稳定分散的磁性纳米粒子,有效地克服了传统工艺的缺点[12-13]。
本文利用纤维素负载磁性纳米Fe3O4制备出新型、无机-有机 Fe3O4/纤维素复合材料,并将其用于处理亚甲基蓝模拟的印染废水,优化吸附工艺条件,研究吸附动力学,推测反应机理,为该材料的实际应用提供理论基础和实验参考。
1 实验部分
1.1 试剂与仪器
微晶纤维素、FeCl2·4H2O、NH3·H2O、亚甲基蓝、 硫酸等均为分析纯。
HWCL-1型恒温磁力搅拌器;TGL-16G型离心机;GJ101型电热鼓风干燥箱;BL6-180A型超声波清洗仪;SP-754型紫外可见分光光度计。
1.2 Fe3O4/纤维素复合材料的制备
1.2.1 纳米纤维素的制备 将1.0 g微晶纤维素(MCC)粉末分散到烧瓶中的13 mL水中,在搅拌下缓慢滴加7 mL 98%的硫酸,在50 ℃下连续搅拌水解2 h。加入大量的水(50 mL)淬灭水解,并离心(3 300 r/min)30 min。用水洗至中性,再利用超声波使其分散在水中。得到纳米纤维素的乳白色胶体分散体。
1.2.2 Fe3O4纳米颗粒的制备 使用250 mL烧瓶将0.25 g FeCl2·4H2O溶解于20 mL去离子水中,在高速搅拌下缓慢滴加10 mL 2.6%的NH3·H2O,在80 ℃反应30 min。 用去离子水洗涤,并进行磁分离,在100 ℃干燥2 h,得到黑色纳米Fe3O4颗粒。其原理为:
4Fe2++O2+8OH-=4FeOOH+2H2O
2FeOOH+Fe2++2OH-=Fe3O4↓+2H2O
Fe2+→ Fe(OH)2→ FeOOH → Fe3O4
1.2.3 Fe3O4/纤维素复合材料的制备 使用250 mL烧瓶将0.25 g氯化亚铁和一定量的纤维素溶于20 mL去离子水中,缓慢滴加10 mL 2.6%的NH3·H2O,在高速搅拌且温度为80 ℃反应30 min。用去离子水洗涤并进行磁分离,在100 ℃干燥2 h。得到黑色Fe3O4/纤维素复合材料。
1.3 亚甲基蓝的吸附实验
将2 mg Fe3O4/纤维素复合材料和2 mL浓度10 mg/L的染料溶液加入5 mL烧杯中,在22 ℃下恒温振荡60 min,每间隔10 min取样1次,利用磁铁收集吸附剂,使用UV-Vis分光光度计测量上清液中亚甲基蓝的浓度,计算吸附能力(Q)和去除率(E)。
Q=[(C0-Ce)V/W]×100%
(1)
E=[(C0-Ce)/C0]×100%
(2)
式中Q——复合材料对亚甲基蓝的吸附能力,%;
E——去除率,%;
C0——初始染料的浓度,mg/L;
Ce——反应平衡时的染料平衡浓度,mg/L;
V——反应溶液的体积,L;
W——吸附剂的重量,g。
2 结果与讨论
2.1 Fe3O4/纤维素复合材料的XRD图谱
Fe3O4/纤维素复合材料的X射线衍射见图1。
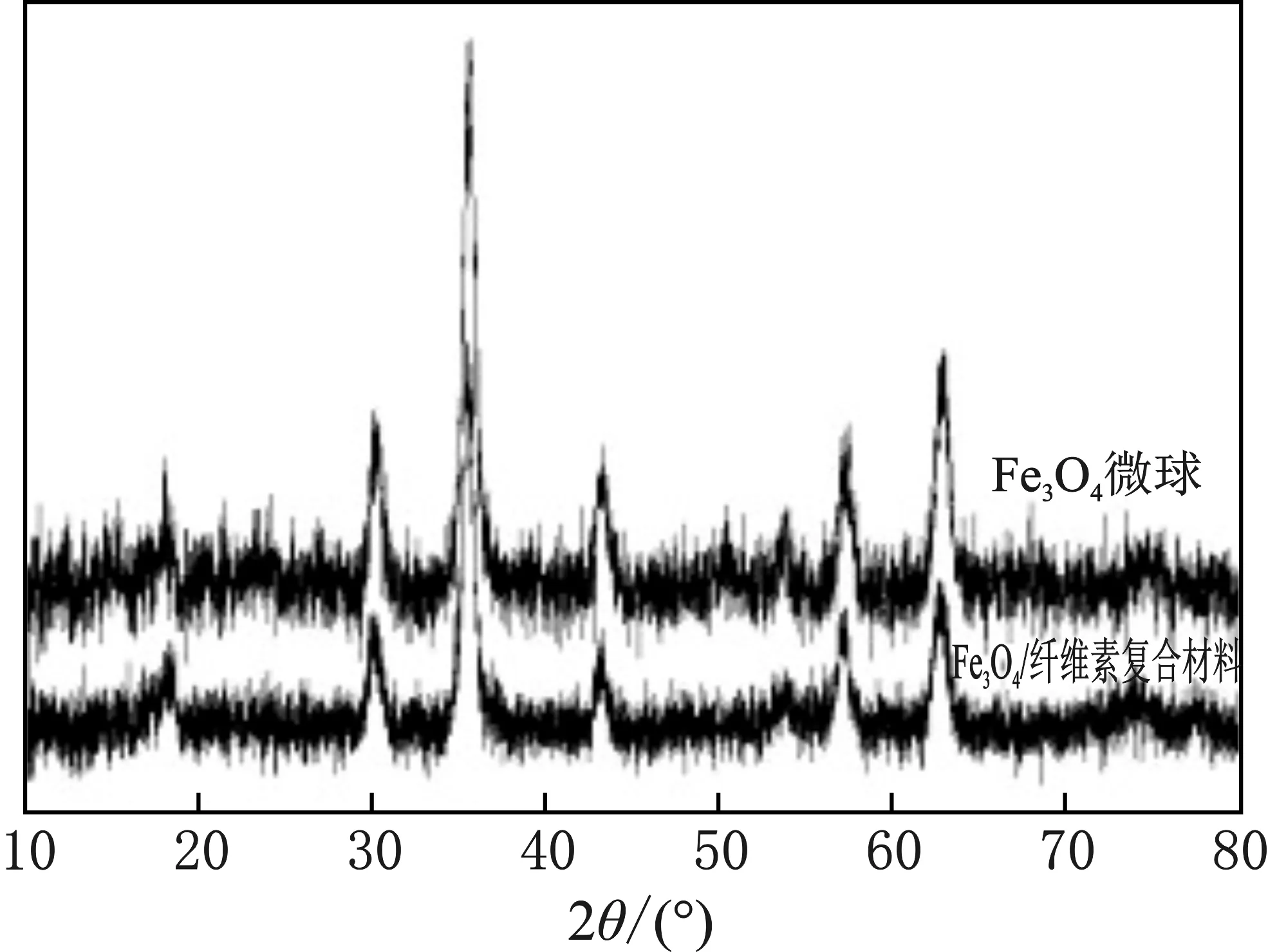
图1 样品的XRD图谱Fig.1 XRD patterns of the samples
由图1可知,2θ=30.1,35.5,43.1,57.0,62.9°分别对应晶面(220)、(311)、(400)、(511)和(440),没有其他杂质峰的出现,与标准卡片JCPDF#19-0629的峰一致,说明复合粒子的衍射峰与纯的Fe3O4的一致,可知Fe3O4已被负载。
2.2 Fe3O4和纤维素的质量比对MB去除的影响
实验条件同1.3节,在吸附剂4.5 mg时,Fe3O4和纤维素质量比对MB去除的影响见图2。
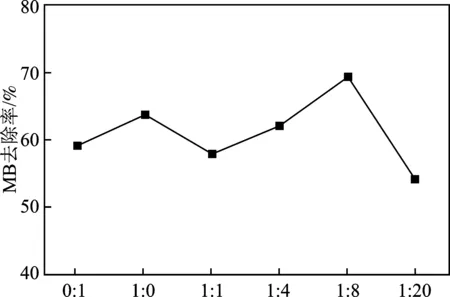
Fe3O4∶纤维素/质量比图2 Fe3O4/纤维素的质量比对MB去除的影响Fig.2 Effects of different absorbents on the removal
由图2可知,纯Fe3O4纳米颗粒和纯纤维素均可去除MB,且纯Fe3O4纳米颗粒对MB去除率略强于纯纤维素,将两者按照一定比例混合后,随着Fe3O4的质量增多,MB的去除效果越明显,在Fe3O4/纤维素为1∶8时对MB的去除效果最佳,但当Fe3O4/纤维素质量比>1∶20时,对MB的去除效果明显减弱,这归功于Fe3O4的吸附作用和纤维素的催化降解,因此采用Fe3O4/纤维素质量比为1∶8的吸附剂。
2.3 吸附剂用量对MB去除效果的影响
实验条件同1.3节,吸附剂用量对MB去除效果的影响见图3。
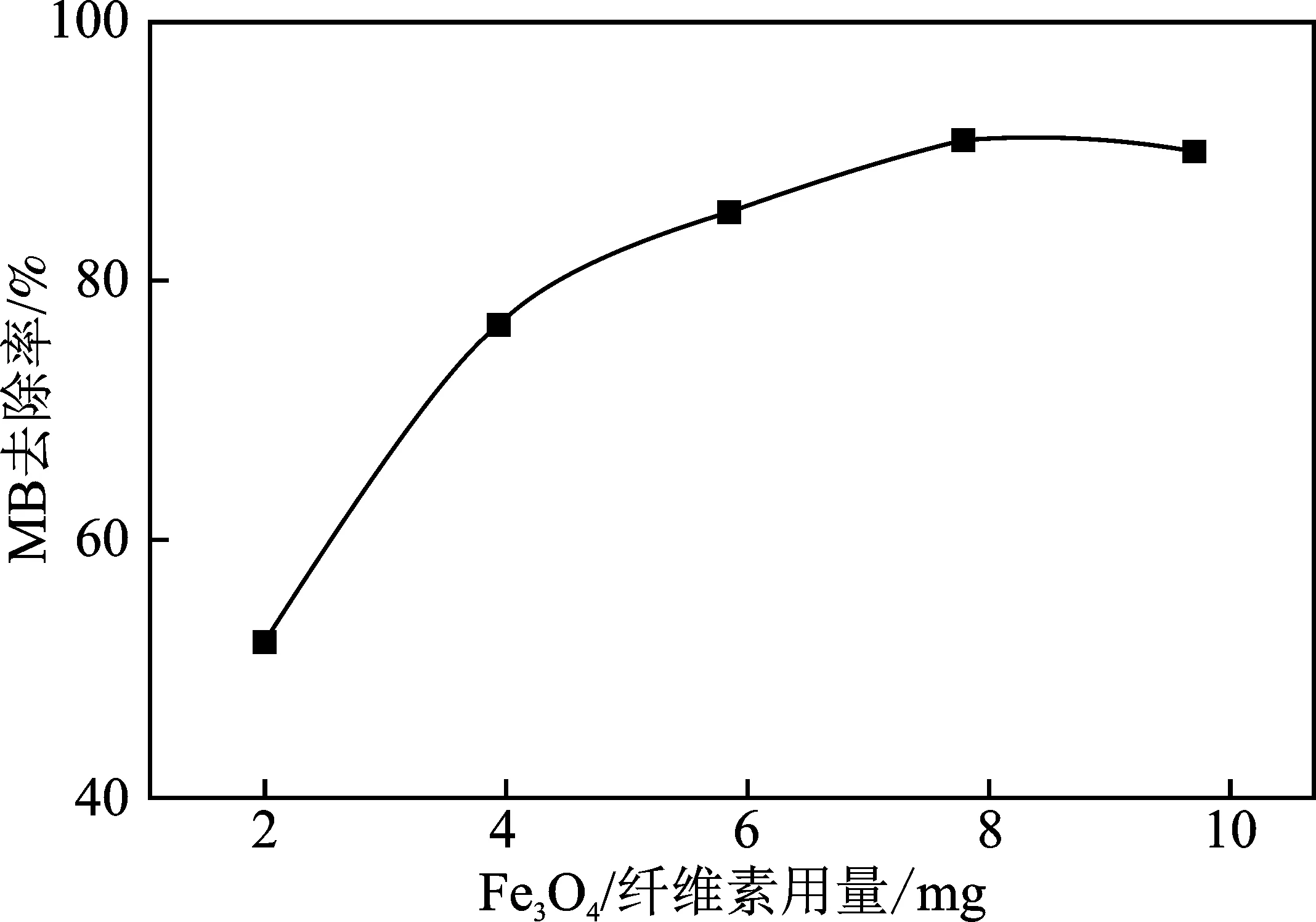
图3 吸收剂用量对MB去除效果的影响Fig.3 Effects of absorbent dosage on the removal
由图3可知,随着吸附剂用量的增大,MB的去除效果逐渐减缓,吸附剂用量8 mg时,对MB的去除效果最佳,吸附剂用量为10 mg时,对MB的去除效果减弱。
2.4 反应时间对MB去除的影响
实验条件同1.3节,在吸附剂用量8 mg时,时间对Fe3O4/纤维素复合材料对MB吸附性能的影响见图4。
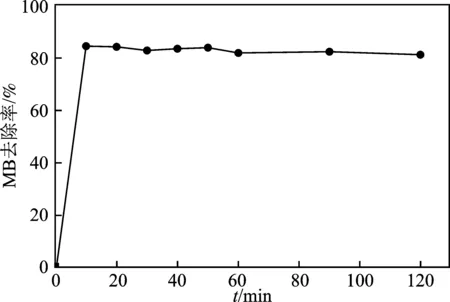
图4 反应时间对MB去除的影响Fig.4 Effects of contact time on the removal
由图4可知,随着反应体系时间的增加,对MB的去除效果先增强后减弱,反应10 min时,达到最佳吸附效果,>10 min时,吸附效果下降,反应时间超过20 min后,吸附效果下降趋势相对减缓。说明最佳时间为10 min。
2.5 初始染料浓度对MB去除的影响
亚甲基蓝溶液模拟废水初始浓度对MB去除的影响见图5(吸附剂 8 mg)。
由图5可知,随着初始染料浓度的增大,Fe3O4/纤维素复合材料对MB的去除效果逐渐减弱。这表明亚甲基蓝的初始浓度越低,Fe3O4/纤维素复合材料的吸附效果越好。这是因为在吸附过程中存在吸附平衡,当达到饱和度即平衡点时,吸附效果达到最佳,当浓度过大,相对应的吸附过程则需要更长的时间。

图5 初始染料浓度对MB去除的影响Fig.5 Effect of initial dye concentration on the removal
2.6 吸附等温线和热力学
用Langmuir吸附等温方程[14-16]对Fe3O4/纤维素对MB的吸附数据进行拟合,结果见图6。
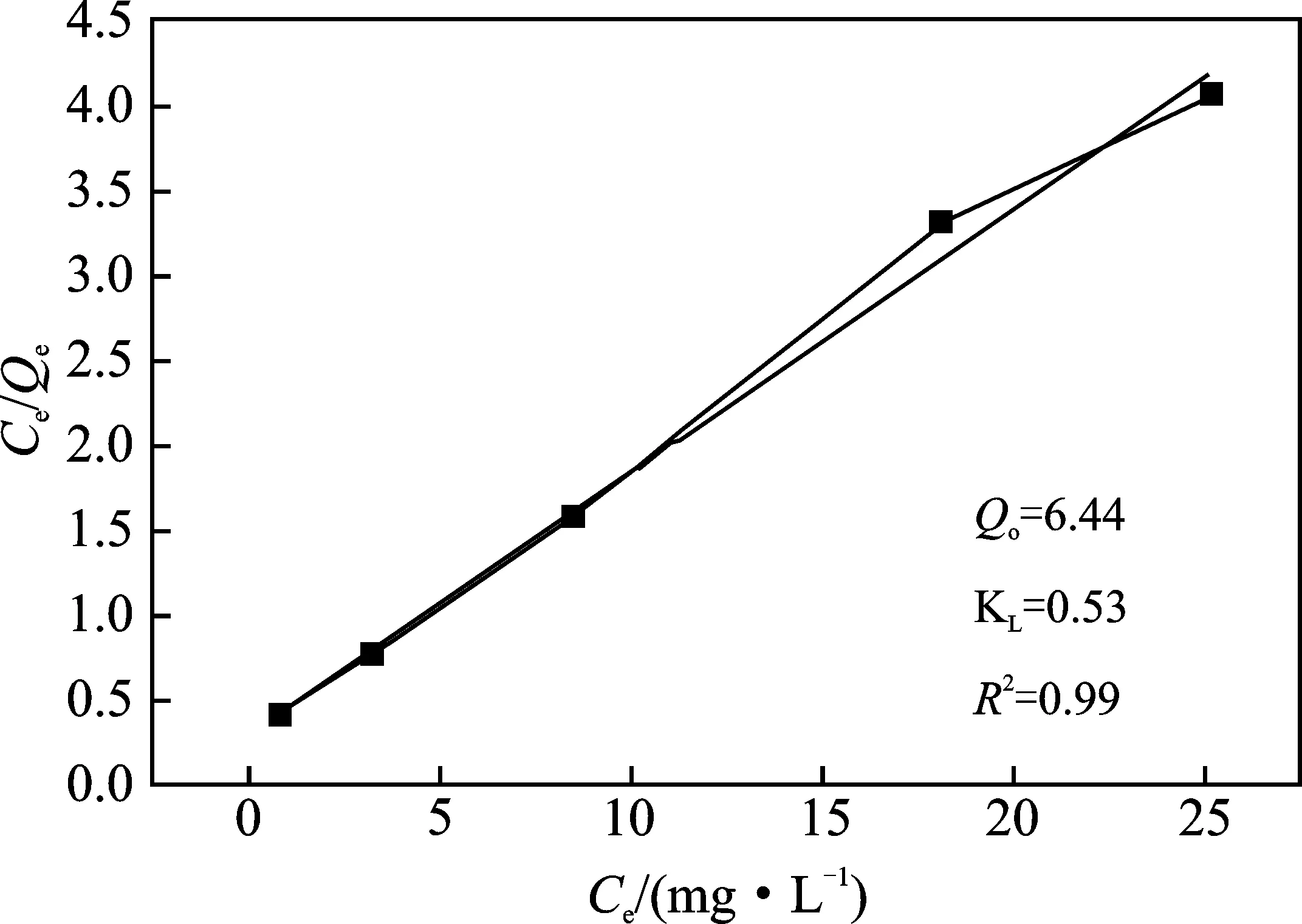
图6 在Fe3O4/纤维素上MB吸附的Langmuir等温线Fig.6 Langmuir isotherm of MB adsorptionon the Fe3O4/cellulose
由图6可知,Fe3O4/纤维素对MB的吸附符合Langmuir等温吸附方程规律。
2.7 Fe3O4/纤维素复合材料的磁性及回收循环
实验证明,Fe3O4/纤维素复合材料保留了Fe3O4的磁性质。将实验后的材料进行清洗回收,在外加磁场(磁铁)的作用下可回收循环使用(见图7)。

图7 Fe3O4/纤维素复合材料的磁分离回收Fig.7 Magnetic separation of Fe3O4/cellulosecomposite materials
3 结论
(1)以氯化亚铁为原料,稀氨水为沉淀剂,在不需要氮气保护的温和条件下制备了Fe3O4纳米颗粒,实验表明,选择10 mg 2.6%的NH3·H2O溶液,80 ℃下快速搅拌反应30 min可以使所制备的Fe3O4纳米颗粒均匀,粒径适宜,并且无杂质。
(2)以纤维素和氯化亚铁为主要原料,一步制备新型 Fe3O4/纤维素磁性纳米复合材料,该新型复合材料吸附性能和磁性能的有力结合使其具有易分离和易回收的特点。
(3)Fe3O4/纤维素复合材料比单一组分对MB的去除效果好,Fe3O4/纤维素质量比为1∶8;吸附剂用量8 mg,反应时间10 min时吸附效果最好,去除率最高可达91%。
(4)Fe3O4/纤维素对MB的吸附符合Langmuir等温吸附方程规律。
