增强T2 FLAIR 与增强T1WI在颅内肿瘤性病变中的对照研究
2019-02-12龚建中乔建兰
龚建中 乔建兰 郗 艳
FLAIR 序 列(fluid attenuated inversion recovery)即液体衰减反转恢复序列,反转恢复时间TI(time of inversion)较长,该序列为施加一个180°脉冲后,磁化矢量反转到负180°,当TI 位于1500 ~2800ms 时,水的磁化矢量恢复为0°,再施加90°、180°自旋回波脉冲,采集信号时水为无信号,而其他组织有信号。顺磁性钆(Gd-DTPA)造影剂主要缩短T1 时间,因此磁共振增强成像主要使用T1WI(T1 加权成像),由于FLAIR 序列反转时间长,具有轻微的T1 效应,因此也可用于增强后成像[1]。目前国内外增强T2 FLAIR 主要应用在脑膜病变和转移瘤中,且研究报道有限。本研究旨在通过对比增强T2 FLAIR 与增强T1WI 成像,探索增强T2 FLAIR 在颅内肿瘤病变中的应用价值。
方 法
1.基本资料及检查方法
收集颅脑肿瘤患者MRI 检查图像。入组标准为:①患者签署加做增强T2 FLAIR 知情同意书;②检查过程中发现颅脑肿瘤性病变;③图像无明显伪影,可用于后期图像处理与评估。最终入组30 例,男性11 例,女性19 例,平均年龄60 岁,年龄范围为32 ~87 岁,肿瘤分类参照表1。
磁共振扫描仪为Siemens MAGNETOM Avanto 1.5T,选择8 通道颅脑线圈;GE Discovery MR 750w 3.0T扫描仪,选择24通道颅脑线圈。取仰卧位,先进行颅脑MRI 平扫序列扫描,即横断位T1WI(GE3.0 使用的是T1 FLAIR 序列)、T2WI、T2 FLAIR、DWI。而后使用高压注射器经肘静脉注射钆喷酸葡胺 (0.1mmol/kg),速率为3ml/s,注射完毕后,先行增强T1WI 横冠矢状位扫描(GE 3.0增强使用的是T1 FLAIR 序列),后行横断位增强T2 FLAIR 扫描,即注射造影剂后4 ~6 分钟进行FLAIR 扫描。增强T2 FLAIR 扫描条件:①西门子1.5T:FOV23cm,层厚5mm,层间距1.5mm,层数19 层,TR8000ms,TE93ms,TI2500ms,采集次数NEX 1,扫描矩阵256×250,带宽为219Hz。②GE 3.0T: FOV24cm,层厚5mm,层间距2.5mm,层 数20 层,TR9000ms,TE90ms,TI2473ms, 采集次数NEX1,扫描矩阵256×224,回波链长度ETL18。
2.图像分析及统计学分析
入组图像由两名经验丰富的神经影像医师(工作5 年以上)进行观察与测量,观察内容包括:①病灶T1WI 与T2 FLAIR 强化程度比较;②脑膜强化显示对比;③FLAIR 病灶周围水肿有无影响病灶边界;④颅内转移瘤统计肿瘤数目。测量增强后病灶同脑白质、脑灰质、脑脊液的信号对比率(Contrast Ratio,CR),西门子1.5T 使用Syngo B17 后处理站进行测量,GE 3.0T 使用AW Volume Share 7后处理站进行测量,选取肿瘤强化最明显处为感兴趣区(region of interest,ROI),在增强后T1WI 和增强后T2 FLAIR 同一层面、相同区域、相同ROI进行测量,减少测量误差,病灶/脑白质信号对比率为CR1,病灶/脑灰质信号对比率为CR2,病灶/脑脊液的信号对比率为CR3,测量有异议处两者商议解决。使用SPSS22.0 进行统计学分析,CR 的均数采用均值±标准差表示,分别对1.5T、3.0T病例的信号对比率进行正态分布非参数K-S 检验,检验结果均符合正态分布。增强T2 FLAIR 与增强T1WI 的CR 均值的比较使用配对样本t 检验,双侧P<0.05 认为差异有统计学意义。
结 果
1.描述性统计分析
肿瘤强化程度:①1.5T 上病例:T1WI 明显9 例,FLAIR 明显1 例,两者相仿2 例,FLAIR 轻度强化3 例;②3.0T 上病例:T1WI 明显14 例,FLAIR 明显0 例,相仿4 例,FLAIR 轻度强化2 例,负强化1例(具体分类参照表1,图像参照图1、2)。
脑膜强化的显示:①1.5T 上:共有8 例存在脑膜强化,T1WI 明显2 例,FLAIR 明显1 例,两者相仿5 例。②3.0T 上:共8 例病灶存在脑膜强化,T1WI 明显3 例,FLAIR 明显1 例,相仿4 例。2 例转移瘤患者,呈现脑膜线样强化特征,但他们的脑膜强化程度T1WI 与FLAIR 相仿(具体分析见表1)。
1 例胶质瘤周围水肿影响增强T2 FLAIR 肿瘤边界的观察(图1D)。在转移瘤数目统计上,所有转移瘤患者转移瘤数目均<5 个,且T1WI 与FLAIR增强均发现了12 个病灶。
2.增强后CR 值的统计分析
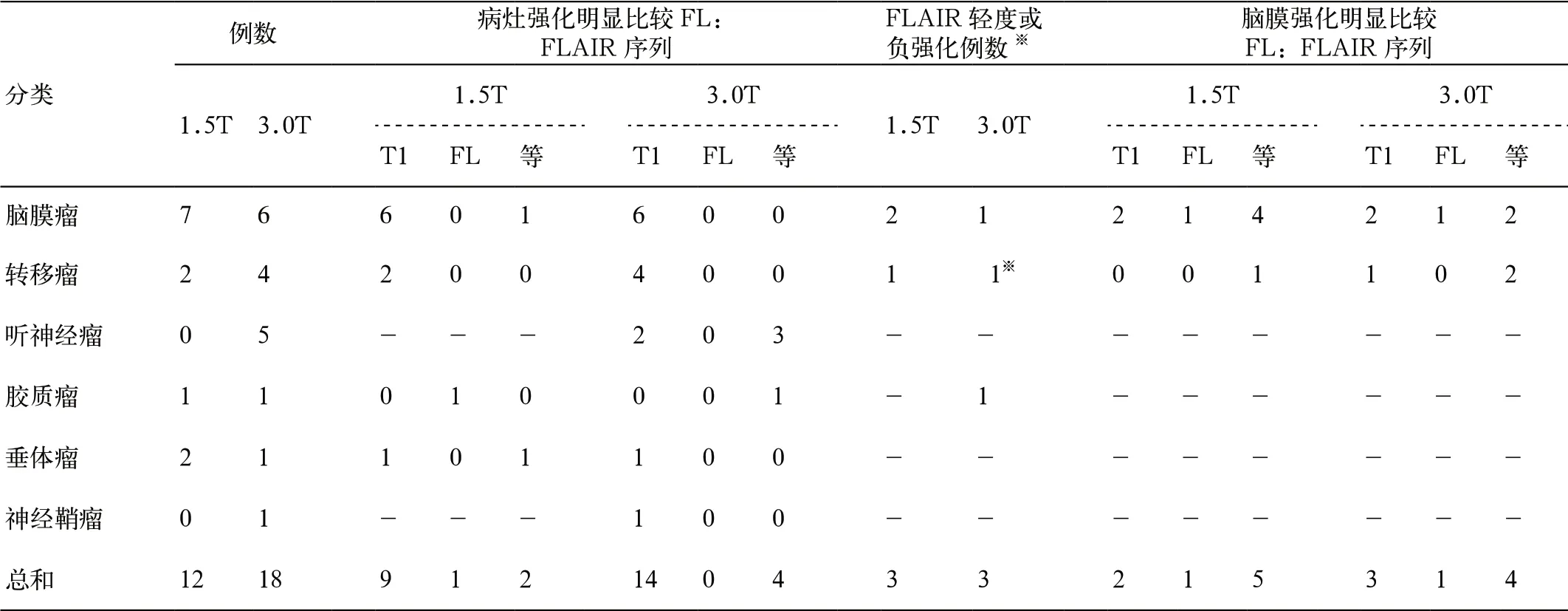
表1 肿瘤的分类和强化程度

表2 1.5T 增强T2 FLAIR 与增强T1WI 的CR 均值的比较
在西门子1.5T 检查的病例中,增强T1WI 与增强T2 FLAIR 信号比率CR,差异有统计学意义的为CR2 与CR3,即增强T2 FLAIR 上病灶同白质、脑脊液的信号比率,较增强T1WI 更高(见表2)。
在GE3.0 检查的病例中,增强T1WI 与增强T2 FLAIR 信号比率CR,差异有统计学意义的为CR1,即增强T1WI 上病灶同灰质信号比率,较增强FLAIR 更高(表3)。

表3 3.0T 增强T2 FLAIR 与增强T1WI 的CR 均值的比较
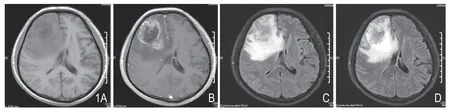
图1 男,54 岁,高级别胶质瘤III-IV 级。A.为T1WI 平扫; B.为T1WI 增强;C.为FLAIR 平扫;D.为T2 FLAIR 增强。该病例增强FLAIR 病灶局部较T1WI 增强强化明显,但是水肿影响肿瘤局部边界的观察。
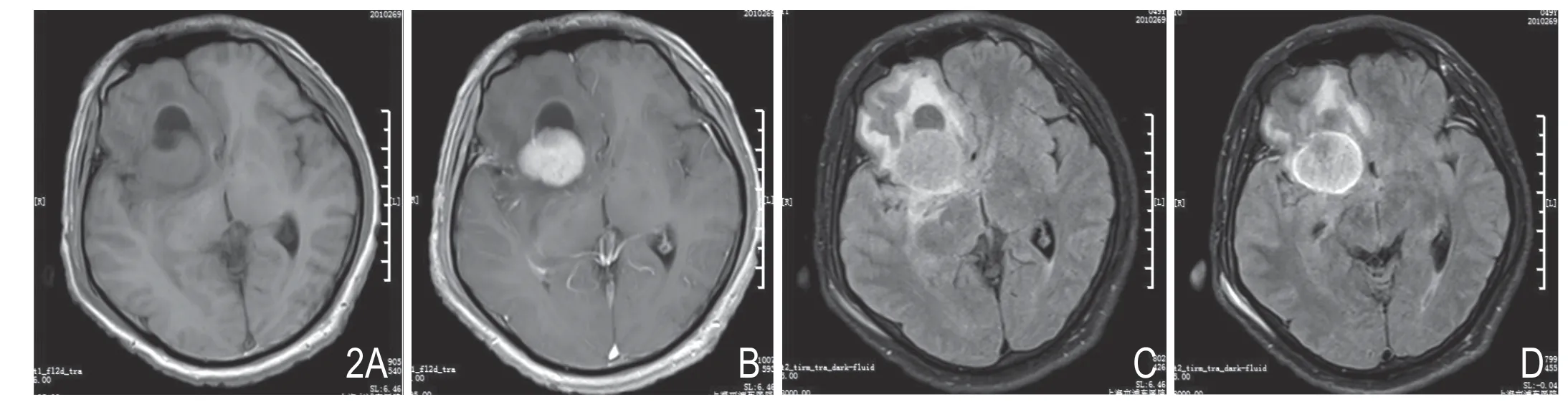
图2 男,47 岁,内皮细胞性脑膜瘤。A 为T1WI 平扫,B 为T1WI 增强,C 为FLAIR 平扫,D 为T2 FLAIR 增强。该病例增强FLAIR 病灶不如增强T1WI 强化明显,但是T2 FLAIR 增强后边缘均匀薄壁样强化为特征性征象,本研究中其他脑内肿瘤、其他序列未见此征象。
3.脑膜瘤在增强T2 FLAIR 特殊征象的描述
本研究中13 例脑膜瘤中,7 例在增强后T2 FLAIR 图像上出现周围均匀薄壁样强化,而在强化前后其他序列上未见此征象,在其他颅内肿瘤中未见此征象(图2D),2 例病理证实为内皮细胞性脑膜瘤,伴发周围脑实质水肿,在增强T2 FLAIR 图像上,在肿瘤与水肿边界区,出现均匀薄壁样强化,该征象将肿瘤边界和水肿区明显区分开。
讨 论
增强MRI 在发现平扫未显示的肿瘤、判断肿瘤血供、观察神经、血管、颅骨、脑膜的侵犯较平扫有优势。常用的MRI 增强造影剂为顺磁性钆(Gd-DTPA),Gd-DTPA 可同时缩短T1 及T2 时间,但以缩短T1 弛豫时间为主,因此增强常使用T1WI 序列。FLAIR 序列具有轻度的T1 效应,也可应用于头颅MRI 增强[1]。颅内病灶强化主要有三大原理:①脑内病变强化主要为血脑屏障的破坏,导致造影剂渗出到细胞间隙内;②脑外病变的强化主要为组织血供丰富;③软脑膜的强化主要为血管炎症导致造影剂渗出到周围脑脊液中[2]。在增强T1WI 图像上,病灶的强化程度依赖于病灶造影剂的浓度,但达到增强浓度峰值时,病灶强化程度会下降,增强T2 FLAIR 序列,理论上讲其强化程度同造影剂浓度的关系同T1WI不同。增强T2 FLAIR 能否应用于颅脑病变,增强T2FLAIR 对比增强T1WI 在颅脑病变检查中有什么优势,增强T2 FLAIR 病灶强化程度同造影剂浓度有什么样的关系,这些问题为近年来增强T2 FLAIR研究的热点,但研究结果具有很大差异和争议[1-9]。
陈金银等[6]则发现早期脑膜病变时,FLAIR 增强可显示T1WI 增强不能显示的病灶,早期脑膜病变导致血管炎症,造影剂少许漏出,达到了FLAIR增强显示的浓度,未达到T1WI 增强的浓度,此时FLAIR 上脑膜强化为渗出性强化,但在病灶的中晚期脑膜病变明显时,两者强化程度则相仿。孔莹等[10]报道了随着Gd-DTPA 造影次数的增加,小脑核团T1WI 信号增高,间接表明脑造影剂会在脑内核团沉积,Gd-DTPA 还会造成肾源性系统纤维化,因此能否降低造影剂使用浓度为需要解决的问题,Mathews等[3]进行了造影剂浓度同T1WI、FLAIR 强化程度的研究,发现造影剂浓度<0.5mmol/L 时,尤其是在0.01 ~0.1mmol/L 时,T2 FLAIR 序列对低浓度造影剂的显示优于T1WI。Jackson 等[8]发现脑脊液造影剂浓度<0.7mmol/L 时,T2 FLAIR 信号强化大于T1WI,在0.1 ~0.3mmol/L 时这种差异最明显,证实了FLAIR 强化需要较低浓度的造影剂即可达到强化效果。但增强T2 FLAIR 会出现脑脊液搏动伪影,使用3D 技术会减少伪影[9]。但我们发现一例脑胶质瘤病例,FLAIR 增强后病灶同水肿分界不清,张乐乐等[4]也有类似报道,表明病灶周围水肿会影响FLAIR 增强后病灶边界的观察。
本研究中,颅内肿瘤增强T1WI 较增强T2 FLAIR 病灶强化程度更明显,西门子1.5T 上增强T1WI 强化更明显率为75%,GE3.0 为78%。在西门子1.5T 图像上,增强T2 FLAIR 病灶同灰质、脑脊液背景的对比度较增强T1WI 明显,同灰质信号对比率相仿,但GE3.0T 图像上,则出现明显不同,增强T1WI的病灶同灰质信号比率较增强T2 FLAIR明显,与灰质、脑脊液对比率两者则相仿。出现这种明显不同的主要原因为GE3.0 图像上增强前后使用的T1 序列为T1 FLAIR 序列所致。Mathews 等[3]研究39 例颅脑病变,使用仪器为GE 1.5T 磁共振,结果14 例病变T1WI 强化明显,15 例病灶FLAIR 强化明显,这与我们的研究不同,可能因为Mathews 等[3]入组病例中有肿瘤患者、脑膜转移患者和脑膜炎症患者,与本研究入组病例不同。他们也指出脑内肿瘤T1WI会强化更明显,但增强T2 FLAIR 在探索脑表面病变和脑膜病变中有优势。张乐乐等[4]研究了颅脑病变增强Cube FLAIR 与增强T1WI 信号比率的关系,使用的是GE 3.0T 仪器,发现增强Cube FLAIR 上病灶/白质、病灶/灰质的信号比率较增强T1WI明显,这与我们的西门子1.5T 结果相似,与GE 3.0T结果不同,在GE 3.0T 检查中,我们使用的是T1 FLAIR序列,这是导致不同结果的主要原因。该文章[4]还指出增强Cube FLAIR 上脑内原发肿瘤边缘强化明显,而T1WI 则中心强化明显,这与肿瘤血供、造影剂浓度、序列不同有关。
本研究中转移病灶数目两者相同,但梅莉等[5]发现FLAIR 增强可显示T1WI 不能显示的转移病灶,并且能够纠正T1WI 发现的假阳性病灶,这应为FLAIR 增强脑血管为低信号,而T1WI 增强脑表面高信号,有时会误诊为小转移瘤,而FLAIR 弥补了这种不足。我们的研究结果表明,56%的病例增强T2 FLAIR 与增强T1WI 脑膜强化程度相仿,31%的病例增强T1WI 明显,13%的病例增强T2 FLAIR明显。由于本组转移瘤病灶较大,是FLAIR 增强不具有优势的可能原因。
部分脑膜瘤会伴有周围脑实质水肿的改变,此时,需要同脑内肿瘤鉴别,我们发现脑膜瘤T2 FLAIR增强有均匀薄壁样强化的特征,而在其他脑内外肿瘤中无此征象,在其他平扫及T1WI 强化图像上也无此征象,这种征象作为脑膜瘤与其他脑内外肿瘤的鉴别征象,Oguz 等[7]报道的脑膜瘤有此征象,且在>2cm 时出现,另外指出囊样转移瘤也会有该征象。
综上所述,增强T2 FLAIR 病灶与背景信号比率和增强T1WI 有差异,但受检查仪器、序列选择的影响,增强T2 FLAIR 较增强T1WI 优势为:需要较少浓度造影剂即可达到强化效果,可发现早期脑膜强化,区分脑表面转移瘤和脑表面小血管。增强T2 FLAIR 较增强T1WI 不足为:病灶周围水影响边界的判断,脑脊液搏动伪影造成脑膜病变的误判。增强T2 FLAIR 脑膜瘤均匀薄壁样强化征象为与其他肿瘤的鉴别征象。我们的研究肿瘤类别多,1.5T 及3.0T上分组病例数较少,所以未进行肿瘤类别与强化信号强度的比较,这是研究的不足和今后我们继续研究的方向。
