虾壳脱钙预处理工艺的优化研究
2019-02-10陈宏乐占线罗立津王美燕
陈宏,乐占线,罗立津*,王美燕
(1.福建省微生物研究所 环境微生物研究室,福州 350007;2.福建中医药大学,福州 350108)
中国每年因加工对虾而产生大量的虾壳,而虾壳含有丰富的几丁质、钙、虾青素、蛋白质、氨基酸和不饱和脂肪酸等物质[1-2]。虾壳由于含有约20%活性钙质,在利用其中几丁质前必须进行脱钙预处理,目前工业上大规模利用虾壳和虾头制备几丁质和壳聚糖的主要方法是用酸碱法[3],使得丰富的钙质和其他可溶性物质被当作污水随意排放,既污染环境又浪费资源。而钙却是动物体内含量最多且最重要的矿物元素之一[4],虾头、虾壳中的活性钙质可提取出来制备钙营养强化剂。因此,研究如何高效提取虾壳中的钙质资源具有重要的现实意义。果酸钙(Calcium citrate malate, CCM) 是新一代优质钙源,与以往的补钙剂相比,具有高溶解性、高生物利用率、低铁吸收阻碍、口味良好、安全无毒五大特点,是国际公认的优质钙源[5]。刘宏超曾报道了用柠檬酸与苹果酸混合液(摩尔比为2∶3)处理碱提后的虾壳,将活性钙成分制成高生物效价的果酸钙,所得果酸钙的溶解度为0.83 g[6],但其提取的果酸钙的溶解度仍然不高,且该工艺需要先通过碱性有机溶剂处理。本研究通过均匀设计试验对虾壳用柠檬酸-苹果酸混合液脱钙预处理的工艺进行优化,建立条件温和、环境友好、产物溶解度高的虾壳脱钙工艺,从而为虾壳资源综合利用的脱钙前处理提供经济可行的方案。
1 材料与方法
1.1 材料与试剂
新鲜虾壳取自福建东威食品有限公司对虾加工车间,用水冲洗干净,清除黏附在虾壳表面上的血污等杂质,80 ℃烘干后,用粉碎机捣碎,过40目筛备用。其余化学药品:柠檬酸、苹果酸、三乙醇胺、氢氧化钠、钙指示剂、乙二胺四乙酸二钠等均为分析纯。
1.2 指标与检测方法
试验以提取液中的柠檬酸苹果酸钙含量为检测指标,取不同试验条件下反应后的提取液,离心,收集上清液50 mL,加去离子水定容至100 mL,参照国家标准《GB 1903.18—2016 食品安全国家标准 食品营养强化剂 柠檬酸苹果酸钙》检测提取液含钙量[7],以钙指示剂指示终点,用乙二胺四乙酸二钠溶液滴定钙离子,通过待测液颜色由紫红色变为纯蓝色的变化判断反应终点。
1.3 试验方法
1.3.1 混合酸摩尔比选定试验
分别配制(A)0.2 mol·L-1柠檬酸和(B)0.2 mol·L-1苹果酸,A∶B分别按2∶2、2∶3、2∶5 3种比例混合A和B,即得3种混合酸溶液:(1)0.1 mol·L-1柠檬酸,0.1 mol·L-1苹果酸;(2)0.08 mol·L-1柠檬酸,0.12 mol·L-1苹果酸;(3)0.057 mol·L-1柠檬酸,0.143 mol·L-1苹果酸。分别取混合酸溶液200 mL置于500 mL的三角瓶中,每瓶加入40 g虾壳粉(即20%m/V添加量),在60 ℃恒温水浴反应4.0 h。反应结束后,离心,取上清液50 mL,测定溶液中的钙离子浓度,由此选定最佳的混合酸配比。
1.3.2 单因素试验
根据预备试验结果,确定混合酸的最佳配比为苹果酸∶柠檬酸的摩尔比为2∶3,分别配制系列混合酸溶液。以提取液中含钙量为考察指标,分别考察混合酸浓度、虾壳投料量、温度、反应时间对虾壳脱钙效果的影响。具体条件如下:
(1)混合酸总浓度:设定反应温度60 ℃,投料量为20%(m/V),时间4.0 h,分别配制系列混合酸溶液,使其柠檬酸浓度为0.004 mol·L-1、0.01 mol·L-1、0.02 mol·L-1、 0.04 mol·L-1、0.08 mol·L-1、0.16 mol·L-1、0.24 mol·L-1,苹果酸为相应摩尔浓度,即分别为0.006 mol·L-1、0.015 mol·L-1、0.03 mol·L-1、 0.06 mol·L-1、0.12 mol·L-1、0.24 mol·L-1、0.36 mol·L-1,则酸总浓度分别为0.01 mol·L-1、0.025 mol·L-1、0.05 mol·L-1、 0.10 mol·L-1、0.20 mol·L-1、0.40 mol·L-1、0.60 mol·L-1。
(2)虾壳投料量:设定混合酸总浓度为0.40 mol·L-1,反应温度60 ℃,时间4.0 h,虾壳投料量(m/V)分别为1.0%、5.0%、10%、15%、20%、25%、30%。
(3)温度:设定混合酸总浓度为0.40 mol·L-1,投料量(m/V)为10%,时间4.0 h,反应温度分别为30 ℃、40 ℃、50 ℃、60 ℃、70 ℃、80 ℃。
(4)时间:设定混合酸总浓度为0.40 mol·L-1,反应温度40 ℃,投料量为10%(m/V),反应时间分别为0.5 h、1.0 h、2.0 h、3.0 h、4.0 h、5.0 h、6.0 h、7.0 h、8.0 h。
1.3.2 均匀设计试验
在单因素试验基础上,选取X1(投料量)、X2(温度)、X3(酸总浓度)、X4(反应时间)试验因素为自变量,以提取液中钙离子的含量为指标,采取拟水平均匀设计U10*(54)进行试验,检测结果用Design Expert 7.0软件进行数据分析,得到回归方程,预测最优反应条件,并对最优所得条件进行验证试验。
表 1 试验因素水平Table 1 Factors and level of experiment
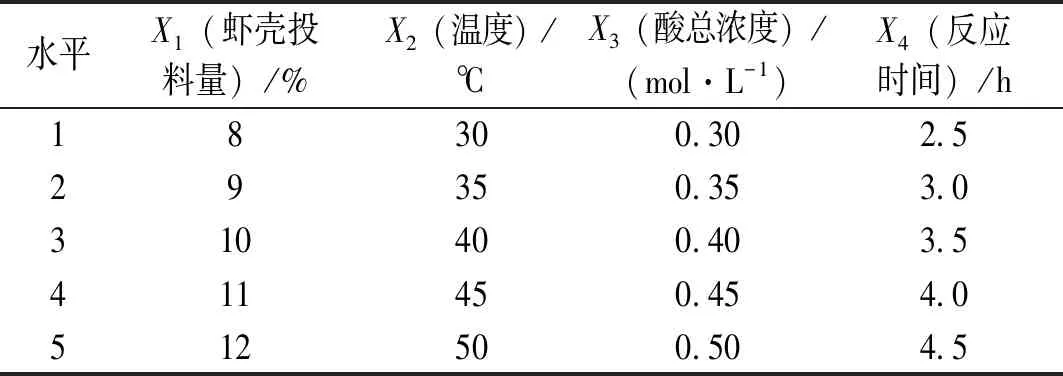
水平X1(虾壳投料量)/%X2(温度)/℃X3(酸总浓度)/(mol·L-1)X4(反应时间)/h18 30 0.302.5 29350.35 3.0 310 40 0.40 3.5 411 45 0.45 4.0 512 50 0.50 4.5
表 2 拟水平均匀设计U10*(54)及试验条件Table 2 Quasi-horizontal uniform design U10*(54)and experimental conditions
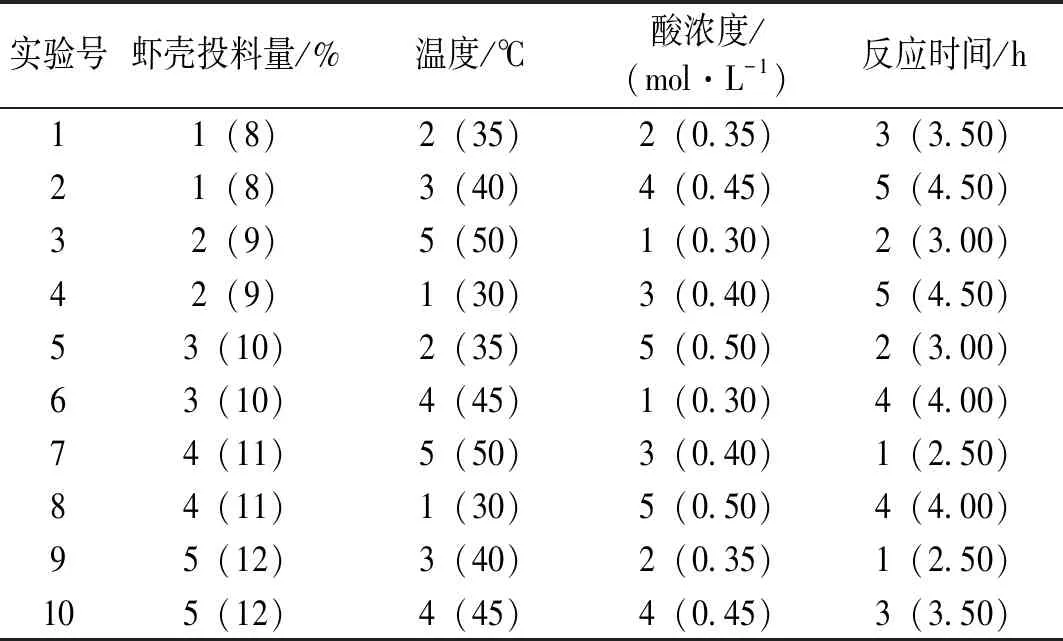
实验号虾壳投料量/%温度/℃酸浓度/(mol·L-1)反应时间/h11(8)2(35)2(0.35)3(3.50)21(8)3(40)4(0.45) 5(4.50)32(9)5(50)1(0.30)2(3.00)42(9)1(30)3(0.40)5(4.50)53(10)2(35)5(0.50)2(3.00)63(10)4(45)1(0.30)4(4.00)74(11)5(50)3(0.40)1(2.50)84(11)1(30)5(0.50)4(4.00)95(12)3(40)2(0.35)1(2.50)105(12)4(45)4(0.45)3(3.50)
1.4 数据分析
上述各项指标取其平均值±标准差为结果。差异性显著分析采用 SPSS软件中Duncan 法进行比较分析,不同小写字母表示组内显著性差异(P<0.05),不同大写字母表示组内极显著性差异(P<0.01)。
1.5 红外光谱定性鉴别
样品的红外光谱采用溴化钾压片法,按照《GB/T 6040-2002 红外光谱分析方法通则》的规定进行试验[8],试样的红外光谱与《GB 1903.18-2016 食品安全国家标准 食品营养强化剂 柠檬酸苹果酸钙》的图谱进行比对。
2 结果与分析
2.1 柠檬酸与苹果酸比例对钙提取率的影响
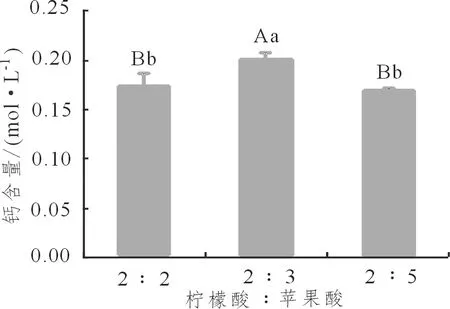
图 1 柠檬酸和苹果酸不同配比 对脱钙效果的影响Figure 1 Effects of different ratio of citric acid and malic acid on decalcification efficiency
由图1可知,在其他反应条件不变的前提下,柠檬酸与苹果酸比例的变化会对虾壳脱钙效果产生影响。当钙和柠檬酸、苹果酸发生络合反应时,其两种酸比例的不同会导致生成的果酸钙的分子结构不同,使得溶解性能有所差异。选定柠檬酸与苹果酸2∶2、2∶3、2∶5 3种配比进行脱钙效果的比较试验,通过实验表明,3种比例之间的钙含量具有极显著性差异,其中2∶3比例是最佳的,所制成的溶液从虾壳中溶出的钙含量最多,钙含量可达到0.199 mol·L-1。依此选定柠檬酸与苹果酸混合的最佳比例为2∶3。
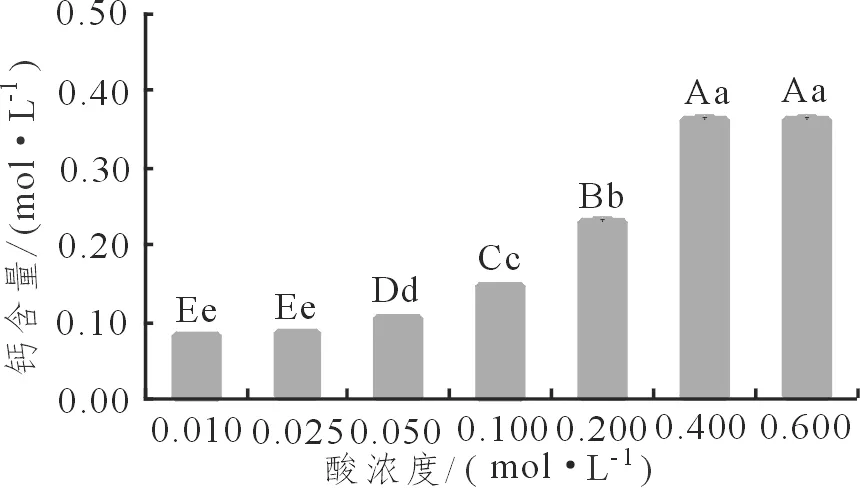
图 2 酸浓度对脱钙效果的影响Figure 2 Effects of acid concentration on decalcification
2.1.1 单因素分析
(1)混合酸浓度对脱钙效果的影响
在实验过程中,观察到当混合酸总浓度为0.60 mol·L-1(即柠檬酸0.24 mol·L-1,苹果酸0.36 mol·L-1)时,虾壳粉会与混合酸溶液反应,可见大量的气泡产生,虾壳粉膨胀。因此,选定的混合酸浓度必须低于0.60 mol·L-1。由图2可知,在其他条件不变的前提下,当混合酸总浓度小于0.40 mol·L-1时,随着混合酸浓度的提高,混合酸从虾壳中溶出的钙含量逐渐提高,当酸总浓度为0.40 mol·L-1时为最大,而当酸浓度大于0.40 mol·L-1时,混合酸溶液从虾壳中溶出的钙含量呈略微下降趋势。故而可知,当混合酸浓度为0.40 mol·L-1时,混合酸溶液从虾壳中溶出的钙最多,提取液钙含量可达0.363 mol·L-1。由此,将0.40 mol·L-1确定为混合酸的最佳浓度。
(2)虾壳投料量对脱钙效果的影响
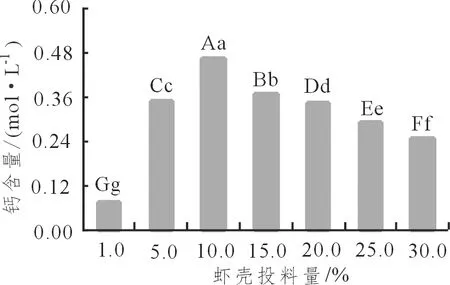
图 3 虾壳投料量对脱钙效果的影响Figure 3 Effects of shrimp shell dosage on decalcification
由图3可知,当投料量小于10.0%(m/V)时,随着投料量的增加,混合酸溶液从虾壳中溶出来的钙含量逐步增加,当投料量大于10.0%时,随着投料量的增加,混合酸溶液从虾壳中溶出来的钙含量逐步减少,在投料量为10.0%时,果酸溶液从虾壳中溶出的钙含量最高,此时果酸钙溶液中的钙离子浓度为0.463 mol·L-1。由此可将10.0%(m/V)确定为虾壳最佳投料量。
(3)反应温度对脱钙效果的影响
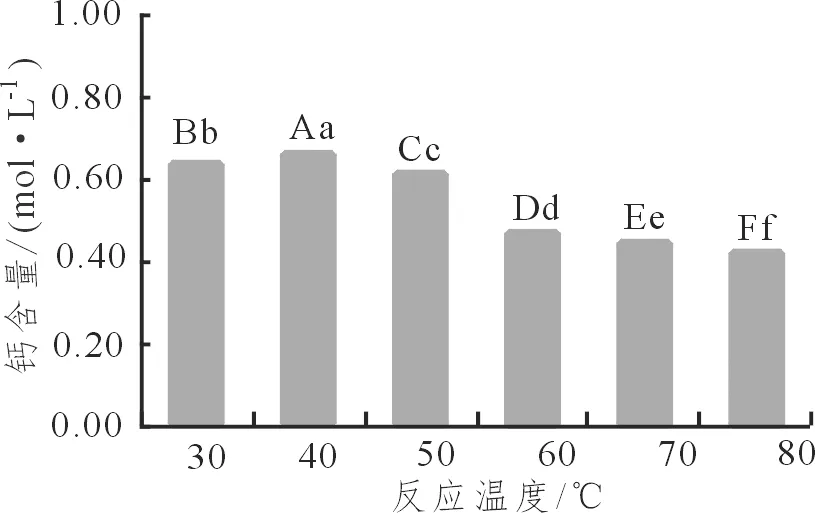
图 4 反应温度对脱钙效果的影响Figure 4 Effects of temperature on decalcification
由图4可知,当反应温度在30~40 ℃时,随着反应温度的提高,果酸钙溶液的钙离子含量增加,当反应温度高于40 ℃时,随着反应温度的提高,果酸钙溶液的钙离子含量反而减少。当温度为40 ℃时,果酸溶液的钙离子浓度为0.659 mol·L-1,由此可将40 ℃确定为最佳反应温度。
(4)反应时间对脱钙效果的影响
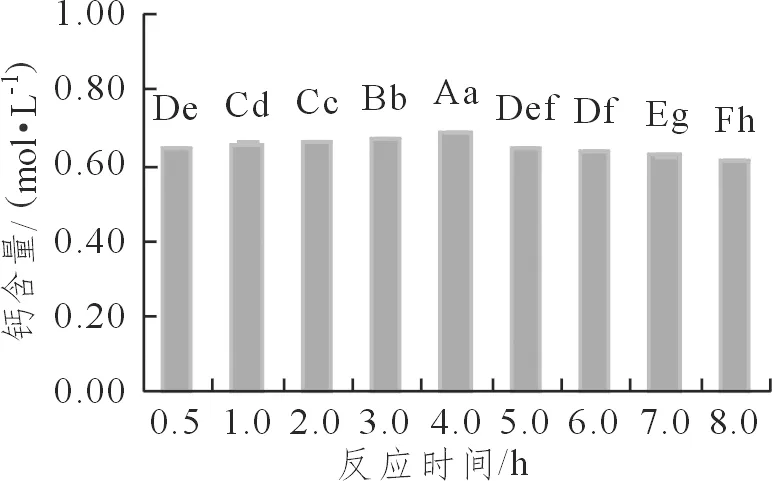
图 5 反应时间对脱钙效果的影响Figure 5 Effects of reaction time on decalcification
由图5可知,在4 h以内,随着反应时间的增加,果酸钙溶液中钙离子含量也逐步增加,当反应时间为4 h时钙离子含量最高达0.687 mol·L-1。当反应时间大于4 h后,随着反应时间的增加,果酸钙溶液中钙离子含量反而减少。因此,将4 h确定为最佳反应时间。
2.1.2 均匀设计试验结果
表 3 均匀设计试验结果Table 3 Uniform design test results

实验号虾壳投料量/%温度/℃酸浓度/(mol·L-1)反应时间/h钙含量/(mol·L-1)18.00 35 0.35 3.50 0.538 28.00 40 0.45 4.50 0.566 39.00 50 0.30 3.00 0.549 49.00 30 0.40 4.50 0.636 510.00 35 0.50 3.00 0.724 610.00 45 0.30 4.00 0.584 711.00 50 0.40 2.50 0.661 811.00 30 0.50 4.00 0.753 912.00 40 0.35 2.50 0.717 1012.00 45 0.45 3.50 0.701
均匀设计是将数论的原理和多元统计相结合创立的一种安排多因素多水平的试验设计,其最主要的优点是可大幅度地减少试验次数,缩短试验周期,从而大量节约人工和费用[9]。本试验涉及4个因素,每个因素取5个水平,若采用正交设计试验,则需用L25(56)表,作25次试验,而选用均匀设计U10*(108),只要作10次试验,借助Design Expert 7.0软件可进行回归分析,依据回归方程可对提取液中钙含量进行预测,从而确定最优参数。
为获得较佳的从虾壳脱钙预处理并制备果酸钙的工艺,需要研究各影响因素及其水平组合对虾壳脱钙效果的影响。因此,在单因素实验基础上进行均匀设计试验。按使用表的推荐用1、3、4、5列。形成拟水平设计表U10*(54)。从表3的均匀设计试验结果可知,实验8(X1=11.00%,X2=30 ℃,X3=0.50 mol·L-1,X4=4.00 h)的钙含量最高,达到0.753 mol·L-1。通过Design Expert 7.0软件分析,经多元一次线性方程逐步回归,得如下回归方程:
Y=0.313 4 + 0.038 5X1-0.003 8X2+ 0.391 0X3-0.017 1X4
(1)
经方差分析得知,F=40.82(P=0.000 5<0.01),回归关系极显著,表明X1(投料量)、X2(温度)、X3(酸浓度)、X4(反应时间)与提取液中钙含量呈极显著的回归关系。
由回归方程可知,X1、X3的系数为正,表明试验指标随因素A、C的增加而增加;X2、X4的系数为负值,则表示试验指标随因素B、D的增加而减少。所以,在确定最优方案时,A、C的取值应偏上限,即X1(投料量)取12.00%,X3(酸浓度)取0.50 mol·L-1;同理,因素B、D的取值应偏下限,即X2(温度)为30 ℃、X4(反应时间)为2.5 h。将以上各值代入上述回归方程,得到Y=0.813,这一结果明显优于表3中的10个试验结果。
2.1.3确证试验结果
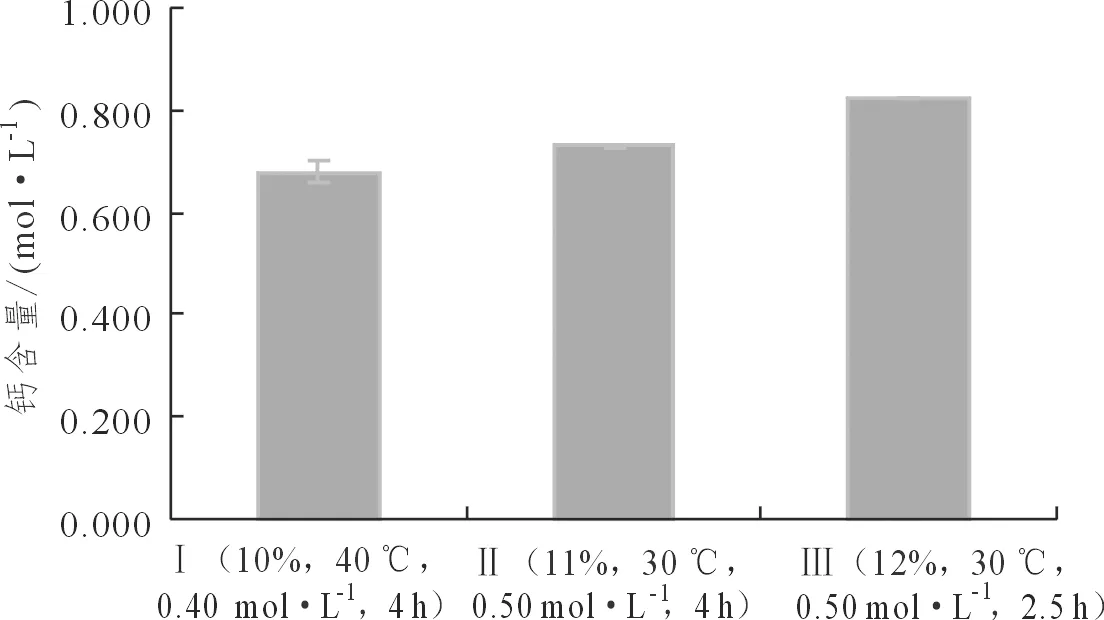
图 6 不同试验条件对脱钙效果的影响Figure 6 Effects of different test conditions on decalcification
表 4 回归模型方差分析Table 4 ANOVA of regression model
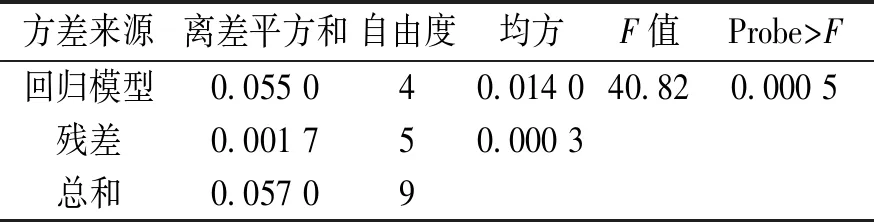
方差来源离差平方和自由度均方F值Probe>F回归模型0.055 0 40.014 0 40.82 0.000 5 残差0.001 7 50.000 3 总和0.057 09
根据回归方程计算得出最佳反应条件,将其与单因素考察最佳条件、均匀设计实验最佳条件进行比较。经确证试验表明,单因素最佳条件Ⅰ(10%,40 ℃,0.40 mol·L-1,4 h)和均匀设计最佳条件Ⅱ(11%,30 ℃,0.50 mol·L-1,4 h)的钙离子浓度分别为0.679±0.021 mol·L-1和0.729±0.001 mol·L-1。根据方程预测最佳条件Ⅲ(12.00%,30 ℃,0.50 mol·L-1,2.5 h)下,溶液中钙的含量确实高于单因素考察最佳条件、均匀设计实验最佳条件,溶液中钙含量达到了0.822±0.002 mol·L-1,略高于理论值。因此,采用此模型优化得到的参数准确可靠(表4),具有实用价值。
2.1.4 果酸钙结晶的红外光谱图
将制得的果酸钙溶液置于-18 ℃冷冻结晶,干燥后,经溴化钾压片法进行红外光谱定性分析,得图7所示光谱图。参考标准[7]进行比对可见,所得谱图与柠檬酸苹果酸钙标准红外光谱图基本一致。由于多分子缔合O-H形成很强的氢键,在3 100~3 500 cm-1区域形成很强、很宽的吸收谱带;由于含有C=O基,在1 540~1 620cm-1区域出现很强的C=O伸缩振动吸收谱带;由于含有的C-O基,在1 100~1 300 cm-1区域之间有几条谱带。
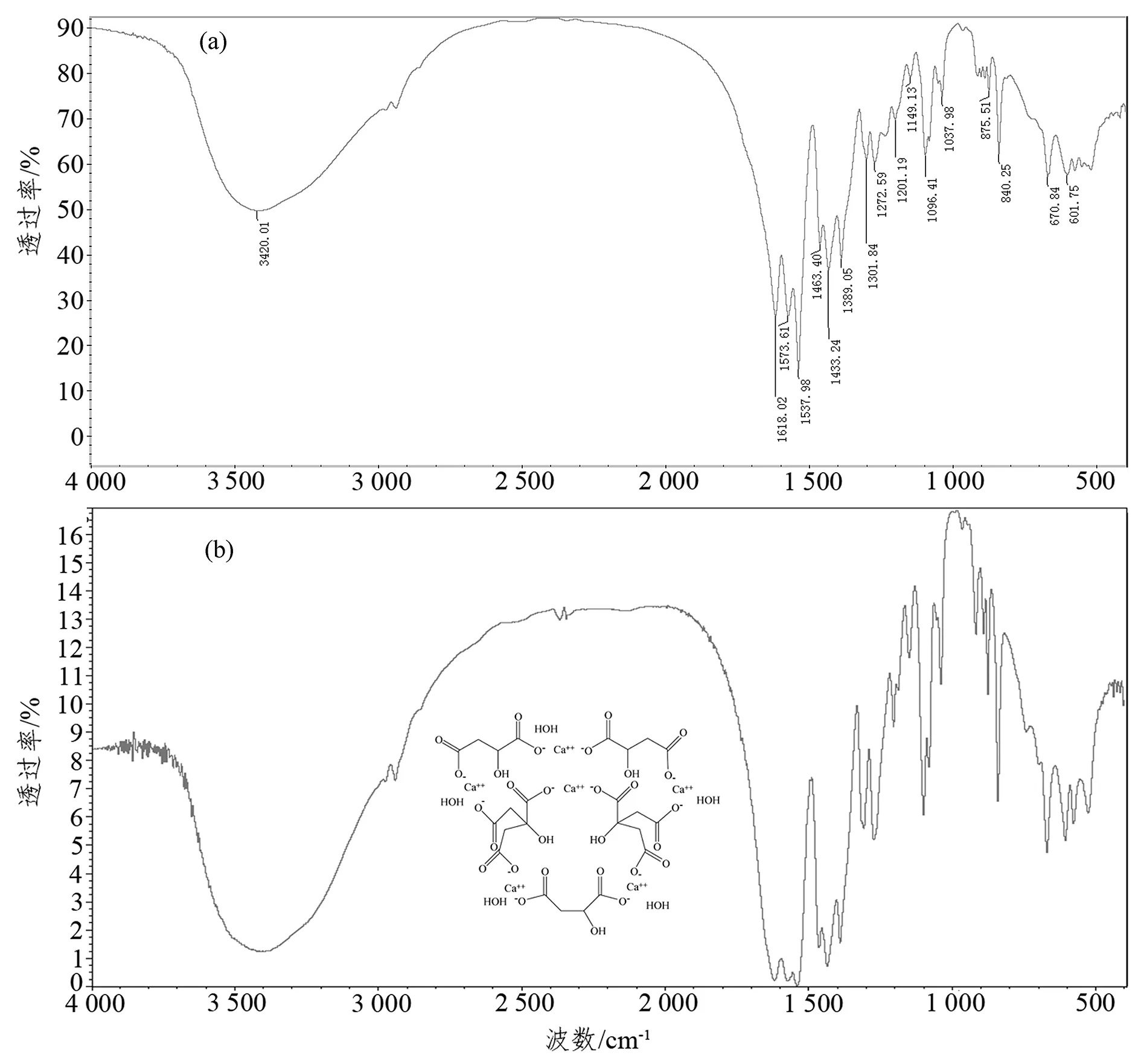
注:(a)实验制得结晶样品的红外光谱图;(b)标准[7]柠檬酸苹果酸钙红外光谱图。图 7 柠檬酸苹果酸钙红外光谱Figure 7 Infrared spectrum of calcium citrate malate
3 结论与讨论
果酸钙(Calcium Citrate Malate , CCM) 是新一代优质钙源。1993年美国专利“果酸钙的合成”首次公布了使用柠檬酸、苹果酸、碳酸钙生成柠檬酸-苹果酸钙复合盐的合成技术方案[10]。国内也有不少的学者进行利用鸡蛋壳、贝壳、牡蛎壳、蟹壳等活性钙质资源制备果酸钙的研究,如,段惠敏将鸡蛋壳通过950 ℃高温煅烧获得蛋壳灰分(CaO),再将其与柠檬酸、苹果酸反应制得果酸钙[11];殷蓉、汪之和等也分别报道了以鸡蛋壳为原料获得了制备果酸钙的不同工艺[12-13],张光杰等采用二次回归正交设计优化鸡蛋壳制备柠檬酸-苹果酸钙的工艺[14];张振谦通过正交实验得到采用中药牡蛎壳及花蛤壳制备柠檬酸-苹果酸钙的最佳原料比、反应条件及结晶条件[15];潘荣楷报道了采用一次煅烧法研究并改进了以贝壳为原料制备苹果酸钙的工艺条件[16];卢进峰报道了对梭子蟹壳中提取甲壳素产生的含钙溶液进行钙回收,制备果酸钙的工艺研究[17]。本研究通过均匀设计选定了虾壳脱钙的最优试验条件,即投料量12.33%,30 ℃,酸浓度0.50 mol·L-1,2.5 h,制得的果酸钙溶液中钙含量达到了0.822±0.002 mol·L-1,高于已有的文献报道。如刘宏超利用虾壳制备果酸钙,选取温度55 ℃,反应10 h,所得到的果酸钙溶解量8.3 mg·mL-1[6];卢进峰利用梭子蟹壳制备果酸钙,在50 ℃反应2.5 h所得果酸钙溶解量9.635 mg·mL-1[17];张光杰等优化后鸡蛋壳制备柠檬酸-苹果酸钙的工艺,选定温度44.6 ℃,所得果酸钙溶解量为0.356 mol·L-1[14]。比较反应条件,经本研究优化的制备工艺,条件温和(30 ℃),时间短(2.5 h),明显提高了虾壳的脱钙效率,为后续的虾壳发酵制备壳聚糖酶和壳寡糖提供了很好的前处理工艺参数。制备所获得的果酸钙溶液,除了果酸钙外,还含有其他营养物质,经干燥后,也可用于畜禽养殖的营养强化剂。
