精准微创的人工耳蜗植入手术
2019-01-14戴朴蒋刈
戴朴 蒋刈
1中国人民解放军总医院耳鼻咽喉头颈外科(北京100853)
2福建医科大学省立临床医学院、福建省立医院耳鼻咽喉科(福州350001)
人工耳蜗植入是治疗重度-极重度感音神经性耳聋的最主要手段,在全球已经有六十万人植入了人工耳蜗,获得了巨大的收益。随着人工耳蜗临床领域的不断扩展,如何进一步提高人工耳蜗植入术的疗效、降低手术并发症、保留残余听力、实现微创是人工耳蜗植入实践的发展目标,微创人工耳蜗植入术手术技巧为其中的一个重要研究方向,术前术后的准确评估是实现精准微创不可缺少的一部分。
随着精准医学概念的提出,微创手术从原来的微创手术入路,到“柔”手术电极植入保留残余听力,发展到现在的疑难耳蜗的精准定位及保留内耳精细结构的微创电极植入。为实现精准微创的耳蜗植入,对耳蜗候选者的术前评估、术中操作和术后康复均提出越来越高的要求。
1 微创耳蜗植入手术设计
微创人工耳蜗植入(minimally invasive cochlear implantation,MICI)自2002年O'Donoghue和Nikolopoulos[1]首先提出针对Nucleus24的小切口微创技术以来,国内外众多专家发表文献报道小切口设计及皮瓣设计,其目的除了外观美观外,还能降低皮瓣感染等并发症。近些年来,更多专家指出微创不单指外观上切口小,更指微创开窗、微创植入,尽可能做到对耳蜗内结构创伤最小。
笔者认为要实现术后切口美观、耳蜗内精细结构和残余听力保护、减少并发症等微创外科目标,需要按照微创理念设计的标准操作步骤进行人工耳蜗植入手术。我们所设计的微创手术的核心内涵包括:两层切口三层缝合的设计,通过肌骨膜瓣对植入体和术区形成完全覆盖的保护,降低严重的皮瓣并发症发生;通过磨制形状深度合适的植入体骨床、固定植入体的设计,降低植入体突起移位对皮瓣的刺激作用;通过电极植入的“柔”手术操作和围手术期用药,尽可能保护内耳精细结构。按照笔者的微创理念设计的标准操作步骤进行的人工耳蜗植入手术,应用于1,065例耳蜗植入患者,严重并发症仅为0.7%,并且没有严重皮瓣感染和植入体脱出的发生,并发症发生率远低于已知国内外文献报道水平[2],为安全有效的人工听觉植入临床提供了可靠的选择。
2 保留残余听力的人工耳蜗植入
大量的临床研究已经证明人工耳蜗植入术后低频听力的保留是可行以及必要的,但仍有耳蜗植入患者出现残余听力丧失的情况[3-7]。人工耳蜗植入术后残余听力损失的可能原因,包括耳蜗造口术时的声损伤、电极插入导致的机械损伤(包括蜗轴及骨螺旋板骨折、基底膜或骨螺旋板撕裂)。其他可能的原因包括耳蜗内液体动态平衡紊乱,细菌感染,新骨形成,或由于耳蜗对电极成分、骨屑或血液的异物反应而导致的耳蜗纤维化[8、9]。保留残余听力的方法是针对人工耳蜗术后残余听力丧失的原因采取相应的措施,避免或尽量减轻电极植入时和植入后耳蜗内的损伤。然而,耳蜗术后残余听力保存不仅与术者操作技巧有关,也和术前患者低频残余听力范围相关。由于各治疗中心纳入的具有残余听力的人工耳蜗植入候选者指征存在差异,可能导致术后残余听力保存率的不一致[8-11]。电极植入路径如圆窗或耳蜗开窗入路和电极植入长度对残余听力保留的影响,也是一直争论的焦点[12、13]。
笔者认为,选择合适的耳蜗电极、电极植入途径、植入速度、围手术期用药是保护耳蜗内结构完整、保存残余听力的关键。根据电极设计选择如直电极、弯电极选择相应的耳蜗开窗方式,均有可能实现残余听力保存。笔者自2011年按照微创理念设计的标准操作步骤对29例有残余听力的患者行微创人工耳蜗植入术,根据选择的耳蜗品牌分别采用圆窗植入和圆窗前下开窗的“进极止芯”技术,其中25例随访18个月后,低频残余听力保留率100%,完全保留率72%(18/25),部分保留率28%(7/25)。17例听力随访4年后,有4例出现残余听力丧失,低频残余听力保留率76.5%(13/17),完全保留率58.8%(10/17),部分保留率17.6%(3/17)。
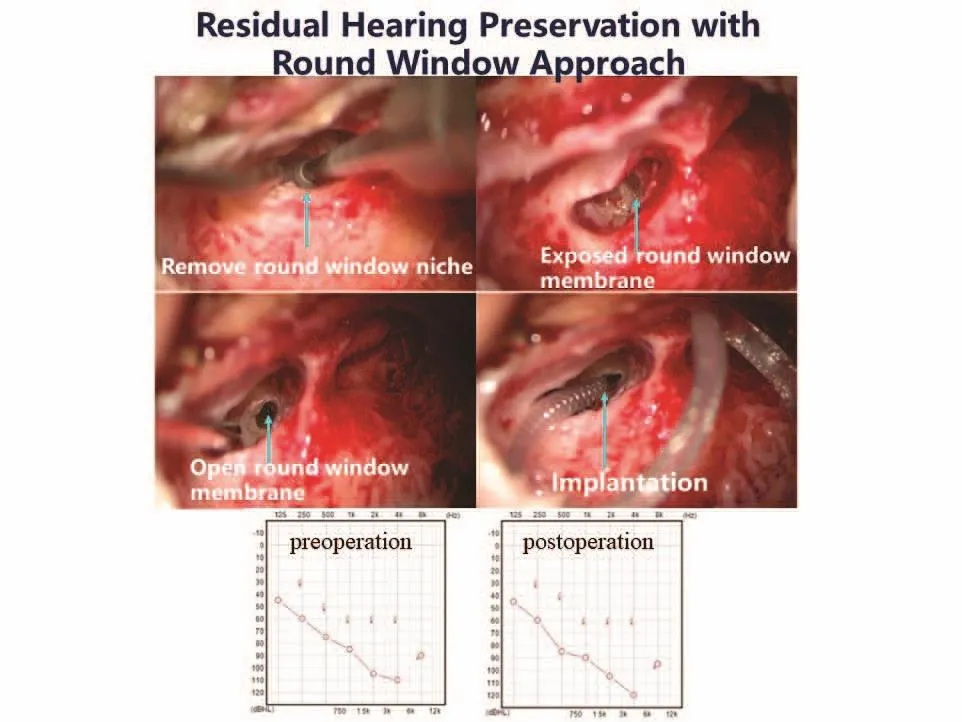
图1 患者,女,11岁,大前庭水管综合征。采用奥地利MED-EL F28超软电极,经圆窗入路,术后残余听力完全保留Fig.1 Patient1,female,11 years old,with enlarged vestibular aqueduct syndrome.In this case,the residual hearing was completely preserved through the round window approach by using MED-EL F28 flexsoft electrode

3 内耳畸形分类标准及耳蜗植入
内耳是人体听觉和平衡感觉的重要器官,内耳功能和结构的异常是导致感音神经性耳聋的主要原因,在所有的感音神经性耳聋患者中,伴有内耳畸形的患者约占总数的20%[14]。然而由于内耳结构复杂,尚未形成内耳畸形统一分类共识。国际上最早报道内耳畸形分类方法是Jackler等1987年报道的[15],主要依据是内耳的胚胎发育过程结合多轨迹体层扫描,将内耳畸形分成伴有耳蜗畸形的内耳畸形和不伴有耳蜗畸形的内耳畸形两大类。目前,国内的许多教材和专著沿用较老的耳蜗畸形分类方法,根据畸形的严重程度分为米歇尔畸形(Michel dysplasia)、蒙底尼畸形(Mondini dysplasia)、宾-亚历山大畸形(Bing-Alexander dysplasia)、赛贝畸形(Scheibe dysplasia)。但以上分类并不能涵盖已知的所有内耳畸形。随着影像技术发展,CT和MRI对骨性和神经结构有较高的分辨能力,拓宽了对内耳畸形的理解,陆续有关于内耳畸形分类标准的设计。其中,目前在临床运用最广的内耳畸形分类方式,是Sennaroglu教授提出并不断修正的分类方法。
Sennaroglu对耳蜗、前庭、半规管、內听道、前庭导水管和耳蜗导水管的畸形进行系统分类[16],其中根据耳蜗前庭发育程度不同分为:耳蜗和前庭完全缺失的Michel畸形;耳蜗完全缺失前庭不同程度发育的耳蜗未发育;耳蜗和前庭形成囊性结构的共同腔畸形;耳蜗和前庭分化,但根据耳蜗大小、耳蜗内蜗轴和蜗管内间隔发育程度,又分为四种类型的耳蜗发育不全和三种类型的耳蜗分隔不全。
4 耳聋基因诊断与畸形耳蜗的诊断及人工耳蜗植入效果的评估
内耳发育畸形表型多样,致病基因通过不同途径参与内耳的发生和发育过程。大量研究表明大前庭水管综合征(前庭水管扩大、Pendred综合征和耳蜗分隔不全II型(IP-II))是由SLC26A4基因突变导致的常染色体隐性遗传性疾病[17],部分由POU3F4基因导致的X连锁隐性遗传疾病的耳蜗分隔不全Ⅲ型(IP-Ⅲ)[18],是通过颞骨CT和分子诊断均可以明确的内耳畸形,也是通过影像学方法能够诊断的遗传性耳聋。与耳聋相关的综合征中,既往有报道携带有SOX10突变的WS患者存在双侧内耳异常,颞骨影像学检查以半规管的缺如和发育不全、前庭导水管扩大以及耳蜗发育不良较常见[19];携带EYA1基因突变的腮耳肾综合征患者存在不同程度的耳蜗发育不良、前庭导水管扩大和面神经移位[20];携带CHD7基因突变的CHARGE综合征患者存在不同程度的半规管发育畸形伴随耳蜗发育不良[21]。通过不同内耳畸形的致聋基因研究,有助于阐释在胚胎发育不同时期,基因对内耳形态功能的影响[22],同时可以协助临床精准诊断。
重度-极重度感音神经性耳聋助听器无效或效果不佳的患者,主要康复手段是人工耳蜗植入,然而不同个体术后效果仍有差异,究其原因除了植入年龄外,不同基因突变影响从耳蜗到听神经范围内不同的病变部位功能可能是其另外的关键因素。在大样本患者群体分析人工耳蜗植入术后效果与不同耳聋基因及其突变类型的相关性,对于预估植入效果、使患者及其家庭有合理的预期十分必要。笔者团队正在进行2,267例人工耳蜗植入患者的基因检测结果及术后听觉言语康复效果的分析,初步发现携带GJB2、SLC26A4、OTOF、TMPRSS3等主要表达于内耳的基因突变的患者耳蜗植入术后言语康复效果佳,而携带同时表达于耳蜗及脑组织的基因ATP6V1B2突变的患者耳蜗植入术后言语康复效果欠佳;与凝血功能相关的耳聋基因PTPN11突变携带者可能易于出血,针对其的耳蜗植入要加强术中及术后出血的防控;对于确诊染色体10q26缺失综合征(OMIM 609625)的患者,因该病涉及严重全身感染倾向,术前需要将此风险向患者家庭交代。由此可见,基因诊断可以为人工耳蜗候选者提供个性化治疗方案,包括全身状况和耐受能力的评估、人工耳蜗术后效果评估、治疗方法及人工耳蜗设备的选择。
5 标准层面的影像重建与耳蜗植入评估
CT是临床工作者用于诊断内耳结构性病变的主要方式。高分辨率螺旋CT对辨识内耳精细结构有较好的帮助[23],并且根据不同需求可运用不同的后处理技术提升显示效果:曲面重组技术可以对颞骨内面神经走行或者听小骨连接等结构全程显示;表面遮盖显示及CT仿真内窥镜显示技术能够多角度、多方位地观察显示听小骨的立体形态;多平面重组技术(multiple planar reformation,MPR)在保持与原图质量一致的前提下,可构建出所需观测结构的任意层面[24],相对于轴位和冠状位图像,MPR重建图像对于内耳结构的显示更加清晰和直观,可避免不同头位角度对图像的影响和测量误差,提高内耳畸形的分型和测量准确率[25]。MPR重建操作简便且不易受人为因素影响[26],但如果没有构建正确的标准层面进行重建,还是会导致测量值与真实值之间存在误差。国内外学者[27、28]已尝试通过影像重建的方法对耳蜗、前庭及半规管等内耳结构进行测量,因对耳蜗结构层面的定位标准不同,测量结果存在差异。
笔者课题组通过构建耳蜗三个标准的测量层面:耳蜗底转长轴层面、耳蜗底转层面及蜗轴中轴层面,对正常人群内耳进行MPR标准层面测量,观察耳蜗轮廓、蜗轴、蜗管内间隔及蜗孔等结构。测量数据在其中一个层面上通过相交的另外两个层面测得一致的数据,可印证层面确立的准确性,避免测量误差和层面构建的误差。同时构建出前庭外半规管层面、上半规管层面及后半规管层面,检测前庭及三个半规管的大小。通过测量耳蜗、前庭、半规管及內听道大小,测量蜗轴及蜗管内间隔的长度,评估内耳精细结构。尤其是对于耳蜗发育不良和耳蜗分隔不全两类畸形,对耳蜗外径、蜗管内间隔和蜗轴的精确测量,是做出正确诊断和准确分型的关键。这项影像层面构建和测量原理与近期面市的奥地利公司的Otoplan软件测量思路不谋而合。
标准层面的MPR重建,除了在耳蜗植入前用于分析耳蜗的精细结构差异,对植入电极的长度进行预测,还可以用于耳蜗植入后对电极植入位置的评估,判断电极对基底膜、蜗轴等耳蜗内精细结构的损伤,实现耳蜗精准植入的评估。
综上所述,微创人工耳蜗植入的手术方法,通过良好的手术径路设计,大大减少人工耳蜗植入的皮瓣并发症,解决了手术的安全性问题,使得医生、患者和家长对人工耳蜗植入更有信心。通过“柔”手术技巧植入电极的方式,能够保护耳蜗内精细结构和残余听力,大大提升人工耳蜗植入后的助听效果和言语分辨率,并为未来的基因治疗和毛细胞再生技术的应用创造良好的基础。通过对内耳畸形分类的标准化探索,以及影像重建对耳蜗结构及植入后电极位置的研究,有望实现个体化电极选择和精准电极植入。耳聋基因诊断的深入广泛研究可能将耳聋的病因分析和植入侧别选择、植入效果预测结合起来,使得耳聋康复更加精准。
