过表达低氧诱导因子-1α(HIF-1α)对体外培养人视网膜血管内皮细胞增殖、炎症反应及血管生成的影响
2019-01-10蔡晖石华宗杨豫湘
蔡晖 石华宗 杨豫湘
视网膜新生血管形成是导致糖尿病视网膜病变、眼底血管栓塞、青光眼等疾病视力丧失的重要原因之一[1-3]。视网膜新生血管的形成是极其复杂的过程,伴随出血、渗出及增殖等病理性改变[4]。研究发现,血管内皮细胞的增殖、迁移及炎症反应是新生血管形成过程中最为重要的环节[5],且人视网膜血管内皮细胞(human retinal capillary endothelial cell,HREC)是研究视网膜新生血管形成过程必不可缺的细胞系之一。已有研究报道,低氧诱导因子-1α(hypoxia inducible factor 1 alpha,HIF-1α)是细胞感受氧含量高低并作出调控反应的关键性分子,具有调节细胞内pH、促进血管生成、诱导自噬、调控凋亡、自身免疫以及促进间充质干细胞自我更新与分化的功能[6-8]。目前关于HIF-1α在HREC中的功能尚不清楚,本研究拟通过在体外培养HREC过表达HIF-1α,同时采用四甲基偶氮唑蓝比色法(MTT)、酶联免疫吸附实验(ELISA)和Western blot分别检测其对HREC增殖、炎症反应及血管生成的影响,为视网膜血管性疾病的治疗提供新的实验依据。
1材料与方法
1.1材料HREC(中山大学中山眼科中心提供),pEGFP-HIF-1α重组载体及pEGFP-C1空白载体(赛业生物科技有限公司),肿瘤坏死因子(tumor necrosis factor,TNF)-α、白细胞介素(interleukin,IL)-1β及IL-6 ELISA试剂盒(Thermo Fisher Scientific,美国),血管内皮生长因子(vascular endothelial growth factor,VEGF)及GAPDH抗体(Abcam),DMEM培养基及胎牛血清(Thermo Fisher Scientific,美国),胰岛素-转铁蛋白-硒添加物(上海艾研生物科技有限公司),内皮细胞生长因子 (上海伟进生物科技有限公司),青霉素、链霉素、MTT及DMSO(Sigma,美国),Lipofectamine 3000转染试剂(Thermo Fisher Scientific,美国),RNA提取试剂盒(Trizol,美国),逆转录试剂盒及荧光定量PCR试剂盒(Takara,日本)。电泳仪(BIO-RAD,美国),E-Gel Imager凝胶成像系统(Invitrogen,美国),ABI 7100荧光定量PCR仪(ABI,美国),细胞培养箱和超净工作台(BIO-RAD,美国),酶标仪(Thermo Fisher Scientific,美国)。
1.2体外培养HRECHREC采用DMEM培养基及体积分数10%胎牛血清于37 ℃、含体积分数5%CO2细胞培养箱中培养,并添加胰岛素-转铁蛋白-硒添加物、内皮细胞生长因子、青霉素(100×103U·L-1)及链霉素(0.1 g·L-1)。常规传代、接种及铺板。
1.3细胞转染待HREC传代至第3-4代时,取对数期生长的细胞进行转染,具体操作如下:取HREC进行6孔板铺板,每孔细胞数约为500×103个,常规培养细胞24 h后,依照Lipofectamine 3000转染试剂操作流程分别转染pEGFP-HIF-1α重组载体和pEGFP-C1空白载体,转染6 h后更换细胞培养液,待转染48 h后收集细胞。
1.4MTT实验取HREC进行96孔板铺板,每孔细胞数约为6000个,细胞培养及转染同上,连续4 d每孔每天加入14 μL MTT(5 g·L-1),细胞培养箱孵育4 h后去掉上清,随后每孔加入150 μL DMSO,在细胞培养箱孵育15 min,最后采用酶标仪测定各组480 nm波长时的吸光度(A)值。
1.5ELISA实验取HREC进行6孔板铺板,细胞培养及转染同上,待转染48 h后收集细胞。参照Thermo Fisher Scientific提供的TNF-α、IL-1β及IL-6 ELISA试剂盒检测各组HREC中TNF-α、IL-1β及IL-6蛋白的含量。
1.6Western blot检测提取HREC总蛋白,常规定量和变性。制备120 g·L-1SDS聚丙烯酰胺凝胶,常规上样、电泳、转膜及封闭,加入抗VEGF及GAPDH一抗4 ℃孵育过夜,TBST洗涤3次,37 ℃孵育二抗 1 h,再次TBST洗涤3次,暗室添加ECL发光液孵育20 s及曝光拍照。
1.7荧光定量PCR实验提取HREC总RNA,逆转录为cDNA,以合成的cDNA作为模板在ABI 7100荧光定量PCR仪上进行定量实验。扩增条件为:98 ℃ 10 min,随后95 ℃ 10 s,55 ℃ 30 s,72 ℃ 30 s,共46个循环。HIF-1α 上游引物:5’-GTTACAGTATTCCAGCAGA-3’,下游引物:5’-GTATGTGGGTAGGAGATG -3’;GAPDH上游引物:5’-TCAAGAAGGTGGTGAAGC-3’,下游引物:5’-AAGGTGGAGGAGTGGGT-3’。反应体系如下:无RNase去离子水 10 μL、cDNA 1 μL、上游引物和下游引物各0.5 μL及SYBR premix 8 μL。

2结果
2.1过表达HIF-1α对体外培养HREC中HIF-1α mRNA和蛋白表达的影响转染人工合成的pEGFP-HIF-1α重组载体或pEGFP-C1空白载体至HREC,并通过荧光定量PCR检测细胞中HIF-1α mRNA和蛋白表达的变化。结果发现,转染pEGFP-C1后HREC中HIF-1α mRNA的表达量为0.50±0.08,而转染pEGFP-HIF-1α后HREC中HIF-1α mRNA表达量为4.63±0.92,差异有统计学意义(P<0.05)。Western blot检测亦发现体外转染pEGFP-HIF-1α可显著增加HREC中HIF-1α蛋白表达(P<0.05)。见图1。
2.2过表达HIF-1α对体外培养HREC增殖的影响过表达HIF-1α可显著促进体外培养HREC增殖,HREC转染pEGFP-HIF-1α后24 h、48 h及72 hA值分别为0.34±0.04、0.57±0.04、0.83±0.05,而HREC转染pEGFP-C1后24 h、48 h及72 hA值分别为0.26±0.03、0.44±0.04、0.61±0.04,两者相比差异均有统计学意义(均为P<0.05)。

图1过表达HIF-1α对体外培养HREC中HIF-1α蛋白表达的影响
2.3过表达HIF-1α对体外培养HREC炎症反应的影响转染pEGFP-HIF-1α后HREC中TNF-α、IL-1β及IL-6蛋白的表达较转染pEGFP-C1后均显著增加,两者相比差异均有统计学意义(均为P<0.05)。结果见表1和图2。

表1TNF-α、IL-1β及IL-6蛋白的表达变化
2.4过表达HIF-1α对体外培养HREC血管生成的影响Western blot检测显示(图3),过表达HIF-1α可显著增加体外培养HREC中VEGF蛋白表达,转染pEGFP-HIF-1α后HREC VEGF蛋白的表达为6.72±0.96,而转染pEGFP-C1后HREC VEGF蛋白的表达为2.31±0.47,差异有统计学意义(P<0.05)。
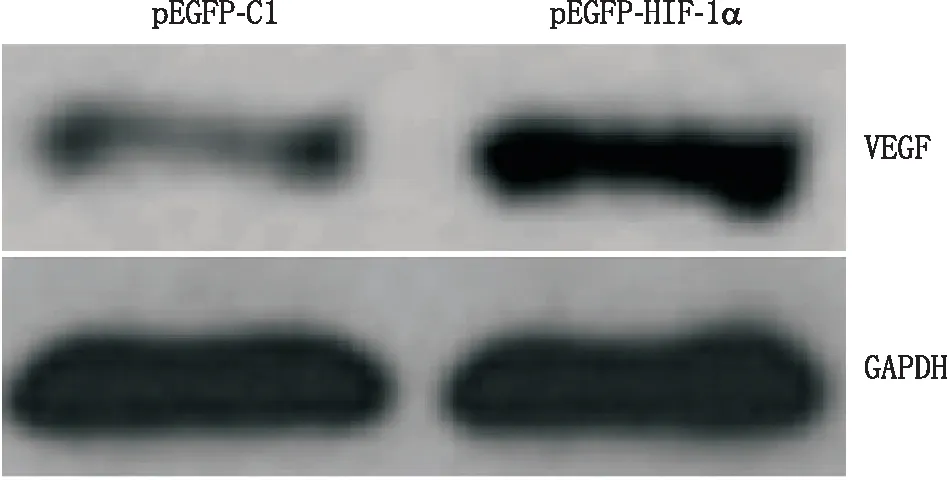
图3过表达HIF-1α对体外培养HREC中VEGF蛋白表达的影响
3讨论
视网膜新生血管性疾病是当今世界范围最主要的致盲性眼病之一,随着我国老龄化程度的提高,其发病率呈明显上升趋势,严重危害人们的身体健康。视网膜新生血管的形成是一个复杂的病理生理过程,缺氧、缺血及高糖状态是诱导视网膜新生血管形成的重要因素[9-10]。HIF-1α是主要的氧调节亚基,在常氧状态下易经泛素酶体途径降解,表达水平较低;而在低氧状态下可与一些基因的氧反应元件(hypoxia response element,HRE)结合,激活细胞内多种低氧反应因子的表达,从而使细胞适应低氧环境[11-12]。
已有研究发现,HIF-1α在大多数癌组织呈现高表达状态,如肝癌、胰腺癌、乳腺癌和肾癌等,HIF-1α可作为这些肿瘤治疗新的分子靶点[13-15]。HIF-1α在其他疾病,如骨折、牙周炎、冠心病和脑缺血性疾病中等亦呈高表达,提示其在这些疾病中亦发挥着重要的调控作用[16-17]。最新研究发现,上调HIF-1α表达可改善心肌和小肠缺血-再灌注损伤[18-19]。HREC与牛视网膜血管内皮细胞相比,具有人体代表性,是研究视网膜新生血管形成过程必不可缺的细胞系之一。目前关于HIF-1α在HREC中的功能尚不清楚,本研究旨在探讨过表达HIF-1α对体外培养HREC增殖、炎症反应及血管生成的影响。
通过MTT实验,我们发现过表达HIF-1α可显著促进体外培养HREC增殖。该结果与过表达HIF-1α促进肿瘤细胞生长的结果一致。细胞因子介导的炎症反应在视网膜新生血管的形成中起着重要作用,TNF-α、IL-1β及IL-6是参与炎症反应的主要细胞因子。本研究发现,过表达HIF-1α可显著增加HREC中TNF-α、IL-1β及IL-6的表达水平,提示过表达HIF-1α可促进体外培养HREC炎症反应。VEGF是必不可少的血管生成因子,可增加内皮细胞的通透性,诱导血管扩张,使血浆蛋白形成纤维蛋白网。VEGF亦能诱导一些基因的表达,产生与细胞迁移、组织重塑有关的蛋白酶,参与新生血管的形成。本实验通过Western blot检测结果发现,过表达HIF-1α可显著增加体外培养HREC中VEGF蛋白表达,提示过表达HIF-1α可增加体外培养HREC血管生成。
综上所述,本研究通过检测过表达HIF-1α对体外培养HREC增殖、炎症反应及血管生成的影响,首次发现过表达HIF-1α可显著促进体外培养HREC增殖、炎症反应及血管生成,该研究将为视网膜血管性疾病的治疗提供新的实验依据。
