防己中不同活性成分综合性实验设计
2019-01-09俞媚华达慎思
俞媚华, 熊 娟, 达慎思
(复旦大学 药学院, 上海 201203)
防己是防己科千金藤属植物粉防己StephaniatetrandraS. Moore的干燥根,早在《神农本草经》中对其就有记载“防己如险健之人,幸灾乐祸,能首为乱阶,若善用之,亦可御敌。其名或取此义。解离,因其纹解也”[1]。民间传统将其用于治疗风湿关节疼痛,湿热肢体疼痛,现代医学研究又发现其具有镇痛、消炎、抗过敏、降血压和保护心肌等作用[2]。防己中含有大量的生物碱,其中大部分是双苄基异喹啉生物碱,汉防己甲素和乙素含量较高,活性也最佳[3]。
“汉防己生物碱的提制和鉴定”一直是复旦大学药学院“实验药物化学I”一个较为经典的实验[4],要求学生掌握总生物碱中酚性叔胺碱和非酚性叔胺碱分离与纯化的方法,了解生物碱类化学成分的沉淀反应,是一个专业性较强的基础实验。但该实验存在一些问题:属验证性实验,学生只需按部就班地完成实验,记录实验现象,专业综合知识得不到体现;实验前学生仅从课本中了解防己药材中含生物碱类成分,没有实验的感性认识;防己药材利用萃取、重结晶的方法进行提取和粗分离,只能得到汉防己甲素和乙素的混合物,不能完全分开;没有化合物的纯化和纯度测定步骤,学生对化合物纯度没有概念;几乎没有使用任何精密的大型仪器。显然这样的实验已经不能满足现行天然药物化学实验教学要求,因此将这个实验设计为综合性实验,使学生将所学的天然药物化学、药物分析学、现代色谱技术、波谱解析等多门课程的知识在实验中综合应用,提高了学生实验技能。
1 防己中不同活性成分综合性实验设计简介
1.1 实验目的
(1) 掌握脂溶性酚性生物碱与非酚性生物碱的提取分离方法;
(2) 了解正交试验优选防己中汉防己甲素和乙素的提取工艺;
(3) 学习柱色谱分离汉防己甲素和乙素;
(4) 熟悉生物碱的一般理化性质及各种检识方法。
1.2 实验原理和主要内容
本实验利用正交实验优选防己中汉防己甲素和乙素的最佳提取工艺,强化天然药物化学中提取这一关键步骤;防己中叔胺型生物碱的亲脂性,采用有机溶剂萃取分离脂溶性生物碱和亲水性生物碱;利用汉防己甲素和乙素结构上的差别——7位取代基的差异,采用柱色谱分离二者[5-6];利用高效液相色谱仪(HPLC)评价防己正交实验结果以及最后分离得到的单体化合物,采用质谱(MS)、核磁共振仪(NMR)、红外(IR)、紫外(UV)等波谱手段解析结构。
2 防己中不同活性成分综合性实验方案
2.1 正交实验优选防己中汉防己甲素和乙素的提取工艺
2. 1.1 正交实验设计
取药材量100 g,选用L9(34)正交表,以浸膏得率、汉防己甲素含量、汉防己乙素含量为综合考查指标,进行了9次实验,分别考查提取次数、提取时间、溶剂用量和乙醇浓度。其中各因素水平具体见表1[7]。
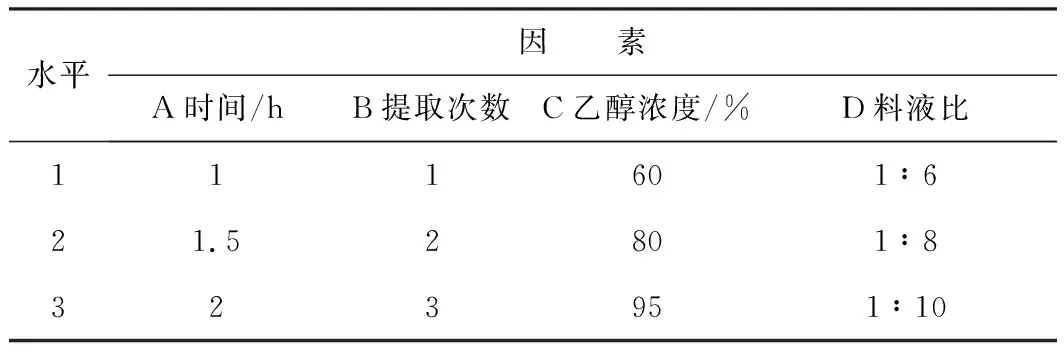
表1 正交实验因素与水平表
2.1.2 综合评价指标的选择
防己生物碱是防己的主要活性成分,其中汉防己甲素和乙素占了总药材的1%左右;故选用这2个成分的含量与浸膏得率(权重比5∶5) 进行综合评分,以综合评分结果进行提取工艺最佳参数的优选。综合评分计算分值方法如下:综合评分=(汉防己甲素、乙素含量总和) / Max(汉防己甲素、乙素含量总和)×0.5+浸膏得率×0.5/Max(浸膏得率)。
2.1.3 检测方法
(1) 汉防己甲素和乙素测定方法。色谱柱C18柱(4.6 mm×250 mm,5 μm);流动相:甲醇-0.1%三乙胺溶液(70∶30);检测波长:280 nm;柱温:30 ℃;流速:1.0 mL/min;进样量:10 μL[8]。
(2) 对照品溶液制备和线性关系考查。精密称取汉防己甲素对照品、汉防己乙素对照品适量,加甲醇制成每1 mL含汉防己甲素50 μg、汉防己乙素25 μg 的混合溶液[9]。取对照品混合溶液5、10、15、20、25、30 μL,分别注入色谱仪,以峰面积的积分值为纵坐标,以对照品溶液的进样量(μg) 为横坐标,绘制标准曲线。由于实验时间有限,此两部分会在预实验时完成。学生实验以讲解HPLC的操作使用为重点。
(3) 供试品溶液制备。精密量取防己提取液50 mL,水浴旋蒸至近干,加1%盐酸15 mL,滤去不溶物,加浓氨水4 mL,加氯仿50 mL萃取3次,合并提取液,蒸干氯仿层,残渣加甲醇溶解,并转移至100 mL量瓶中,加甲醇至刻度,摇匀即得。
2.1.4 实验结果
用SPSS19.0 软件[10]对汉防己甲素和汉防己乙素和浸膏得率的综合评分结果进行统计分析,正交实验结果、极差、方差分析结果见表2、表3、表4。
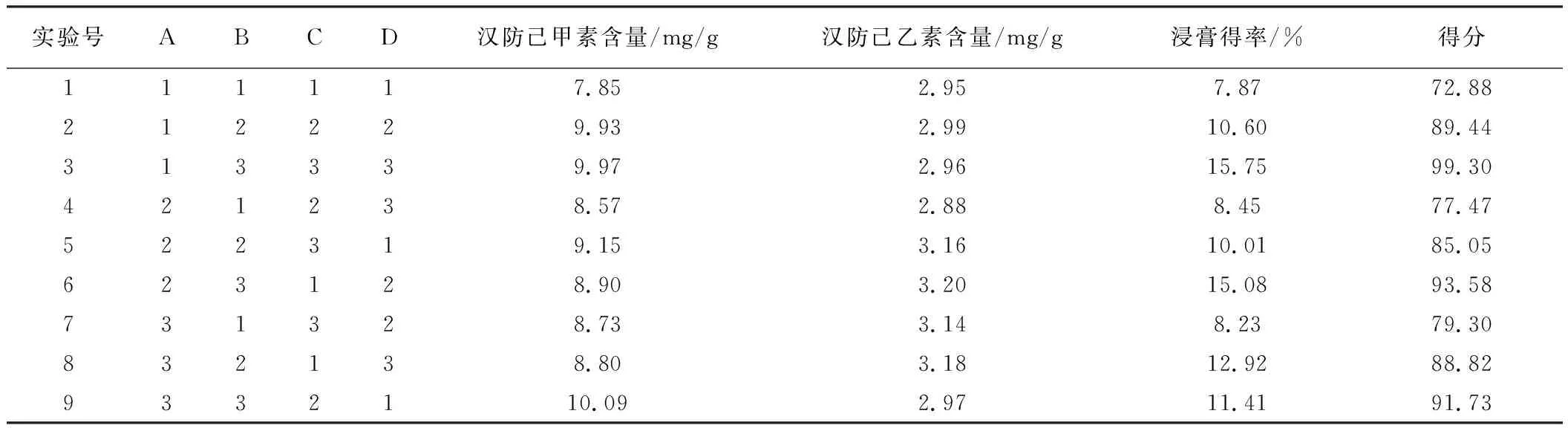
表2 正交实验结果表

表3 极差分析

表4 醇提工艺方差分析
根据极差分析和方差分析结果可见,各因素的影响大小顺序为: B > D > C > A,最佳提取工艺条件为B3D3C3A1,其中因素B 即提取次数有极显著性影响; 其他各因素均未有显著性影响,考虑到60%的乙醇实验室减压浓缩耗时较长,故选择D1C3A1。即防己的提取工艺条件为:以6 倍量95%乙醇提取3 次,每次1 h。
本实验结果为预实验结果,根据每年实验药材批次不同可能会有所不同。每组学生自由选取1个实验方案进行实验,结合各组的实验结果学习如何使用正交实验的方法优化提取工艺。但由于每组学生操作习惯不同,极差和方差可能会偏大。
2.2 防己中活性成分的分离
2.2.1 萃取法提取非酚性亲脂性叔胺生物碱
选取正交实验方案得到的防己乙醇提取液,减压浓缩近干,加入1% HCl,充分搅拌,直至加酸水时溶液不发生浑浊为止,过滤弃去沉淀。滤液滴加浓氨水中和至pH 9左右,此时亲脂性的叔胺碱游离析出,用氯仿500 mL分3次萃取水层,合并得氯仿溶液。以1%氢氧化钠溶液200 mL分3次萃取,再以水20 mL/次洗涤2次。得氯仿层,减压浓缩得粗制非酚性亲脂性叔胺生物碱[11]。
2.2.2 重结晶纯化叔胺生物碱
将非酚性生物碱用加丙酮热溶解,重结晶,待结晶析出后,将母液与晶体分离。母液再浓缩重复处理,尚可得结晶。合并多次结晶,为汉防己甲素和乙素的混合物[12]。
2.2.3 柱色谱分离汉防己甲素和乙素
(1) 装柱:称取20 g硅胶(200~300目)加入50 mL二氯甲烷拌成匀浆,打开柱下活塞,将匀浆一次倾入层析柱内,等待柱子压实;
(2) 上样:取汉防己甲素和乙素的混合物100 mg加入二氯甲烷1 mL溶解后,用滴管将溶液沿着层析柱内壁均匀加入。
(3) 洗脱: 二氯甲烷∶甲醇=20∶1为洗脱剂,进行洗脱,收集流份3 mL左右/份
(4) 薄层色谱检识:以二氯甲烷∶甲醇=10∶1为展开剂,以对照品作对照,相同斑点的组分合并,称重。
2.3 HPLC(面积归一化法)测定纯度
使用正交实验的色谱条件,测定汉防己甲素和乙素的纯度,结果表明汉防己甲素纯度为98.93%、汉防己乙素纯度为98.85%。
2.4 汉防己甲素和乙素的结构鉴定
化合物1为白色针状结晶(丙酮中结出),熔点150~152 ℃/217~218 ℃。UV(MeOH) 谱图中在230、280 nm处有吸收峰,说明化合物1中有苯环结构。IR谱图中在1 605、1 462 cm-1处的吸收峰也证明化合物1中有苯环存在。EI-MS图谱中给出[M + H]+.峰为623,高分辨质谱给出分子式:[C38H43N2O6]+.,计算不饱和度为18,说明化合物1有可能是双苄基异喹啉生物碱。结合化合物1的1H-NMR(400 MHz, CDCl3)数据δ ppm: 3.72(1H, d,J= 9.6 Hz, H-1), 2.36(3H, s, NCH3), 2.91(1H, m, Ha-3), 3.48(1H, m, Hb-3), 2.39(1H, m, Ha-4), 2.89(1H, m, Hb-4), 6.29(1H, s, H-5), 3.75(3H, s, 6-OCH3), 3.18(3H, s, 7-OCH3), 2.48(1H, dd,J= 14.4, 1.8 Hz, Ha-α), 2.67(1H, dd,J= 14.4, 10.2 Hz, Hb-α), 6.52(1H, d,J= 2.2 Hz, H-10), 3.91(3H, s, 1-OCH3), 6.81(1H, d,J= 8.4 Hz, H-13), 6.86(1H, dd,J= 8.4, 2.4 Hz, H-14), 3.84(1H, d,J= 11.4, 6.0 Hz, H-1′), 2.64(3H, s, N′-CH3), 2.83(1H, m, Ha-3′), 3.39(1H, m, Hb-3′), 2.69(1H, m, Ha-4′), 2.91(1H, m, Hb-4′), 6.52(1H, s, H-5′), 3.38(3H, s, 6′-OCH3), 6.00(1H, s, H-8′), 2.77(1H, dd,J= 11.4, 12.6 Hz, Ha-α), 3.22(1H, dd,J= 12.6, 6.0 Hz, Hb-α′), 6.27(1H, dd,J= 8.4, 2.4 Hz, H-10′), 6.77(1H, dd,J= 8.4, 2.4 Hz, H-11′), 7.13(1H, dd,J= 8.4, 2.4 Hz, H-13′), 7.34(1H, dd,J= 8.4, 2.4 Hz, H-14′)。与文献对照[13],证明化合物1为汉防己甲素。
化合物2为白色粒状结晶(丙酮中结出),熔点177~179 ℃/237~238 ℃。UV和IR谱图与化合物1相似。EI-MS图谱中给出[M + H]+.峰为609,高分辨质谱给出分子式:[C37H41N2O6]+.,计算不饱和度为18,说明化合物2也可能是双苄基异喹啉生物碱。结合1H- NMR(400 MHz, CDCl3) δ ppm: 2.37(3H, s, 2-NCH3), 2.39~2.45(1H, m), 2.53~2.57(1H, m), 2.68(3H, s, 2′-NCH3), 2.70~3.03(7H, m), 3.23~3.31(1H, m), 3.39(3H, s, 6′-OCH3), 3.41~3.65(2H, m), 3.74~3.78(1H, m, H-1), 3.78(3H, s, 6-OCH3), 3.88~3.94(1H, m, H-1′), 3.93(3H, s, 12-OCH3), 6.05(1H, s, H-8′), 6.31(1H, s, H-5), 6.34(1H, dd,J=8.4, 2.4 Hz, H-10′), 6.55(1H, s, H-5′), 6.57(1H, s, H-10), 6.82(1H, dd,J=8.4, 2.4 Hz, H-11′), 6.86(2H, br s, H-13, H-14), 7.13(1H, dd,J= 8.4, 2.4 Hz, H-13′), 7.36(1H, dd,J=8.4, 2.4 Hz, H-14′)。与文献对照[14],证明化合物2为汉防己乙素。
3 结语
通过上述实验设计,将“汉防己生物碱的提制和鉴定”设计成为综合性实验,增加了正交法优化提取工艺的步骤,使原本简单枯燥的提取步骤也变得有意义起来。在正交实验里,学生不仅可以学习如何从植物中提取有效成分,更可以学会如何使工艺最优化;用多种提取分离方法提取分离纯化生物碱类化合物,通过酸提碱沉、有机溶剂萃取、重结晶和柱色谱法联合使用,使学生熟悉天然药物化学中最常用的几种分离纯化化合物的操作方法;增加纯度测定和结构解析的方法,使学生掌握HPLC、红外和紫外分光光度计的简单使用。通过质谱、核磁共振等波谱技术分析单体化合物结构,使学生对结构解析的过程有一定的感性认识。
综上所述,以防己作为一个典型案例,使学生对植物药的研究有一个较为全面的了解, 其中包括天然药物化学、药物化学、药物分析等多学科内容。这样的实验教学模式的设计[15]不仅可以培养学生动手实践能力、综合知识运用能力,更能使学生尽早地接触科研,参与科研,大大缩短学习的适应期,培养出“知识、能力、素质”综合发展的创新型人才。
