第三脑室脊索样胶质瘤1例并文献复习
2019-01-09丁江伟周刚丁大领王凯王树凯
丁江伟 周刚 丁大领 王凯 王树凯*
(1郑州大学第一附属医院神经外科; 2郑州人民医院神经外科,河南 郑州 450000)
脊索样胶质瘤(chordoid glioma, CG)是一种主要发生于第三脑室下丘脑区的具有独特病理特征的肿瘤,临床较为罕见。近期郑州大学第一附属医院收治1例CG病例,并结合文献复习其临床及病理学特征,现报告如下。
患者男性,20岁,以“间断性头痛4 d,加重1 d”主诉入院,查体无明显特殊异常,术前激素:促卵泡生成素 4.24 mIU/mL;黄体生成素4.41 mIU/mL;泌乳素9.26 ng/mL;睾酮3.94 ng/mL;游离三碘甲状腺原氨酸5.74 pmol/L;游离甲状腺素10.20 pmol/L;促甲状腺激素1.47 μIU/mL;生长激素0分<0.05 ng/mL,促肾上腺皮质激素(adreno-cortico-tropic- hormone, ACTH)上午8点5.16 pg/mL,ACTH下午4点5.58 pg/mL,皮质醇上午8点5.65 pg/mL,皮质醇下午4点3.07 pg/mL,头颅MRI平扫+增强(图1):鞍上池及三脑室前份可见一团块状等T1混杂稍长T2信号影,视交叉受压下移。垂体高度约5 mm,后份可见小片状长T1长T2信号影垂体柄呈受压改变。双侧颈内动脉海绵窦段位置对称。增强后鞍上池及三脑室前份病变可见明显较均匀强化,后份异常信号不强化呈低信号,直径约4 mm。松果体区可见一囊性不强化灶,大小约8 mm×5 mm(长径×短径)。诊断意见:①鞍上池三脑室前份富血供实行占位,考虑生殖细胞瘤;②垂体后叶乏血供异常,拉克氏囊肿可能;③松果体囊肿。
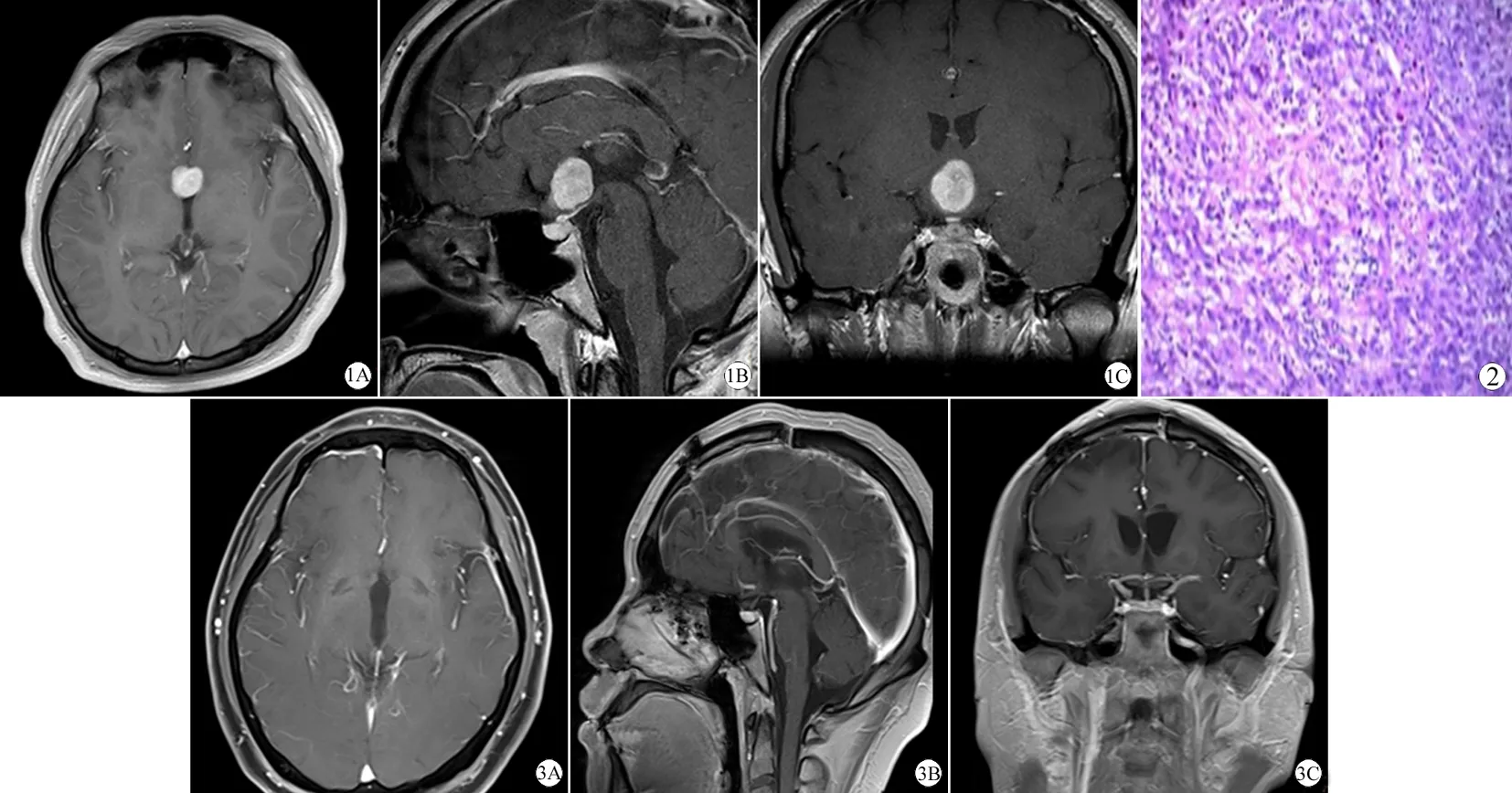
图1 术前MRI示:第三脑室占位
A: T1加权轴位增强扫描可见第三脑室内占位明显强化;B: T1加权冠状位增强扫描;C: T1加权矢状位增强扫描
图2 组织学病理:上皮样肿瘤细胞增生,多数细胞呈索条状、梁状或巢团状排列,细胞体积中等偏大,胞浆丰富、红染,核染色质淡,部分可见核仁;间质黏液样变性,伴散在及灶状嗜酸性粒细胞、淋巴细胞和浆细胞浸润(伊红染色,×200)
图3 术后5个月复查增强MRI
A: 轴位术后切除情况; B: 冠状位术后切除情况; C: 矢状位术后切除情况(第三脑室CG完全切除且未见肿瘤复发)
手术病理及预后:右侧额部跨冠状缝过中线马蹄形切口,显微镜下右侧纵裂牵开额叶,深入5 cm后,切开透明隔,可见质韧的病变组织,血供一般。病变组织完整剥除。术后病理(图2):鞍区占位肿瘤,结合形态及免疫组化考虑CG,WHO II级,免疫组化: GFAP(+)S-100(+)Oligo(-),CD34(+)IDH1(-),P53(灶+),ki-67(约5%),EMA(灶+),PR(灶+),TTF(+),E-cad(膜-),SALL-4(-),OCT-4(灶+),Galectin-3(+),CK(+),p63(-),Calponin(-),SOX-10(-),ERG(散-)。术后120 d后随访:患者意识清醒,四肢肌力5级,高级智能活动正常。记忆力减退,顺行性遗忘,体重较前明显加重,面部痤疮,可能与术后下丘脑损伤摄食中枢、激素应用有关,复查头颅MRI(图3),未见肿瘤复发迹象,仍在继续随访中。
讨论:CG是一种罕见、生长缓慢的肿瘤,同时具有神经胶质和脊索瘤的特征,Wanschitz[1]等1995年报道了一种定位第三脑室的肿瘤,肿瘤类似于脊膜瘤,但表现为胶质纤维酸蛋白的免疫阳性,并将其分类为脑膜瘤的变种。Brat等[2]于1998年首次将其定性为一种独特的临床病理类型:CG,2000年WHO神经系统分型中将其命名为第三脑室CG,并被划分为一种来源不明的特殊类型肿瘤,WHO II级。
发病年龄12~70岁,平均年龄约46岁,以中老年女性多见,亦可少见于儿童及青年[3-4],本例青年男性,相对少见。临床上无特殊表现,多与肿瘤压迫临近组织有关(多为垂体、下丘脑、丘脑、视交叉等),如头痛、体重减轻、内分泌紊乱(甲状腺功能减退、尿失禁、闭经)、神经症状(共济失调、尿失禁、嗅觉丧失)、精神障碍等,若肿瘤位于其他组织则表现为相应临近组织受压症状,曹晓昱等[3]报道一例左侧小脑占位,表现为共济失调、Romber征(+)。该病例间断性头痛无特异性表现。
第三脑室脊索样胶质瘤,顾名思义三脑室内占位性胶质瘤,但并非所有脊索样胶质瘤都发生于三脑室,曹晓昱等[3]报道一例小脑部位脊索样胶质瘤,Jain D等[5]发现枕部病变脊索样胶质瘤,Goyal等[4]报道过一例左侧颞顶叶CG,肿瘤实行多见,可伴囊变,头颅MRI表现:T1低信号T2高信号,注入强化剂后均一强化,该病例呈等T1混杂稍长T2信号影,增强后明显较均匀强化,与文献报道基本一致。
病理诊断是CG诊断的金标准,且免疫组化必不可少。脊索样胶质瘤的光镜表现为明显的嗜碱性黏液样背景下排列成簇状、条索状上皮样细胞,肿瘤细胞具有丰富的嗜酸性细胞质和均匀的圆卵圆核。显著淋巴细胞浸润具有特异性,并可见大量Russell小体,周围的非肿瘤组织可见Rosenthal,罕见有丝分裂、血管增生及细胞坏死。超微结构:肿瘤细胞圆形或梭形,细胞核多不规则,细胞表面见散在分布短绒毛,较多半桥粒样结构连接细胞膜及其下的基板。可见中间连接为代表的细胞间连接。胞质内细胞器呈环带状分布,为扩张的粗面内质网,中间带主要为高尔基体,细胞顶端下为多量带有致密分泌颗粒的线粒体,而细胞顶端充满平行排列的中间丝并围绕核呈同心圆状排列。文献报道免疫组化显示:几乎所有病例胶质纤维酸性蛋白(GFAP)和波形蛋白(vimentin,Vim)弥漫性强阳性。此外,上皮膜抗原(EMA)、细胞角蛋白、CD34和S100蛋白也可阳性,阳性率分别为:67%、71%、88%、75%[3]。该病例GFAP(+),EMA(灶+)、S-100(+)、CD34(+)与文献报道基本一致,其他P53(灶+)、PR(灶+)、TTF(+)、OCT-4(灶+)、Galectin-3(+)、CK(+)。ki-67(约5%)。Ni HC等[6]报道一种单克隆抗体D2-40在脊索样胶质瘤中呈灶性或弥漫性阳性,或许可以作为CG的补充标记。
唐广山等[7]认为成年人位于第三脑室前部及三脑室内不规则、边界清晰肿块,并压迫视交叉或下丘脑,肿瘤T1WI等、低信号,T2WI等,高信号,DWI呈低信号,增强后明显强化,但瘤体不浸润临近脑实质,应考虑CG,因本病罕见应于以下疾病相鉴别[8]:①脊索样脑膜瘤:多位于幕上且多于硬脑膜相连,好发于青少年,光镜下与脊索样胶质瘤相似,有梭形或上皮样细胞组成,呈索条、小梁状,但脊索样脑膜瘤可伴有典型的自身结构(瘤细胞或微血管的旋涡状结构、砂粒体和核内假性包涵体),且脑膜瘤GFAP始终阴性、Vimentin阳性表达。②脊索瘤:该肿瘤不属于神经系统肿瘤,常累及脑和脊髓,发于颅内者常见于斜坡,病理可见PAS染色阳性的液滴状细胞,无淋巴、浆细胞浸润,Vim弥漫强阳性,S-100可阳性,但GFAP阴性可与CG鉴别。③颅咽管瘤 位于鞍区或三脑室,源于垂体原基残余,组织学上有造釉细胞型和乳头型两种,GFAP阳性,易于CG鉴别。
CG被认为是一种低级别的肿瘤,根治性手术切除是有效的治疗策略。Desouza等[9]认为,终板入路可以很好的显示视交叉,可减少对视力损伤,但对显示肿瘤上级欠佳,对于体积较大肿瘤,尤其肿瘤位于鞍上可用经皮质侧脑室或胼胝体穹窿入路。由于病变位置靠近下丘脑、垂体等重要解剖结构,增加了手术死亡率及并发症风险, 使得很难完全切除肿瘤,部分患者的预后较差。CG术后并发症与手术入路、下丘脑、垂体损伤等有关[3],术后较高的死亡率和致残率,肿瘤次全切或部分切除患者立体定向放射外科可能不失为一种替代方法[3],到目前为止,没有任何化疗方案被证明是有效的。