肾缺血再灌注通过促凋亡途径加重糖尿病小鼠肾损伤
2019-01-08韩庆玲郑德义李伟人王志伟
韩庆玲, 郑德义, 李伟人, 王志伟, 杜 娇, 王 毅
糖尿病(diabetes mellitus,DM)是一组以高血糖为特征的代谢性疾病,糖尿病时长期存在的高血糖,导致各种组织损伤,特别是肾、心脏、血管和神经等多器官组织的慢性损害及功能障碍[1]。实验研究[2-3]显示糖尿病会加重器官对缺血的损伤,降低器官缺血的预后。肾脏是机体维持内环境稳定的重要器官,临床上不同病因如麻醉、手术或移植等引起循环休克都可以导致肾缺血再灌注损伤,肾缺血再灌注是急性肾功能衰竭的病因之一[4]。但是,在糖尿病的病理基础上,遭受以上病变所致的急性肾功能损伤及其发病机制尚不完全清楚。该实验从凋亡方面探索肾缺血再灌注加重糖尿病肾损伤的机制,为临床研究糖尿病合并肾缺血再灌注损伤病理生理机制及防治措施提供实验依据。
1 材料与方法
1.1主要实验试剂及仪器链脲佐菌素购自美国Sigma公司;无创微动脉夹购自北京中科恒天科技有限公司;抗体Bcl-2、Bax、β-actin购自英国Abcam公司;抗体Caspase-3购自美国Millipor公司;RIPA裂解缓冲液、ECL显色液购自上海碧云天生物技术研究所;GelDoc XR System凝胶成像系统购自美国BIO-RAD公司。
1.2实验分组及模型建立清洁级雄性C57BL/6J小鼠,18~20 g,由北京华阜康生物科技股份有限公司提供(SCXK 2014-0004)。28只C57 BL/6J小鼠随机分为正常血糖假手术组(Sham组)6只,糖尿病假手术组(DM+Sham组)6只,正常血糖肾缺血组(I/R组)8只,糖尿病肾缺血组(DM+I/R组)8只。小鼠饲养在清洁、通风良好的环境中,自由饮食水,12 h昼夜节律。
1.3糖尿病及肾缺血再灌注损伤模型建立参考文献[5]建立1型糖尿病小鼠模型,小鼠禁食不禁水12 h后,将链脲佐菌素以0.5%的浓度溶于0.1 mol/L无菌柠檬酸-柠檬酸钠缓冲液(pH 4.5),以55 mg/kg连续5 d腹腔注射,自由进食水,观察72 h后,用血糖仪检测鼠尾静脉血糖浓度,血糖浓度>16.7 mmol/L,小鼠出现多尿,体重下降表现,表示糖尿病模型成功。继续喂养糖尿病小鼠4周后,建立肾缺血再灌损伤模型:小鼠腹腔注射3.6%(10 ml/kg)水合氯醛麻醉后,脱去腹部毛发,碘伏常规消毒后,沿腹正中做大约2.5手术切口,找到并分离左右肾动静脉,用无创微血管夹夹闭,肾脏由鲜红色变为暗紫色,30 min后,松开微血管夹恢复血流灌注,肾脏迅速恢复正常颜色,假手术组只分离肾动静脉不夹闭,逐层关闭腹腔。整个手术过程中,小鼠都放置在加热毯上以保持体温恒定在(37±0.5)℃,术区以生理盐水湿纱布覆盖。
1.4实验方法
1.4.1肾功能检测 按照试剂盒说明书取血清,采用贵州省人民医院检验科全自动生化分析仪 (日本日立公司)进行血清尿素氮与肌酐的检测。
1.4.2Western blot 检测肾组织凋亡蛋白的表达 取肾组织,加入RIPA裂解缓冲液用组织研磨器研磨匀浆后,提取肾脏总蛋白并定量变性。取10 μl总蛋白加入预制好的15%聚丙烯酰胺凝胶中,先用80 V电压分离30 min,然后再调至120 V分离1.5 h。半干转法将蛋白转移至聚偏氟乙烯(PVDF)膜上(16 V,16 min)。室温下5%的脱脂奶粉封闭1 h,然后用含有目的蛋白抗体的一抗稀释液孵育(Bax,兔抗,1 ∶500稀释;Bcl-2,兔抗,1 ∶500稀释;Caspase-3,兔抗,1 ∶200稀释;β-actin,鼠抗,1 ∶200稀释)于4 ℃冰箱摇床上孵育过夜。TPS漂洗3次,每次10 min,后用含辣根过氧化物酶标记的相应二抗(1 ∶1 000稀释)稀释液室温下孵育1 h。再次经TPS洗涤3次,每次10 min,加入ECL显色液用GelDoc XR System凝胶成像系统检测。以β-actin表达水平作为内参,应用Image J进行条带分析,目的蛋白的表达量以目的蛋白与内参照蛋白平均光密度的比值表示。

2 结果
2.1各组小鼠血糖、体重、血清肌酐、尿素氮情况肾脏缺血再灌注术前,测小鼠空腹血糖和体重,Sham组与I/R组比较无明显差异;分别与Sham组及I/R组比较,DM+Sham组和DM+I/R组小鼠血糖明显升高、体重显著减轻(P<0.05)。通过检测各组血清肌酐、尿素氮显示,与Sham组比较,DM+Sham组、I/R组及DM+I/R血清肌酐、尿素氮升高(P<0.05),表明糖尿病及肾缺血再灌注导致肾功能损害,但DM+I/R表现更严重的肾功能损害。与DM+Sham组比较,DM+I/R组血肌酐、尿素氮明显增高(P<0.05),说明肾I/R加重肾功能损害。见表1。
2.3Westernblot检测凋亡蛋白在各组小鼠模型肾组织中的表达Western blot检测各组小鼠肾组织Bax 、Bcl-2和Caspase-3蛋白表达,结果显示:与Sham组比较,DM+Sham组和I/R组Bax和Caspase-3的蛋白表达水平升高(P<0.05),而Bcl-2蛋白表达水平降低(P<0.05);与DM+Sham组和I/R组比较,DM+I/R组小鼠肾组织中Bax和Caspase-3蛋白表达水平明显增加(P<0.05),而Bcl-2蛋白表达水平明显降低(P<0.05)。见图1。
3 讨论
糖尿病发病率持续增高趋势,根据国际糖尿病联盟(IDF)最新报告,2017年全球约4.25亿成人患糖尿病,预计到2045年,糖尿病患者可能达到6.29亿[6]。随着糖尿病病程的延长,可伴发多器官功能障碍,其中糖尿病肾病为糖尿病引起的微血管并发症,是引起终晚期肾病的首要原因[7]。肾脏是能量需求大、微循环丰富的器官,对缺血再灌注损伤极为敏感[8],肾缺血再灌注损伤是急性肾损伤最常见的原因之一,临床上主要继发于低血容量休克、心血管外科手术及肾移植等[9]。目前针对糖尿病肾损伤报道较多,但糖尿病肾急性缺血再灌注损伤国内外尚少报道。所以糖尿病肾缺血再灌注损伤值得引起重视。目前研究[10]表明,肾脏缺血再灌注损伤的机制可能与内质网应激,氧化应激,炎症,内皮功能障碍等有关。但是,肾缺血再灌注加重糖尿病肾损伤的发生机制尚不清楚。
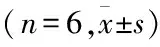
表1 4组小鼠术前空腹血糖、体重及术后肾功能情况比较
与Sham组比较:*P<0.05;与I/R组比较:#P<0.05;与DM+Sham组比较:▽P<0.05

图1 凋亡相关蛋白在各组小鼠肾组织中表达
A:Bax;B:Bcl-2;C:Caspase-3;与Sham组比较:*P<0.05;与I/R组比较:#P<0.05;与DM+Sham组比较:▽P<0.05
本实验通过腹腔连续注射低剂量链脲佐菌素制作糖尿病动物模型,建模成功后观察4周,检测小鼠空腹血糖及体重,结果显示糖尿病小鼠空腹血糖明显高于正常血糖小鼠,而糖尿病小鼠空腹体重却明显低于正常血糖小鼠,说明糖尿病模型成功建立。本实验采取夹闭双侧肾动脉30 min,再灌注12 h造肾缺血再灌注模型,显示缺血小鼠血清肌酐尿素氮明显高于假手术组,且糖尿病缺血组小鼠血清肌酐尿素氮明显高于正常血糖缺血组,说明肾缺血模型建立成功,且肾缺血加重了糖尿病肾功能的损伤。
细胞凋亡是细胞在一定的生理或病理条件下,受多种基因精确调控的主动的、程序化的死亡过程,是机体重要稳态的重要调控机制[11]。调控细胞凋亡的Bcl-2家族在细胞凋亡转导通路中发挥了极为重要的调控作用[12]。Bcl-2家族中,Bcl-2是抑凋亡基因,Bax是促凋亡基因。Caspase家族是细胞凋亡过程中发挥关键作用的一组半胱氨酸蛋白酶,其中的Caspase-3是最重要的细胞凋亡效应蛋白酶之一,是凋亡的执行者[13]。Bcl-2可以抑制细胞色素C从线粒体释放到细胞质从而抑制细胞凋亡的发生。而Bax可以通过与Bcl-2形成二聚体而抑制Bcl-2的表达及活性[14]。Bcl-2与Bax是一个平衡体系,Bax表达过度,则Bcl-2表达下调可活化Caspase-3,从而促进细胞凋亡,反之则抑制细胞凋亡[15]。本实验结果显示,凋亡相关蛋白Bax、Caspase-3在正常血糖缺血组和糖尿病假手术组升高,在糖尿病缺血组升高更明显,而Bcl-2在正常血糖缺血组和糖尿病假手术组降低,在糖尿病缺血组降低更明显。本实验结果表明凋亡参与了糖尿病加重肾缺血再灌注损伤,凋亡相关蛋白Bax、Bcl-2、Caspase-3的变化起调控作用。目前本实验只是初步探测了糖尿病肾缺血中凋亡相关蛋白的表达变化,关于其上下游的调控机制和三者之间的相互关系还需进一步探索。
