碳热还原氮化法制备超细AlN粉体的过程及特性
2019-01-05魏鑫张浩孙登琼田晨光刘翔宇崔嵩汤文明
魏鑫,张浩,孙登琼,田晨光,刘翔宇,崔嵩,汤文明
碳热还原氮化法制备超细AlN粉体的过程及特性
魏鑫1,张浩2,孙登琼2,田晨光2,刘翔宇1,崔嵩3,汤文明1
(1. 合肥工业大学 材料科学与工程学院,合肥 230009; 2. 合肥圣达电子科技实业有限公司,合肥 230088;3. 中国电子科技集团公司 第43研究所,合肥 230088)
将超细Al2O3粉、纳米碳黑和有机粘结剂混合,通过挤压成形和排胶处理制成多孔前驱体,然后高温煅烧发生碳热还原氮化反应,最后脱除残余的碳,得到AlN粉体。对AlN粉体的形貌、结晶度、晶粒尺寸、平均粒度以及O、N、C含量进行观察与分析。结果表明,经360 ℃/2 h排胶后的前驱体为多孔结构,比表面积大,孔隙为球形。1 650 ℃以上温度下煅烧的产物中无Al2O3,AlN合成过程趋于完成,与热力学计算结果相吻合。脱碳温度对粉末C含量影响最大,其次是进料速率。多孔前驱体在1 700 ℃下煅烧12 h,然后在温度为700 ℃、纯氧气氛、进料速率为4 kg/h的条件下脱碳,得到的AlN粉体O,N,C含量分别为0.77%,33.42%和323×10−6,粉末颗粒圆整,粒径分布范围较窄,平均粒径50=1.36 µm。AlN粉体特性与国外同类产品接近。
氮化铝粉体;碳热还原氮化法;前驱体;粉体特性;煅烧
随着现代微电子技术的飞速发展,电子元器件和整机都朝着微型化、轻量化、集成化、高可靠性和大功率输出等方向发展,从而对基板和封装材料的散热性能提出更高要求。氮化铝(AlN)的热导率高,最高达到320 W/(m·K),绝缘性良好(电阻率>1016Ω·m),介电常数(1 MHz下为8.9)和介电损耗低,具有与Si、GaAs等半导体材料相匹配的热膨胀系数(AlN:4.3×10−6/K,Si:3.5×10−6/K,GaAs:6.4×10−6/K)以及良好的化学稳定性、环保无毒等优点,成为最理想的陶瓷基板材料之一[1−5]。高质量AlN粉体的合成是制备高性能AlN陶瓷块体的前提。高性能AlN粉体的制备方法很多,目前可实现规模生产的主要有Al2O3碳热还原氮化法和铝粉直接氮化法[6−8]。Al2O3碳热还原氮化法就是将混合均匀的Al2O3和C粉体在流通的氮气气氛下煅烧,产品具有纯度高、粒径小且粒度分布均匀等优点,但存在工艺时间较长、氮化温度较高,而且合成的AlN粉还需除碳,工艺控制难度高,杂质氧进入AlN晶格而降低其热导率等方面的不足[9−10]。为了保证Al2O3与C两相均匀分布,促进反应过程充分进行,减少原料残留,前驱体的制备是关键。秦明礼等[11]将硝酸铝、葡萄糖和尿素的水溶液混合,加热分解,低温煅烧制备出无定形Al2O3和无定形碳均匀分布的前驱体,在1 550 ℃条件下煅烧90 min实现完全转化。茅茜茜等[12]采用直接发泡与注凝成形相结合的方法制备出孔隙率大于80%的Al2O3+C泡沫前驱体,碳热还原氮化反应速率显著提高,1 650 ℃下煅烧后得到的AlN粉体平均粒径不超过1 µm,N含量(质量分数)达32.9%。WANG等[13]研究发现,在前驱体中添加适量的CaF2和YF3,可有效提高氮化速率,并提高AlN粉体颗粒的球形度。尽管如此,国内高纯超细AlN粉体的制备及产业化仍处于起步阶段,关键技术与国外先进水平存在很大差距,Al2O3碳热还原氮化法制备的AlN粉体在O、N、C含量控制及粉体形态与尺寸均匀性等方面存在明显不足,亟需开展进一步的研究工作。本文作者以高纯超细Al2O3粉体和纳米碳黑作为原料,制备多孔前驱体,研究煅烧温度、时间以及脱碳温度、气氛等对AlN粉体的形貌与O、N、C含量,以及粉末的粒度分布等特性的影响,为工业化合成制备高品质AlN粉体奠定技术基础。
1 实验
1.1 AlN粉体制备
原料包括高纯Al2O3粉,纯度99.9%,粒度50= 0.5 µm;纳米碳黑,纯度99.9%,粒度50=40 nm;有机粘结剂,纯度99.9%。均为市售。
按照物质的量比(Al2O3):(C)为1:3.5、粘结剂的添加量(质量分数)约为5 %的比例称量Al2O3粉、碳粉和粘结剂,通过湿法球磨混合均匀(用材质为Al2O3的磨球,球磨5 h),经挤压成形后,置于排胶炉中,在N2气氛下进行排胶,得到多孔的前驱体。将前驱体样品放入合成炉中,通入高纯N2气,气体流量控制在200~250 L/min。前驱体随炉升至设定的煅烧温度(1 600~1 750 ℃)后保温煅烧,充分进行碳热还原氮化反应。将煅烧产物AlN置于脱碳炉中进行脱碳处理,脱碳气氛为氧气与氮气按一定比例混合的混合气体。最后将脱碳后的AlN进行粉碎,获得超细AlN粉体。
1.2 性能测试
采用STA449 F3型同步热分析仪分别对有机粘结剂与球磨后的混合料进行热重分析,建立热失重曲线,确定前驱体的排胶温度;采用GeminiVI12390型比表面积测试仪测试去除粘结剂后的多孔前驱体的比表面积;采用X'Pert PRO MPD型X射线衍射仪对未脱碳的煅烧产物进行物相分析,测试参数:Cu靶(Kα射线),管电压和管电流分别为40 kV和40 mA,扫描速率为2 (°)/min,扫描范围为20°~90°。基于煅烧产物的XRD谱,采用下式近似计算AlN相的结晶度:

AlN的晶粒尺寸()用Scherrer公式计算:
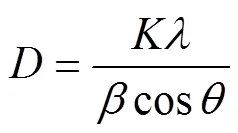
式中:为X射线衍射峰的半宽高;取0.89;为X射线波长(0.154 nm);为衍射角。选取煅烧产物的XRD谱上位于2=33°,36°和38°的AlN三强峰,分别计算,然后求平均值,为AlN的平均晶粒尺寸。
高温煅烧后的样品以及脱碳后的样品,其形状与多孔前驱体试样相同,并且都为多孔结构。采用ON836氧氮含量分析仪分别测定煅烧样品及其脱碳并粉碎后的粉体的O、N含量,用CS844-MC碳含量分析仪测定其C含量;采用SU8020型场发射扫描电镜观察多孔前驱体的截面形貌及其煅烧产物AlN粉体颗粒的截面形貌,以及脱碳并粉碎后的AlN粉的颗粒形貌;采用Master Sizer 2000型激光粒度分析仪测量脱碳后的AlN粉体平均粒度。
2 结果与讨论
2.1 前驱体特性
图1所示为有机粘结剂以及粘结剂与Al2O3粉、碳粉混合均匀后挤压成形制成的前驱体的热重分析曲线。由图1可见,低于100 ℃,粘结剂的质量减少7.83%,对应于其中的水分挥发;100~270 ℃之间,质量变化很小,说明其排胶过程并未发生;270~330 ℃之间,粘结剂质量急剧下降,质量损失率为66.48%,为粘结剂的热分解过程,同时释放大量的气体,在前驱体中起到造孔的作用;随着温度进一步升高至330~390 ℃,粘结剂的分解趋于平缓,质量损失率仅为7.34%;此后,粘结剂质量几乎无变化,其热分解反应基本完成。与此相对应地,混合料在270 ℃之前质量变化较小,在270~330 ℃之间发生剧烈的质量变化,质量减少6.55%,在330~390 ℃之间,混合料的质量变化趋缓,质量损失率仅为1.75%。说明前驱体的排胶过程主要发生在270~330 ℃,但为实现粘结剂的完全排除,排胶温度应在330 ℃以上,本研究设定前驱体的脱胶温度为300,330,360和390 ℃。
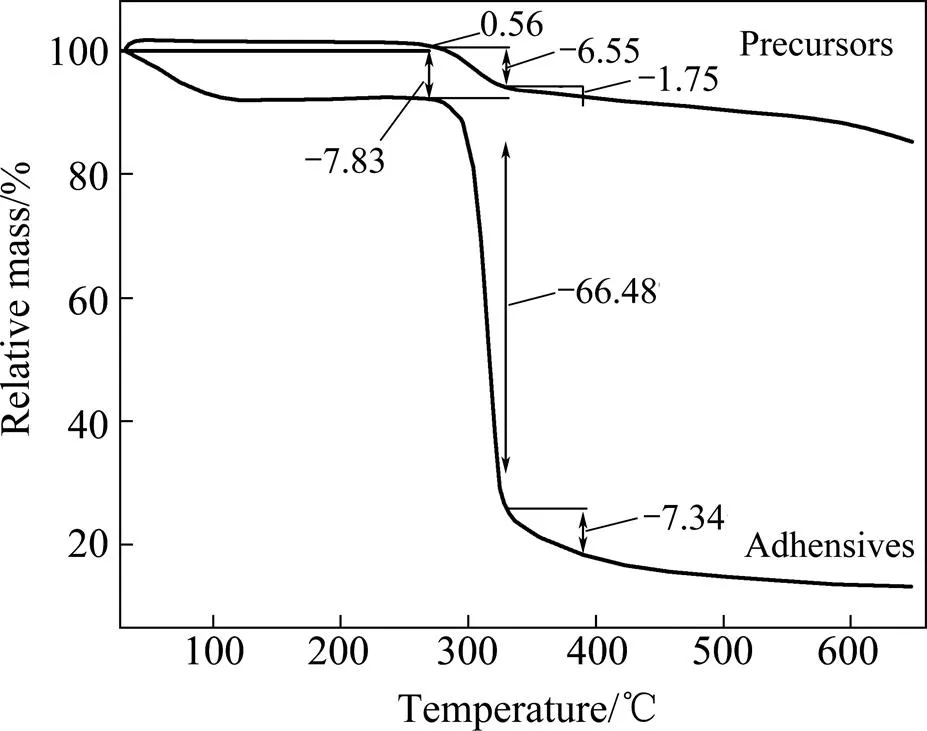
图1 前驱体和粘结剂的热重曲线
图2所示为不同温度下排胶后的前驱体截面SEM形貌。由图可见排胶后的前驱体为多孔结构,随排胶温度从300 ℃升高至360 ℃,孔隙的数量逐渐增多,尺寸逐渐增大,由不足10 µm增大至约20 µm,其形貌也由不规则形转变为球形或多角形。在390 ℃排胶时,前驱体中的孔隙发生坍塌,形成不规则的扁平气孔。通常,前驱体中连通的孔隙越多,越有利于碳热还原氮化反应过程中环境中的N2向前驱体内部扩散,并与孔隙中的物质进行交换,降低孔隙中的氧分压,促进碳热还原氮化过程的充分进行。

图2 不同温度下排胶后的前驱体截面SEM形貌
(a) 300 ℃; (b) 330 ℃; (c) 360 ℃; (d) 390 ℃
图3所示为多孔前驱体的比表面积随排胶温度的变化。由图可见,排胶过程中随温度升高,前驱体比表面积的变化呈现3个阶段的特征:第1阶段(300~320 ℃):粘结剂分解缓慢,前驱体质量损失较少,前驱体比表面积增大较缓慢;第2阶段(320~ 360 ℃):前驱体的质量加速减少导致比表面积快速增加;第3阶段 (360~390 ℃):由于前驱体中绝大多数粘结剂已分解,所以质量变化小,比表面积增大的幅度减小。也就是说,360 ℃排胶后,前驱体中的粘结剂绝大部分已分解,结合图2所示前驱体排胶后的形貌,认为最佳的前驱体排胶温度为360 ℃。表1所列为360 ℃下排胶时间对多孔前驱体比表面积的影响。由表1可知,随排胶时间延长,前驱体的比表面积增大,2 h后基本趋于稳定,甚至有缓慢减小的趋势,由此确定2 h为最佳的保温排胶时间。
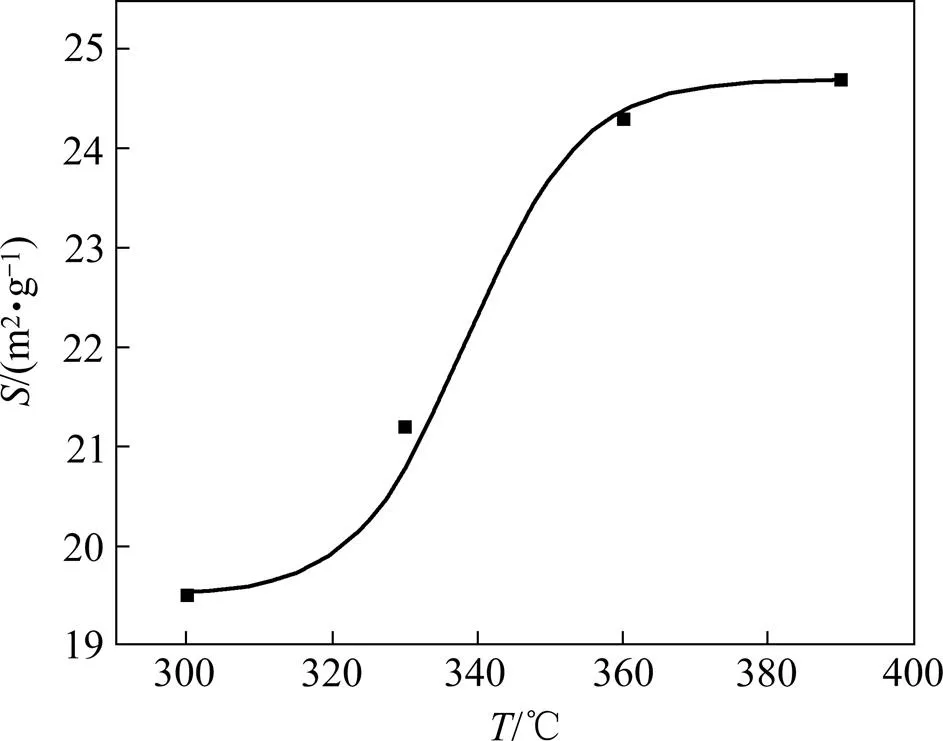
图3 前驱体比表面积随排胶温度的变化

表1 360 ℃保温不同时间后前驱体的比表面积
2.2 煅烧产物特性
图4所示为前驱体分别在1 600,1 650,1 700,和1 750 ℃下煅烧10 h后的XRD谱,表2所列为煅烧样品中AlN的平均晶粒尺寸与结晶度。由图4可见,1 600 ℃的煅烧产物中AlN衍射峰最强,但仍有明显的Al2O3衍射峰,说明在此温度下绝大多数的Al2O3已转变成AlN,但还有一定残余量。1 650 ℃的煅烧产物只存在AlN衍射峰,无Al2O3衍射峰,Al2O3已经完全转化为AlN。当煅烧温度升至1 700和1 750 ℃时,煅烧产物的XRD谱与1 650 ℃时的基本一致。从表2可知,AlN的结晶度与平均晶粒尺寸均随煅烧温度升高逐渐增大,当煅烧温度过高(1 750 ℃)时,AlN结晶度及平均晶粒尺寸却有小幅下降,可能与AlN晶粒的再结晶细化有关。值得注意的是,由于前驱体中的碳源为无定形结构,因此,煅烧产物中即使还有残留的碳,在其XRD谱中也未显现碳的衍射峰。
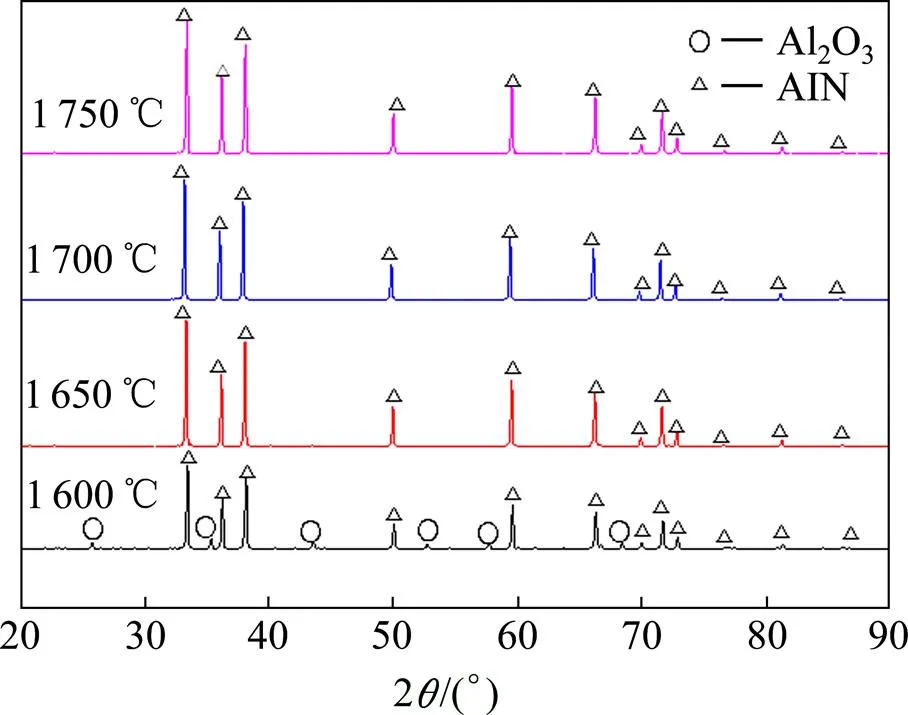
图4 前驱体在不同温度下煅烧10 h后的XRD谱
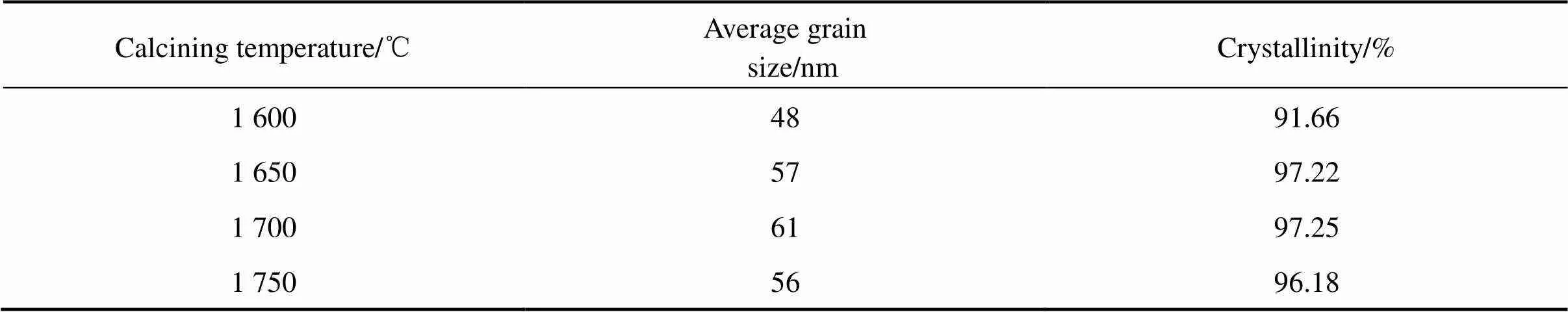
表2 煅烧样品中AlN的平均晶粒尺寸与结晶度
碳热还原氮化法合成AlN粉体要求反应原料中的碳源保持过量,不仅能促进Al2O3的转化,而且有利于制备出粒径均匀的AlN粉体,同时,AlN粉的比表面积也随C含量增加而变大[14]。理论上,完全反应所需Al2O3和C的物质的量比(Al2O3):(C)为1:3,为了保证碳源过量,(Al2O3):(C)通常为1:3.5~3.6,在Al2O3完全转化的情况下,煅烧产物中剩余的C含量在6.8%~8.1%(质量分数,下同)之间。表3所列为不同温度下煅烧12 h后所得AlN的O、N和C元素含量。由表3可知,1 600 ℃煅烧的产物O含量很高,为9.60%,而N含量很低,仅为27.60%,C含量偏高,为15.75%。这归因于煅烧温度过低,煅烧产物中仍有较多的Al2O3和C残余。当前驱体在1 650 ℃煅烧时,煅烧产物的O含量急剧降低至0.88%,C含量降至7.96%,同时,N含量大幅提高到33.6%;煅烧温度继续升高到1 700 ℃以上时,煅烧产物中的O、C含量小幅下降,N含量没有明显变化。
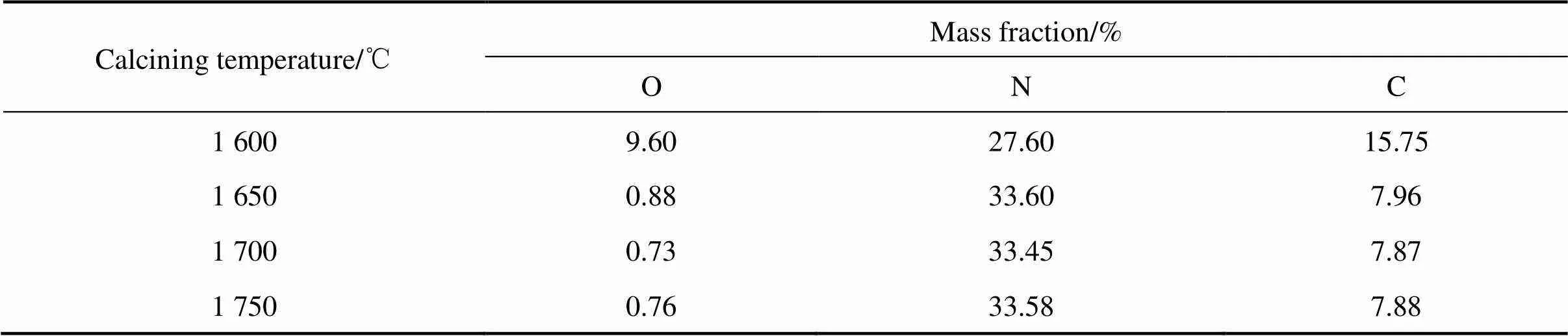
表3 煅烧样品的O,N,C含量

表4 1 700 ℃温度下煅烧时间对煅烧样品O,N,C含量的影响
表4所列为1 700 ℃温度下煅烧时间对煅烧样品O、N、C含量的影响。煅烧时间为10 h时,煅烧样品的O含量偏高,达到1.25%,N含量偏低,只有31.47%;延长煅烧时间至12 h时,产物中的O含量快速降低至0.73%,N含量则提高到33.45%;继续延长时间至15 h,煅烧产物的O含量虽略有降低,N含量略有增大,但与12 h的煅烧产物相比,变化不大。
延长前驱体的煅烧时间,不仅增加能耗,降低生产效率,降低设备的寿命,还对煅烧产物中AlN颗粒形态及尺寸产生不利影响。图5所示为1700℃煅烧不同时间后的AIN颗粒截面SEM形貌。考虑到煅烧产物中AlN颗粒被残余的C包裹,难以从表面观察到,因此,将煅烧产物颗粒脱碳后,再用刀片切开,观察断面形貌。煅烧10 h的产物AlN颗粒尺寸不足1 µm,呈不规则球形,颗粒间相互连接,内含连通的孔隙 (见图5(a)所示)。煅烧时间延长至12 h时,所得AlN颗粒的尺寸和形态与煅烧10 h产物基本一致,但AlN粉体颗粒的圆整度有所增加(图5(b)所示),颗粒形状趋于球形,这对AlN粉体的后续成形过程有利。时间延长至15 h时,AlN粉体颗粒明显长大,颗粒尺寸约为2 µm,球形度进一步增大,AlN颗粒间发生局部烧结,孔隙减少(见图5(c)),对后续的脱碳及粉碎工艺都产生不利影响。因此,前驱体的最佳煅烧条件为煅烧温度1 700 ℃,时间12 h。

图5 1 700 ℃煅烧不同时间后的AIN颗粒截面SEM形貌
Fig.5 Section SEM images of the AlN particles calcined at 1 700℃ for different and times
(a) 10 h; (b) 12 h; (c) 15 h
2.3 碳热还原氮化反应热力学
Al2O3碳热还原氮化法合成AlN的化学反应方程式为:
Al2O3(s)+3C(s)+N2(g)→2AlN(s)+3CO(g)(3)
基于热力学数据[15],推导出该反应的吉布斯自由能差为:
Δ=708.101−0.373 518+8.314×10−3×ln(4)
式中:Δ为反应吉布斯自由能差,kJ/mol;为反应温度,K;为反应熵,=(CO/θ)3/(N2/θ) (式中:CO和N2分别为CO和N2的平衡分压,kPa;P为常数100 kPa)。在本研究中,1 h内产出的煅烧产物AlN粉经脱碳后的质量约为5 kg, AlN粉的产出率约为5 kg/h,按Al2O3全部转化为AlN的理想状态计算,在产出5 000/41=121.95 mol/h的AlN同时,产出121.95×3/2=182.93 mol/h的CO。煅烧炉内气压设定为101.667 kPa,保持炉内正压。N2流量设定为12 000 L/h,氮气密度为1.153 kg/m3,则N2的流量为494.14 mol/h。根据理想气体状态方程:(式中:为理想气体的压强,kPa;为理想气体的体积,m3;为理想气体中气体物质的量,mol;为一般气体常数,为8.314 J/(mol·K);为理想气体的绝对温度,K),在恒温、恒容条件下,气氛中气体CO与N2的分压比等于其物质的量比,即CON2=182.93/494.14= 0.37,气氛中的N2分压约等于炉内气压,即N2= 101.667 kPa,则CO=37.617 kPa,代入公式=(CO/θ)3/(N2/θ),得到反应熵=0.052,代入式(4),得:
Δ=708.101−0.373518+8.314×10−3×ln0.052 (5)
用式(5)计算出该反应处于平衡状态(Δ=0)时,=1 777.8 K(1 504.7 ℃)。也就是说,当煅烧温度达到1 504.7 ℃以上时,Al2O3碳热还原氮化反应就有可能发生。虽然在1 600 ℃煅烧,该反应可以发生,但反应驱动力较低(Δ1 600 ℃=−57.9 kJ/mol),AlN转化率较低。随煅烧温度升高,该反应的热力学驱动力增大,反应速率及AlN转化率提高。综合上述反应热力学与动力学因素,在1 700 ℃煅烧12 h,AlN转化完全,可获得高纯的AlN产物,与2.2节的实验结果相吻合。
2.4 AlN脱碳
对煅烧后的产品进行脱碳处理,去除其中残余的自由碳,是Al2O3碳热还原氮化反应法制备高纯AlN粉体必要的工艺步骤。AlN的脱碳效果与脱碳温度、脱碳气氛中氧气与氮气的体积比((O2)/(N2))及进料速率这3个因素关系最为密切。根据前期研究的经验,按3因素、2水平的正交实验设计,如表5所列,对1 700 ℃/12 h条件下煅烧后的样品进行AlN的脱碳实验,以C含量为主要考察指标,对实验结果进行极差分析,研究脱碳温度、进料速率及脱碳气氛中的氧气与氮气体积比((O2)/(N2))这3个因素对脱碳效果的影响,结果列于表6。
表6中:1、2分别每个因素下对应水平为1或2的实验结果的和;1、2分别为每个因素下对应水平为1或2的实验结果的平均值;为极差,根据的值确定这3个因素对脱碳效果影响的主次,max−min。
根据和值大小,得出温度为700 ℃,(O2):(N2)=1:0(即采用纯氧气气氛),进料速率为4 kg/h时(表6中的实验1)脱碳效果最好;由极差值得出温度为影响脱碳效果的第一因素,其次是进料速率,气氛中O2与N2的体积比对脱碳效果的影响最小。

表5 煅烧样品的脱碳正交实验设计
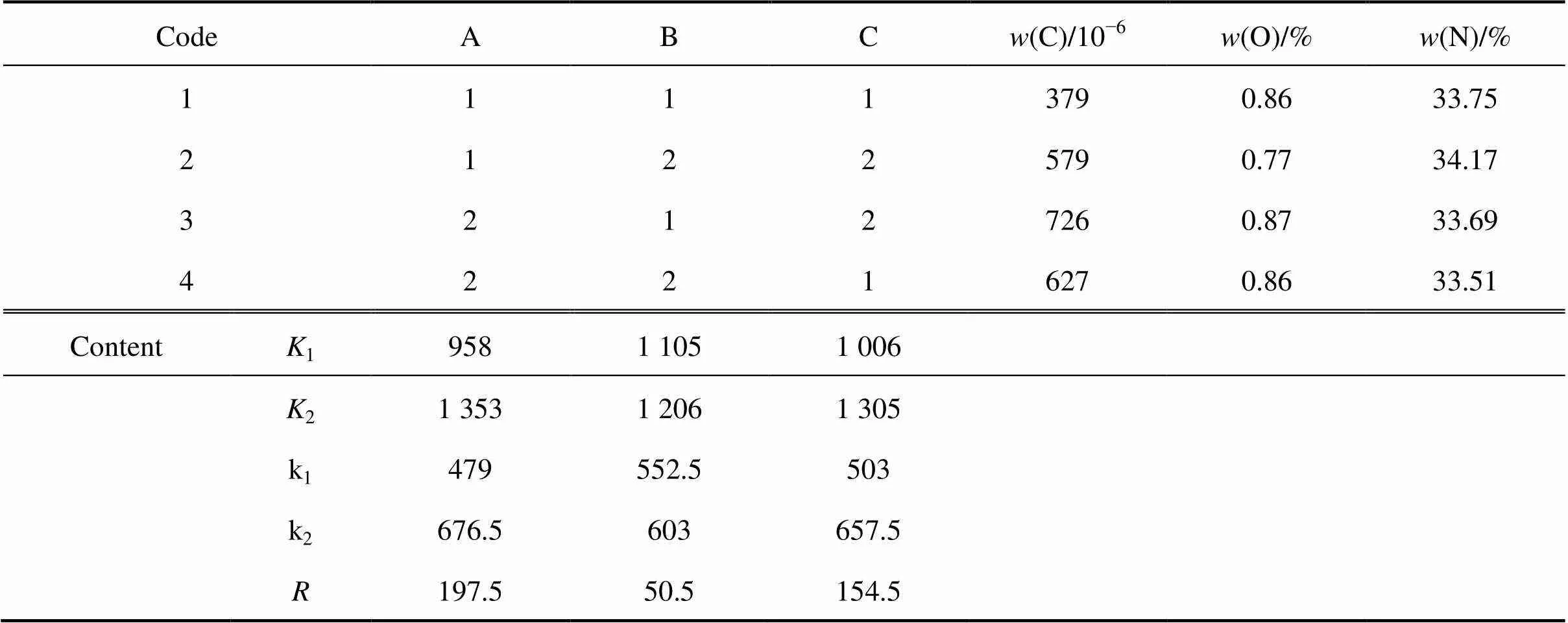
表6 煅烧样品的脱碳正交实验结果
图6所示为煅烧样品及其在最优工艺条件下脱碳后的SEM形貌。由图6可知,煅烧产物AlN在脱碳前,颗粒表面被大量细小的碳颗粒所覆盖,脱碳后,包裹在AlN颗粒表面的碳基本去除完全,AlN颗粒尺寸均约为1μm,颗粒呈圆球形,整体的粒度分布较均匀。图7和图8所示分别为脱碳后的样品经粉碎后所得AlN粉末的SEM形貌与粒度分布,由图可见AlN粉体颗粒较圆整,粉体粒度呈现正态分布,粒径分布范围较窄(0.3~4 µm),平均粒径50=1.36 µm。该AlN粉体的O,N,C含量分别为0.77%,33.42%及323× 10−6,整体指标与日本德山曹达H级AlN粉(平均粒径1.2 µm,O含量0.8%,C含量280×10−6)[16]的水平相近。

图6 煅烧样品及其脱碳后的SEM形貌

图7 经过脱碳与粉碎后的AlN粉体SEM形貌
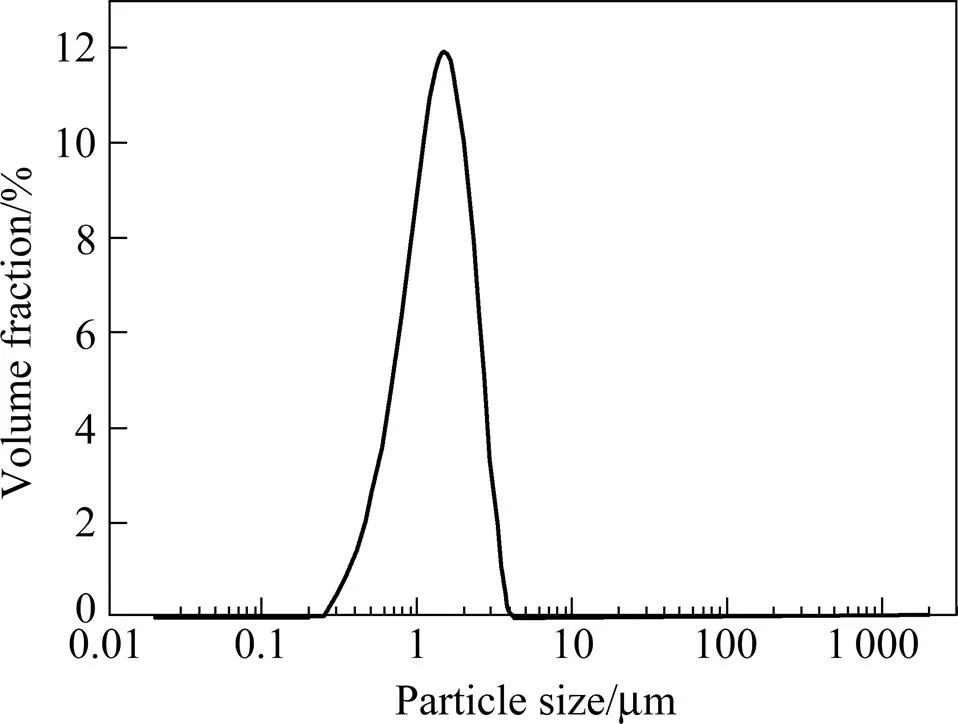
图8 经过脱碳与粉碎后的AlN粉体粒度分布曲线
3 结论
1) 将高纯超细Al2O3粉、纳米碳黑和有机粘结剂混合均匀,通过挤压成形制成的前驱体,在360 ℃/2 h排胶后为多孔结构,孔隙为球形,尺寸较小,孔隙率高,比表面积大。
2) 多孔前驱体在煅烧过程中发生碳热还原氮化反应,随煅烧温度升高,煅烧产物中的Al2O3减少,AlN增多,AlN结晶度及平均晶粒尺寸逐渐增大,1 650 ℃以上的煅烧产物中无Al2O3,AlN合成过程趋于完成。该实验结果与热力学计算结果相吻合。1 700 ℃/12 h条件下煅烧后的样品中O、N、C含量较理想,分别为0.73%,33.45%和7.87%,AlN颗粒球形度高,粒度<1 µm。
3) 在影响煅烧产物AlN脱碳效果的诸多因素中,温度的影响最大,其次是进料速率,气氛中O2与N2之体积比的影响最小。在700 ℃、(O2)/(N2)=1:0、进料速率为4 kg/h的条件下脱碳效果最佳,所得AlN粉体的O、N、C含量分别为0.77%,33.42%及323×10−6,粉体颗粒圆整,粒径分布范围较窄,平均粒径50=1.36 µm。该AlN粉体的总体特性与国外先进水平接近。
[1] YOSHIKAZU K, MASAKI I, ATSUO Y. Low temperature synthesis of AlN by addition of various Li-salts[J]. Journal of European Ceramic Society, 2004, 24 (15/16): 3801−3806.
[2] MUSSLER B H. Advanced materials & powders[J]. American Ceramic Society Bulletin, 2000, 79(6): 45−47.
[3] SHEPPARD L M. Aluminum nitride: a versatile but challenging material[J]. American Ceramic Society Bulletin, 1990, 69(11): 1801−1812.
[4] ZHOU Heping, LIU Yaocheng, WU Yin. Development of aluminum nitride ceramics[J]. Journal of the Chinese Ceramic Society, 1998, 26(2): 517−522.
[5] TUMMALA R R. Ceramic and glass-ceramic packaging in the 1990[J]. Journal of the American Ceramic Society, 1991, 74(5): 895−895.
[6] 张浩, 崔嵩, 何金奇. 高性能氮化铝粉体技术发展现状[J]. 真空电子技术, 2015(5): 14−18. ZHANG Hao, CUI Song, HE Jingqi. Technology development status of high performance aluminum nitride powder[J]. Vacuum Electronics, 2015(5): 14−18.
[7] KOMEYA K. Synthesis of AlN by direct nitridation of aluminum alloys[J]. Journal of the Ceramic Society of Japan, 1993, 101(5): 1317−1323.
[8] KIMURA I. Synthesis of aluminum nitride powder by carbothermic reduction[J]. Journal of Materials Science Letters, 1989, 8(1): 303−306.
[9] 邹东利, 阎殿然, 何继宁, 等. AlN陶瓷粉末的主要制备方法及展望[J]. 山东陶瓷, 2006, 29(4): 10−13. ZOU Dongli, YAN Dianran, HE Jining, et al. The main preparation methods and prospect of AlN ceramic powder[J]. Shandong Ceramics, 2006, 29(4): 10−13.
[10] VIRKAR A V, BARRETT J T, CUTLER R A. Thermodynamic and kinetic effects of oxygen removal on the thermal conductivity of aluminum nitride[J]. Journal of American Ceramic Society, 1989, 72(1): 2031−2042.
[11] QIN Mingli, QU Xuanhui, LIN Jianliang, et al. Synthesis of ultrafine aluminum nitride powder by a low-temperature carbothermal reduction process[J]. Key Engineering Materials, 2002, 224/226(5): 531−534.
[12] MAO Xixi, LI Jun, ZHANG Hailong, et al. Synthesis of AlN powder by carbothermal reduction-nitridation of alumina/carbon black foam[J]. Journal of Inorganic Materials, 2017, 32(10): 1115−1119.
[13] WANG Qi, GE Yiyao, KUANG Jianlei, et al. Effects of additives on the synthesis of spherical aluminum nitride granules by carbothermal reduction-nitridation process[J]. Journal of Alloys & Compounds, 2017, 696(5): 220−225.
[14] QIN Mingli, DU Xueli, WANG Jian, et al. Influence of carbon on the synthesis of AlN powder from combustion synthesis precursors[J]. Journal of the European Ceramic Society, 2009, 29(4): 795−799.
[15] 巴伦. 纯物质化学手册[M]. 第3版. 程乃良, 牛四通, 徐桂英, 译. 北京: 科学出版社, 2003: 42, 48, 209, 403, 1081. Ballon. Thermochemical Date of Pure Substances[M]. 3rd Edition. CHENG Nailiang, NIU Sitong, XU Guiying, translated. Beijing: Science Press, 2003: 42, 48, 209, 403, 1081.
[16] TOKUYAMA Co. Ltd. High purity aluminum nitride powder [EB/OL]. http://www.tokuyama.co.jp/business/specialtyproducts/ shapal/products/aln_powder_granules.html, 2018−04−19.
Syntheses and characteristics of ultrafine AlN powder by carbothermal reduction-nitridation
WEI Xin1, ZHANG Hao2, SUN Dengqiong2, TIAN Chenguang2, LIU Xiangyu1, CUI Song3, TANG Wenming1
(1. School of Materials Science and Engineering, Hefei University of Technology, Hefei 230009, China; 2. Hefei Shengda Electronic Technology Industry Co. Ltd., Hefei 230088, China; 3. 43 Institute, China Electronics Technology Group Corporation, Hefei 230088, China)
The porous precursors were fabricated by extruding the mixture of superfine Al2O3powder, nano carbon black and organic binder, and then adhesives-discharging. The precursors were calcined at high temperature to form AlN via the carbothermal reduction-nitridation reaction. Finally, the residual carbon was removed from the AlN calcined bodies and the AlN powder was obtained. Morphology, crystallinity, grain size, average particle size and the O, N and C contents of the AlN powder were investigated. The results show that the precursor has a porous structure with a high special surface area and spherical pores after adhesives-discharging at 360 ℃ for 2 h. After calcining at 1 650 ℃ and above, the product is composed of AlN, no Al2O3residues is detected, indicating fulfillment of the AlN synthesis process. This experimental result agrees well with the thermodynamic calculation. The decarburization temperature has the greatest effect on the C content of the AlN powder and the feed rate is in the second place. The AlN powder synthesized by calcining at 1 700 ℃ for 12 h and decarburizing at 700 ℃ under the conditions of the pure oxygen atmosphere and the feed rate of 4 kg/h has a composition of 0.77% O, 33.42%N and 323×10−6C. The powder also has a high degree of sphericility, a narrow particle size distribution and an average particle size (50) as low as 1.36 μm. Such characteristics of the AlN powder are close to those of the foreign similar products.
AlN powder; carbothermal reduction-nitridation; precursor; powder characteristics; calcining
TQ174
A
1673-0224(2018)06-624-08
安徽省科技攻关项目(1604a0902162);合肥工业大学大学生创新项目(2018CXCY059)
2018−04−18;
2018−06−29
汤文明,教授,博士。电话:13033050802;E-mail: wmtang69@126.com
(编辑 汤金芝)
