高效液相色谱-荧光检测法与抗生素微生物检定法测定那西肽预混剂含量的比较研究
2018-12-29林仙军周芷锦
■林仙军 周芷锦 王 彬
(浙江省兽药饲料监察所,浙江杭州311101)
那西肽(Nosiheptide)是一种含硫多肽类畜禽专用抗生素[1],能够抑制细菌蛋白质合成,低浓度抑菌,高浓度杀菌,对葡萄球菌、梭状芽孢杆菌等革兰氏阳性菌有较强的抗菌活性[2]。那西肽能促进猪[3]、鸡生长[4],提高饲料转化率,既可以作为饲料添加剂,又可作为兽药预混剂,广泛应用于畜牧业生产中。那西肽预混剂的质量标准收载于《兽药质量标准》2017年版(化学药品卷)[2],包括1 000 g∶20 g(2 000万单位)、1 000 g∶40 g(4 000万单位)和1 000 g∶80 g(8 000万单位)等6个规格,该标准采用抗生素微生物检定法[5]测定那西肽的含量,结果较准确、可靠,是传统的测定方法。但由于抗生素微生物检定法灵敏度较差[6],检测周期长,不适宜批量检测,对于偏离估计效价10%以上的样品需重新估价检测,对于有干扰或极低含量的样品则存在误差较大或无法测定等问题。
目前,那西肽的检测方法主要有气相色谱-质谱联用法[7]、高效液相色谱紫外检测法[8-9]、高效液相色谱荧光检测法[10-12]和微生物检定法[2]等。农业部公告第2382号[13]发布的那西肽发酵液干燥品配制的那西肽预混剂质量标准中规定,采用高效液相色谱紫外检测法测定那西肽组分,采用抗生素微生物检定法测定含量。
为了准确测定那西肽预混剂中那西肽的含量,参考饲料中那西肽的检测方法[11],研究了高效液相色谱-荧光检测法测定那西肽预混剂含量的方法,方法操作简便,灵敏度高,对建立的方法与抗生素微生物检定法进行比较,以期为兽药质量标准提供新的选择。
1 材料与方法
1.1 试剂与仪器
那西肽对照品购自中国兽医药品监察所,批号为K0431212,按C51H43N13O12S6计,含量88.6%,每1 mg相当于928那西肽单位;乙腈、甲醇和N,N-二甲基甲酰胺等为色谱纯;乙二胺四乙酸二钠、硼酸钠、硼酸、乙醇、氯化钠、磷酸氢二钾和氢氧化钾等为分析纯;实验用水为milli-Q超纯水。那西肽预混剂供试品(浙江汇能生物股份有限公司提供)分别为1 000 g∶20 g(2000万单位,批号为 117102501)、1 000 g∶40 g(4000万单位,批号为117102504)和1 000 g∶80 g(8 000万单位,批号为117102507);藤黄微球菌[CMCC(B)28001];抗生素检定培养基Ⅱ号(pH值6.5~6.6,杭州微生物试剂有限公司提供)。
硼酸混合溶液:取0.05 mol/l硼酸钠溶液1 000 ml,加0.2 mol/l硼酸溶液10 ml。取上述溶液-水-乙醇(1∶1∶2),混合,摇匀,即得。临用前配制。
灭菌磷酸盐缓冲液:取磷酸氢二钾13.3 g与氢氧化钾6.6 g,加水溶解成1 000 ml,滤过,在115℃灭菌30 min。
Waters 2695-2475高效液相色谱仪(配Empower 2软件);梅特勒-托利多(METTLER TOLEDO)XS-205电子天平(精度为0.01 mg);上海民桥精密科学仪器有限公司SL502 N电子天平(精度0.01 g);梅特勒-托利多(METTLER TOLEDO)FE20 pH计;昆山市超声仪器有限公司KQ-500E型超声波清洗器。多功能微生物自动测量分析仪(北京先驱威峰技术开发公司,ZY-3001V);37℃恒温培养箱;钢管自动放置器(北京先驱威峰技术开发公司,ZY-300G);三洋MLS-3780高压蒸汽灭菌锅;Thermo Scientific A2生物安全柜。
1.2 高效液相色谱法
取那西肽预混剂适量(约相当于那西肽10 mg),于100 ml量瓶中,加入N,N-二甲基甲酰胺稀释,置超声波清洗器中超声5 min,取出,冷却至室温,定容;过滤,取续滤液1.00 ml置100 ml量瓶中,用N,N-二甲基甲酰胺稀释至刻度,摇匀,过0.45 μm尼龙滤膜,上机测定。对照品溶液同法操作。
1.2.2 液相色谱参考条件
色谱柱为Waters Symmetry C18(4.6 mm×250 mm,5.0 μm);荧光检测器激发波长327 nm,发射波长521 nm;柱温为30℃;流速为1.0 ml/min;进样量为20 μl;流动相为0.02%磷酸溶液(A)和乙腈(B),梯度洗脱程序见表1。
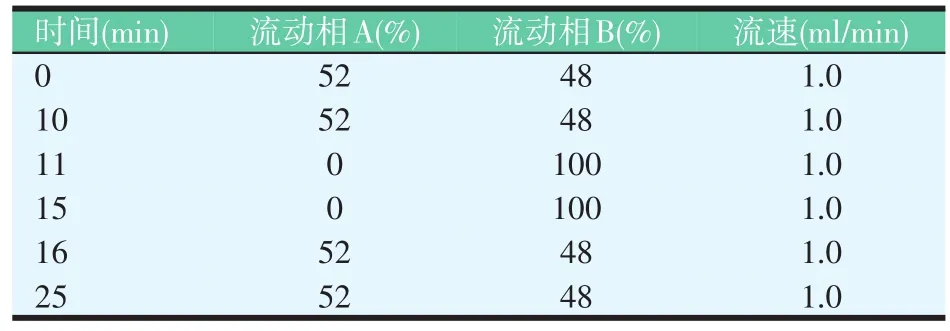
表1 流动相梯度洗脱程序
1.3 抗生素微生物检定法
1.3.1 对照品溶液和供试品溶液的配制
依据《兽药质量标准》2017年版那西肽预混剂抗生素微生物检定法二剂量法配制。取那西肽预混剂适量,于100 ml量瓶中,加入硼酸混合溶液使成每1 ml中约含250单位的溶液,在37℃恒温充分搅拌2 h,取上清液,再用灭菌磷酸盐缓冲液-乙醇(85∶15)的溶液稀释成浓度分别为每1 ml含2单位和0.5单位的溶液,作为供试品溶液的高、低浓度。对照品溶液同法操作。
1.3.2 培养基的制备与培养
取平底双碟8套,放置水平台面上,分别加入已灭菌、热的培养基约20 ml,于碟底均匀摊布,待凝固,作为底层;另取已灭菌温度降至约50℃的培养基适量,加入藤黄微球菌的菌悬液适量,能得清晰的抑菌圈,标准品溶液的高浓度所致的抑菌圈直径在18~22 mm,摇匀,在每个双碟中分别加入5 ml菌悬液,在底层均匀摊布,作为菌层;待培养基凝固后,在双碟中等距离安置不锈钢小钢管4个,将对照品溶液与供试品溶液按顺序滴加于不锈钢小钢管内,用陶瓦圆盖覆盖,在37 ℃培养16~18 h。
1.4 结果
取那西肽预混剂供试品按照高效液相色谱法和抗生素微生物检定法分别测定,每个平行测5份,结果按占标示量的百分比表示。
2 结果与分析
2.1 高效液相色谱结果分析
按照1.2测定,对照品溶液和供试品溶液典型色谱图见图1~图2,那西肽预混剂测定结果见表2。
首先,南通鹏越纺织有限公司应在本身优势产品的基础上,增加技术创新的财力物力和人力的投资。一定要及时突破“老客户、老关系”维持公司生产经营的观念思路。再者,加大“专业人才”的引进和培养。公司在研发新产品新技术的道路上,一定要能“舍得”,适时引进优秀的纺织人才和经验丰富的人才。最后,制定健全完善的人员创新激励机制。不仅对切实为公司创新的人才进行物质激励、精神激励,而且为创新人员创造更多的学习机会,帮助他们能在创新的道路上走得更快更远。更为重要的是,能创造生产出公司的“主打品牌”纺织品,增强公司的文化软实力。
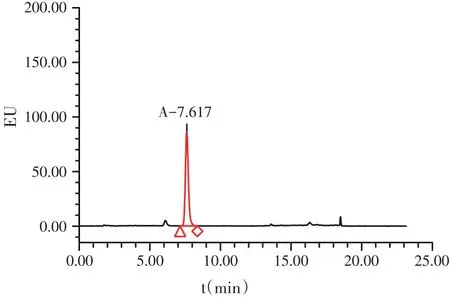
图1 对照品溶液(浓度为1 μg/ml)色谱图(A:那西肽)
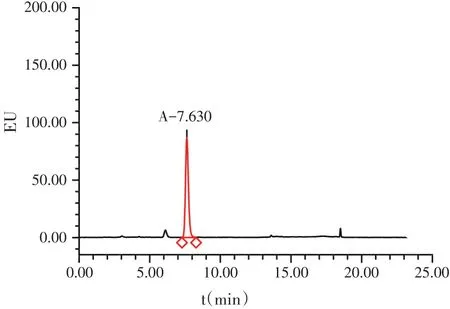
图2 那西肽预混剂供试品溶液(批号为117102501)色谱图(A:那西肽)
2.2 微生物检定法结果分析
用多功能微生物自动测量分析仪测量各抑菌圈的直径,并照生物检定统计法进行可信限率检验与效价计算,当可信限率不大于5%时,检测结果有效,测定结果见表2。
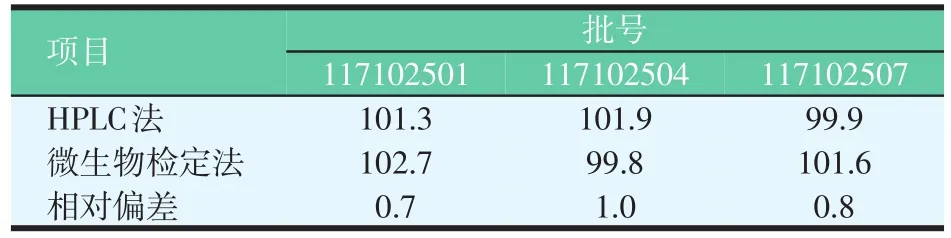
表2 HPLC法和抗生素微生物检定法测定那西肽预混剂含量结果比较(占标示量百分比平均值,n=5,%)
2.3 结果比较
HPLC法和抗生素微生物检定法测定的结果进行比较,HPLC法每批5次测定相对标准偏差均在2.0%以内,抗生素微生物检定法可信限率均在5.0%以内,两种方法占标示量百分比平均值的相对偏差在1.5%以内,表明结果无显著差异。
3 讨论
3.1 那西肽降解因素考察
那西肽作为多肽类抗生素,其贮藏条件要求密闭、阴凉干燥。那西肽溶液在光照、高温、碱、高湿、金属离子和氧化等条件下易降解[11]。取那西肽标准溶液(100 μg/ml)1.0 ml,置100 ml量瓶中,进行室温、避光、不避光、254 nm强光、4℃、-20℃等保存24 h后测定。结果,24 h内,温度和日光照射影响较小;254 nm强光照射影响较大,下降了近50%。因此,在实际的实验操作中要避免强光的照射。那西肽在氢氧化钠溶液中不稳定,已降解完全,剩余那西肽为0;在过氧化氢溶液中约降解10%;在盐酸溶液中稳定,几乎没有降解。因此,在样品前处理时要综合考虑,减少或避免这些不利因素的干扰,保证样品检测条件的一致性和稳定性,确保检测结果的准确。
3.2 乙二胺四乙酸二钠溶液的影响
实验参考了饲料中那西肽的测定方法,先加入0.2 mol/l乙二胺四乙酸二钠溶液1 ml,再加入N,N-二甲基甲酰胺,导致对照品溶液和供试品溶液浑浊,那西肽不能全部溶解。而直接加N,N-二甲基甲酰胺,对照品溶液澄清,那西肽预混剂供试品溶液由于受辅料的影响显浑浊。对两种溶解方式进行了比较,分别取溶液进样检测,发现直接加N,N-二甲基甲酰胺溶解的对照品和供试品溶液,相应的响应值高约3%,说明如果先加0.2 mol/l乙二胺四乙酸二钠溶液1 ml,再加N,N-二甲基甲酰胺有可能对测定结果产生影响,这要看对照品和供试品溶解的程度,这种方式不可取。
3.3 流动相的选择
比较了磷酸盐缓冲液、磷酸溶液和水等与乙腈组成的体系对那西肽峰色谱的影响,结果发现磷酸溶液-乙腈作为流动相,那西肽峰型最好。优化后,最终确定流动相为0.02%磷酸溶液/乙腈为52/48(V/V),流速为1.0 ml/min。由于那西肽预混剂基质比较复杂,有些样品杂质峰较多,会对检测造成干扰,影响检测的准确性。因此,在那西肽主峰出峰后设置一个梯度洗脱程序,用高有机相冲洗色谱柱,使杂质冲洗充分,确保杂质不对检测造成影响。
3.4 线性考察
取配制的标准系列工作溶液进样检测,以峰面积Y对浓度X(μg/ml)作标准曲线,以那西肽峰得出回归方程为Y=6.001 6×105X-2.988 7×104,相关系数R2为0.999 9,那西肽在 0.1~25.0 μg/ml的浓度范围内呈现良好的线性关系,能够满足那西肽预混剂含量的测定。
3.5 两种方法优缺点分析
抗生素微生物检定法作为抗生素检测的传统方法,通过对标准品和供试品溶液所产生抑菌圈直径大小的比较分析,所得的实验结果直观可靠,且真实地反映了抗生素的抑菌能力[14]。但实际操作中,对人员操作技能要求较高,影响因素较多,测定用菌悬液不易保存,需定期传代,单次实验耗时较长等问题[15]。而高效液相色谱法操作简单,影响因素较少、抗干扰强、用时短、结果准确、可靠。
4 结论
高效液相色谱-荧光检测法与抗生素微生物检定法测定那西肽预混剂含量结果无显著差异,两种方法均可以用于那西肽预混剂的含量测定。高效液相色谱-荧光检测法方便快捷,能够提高检验的质量和效率。
