白苦败痢散对靶动物猪的安全性试验
2018-12-29张鹤平刘建钗刘彦威许剑琴闫金坤杨俊琦刘利强李广东孟宪华马云飞王九峰
张鹤平,刘建钗,刘彦威,许剑琴,闫金坤,杨俊琦,刘利强,李广东,孟宪华,马云飞,王九峰
(1.中国农业大学动物医学院,北京 海淀 100193;2.河北工程大学生命科学与食品工程学院,河北 邯郸 056021;3.邯郸市动物医学重点实验室,河北 邯郸 056021;4.河北省畜牧站,河北 石家庄 050035)
白苦败痢散由白头翁、苦参、败酱草、厚朴、葶苈子组成,是治疗猪腹泻的中药复方制剂。该药以白头翁汤的组方[1-2]和治疗原则结合临床症状、生产性能等为评价指标,通过前期临床试验进行中药复方筛选并确定中药组方,前期经过小鼠急性毒性试验和长期毒性试验[3-4],显示该制剂安全。通过小鼠的抗炎、防治腹泻和体外抑菌、杀菌药效学试验,表明白苦败痢散具有相关的药效作用。在此基础上,进一步研究白苦败痢散对临床发病猪的治疗效果。为了评价白苦败痢散临床应用于靶动物猪的安全性,明确安全剂量范围,试验依据农业部《兽药研究技术指导原则汇编》有关规定,通过不同剂量灌服给药的方式开展白苦败痢散对猪的安全性试验,为其临床用药提供试验依据[5]。
1 材料与方法
1.1 材料
1.1.1 试验药品 白苦败痢散,中试批号:20160301;规格0.5 g/g,每1 g散剂中含0.5 g生药;中试生产厂家:北京中农劲腾生物技术股份有限公司。
1.1.2 试验动物 4日龄健康三元杂交哺乳仔猪32头。试验在邯郸市某猪场进行,试验动物在哺乳猪舍内使用产床饲养。按猪场常规程序进行消毒、免疫。
1.2 试验动物分组及给药(处理) 根据《兽用中药、天然药物临床试验技术指导原则》,选择4窝窝次相近,窝仔数在8头左右的4日龄健康三元杂交哺乳仔猪,每窝仔猪数均调为8头。4窝仔猪随机分为4组,以推荐的临床用药剂量(2 g/kg·bw)设置白苦败痢散1、3、5倍剂量组,白苦败痢散以生理盐水稀释成10 mL,每天上午9:00灌服给药;对照组灌服生理盐水10 mL,每天1次,连续7 d。分组及处理见表1。

表1 白苦败痢散对靶动物的安全性试验分组设计
1.3 观察指标
1.3.1 临床表现 每天上午10:00、下午2:00观察记录试验动物精神状态、哺乳、行为、粪便形态、死亡情况及中毒情况等。对死亡试验动物及时剖检并记录剖检结果。
1.3.2 生产性能 试验前和试验后(于试验第1天、第8天)对仔猪逐头进行称重,根据给药前后猪只体重,计算每组猪的平均增重。
1.3.3 血液生理学、生化学检测 给药第8天,将每组8头猪通过前腔静脉采血,分为EDTA抗凝处理和非抗凝处理,非抗凝处理血液静置1.5 h后,10 000 r/min(4℃)离心5 min,取血清于-20℃保存。抗凝处理的血液用于血液生理指标检测,非抗凝处理的血液分离得到血清用于血清生化指标检测。在邯郸市第一医院血液化验室进行血液生理和生化指标检测。对每头猪采血进行血液生理指标(白细胞、红细胞、血红蛋白、红细胞压积等)和血液生化指标(谷丙转氨酶、谷草转氨酶、尿素氮、肌酐、总蛋白等)检测。随即进行剖检病变观察和脏器指数测定。
1.3.4 脏器指数测定 给药第8天,每组随机选取3头试验仔猪分别称重并剖检,对心、肝、脾、肺、肾进行称重,计算脏器系数。观察脏器病理变化,并取心、肝、脾、肺、肾组织样品置于4%多聚甲醛中固定,进行常规石蜡切片做组织病理学观察。
根据下列公式计算各器官与体重的比值,即脏器系数。
脏器系数 =脏器重量(g)/体重(g) ×1 000‰
1.3.5 组织病理学观察 试验结束时,剖检,肉眼观察、记录上述各组剖检试验仔猪各脏器、组织是否有病理变化,包括心脏、肺脏、肝脏、肾脏、脾脏、肠道等。将4%多聚甲醛固定的肝脏、脾脏、肺脏、肾脏进行常规石蜡切片,H.E.染色,观察病理组织学变化。
1.4 结果分析 统计分析将采用SPSS 20.0统计分析软件进行计算。用单因素方差分析和多重比较对数据进行分析和差异显著性比较,试验结果以平均数 ±标准差(±S)表示,P<0.05表示差异显著。
2 结果
2.1 临床观察 试验期内,对照组、1倍剂量组、3倍剂量组、5倍剂量组所有试验动物健康状况良好,精神状况、哺乳、行为、粪便情况均正常。整个试验期间试验动物均无死亡。
2.2 各组试验猪体重、平均增重的变化 表2表明,试验前各试验组猪体重无显著差异,试验结束时,各试验组平均增重无显著差异(P>0.05)。

表2 白苦败痢散对猪体重的影响 (n=8)
2.3 血液生理指标的变化 分别检测各试验组仔猪血液中红细胞计数(RBC)、白细胞计数(WBC)、血红蛋白测定(HGB)、红细胞压积(HCT)、平均红细胞体积(MVC)、血小板计数(PLT)、红细胞平均血红蛋白含量(MCH)、平均红细胞血红蛋白浓度(MCHC)。表3表明,各试验组间仔猪的各项指标均无显著差异(P>0.05)。
2.4 血清生化指标的变化 分别检测各试验组仔猪血清谷丙转氨酶(ALT)、谷草转氨酶(AST)、总蛋白(T/P)、尿素氮(BUN)、肌酐(CRE)含量。 表4 表明,各试验组间仔猪的各项指标均无显著差异(P>0.05)。表4表明白苦败痢散对靶动物猪肝脏、肾脏功能无不良影响。
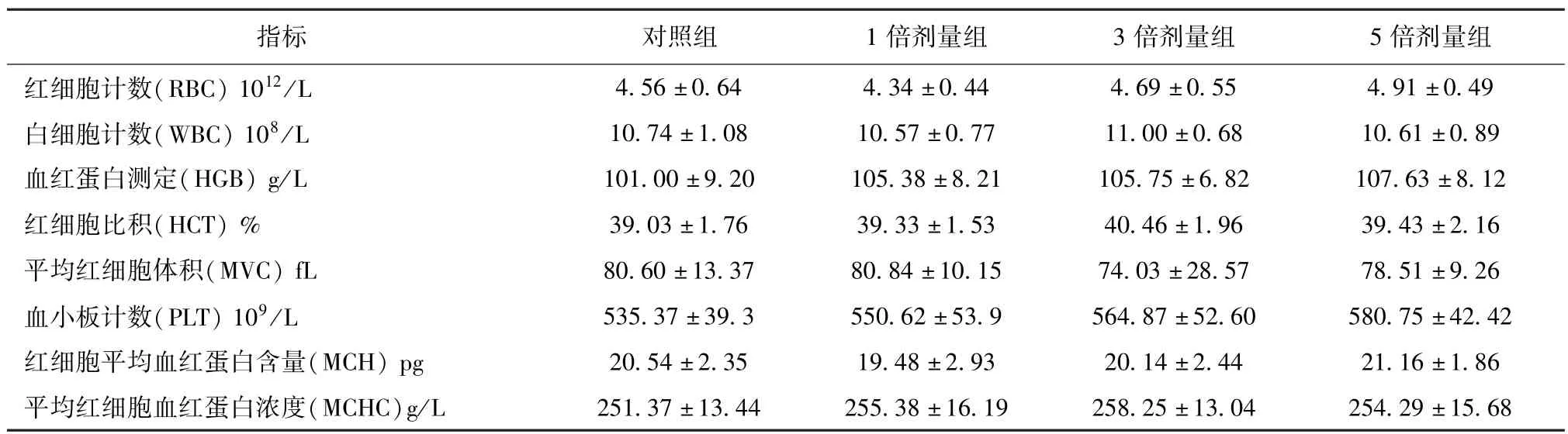
表3 白苦败痢散对猪血液生理指标的影响 (n=8)

表4 白苦败痢散对猪血清生化指标的影响 (n=8)
2.5 病理学变化和对脏器指数的影响 剖检病理变化观察结果显示,各组试验仔猪主要脏器的形态、大小、颜色等均未见明显异常变化。未见出血点、水肿、增生等病理变化。
表5表明,与对照组仔猪的心、肺、脾、肝、肾脏器指数相比,白苦败痢散1、3、5倍剂量组均未见显著异常(P>0.05)。病理剖检观察,各组试验仔猪的主要脏器未见出血点、水肿、增生等病理变化。对心、肺、脾、肝、肾、十二指肠等重要器官进行组织切片,H.E.染色结果相比显示,与对照组相比,白苦败痢散1、3、5倍剂量组仔猪各器官的组织形态结构完整,无明显病理变化。

表5 白苦败痢散对猪脏器指数的影响 (n=3)
2.6 组织学观察 给药结束后,分别对空白对照组猪、1倍剂量组猪、3倍剂量组猪、5倍剂量组猪中随机选取3头猪,采集心、肝、脾、肾、肺等各部位组织,肉眼观察无病理变化。将各组织切片进行H.E.染色,显微镜镜检观察也无病理变化。中插彩版图1为白苦败痢散对照组、1倍剂量组猪、3倍剂量组猪、5倍剂量组的组织学切片。结果显示,所有猪的心脏、肝、脾、肺、肾等均未发现明显的组织病理学变化。(1)心脏中的心肌结构正常,心外膜、心内膜结构正常;(2)肝脏中肝细胞结构正常,中央静脉及周围呈放射状排列的肝索清晰、排列整齐;(3)脾脏红髓、白髓分界明显,脾小体之间红髓清晰可见;(4)肾中肾小球、肾小管结构完整,近曲小管、远曲小管结构正常;(5)肺组织结构正常,肺泡腔、肺泡囊清晰,肺泡隔结构正常。
3 结论与讨论
猪腹泻由多种致病因素造成,主要包括病原微生物(细菌、病毒、寄生虫等)、营养性因素、气候性因素及其他因素。各生长阶段猪都可发病,以仔猪腹泻最为多发[8-10]。腹泻会导致猪存活率降低、生长发育缓慢甚至停滞、饲料报酬降低,严重影响养猪业的生产效益。兽医临床多使用抗菌素类药物治疗,导致细菌耐药性升高,抗菌药物疗效降低,药物残留对食品安全和公共卫生也产生威胁[11]。应用高效、低毒、低残留、低耐药性的药物用来防治猪腹泻,是需要迫切解决的问题。许多中药对猪腹泻有治疗作用,且具有毒性低,不易产生耐药性,无药物残留、治疗效果显著、提高机体免疫力、价格低廉等优点[12]。
白头翁苦寒,清热解毒,凉血止痢,为君药。苦参苦寒,败酱草辛苦寒,清热燥湿,解毒消痈,共为臣药。厚朴苦温,行气燥湿,降逆平喘,行胃肠之滞气并降肺气平喘;葶苈子辛苦寒,泻肺平喘,行水消肿,共为佐使药。全方共奏清热解毒,凉血止痢,降气平喘,调整胃肠功能,提高机体免疫力之功效。
靶动物安全性试验是为了了解不同剂量受试兽药作用于靶动物后,从有效作用到毒性作用,或到致死作用的持续动态变化的过程。进行靶动物安全性试验的目的是考察受试兽药在靶动物使用时的安全性及安全剂量范围,为进一步制定临床试验给药方案提供依据。观察指标包括临床体征观察、血液生理生化指标、二便(粪便、尿)等,有条件或必要时可进行剖检和组织病理学检查[7,13-14]。
本研究在前期经过小鼠急性毒性试验和长期毒性试验,确定白苦败痢散对小鼠的安全性的基础上,主要通过临床观察、血液生理生化指标检测、脏器指数观测、组织病理学变化研究白苦败痢散对猪的安全性。以推荐的白苦败痢散临床用药剂量为基础设置了1倍剂量组、3倍剂量组、5倍推荐剂量组共3个剂量组。研究表明,整个试验期间所有试验动物的精神状态、哺乳、饮水、粪便等均未出现异常,血液学、血液生化指标未见显著差异。剖检未发现明显的病理学变化。与对照组相比,1倍推荐剂量组、3倍推荐剂量组、5倍推荐剂量组的平均增重无显著性差异。
结果表明,临床推荐剂量的1倍、3倍、5倍的白苦败痢散对靶动物猪是安全的。
