海藻酸钠-月桂酰壳聚糖在盐酸中对碳钢的缓蚀作用
2018-12-20谭福能
谭福能
(文山学院 化学与工程学院,文山 663000)
腐蚀是工业和社会生产中最为广泛的破坏因素之一,据统计,在中国由腐蚀造成的直接或间接经济损失约占国民生产总值的3%~4%[1]。腐蚀虽然不可避免,但却可以人为控制并使之尽可能减缓。据统计,如果充分利用现有的腐蚀与防护技术,腐蚀带来的经济损失可以减少1/5~1/4[2]。
缓蚀剂是只需少量就能减缓金属腐蚀速率的化学物质。除了与被保护材料的种类和性质以外,其保护效果还与腐蚀介质的温度、性质等密切相关。近年来,为减少缓蚀剂的流失,缓蚀剂大多被应用于循环系统[3-5]。在实际应用中,缓蚀剂对产品质量、生产过程的影响,以及生产成本等都应全面考虑[6]。
许多传统缓蚀剂是有害的,如铬酸盐、汞盐等都是有毒的,而有机膦酸盐、磷酸盐、多聚磷酸盐等含磷缓蚀剂容易引发水体富营养化[7-10]。因此,开发绿色环境友好型缓蚀剂具有重大意义。海藻酸钠(SA)是一种天然多糖,广泛存在于海带等褐色海藻中,其稳定性、溶解性、成膜性和安全性较高,已有研究表明海藻酸钠具备一定缓蚀作用[11]。壳聚糖(CS)是自然界中仅次于纤维素的碱性多糖,其储量丰富,且具有优良的成膜性和生物降解性。壳聚糖分子中存在大量的-NH2和-OH,可提供大量孤对电子,对金属有较强的吸附作用,可作为绿色缓蚀剂,但壳聚糖分子中的氢键作用使得其溶解性较差,从而影响其缓蚀性能,限制了其应用范围[12-13]。因此,研究新型壳聚糖衍生物缓蚀剂具有重要意义。
本工作将壳聚糖进行疏水改性成月桂酰壳聚糖(LYCS),接入疏水基团使壳聚糖具有两亲性,再以戊二醛作为交联剂,制备海藻酸钠-月桂酰壳聚糖(SA-LYCS),研究了海藻酸钠-月桂酰壳聚糖在盐酸溶液中对碳钢的缓蚀行为。
1 试验
1.1 试验仪器及试剂
试验仪器有DHG-9076A型傅里叶红外变换光谱仪(日本岛津公司),CHI760电化学工作站,饱和甘汞电极(上海雷磁仪器厂),铂电极(上海雷磁仪器厂)。试验所需试剂有壳聚糖(国药集团上海试剂一厂),海藻酸钠(上海笛柏化学品技术有限公司),甲磺酸、月桂酰氯(巴斯夫化工有限公司),戊二醛(分析纯),浓盐酸(分析纯),无水乙醇(分析纯),饱和氯化钾溶液(分析纯),丙酮(分析纯),环氧树脂,聚酰胺固化剂,琼脂。
1.2 海藻酸钠-月桂酰壳聚糖的制备
海藻酸钠-月桂酰壳聚糖的制备分两步:第一步,对壳聚糖分子上的羟基进行改性;第二步,通过戊二醛将月桂酰壳聚糖上的氨基与海藻酸钠进行化学交联。具体合成路线见图1。

图1 SA-LYCS的合成路线Fig. 1 Synthetic route of SA-LYCS
在烧杯中加入25 mL甲磺酸,1 g壳聚糖,搅拌使其充分溶解;边搅拌边向壳聚糖混合液中加入2 g月桂酰氯,再加入40 mL冰水,得到絮状悬浮液,分层,收集下层产品;分别用无水乙醇洗涤产品三次,把产品置于50 ℃真空干燥箱中干燥24 h,得到月桂酰壳聚糖[14]。
在烧杯中加入0.25 g海藻酸钠,15 mL蒸馏水,不断搅拌使其溶解完全,然后加入1 g制备的月桂酰壳聚糖,继续搅拌至全部溶解;边搅拌边加入5 mL戊二醛,使其反应30 min;待溶液变为黏稠状后离心抽滤,抽滤后产物用丙酮洗涤三次,然后在50 ℃真空干燥12 h,取出产物研碎即得到海藻酸钠-月桂酰壳聚糖产品,共制得产品1.45 g。
1.3 红外光谱表征
分别将壳聚糖和制得的月桂酰壳聚糖、海藻酸钠-月桂酰壳聚糖研碎成粉末、充分干燥,用KBr压片法制备红外光谱试样。红外光谱测量的扫描范围为400~4 000 cm-1。
1.4 失重试验
将15.3 mm×15.3 mm×30.3 mm的Q235碳钢样用水相砂纸打磨,蒸馏水洗涤后再用丙酮去油、无水乙醇脱水,干燥后称量。然后将碳钢试样浸泡在1 mol/L盐酸溶液中,试验温度分别为298,303,308,313,323 K,试验时间为3 h。腐蚀完毕后取出试样,以蒸馏水超声清洗腐蚀物, 无水乙醇洗净擦干后,称量并记录其质量。采用失重法即腐蚀前后碳钢试样的质量差计算其腐蚀速率,如式(1)所示。
v=(m0-m)/At(1)
式中:v为金属在腐蚀介质中的腐蚀速率,g/(m2·h);A为金属试样的表面积,m2;t为试验周期,h;m0为腐蚀前的质量,g;m为腐蚀并清除腐蚀产物后的质量,g。根据式(2)计算缓蚀率ηw。
ηw=(v0-v)/v0×100%(2)
式中:v0为与空白溶液相应的腐蚀速率,g/(m2·h);v为与加入缓蚀剂后溶液相应的腐蚀速率,g/(m2·h)。
1.5 电化学试验
电化学试验在CHI760电化学工作站上并采用三电极系统进行。其中,铂电极为辅助电极,饱和甘汞电极为参比电极,预处理好的碳钢作为工作电极。工作电极与腐蚀介质的接触面积为0.5 cm2, 其余部分用环氧树脂固封。腐蚀介质为1 mol/L盐酸溶液,试验温度为308 K。
极化曲线测试前将预处理好的碳钢电极在待测腐蚀液中浸泡15 min,扫描方式是从阴极向阳极的全过程扫描,扫描范围是-0.8~-0.2 V,扫描速率为0.5 mV/s。
电化学阻抗谱测试频率范围为10 mHz~100 kHz,在开路电位下施加幅值为±5 mV的交流激励信号[15]。极化阻抗、溶液阻抗、双电层电容通过ZsimpWin软件处理获得。
2 结果与讨论
2.1 红外光谱
壳聚糖、月桂酰壳聚糖、海藻酸钠-月桂酰壳聚糖的红外光谱如图2所示。对比壳聚糖和月桂酰壳聚糖的红外光谱曲线可见两者存在以下不同之处:在月桂酰壳聚糖的红外谱线的2 960~2 820 cm-1处,出现了明显的-CH3的伸缩振动峰,在1 739~1 643 cm-1处出现了明显的-CH3弯曲振动的吸收峰,在1 162 cm-1处出现了C -O-C的非对称伸缩振动吸收峰。以上特征峰的出现说明壳聚糖发生了酰基化反应,生成了月桂酰壳聚糖。在海藻酸钠-月桂酰壳聚糖红外光谱曲线上,由于月桂酰壳聚糖和海藻酸钠发生了交联,使得1 077 cm-1处月桂酰壳聚糖的结晶峰移动到1 028 cm-1,这是由于戊二醛在月桂酰壳聚糖和海藻酸钠之间的交联反应产生了更强的氢键作用,扰乱了结晶的形态。

图2 壳聚糖(CS)、月桂酰壳聚糖(LYCS)、海藻酸钠-月桂酰壳聚糖 (SA-LYCS)的红外光谱图Fig. 2 IR spectra of chitosan(CS), lauroyl chitosan (LYCS) and sodium alginate-lauroyl chitosan (SA-LYCS)
2.2 失重试验
从图3可以看出:在同一温度下(308 K),海藻酸钠-月桂酰壳聚糖的缓蚀率要优于壳聚糖的,且其含量越高越明显。这是由于改性后的壳聚糖引入了疏水基团。同时,改性后壳聚糖具有两亲性,使得SA-LYCS的溶解性要优于CS的,这也扩展了其应用范围。
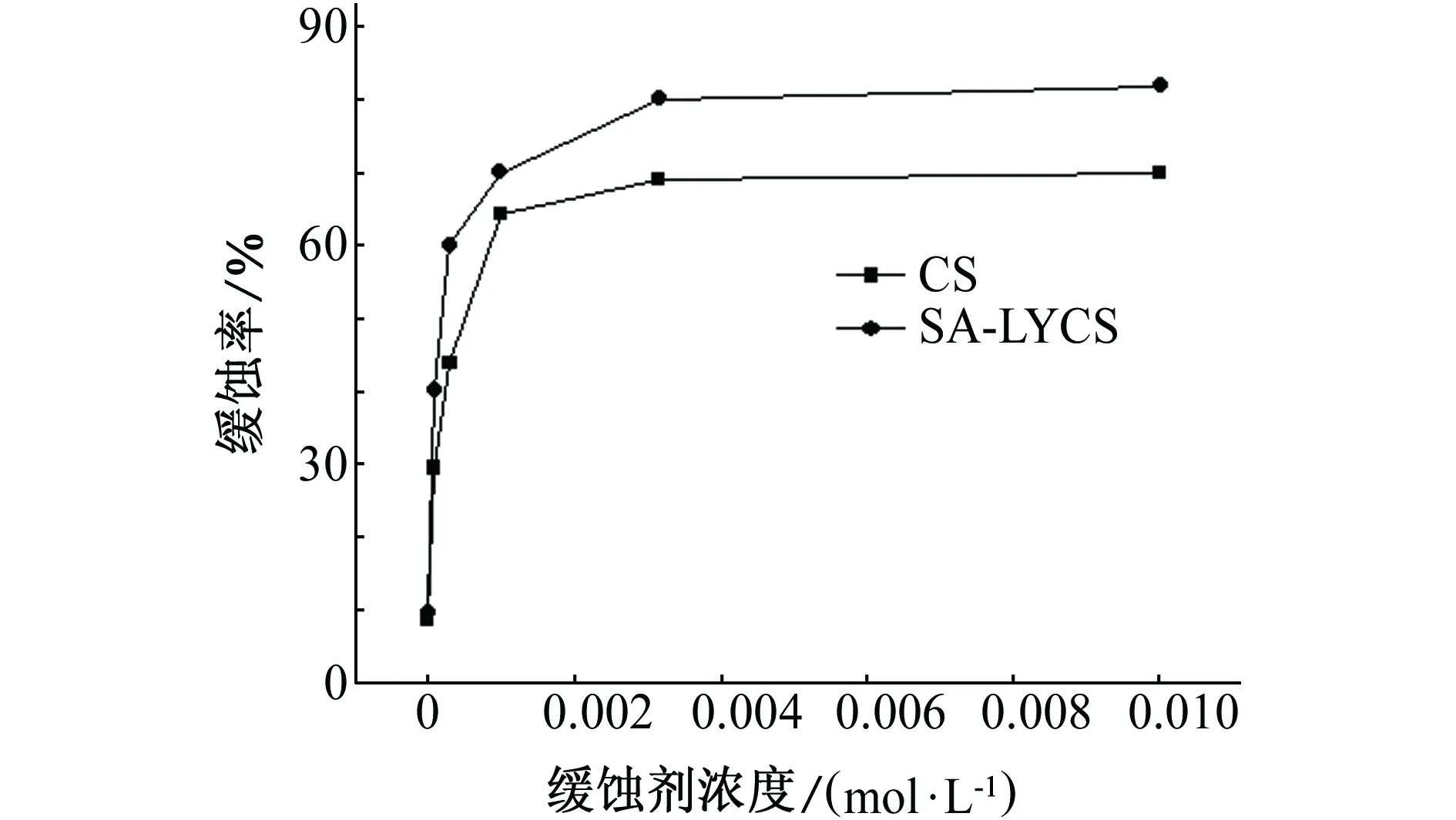
图3 不同缓蚀剂含量下壳聚糖和海藻酸钠-月桂酰壳聚糖缓蚀率对比(308 K)Fig. 3 Comparison of inhibition efficiency between CS and SA-LYCS at different concentrations (308 K)
从图4可以看出:藻酸钠-月桂酰壳聚糖的含量越高其缓蚀效果越好,当藻酸钠-月桂酰壳聚糖的浓度达到0.001 mol/L后,缓蚀率提高较慢,趋于稳定;同一缓蚀剂含量下,随温度升高,藻酸钠-月桂酰壳聚糖的缓蚀效率先增加后减小,在308 K时达到最佳,为81.86%。
2.3 吸附模型
按缓蚀剂在金属表面的吸附机理,其吸附模型通常可分为Frumkin,Langmuir和Temkin等。大多数研究者认为,Langmuir模型是研究有机缓蚀剂的最优模型之一[16],其表达式为
(3)
式中:θ为缓蚀剂对碳钢表面的覆盖度,近似等于缓蚀率ηw;c为缓蚀剂的浓度;K为吸附平衡常数,可通过式(4)计算得到。
(4)
式中:T为热力学温度;R为气体常数;ΔGm为吸附吉布斯自由能。
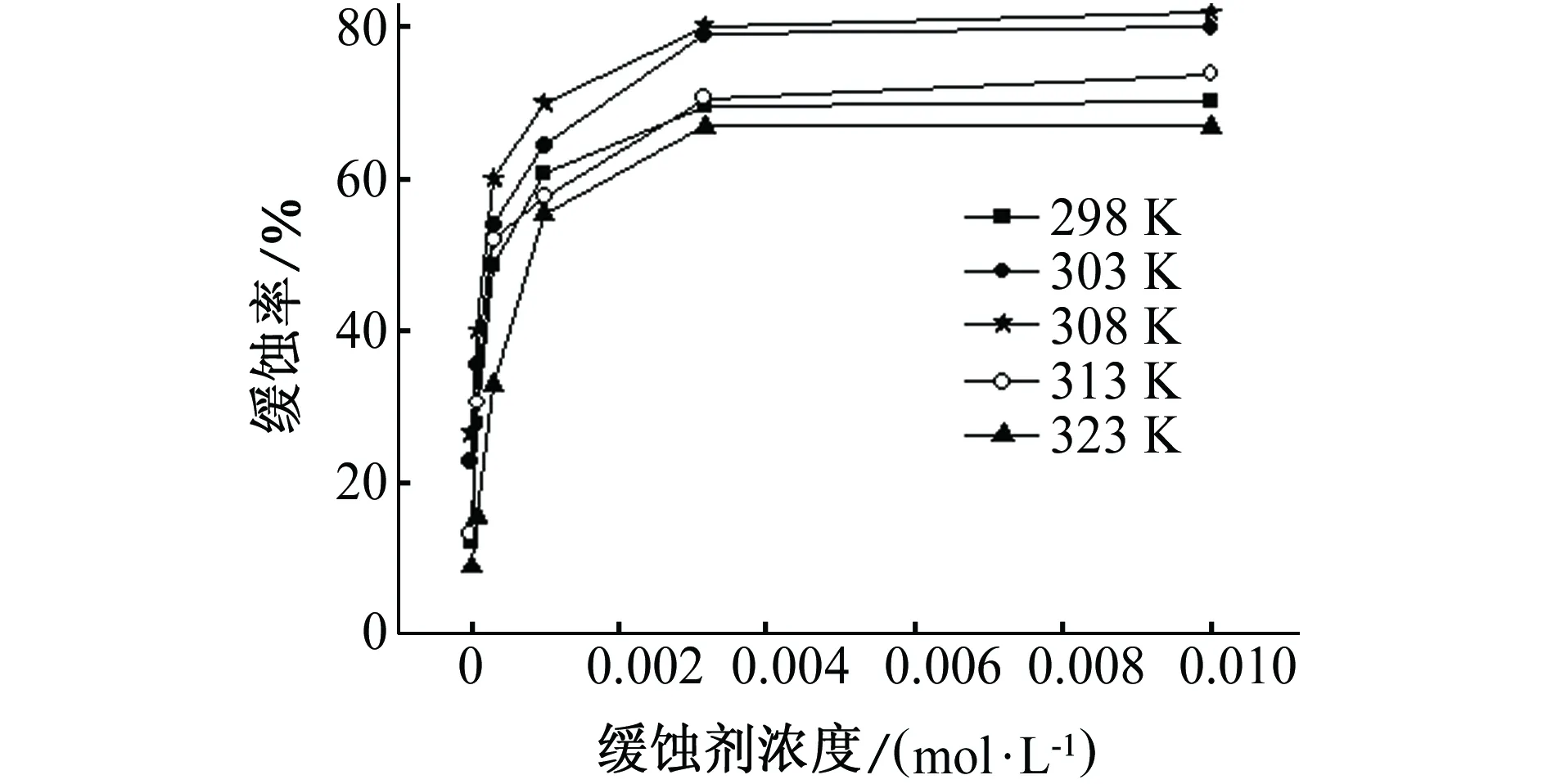
图4 不同温度和缓蚀剂含量下海藻酸钠-月桂酰壳聚糖的缓蚀率Fig. 4 Inhibition efficiency of SA-LYCS at different concentrations and different temperatures
根据失重试验得到的数据,对c/θ与c作图,可得到c/θ与c的线性相关图,对直线进行回归处理,可以得相关参数。
图5为不同含量海藻酸钠-月桂酰壳聚糖在碳钢表面的Langmuir等温线。从图5可见:在不同温度下,c/θ与c呈良好的线性关系,线性相关系数分别为0.999 41(303 K),0.999 13(308 K),0.999 54(313 K),0.999 91(323 K);拟合出的直线的斜率分别为1.134,1.256,1.165,1.089。线性相关系数和斜率都接近于1,表明海藻酸钠-月桂酰壳聚糖的吸附符合Langmuir吸附方程。
拟合直线在纵轴上的截距即为吸附平衡常数K的倒数。根据拟合结果得到不同温度下海藻酸钠-月桂酰壳聚糖在碳钢表面的吸附平衡常数分别为1.81×105(303 K),1.74×105(308 K),1.72×105(313 K)和1.75×105(323 K)。再根据式(4)求得不同温度下的ΔGm分别为-40.59 kJ/mol(303 K),-41.16 kJ/mol(308 K),-41.79 kJ/mol(313 K)和-43.18 kJ/mol(323 K)。海藻酸钠-月桂酰壳聚糖在不同温度下的吸附吉布斯自由能ΔGm均小于0,说明此吸附是一个自发过程。通常ΔGm的绝对值小于40 kJ /mol时,可以认为缓蚀剂分子是以物理吸附为主,而ΔGm的绝对值大于40 kJ/mol时,则可认为缓蚀剂分子是以化学吸附为主[16-19]。海藻酸钠-月桂酰壳聚糖在不同温度下的ΔGm的绝对值均在40 kJ/mol左右,因此可认为海藻酸钠-月桂酰壳聚糖分子在碳钢表面的吸附过程同时存在物理吸附和化学吸附,且化学吸附作用大于物理吸附作用。

图5 不同含量海藻酸钠-月桂酰壳聚糖在碳钢表面的Langmuir吸附等温线Fig. 5 Langmuir adsorption isotherm of SA-LYCS on surface of carbon steel at different concentrations
2.4 极化曲线
图6为碳钢在添加不同量海藻酸钠-月桂酰壳聚糖盐酸溶液中的极化曲线。表1为极化曲线相应的拟合参数。Jcorr为电极的腐蚀电流密度,Ecorr为自腐蚀电位,βc和βa分别为阳极和阴极Tafel拟合斜率。按(5)式计算缓蚀率ηp,从而定量判断不同浓度缓蚀剂溶液的缓蚀效果。
ηp=(1-Jcorr/Jcorr,0)×100%(5)
式中:Jcorr为添加缓蚀剂溶液中的腐蚀电流密度,Jcorr,0为空白溶液中的腐蚀电流密度。
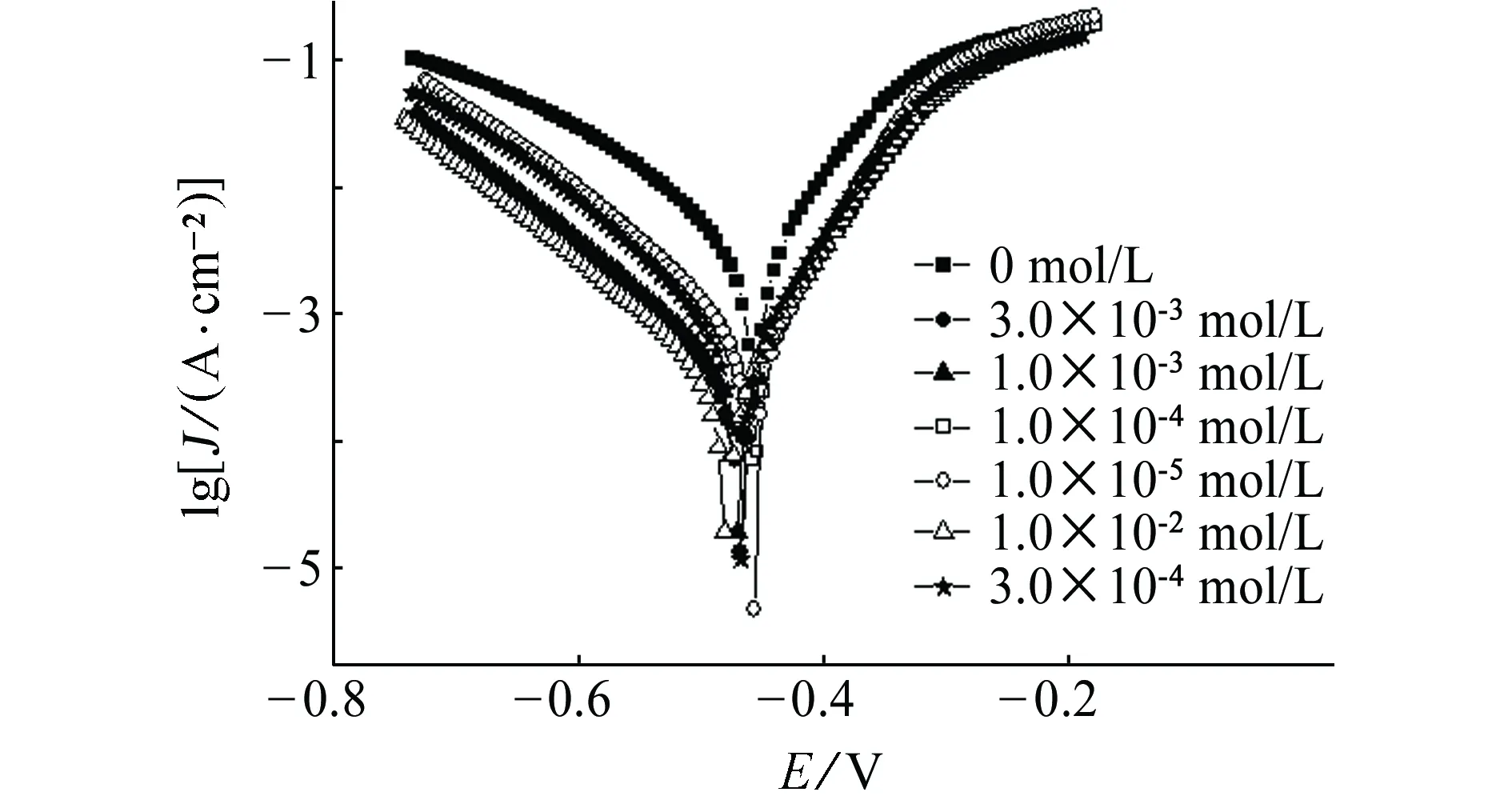
图6 碳钢在添加不同量海藻酸钠-月桂酰壳聚糖盐酸溶液中的极化曲线Fig. 6 Polarization curves of carbon steel in HCl solution added with different concentrations of SA-LYCS
从图6可看出:不同缓蚀剂含量下,阴极和阳极曲线都存在明显的Tafel区域。在缓蚀剂浓度为1.0×10-5~1.0×10-2mol/L时,随着海藻酸钠-月桂酰壳聚糖含量的增加,自腐蚀电位向负电位方向移动,阴极极化曲线向负电位方向移动较为明显,而阳极极化曲线位置变化较小,这说明海藻酸钠-月桂酰壳聚糖主要对阴极反应起抑制作用。从极化曲线形状可清楚看出,阳极曲线互相平行甚至接近重合,这说明缓蚀剂的添加并未显著改变阳极金属溶解反应的动力学参数,发生在金属表面阳极的腐蚀反应受到的抑制较小[20-21]。
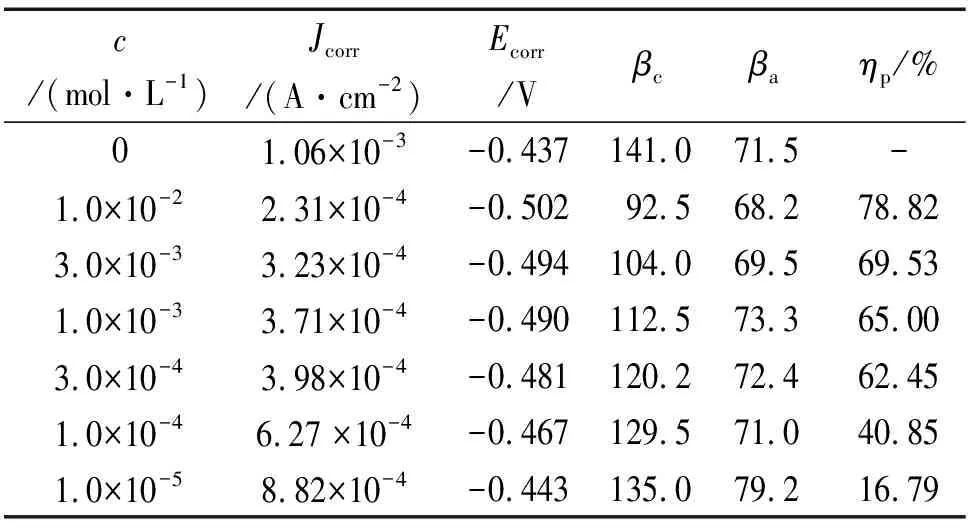
表1 碳钢在添加不同量海藻酸钠-月桂酰壳聚糖盐酸溶液中极化曲线的拟合参数Tab. 1 Fitted parameters of polarization curves of carbon steel in HCl solution added with different concentrations of SA-LYCS
从表1中看到:添加海藻酸钠-月桂酰壳聚糖后,腐蚀电流密度明显减小,并随海藻酸钠-月桂酰壳聚糖含量的增加而减小;缓蚀率随海藻酸钠-月桂酰壳聚糖含量的增加而明显增大,这说明在酸性溶液中海藻酸钠-月桂酰壳聚糖对碳钢具有较好的缓蚀效果,当海藻酸钠-月桂酰壳聚糖浓度为1.0×10-2mol/L时,缓蚀率达78.82%;随着海藻酸钠-月桂酰壳聚糖含量的增大,βc变小,而βa略有增大,这也说明海藻酸钠-月桂酰壳聚糖是以抑制阴极反应为主的混合型缓蚀剂。
2.5 电化学阻抗谱
图7为碳钢在添加不同量海藻酸钠-月桂酰壳聚糖盐酸溶液中的电化学阻抗谱,用图8所示的等效电路对电化学阻抗谱进行拟合,拟合得到的参数列于表2。然后根据式(6)计算缓蚀率ηR。其中,Rs为溶液电阻,Rct为电荷转移电阻,Cdl为双电层电容。
ηR=(Rct-Rct,0)/Rct×100%(6)
式中:Rct,0和Rct分别为空白溶液和添加缓蚀剂溶液中的电荷转移电阻。
从图7中可以看到:电化学阻抗谱的半径随海藻酸钠-月桂酰壳聚糖含量的增加而增大,这说明电荷转移电阻不断增大。电荷转移电阻越大,金属离子化过程的阻力就越大,金属腐蚀速率越小,因此电荷转移过程是控制碳钢腐蚀的影响因素。而电化学阻抗谱的低频直线部分为传质阻抗,直线斜率较小,这可能是由于碳钢表面不够平整所致。
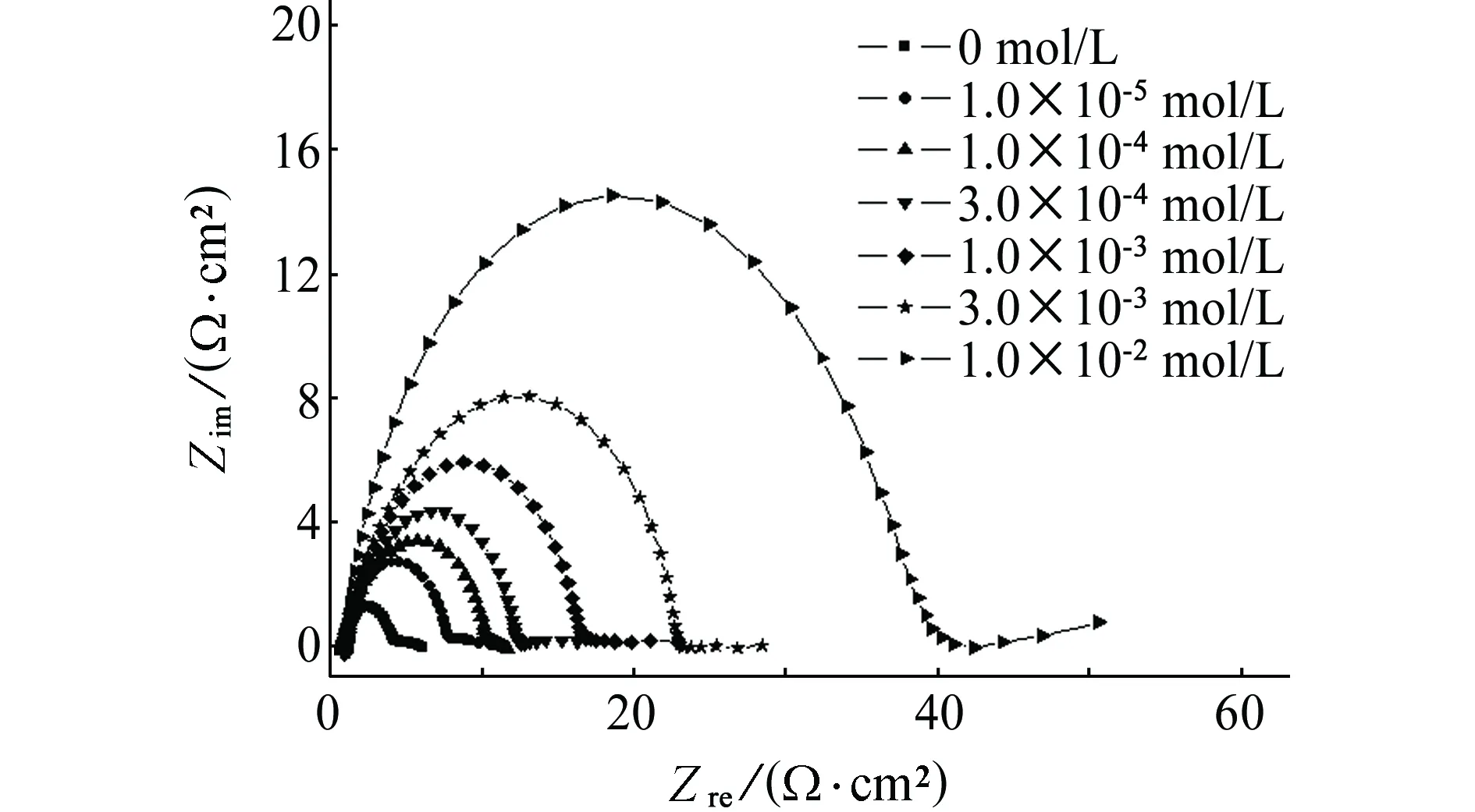
图7 碳钢在添加不同量海藻酸钠-月桂酰壳聚糖盐酸溶液中的电化学阻抗谱Fig. 7EIS of carbon steel in HCl solution added with different concentrations of SA-LYCS
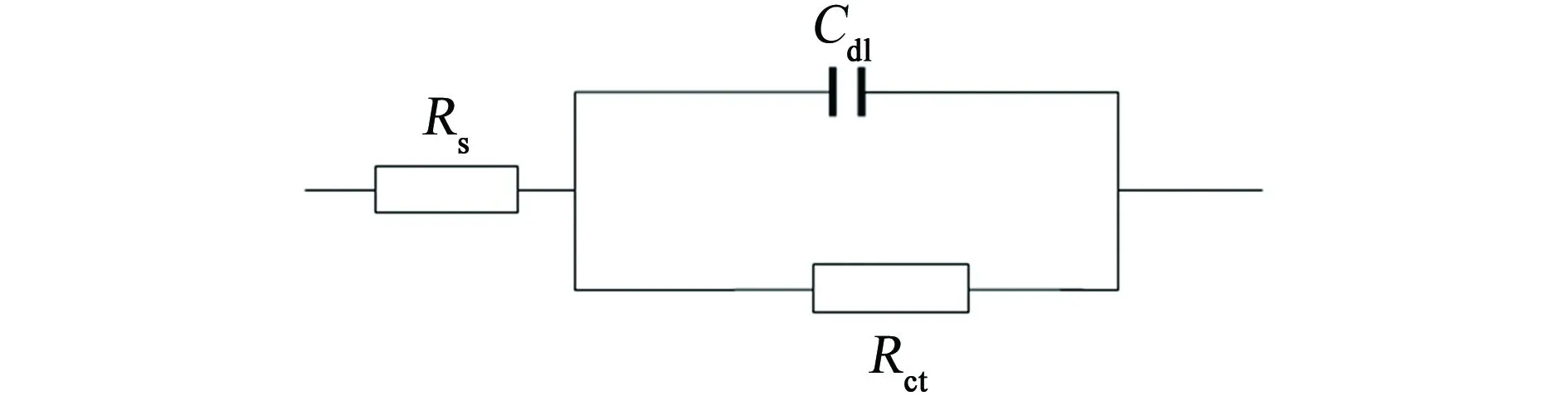
图8 电化学阻抗谱的等效电路Fig. 8 Equivalent circuit of EIS
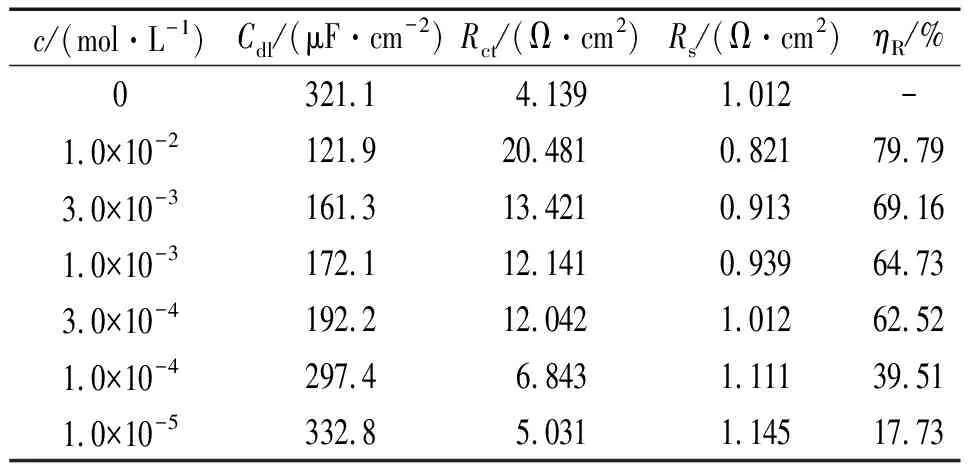
c/(mol·L-1)Cdl/(μF·cm-2)Rct/(Ω·cm2)Rs/(Ω·cm2)ηR/%0321.14.1391.012-1.0×10-2121.920.4810.82179.793.0×10-3161.313.4210.91369.161.0×10-3172.112.1410.93964.733.0×10-4192.212.0421.01262.521.0×10-4297.46.8431.11139.511.0×10-5332.85.0311.14517.73
从表2中可以看到:电荷转移电阻随海藻酸钠-月桂酰壳聚糖含量的增大而增大。这可能是因为在酸性条件下,海藻酸钠-月桂酰壳聚糖的分子链上有含C、N、O等元素的官能团,C、N、O等元素中的孤对电子可以与金属元素的空轨道发生配位作用,使缓蚀剂分子在金属表面吸附,形成保护膜。同时,海藻酸钠-月桂酰壳聚糖的分子链还具有一定的疏水作用。这些都可有效减缓金属的腐蚀,有效抑制电荷的转移,导致电荷转移量减小。海藻酸钠-月桂酰壳聚糖含量越大,双电层电容Cdl值越小。这是由于海藻酸钠-月桂酰壳聚糖分子附着到金属表面需要取代上面的水分子,而海藻酸钠-月桂酰壳聚糖分子的介电常数小于水分子,因此海藻酸钠-月桂酰壳聚糖含量越大,电极表面双电层的电容越小[22]。随着海藻酸钠-月桂酰壳聚糖含量的增大,电荷转移电阻增大,双电层电容减小,缓蚀率提高,这与失重试验和极化曲线结果基本一致。
3 结论
(1) 海藻酸钠-月桂酰壳聚糖对碳钢具有较好的缓蚀作用,其缓蚀率较壳聚糖的有所提高,且随着海藻酸钠-月桂酰壳聚糖含量的增加,缓蚀率增大。
(2) 海藻酸钠-月桂酰壳聚糖是以抑制阴极反应为主的混合型缓蚀剂,且缓蚀剂的加入未改变碳钢的腐蚀机理,即阴极发生析氢反应,阳极发生溶解反应。海藻酸钠-月桂酰壳聚糖可在碳钢表面形成一层吸附层,阻止了电荷的传递。
(3) 海藻酸钠-月桂酰壳聚糖作为一种天然无毒的新型缓蚀剂,在盐酸体系中对碳钢具有一定缓蚀作用,虽然缓蚀效果尚不及传统的化学合成缓蚀剂,但其具有绿色环保、来源广泛的优点,且可通过化学改性改善缓蚀效果,因此有望成为一种新的环境友好型酸洗缓蚀剂。
