玉米及其秸秆中氮含量的测定
2018-12-18朱健范菲菲韦时宏
朱健 范菲菲 韦时宏
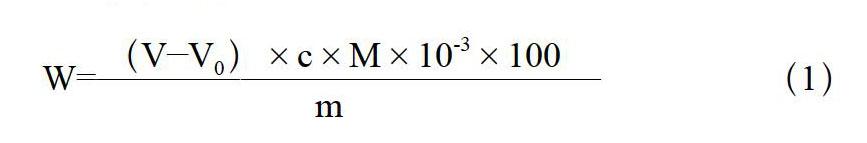

摘 要:玉米是我国主要粮食作物之一,每年可以产生大量秸秆。秸秆作为种植业中主要的副产品,是农村重要的物质资源,可以作为农村生产生活中的肥料、饲料、燃料及原料。秸秆的综合利用对于促进农业发展有重要的意义。植物在生长发育过程中需要多种营养元素,而氮素尤为重要。在所有必须营养元素中,氮是限制植物生长和形成产量的首要因素。它可以改善作物品质,也是植物体细胞原生质中的基本物质,是植物内每个活细胞的重要组成部分。除此以外,氮还是制造叶绿素的重要物质,它能够促进植物叶片浓绿,使植物生长的更茂盛。还参与植物体内蛋白质和核酸的合成,促进植物细胞不断的分裂和增长,使植物枝叶的叶面积逐渐增大。因此植物全氮能够直接反应植物的氮素营养状态。可用于植物营养诊断和施肥方案的判断。因此玉米及其秸秆中氮含量的测定可以了解植株内所含能量的情况,以便对玉米及其秸秆合理运用。
关键词:玉米;秸秆;全氮
中图分类号:S513 文獻标识码:A DOI:10.11974/nyyjs.20180932001
植物从土壤中所吸收的氮素是无机态的,当氮素进入植物体内后,通过各种中间产物而迅速形成蛋白质,所以氮是蛋白质中主要组成部分。测定植物含氮量不仅是了解植物的品质,更是了解植物自土壤中所吸收的氮量,从而为如何施用氮肥保持土壤中氮素的平衡做理论依据。
1 材料与方法
1.1 仪器及设备
高硼硅玻璃消解管(GC-20-K);小曲颈漏斗;电热消解仪;半微量定氮蒸馏器(KDN系列凯氏定氮仪);半微量滴定管(10mL);分析天平(感量0.0001g);实验室用植物粉碎机;锥形瓶(250mL);分样筛(孔径0.45mm/40目)。
1.2 试剂
混合催化剂,硫酸钾(K2SO4)100g,硫酸铜(CuSO4·5H2O)10g及硒粉0.5g,分别研磨成粉,仔细混匀过40目筛;浓硫酸[H2SO4,分析纯];氢氧化钠溶液[c(NaOH)=10mol·L-1]:400g氢氧化钠放入1L的烧杯中,加入500mL的无CO2蒸馏水溶解,冷却后,用无CO2蒸馏水定容至1L,充分混匀(储用期间避免与大气CO2接触),储于塑料瓶中;混合指示剂,溶解0.25g的溴甲酚绿(C21H14Br4O5S)(HG3-1220)和0.05g的甲基红(C15H15N3O2)(HG3-958)与50mL的95%乙醇中;硼酸指示剂溶液,溶解20g硼酸(H3BO3)于950mL的蒸馏水中,冷却后,加入20mL的混合指示剂,充分混匀后,小心滴加氢氧化钠溶液[c(NaOH)=0.1mol·L-1],直至溶液呈紫红色(pH约4.5),稀释成1L;盐酸标准溶液[c(HCl)=0.05mol·L-1],先配制[c(HCl)=0.1mol·L-1]的盐酸溶液,标定后稀释5倍;GBW10048(GSB-26)芹菜。
1.3 玉米及其秸秆的采集和处理
玉米及其秸秆为2017年9月28号采摘,为避免放置时间过长而营养元素发生变化也避免其发生霉变,采摘后及时进行了制备。新鲜的玉米及其秸秆采摘后及时进行了杀青处理,即把新鲜的玉米及其秸秆放入电热鼓风干燥烘箱中在120℃的温度下烘0.5h,然后放到准备好的干净地板砖上均匀铺成一层风干4h。后将烘干的玉米粒、秸秆用植物粉碎机进行粉碎处理,后用0.3~0.5mm孔径筛子筛虑。烘干后的样品用密封性完好的塑料袋进行封存以备使用。
1.4 植株全氮分析
1.4.1 分析原理
植株中的含氮化合物的分析,是利用浓硫酸及少量的混合催化剂,在强热高温下分解处理,使氮素转变成为NH4+[主要形成NH4SO4-1及(NH4)2SO4],但原有植株中的NO3-N并没有变成NH4+,其量极微。当加入NaOH呈强碱性,pH超过10h,NH4+则全部变为NH3而逸出,经过蒸馏用硼酸(H3BO3)液吸收,使之结合成四硼酸铵,加入指示剂再用酸标准溶液滴定(溴甲酚绿和甲基红作混合指示剂,其终点为桃红色),由酸标准液的消耗量计算出氮量[1]。
1.4.2 操作步骤
1.4.2.1 植株样的消煮
称取过0.45mm筛干燥植株样品0.1500g,放入干燥的高硼硅玻璃消解管(GC-20-K)中,加入1.5g的混合催化剂,注入2.4mL的浓硫酸,摇匀,盖上小曲颈漏斗,放在电热消解仪上,先用200℃的温度加热10min,再改用400℃继续加热,使硫酸大量冒烟,待消煮液及颗粒变为白稍带绿后,再消煮30min,摇晃时无黑色炭粒附着即可取出,放置冷却[2]。
1.4.2.2 氨的测定
将冷却的高硼硅玻璃消解管(GC-20-K)置于定氮仪上,于250mL的三角瓶中加入2%的硼酸15mL,加3滴混合指示剂,将三角置于定氮仪冷凝器的承接管下,在试样消化管中加入10mL40%的氢氧化钠,开机蒸馏2min,取下三角瓶,用酸标准溶液滴定至紫蓝色或者紫红色。同时进行空白实验,以校正试剂和滴定误差。
1.4.3 注意事项
5mL硼酸吸收液,可以有效地吸收约5mg氮,此量约为方法中植株样所释放出总氮量的5倍。混合指示剂最好在使用时与硼酸溶液混合;如果混合过久,则可能有终点不灵的现象出现。
高硼硅玻璃消解管的使用温度不能超过450℃。
为保证获得精确的测定结果,蛋白质含量≥1g/100g时,结果保留3位有效数字;蛋白质含量≤1g/100g时,结果保留2位有效数字。在重复性条件下获得的2次独立测定结果绝对值不得超过算术平方值的10%[3]。
1.5 结果计算
1.5.1 计算公式
(1)式中:W——植株试样中蛋白质的含量:g.100g-1;c——盐酸标准溶液的浓度:[c(HCl)=0.05mol·L-1];V——植株试样测定时所消耗鹽酸的体积:mL;V0——空白测定消耗的盐酸体积:mL;M——氮的摩尔质量(M(N)=14g·mol-1);m——植株试样的质量:g;10-3——将mL换算成L的系数;2次平行测定结果绝对值不得超过算术平方值的10%[3]。
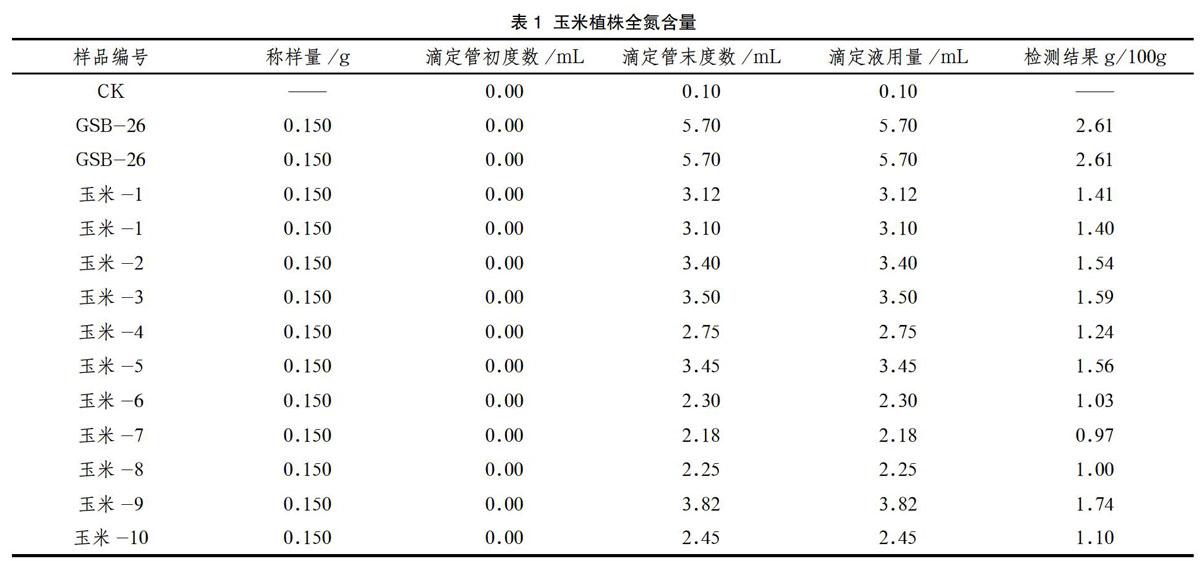
1.5.2 结果
2 结论与讨论
使用半微量定氮蒸馏器(KDN系列凯氏定氮仪)测定玉米及其中全氮成分含量,具有较高的准确度和良好的精密度。能够准确地测定玉米及其秸秆中氮的含量,以便对玉米及其秸秆的合理利用提供理论依据。
参考文献
[1]中国科学院南京土壤研究所.土壤理化分析[M].上海:上海科学技术出版社,1978.
[2] Honda.C.Rapid Procedure for Determination of Nitrogen in Soil by Kjeldahl Method[J].J.Sci.soil Manure,1962(33):195-200.
[3] GB 5009.5-2016食品安全国家标准 食品中蛋白质的测定[S].北京:中华人民共和国卫生部,2016.
