腹腔镜超声引导下射频消融治疗大肠癌肝转移的临床应用分析
2018-12-17王桃英杜苗苗
申 健 加 静 王桃英 王 煜 杜苗苗
近年来,随着人们饮食结构和社会环境的改变,大肠癌的发病率逐渐增加。大肠癌是消化道最常见的肿瘤之一,在我国的发病率高居全国第三位,病死率也较高,最常见的转移是肝转移[1-2]。有研究显示[3-4],约有15% ~ 25%的大肠癌患者在初次被确诊时就出现肝转移,而约有40% ~ 50%的患者在疾病进展过程中出现肝转移。目前,手术切除是治疗大肠癌肝转移的主要手段之一,但大多数患者因为出现肝内多发转移、肝外转移以及肝脏储备功能差等原因而错失手术机会[5-6]。近年来有研究显示,腹腔镜超声引导下射频消融大肠癌肝转移临床效果显著,但目前国内对此方面的研究还相对较少[7],故本研究分析了腹腔镜超声引导下射频消融大肠癌肝转移的临床应用,具体内容报道如下。
资料与方法
一、一般资料
本文研究对象为2014年4月至2016年4月我院收治的110例大肠癌肝转移患者,随机分为对照组与观察组,各55例。对照组患者行传统开腹手术,观察组患者行腹腔镜超声引导下射频消融大肠癌肝转移治疗。对照组女性24例,男性31例,年龄36 ~ 77岁,平均(55.97 ± 2.39)岁;其中直肠癌17例,乙状结肠癌12例,升结肠癌11例,降结肠癌8例,横结肠癌7例;肝转移灶数目为1 ~ 8个,平均数目为(3.12 ± 0.34)个,肝转移灶直径为1 ~ 5 cm,平均直径为(2.41 ± 0.37)cm。观察组女性27例,男性28例,年龄34 ~ 76岁,平均(54.68 ± 2.51)岁;其中直肠癌19例,乙状结肠癌14例,升结肠癌10例,降结肠癌7例,横结肠癌5例;肝转移灶数目为2 ~ 7个,平均数目为(3.62 ± 0.28)个;肝转移灶直径1 ~ 4 cm,平均直径为(2.19 ± 0.27)cm。两组一般资料经比较,差异无统计学意义(P> 0.05)。两组患者均签署知情同意书,并获得我院医学伦理委员会批准。
二、纳入和排除标准
1. 纳入标准
①经电子肠镜检查和病理检查确诊为大肠癌,且肿瘤位置及病理类型明确;②经MRI、CT确诊为大肠癌肝转移;③肝功能Child-Pugh分级为A或B;④未合并急性肠梗阻。
2. 排除标准
①有肝切除或消融禁忌症;②存在腹部开放手术史者;③肿瘤出现多器官转移者;④存在心、肺等重要器官功能不全者;⑤难治性凝血机制不良者;⑥发生门静脉癌栓者;⑦肿瘤出现肝外其它部位转移。
三、方法
对照组患者进行传统开腹手术。患者取仰卧位,采用全身麻醉,患者在进入全麻状态后,手术切口的选择根据肿瘤的部位,然后手术切开各层组织进入腹部,在直视情况下根治性切除大肠癌以及进行消化道重建,然后再进行肝转移灶的切除,最后缝合手术切口,留置引流管。
观察组患者采用腹腔镜超声引导下射频消融大肠癌肝转移的手术方法。术前常规检查,对患者的心肺等重要器官进行评估,并排除手术禁忌证。患者取仰卧位,采用全身麻醉,麻醉成功后建立气腹,在脐周戳4 ~ 5个Trocar孔,然后进行腹腔探查,观察大肠肿瘤的位置、大小等情况,在腹腔镜下进行根治性切除大肠肿瘤,并进行消化道重建,然后进行肝转移灶射频消融治疗,在进行射频消融前常规切取肝肿瘤组织进行病理检查。在剑突下放入10 mm Trocar,在超声辅助下利用腹腔镜进行肝脏肿瘤位置、大小以及数目的确定,并利用超声进行定位,确定肿瘤的具体位置以及进针深度等,然后在腹腔镜监视下,从腹壁或者Trocar进针至肿瘤位置,利用超声再次进行定位,然后展开电极针伞端,将肿瘤的位置锁定住,利用射频消融器对肝转移灶进行消融,射频针采用Cool-tip集束消融电极(ACT2025)和射频发生器(柯惠医疗),根据肿瘤的大小来选择不同规格的射频消融针具,射频消融器功率设为150 ~ 200 W,靶向温度设置为90 ~ 110 ℃,以肿瘤为中心,以肝组织周围0.5 ~ 1.0 cm为范围进行消融,完成消融后,应及时通过超声对消融的范围和效果以及周围肝组织的消融变化进行复查。对于位于肝表面的肿瘤,为了防止膈肌或空腔脏器受到损伤,射频针经皮穿刺至肿瘤进行消融时,应在腹腔镜下将周围的空腔脏器拨开同时牵拉左右三角韧带及镰状韧带。对于位于肝实质内的肿瘤,则应该暂时终止气腹,在超声辅助引导下进行穿刺进针至肿瘤位置后重新建立气腹,然后再开始进行上述射频消融治疗。对于特殊位置的肿瘤可以采用多点重叠消融的策略,每个点消融时间为15 ~ 25 min,从而达到最佳的消融效果。
采用电话或者上门调查随访,随访截止时间2018年4月,统计两组复发率以及存活情况。
三、观察指标
对比两组的手术时间、术中出血量、术后首次排气时间和住院时间,以及术后并发症的发生率和治疗后1年及2年生存率。
四、统计方法
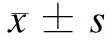
结 果
一、两组临床指标对比
与对照组相比,观察组的手术时间、术中出血量、术后首次排气时间和住院时间均显著较短(较少),差异均有统计学意义(P< 0.05),见表1。

表1 临床指标对比
二、两组术后并发症发生率比较
两组主要并发症为肠梗阻、肺部感染、吻合口瘘,观察组的并发症总发生率为3.6%,显著低于对照组的21.8%,差异有统计学意义(P< 0.05),见表2。

表2 两组术后并发症发生率比较 [n(%)]
注:*与对照组比较,χ2= 8.185,P= 0.004
三、两组治疗后1年和2年生存率比较
两组治疗后1年和2年生存率比较,差异均无统计学意义(P> 0.05),见表3。
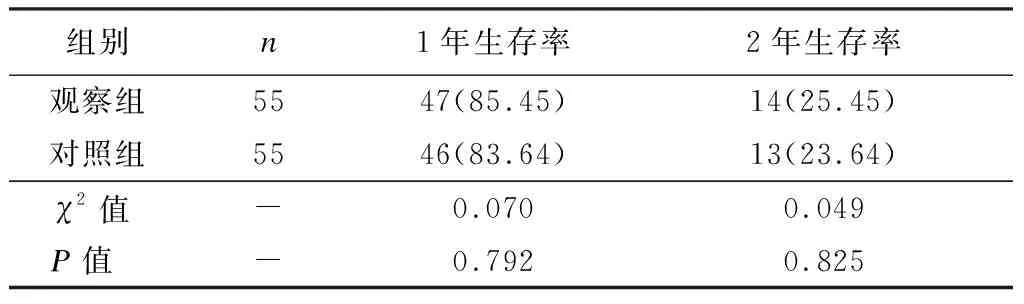
表3 两组治疗后1年和2年生存率比较 [n(%)]
讨 论
作为临床常见的恶性肿瘤之一,大肠癌包括结肠癌和直肠癌[8-9],该疾病的发生与遗传因素、大肠慢性炎症、高脂肪低纤维素饮食、大肠腺瘤及环境因素、血吸虫病、吸烟等有关[10]。大肠癌早期症状并不明显或者无症状,随着病情的不断发展,患者会出现腹痛、腹部包块、肠梗阻、大便习惯改变、发热、消瘦、伴或不伴贫血等症状,并也可因转移、浸润从而引起受累器官的改变,最常见的转移器官为肝脏。手术切除是治疗大肠癌肝转移的主要手段之一[11-12];近年来,随着腹腔镜技术的不断发展,逐渐在临床得到广泛的应用。有研究显示[13],在腹腔镜下超声辅助引导射频消融可以有效治疗大肠癌肝转移,且临床效果显著。射频消融技术是对射频针进行加热,利用其热效应使肿瘤细胞发生凝固坏死,从而达到消灭肿瘤的目的,手术损伤小,患者术后恢复较快,而且在腹腔镜和超声的辅助下,可以相对准确的判断肿瘤的位置和大小,提高了手术的准确性[14-16]。但是腹腔镜手术对术者的要求较高[17-18],术者需熟练掌握腹腔镜手术的操作方法和步骤,必要时可联合传统开腹切除手术来提高治疗效果。
本研究结果显示:与对照组相比,观察组患者的手术时间、术中出血量、术后首次排气时间和住院时间均显著较短(较少),这说明腹腔镜超声引导下射频消融大肠癌肝转移与传统开腹手术相比,不仅可以有效减少手术时间和术中出血量,对患者的损伤较小,而且术后恢复较快,这与国内学者张雯雯等报道内容相近[19];两组患者术后并发症发生情况对比方面,观察组显著低于对照组,两组患者治疗后一年和两年生存率无显著差异,这说明与传统开腹手术相比,采用腹腔镜超声引导下射频消融大肠癌肝转移的手术方法能够有效的减少患者术后肠梗阻,肺部感染,吻合口瘘并发症的发生,从而减轻患者的痛苦,而两组患者术后生存率无显著差异,这与国内学者高楠等报道内容相近[20]。
综上所述,与传统的开腹手术相比,采用腹腔镜超声引导下射频消融大肠癌肝转移的手术方法患者术中出血量少,手术时间短,也缩短了患者术后恢复时间及住院时间,并且降低了患者术后肠梗阻,肺部感染,吻合口瘘并发症的发生率,减轻了患者痛苦,因此在临床上值得进一步推广应用。
