肉制品中喹诺酮残留检测
2018-12-14张宏博王洋王燕王岩靳志敏范鑫郑玉山
张宏博 王洋 王燕 王岩 靳志敏 范鑫 郑玉山
摘 要:喹诺酮类药物是具有4-喹诺酮基本结构并且由人工合成的抗生素类药物,是一种人畜共用药,食用含有喹诺酮残留的食品会对人体造成危害。本实验参照GB/T 21312-2007,采用液相色谱-质谱/质谱法对羊肉中6种喹诺酮类药物的残留量进行检测。检测结果显示,环丙沙星、氧氟沙星、培氟沙星、諾氟沙星、恩诺沙星、洛美沙星检出限分别为0.06μg/kg、0.02μg/kg、0.07μg/kg、0.05μg/kg、0.06μg/kg、0.05μg/kg;回收率为84.1%~102.1%,各物质的精密度依次是10.5%、7.4%、8.5%、6.8%、6.9%、7.2%;空白对照值为零;本次实验所采集的12种羊肉样品均未检出环丙沙星、氧氟沙星、培氟沙星、诺氟沙星、恩诺沙星、洛美沙星这6种抗生素类药物,符合农业部标准。
关键词:液相色谱-质谱/质谱法 喹诺酮类药物 氧氟沙星 环丙沙星 诺氟沙星
1 引言
抗生素类兽药长期无节制的使用会导致动物免疫力下降,同时降低了疫苗的作用,进而使细菌疾病成为家禽的重点传染疾病[1]。喹诺酮是一类人畜通用药,因其具有组织浓度高、药物保留性好、抵抗多种细菌、杀菌作用强、抗菌时间长等特点而被广泛应用于水产和畜禽等疾病的治疗[7]。尽管喹诺酮药物有诸多优良品质,但仍需重视其毒副作用,如造成肝损害、引发周围神经病变时间加快,甚至可能产生不可逆的转变——导致肌无力症状的患者病情加重等[8]。
喹诺酮是羊肉检测中最为常见的一种兽药残留,其严重影响羊肉制品的安全及羊养殖业的发展,也已成为我国羊肉食品出口的主要制约因素。因此,检测羊肉中喹诺酮的残留对于食品安全管控有重大意义。
2 材料与方法
本实验参照GB/T 21312-2007农业部第235号公告,利用液相色谱-质谱/质谱法检测羊肉中培氟沙星、诺氟沙星、恩诺沙星、氧氟沙星、洛美沙星、环丙沙星6种喹诺酮的残留量。
2.1 设备
实验设备如表1所示。
2.2 试剂
除特别标注外,此次实验中所使用的试剂全部都为色谱纯,水为GB/T 6682规定的一级水,实验试剂如表2所示。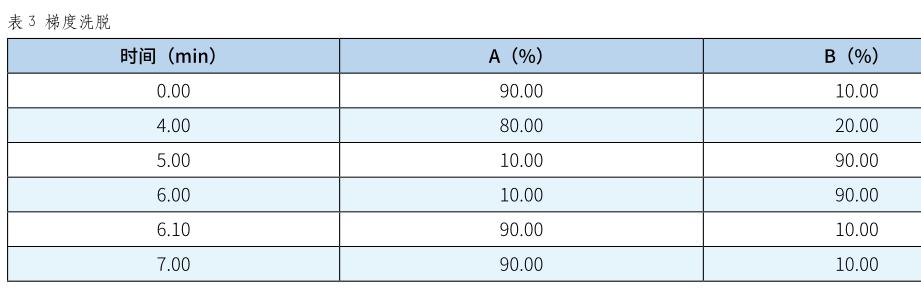
2.3 喹诺酮类药物的检测方法
2.3.1 提取
称取5g试样(精确至0.01g),装于50mL具螺旋盖聚四氟乙烯离心管中,之后加入10mL甲酸-乙腈(2∶98)溶液,立即盖盖剧烈振摇,旋涡震荡1分钟,超声提取10分钟,4000r/min离心5分钟,然后将乙腈层移入另一干净的聚四氟乙烯离心管中。向离心后的沉淀物中再加入10mL甲酸-乙腈(2∶98)溶液摇匀,旋涡震荡1分钟,4000r/min离心5分钟,合并乙腈提取液,待净化。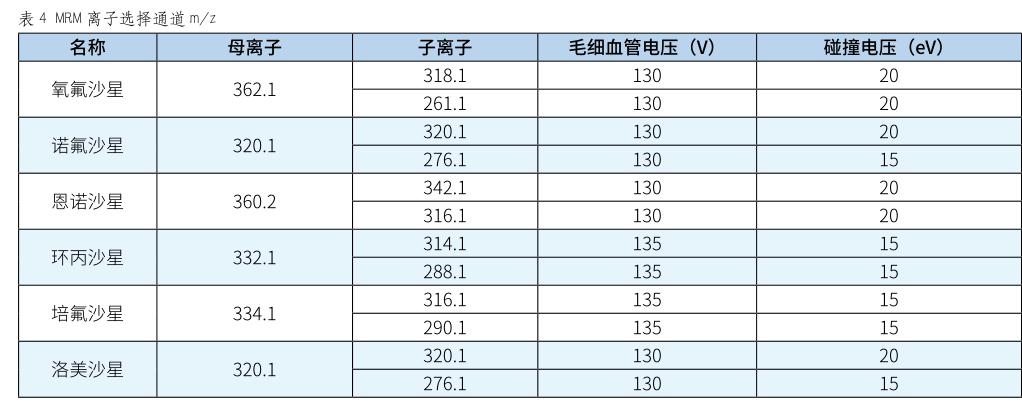
2.3.2 净化
向提取液中加入15mL乙腈饱和正己烷溶液,漩涡震荡2分钟,4000r/min离心5分钟,除去上层正己烷,氮吹至干。准确加入1mL初始比例流动相溶液,超声1分钟,旋涡震荡1分钟溶解残渣,将溶液过0.22μm微孔滤膜,供高效液相色谱-质谱/质谱测定。
2.3.3 高效液相色谱-质谱/质谱法测定
液相色谱条件:色谱柱固定相类型为C18、色谱柱型号为ZORBAX Eclipse Plus C18;规格:2.1×100mm×1.8μm;柱温:40℃;室温:22℃;流动相组成:A为0.05%甲酸/水、B为乙腈;流速:0.3mL/min;进样量:3μL。
最优质谱条件:离子源(电喷雾正离子源);检测方式:多反映监测;电喷雾电压:4 0 00 V;离子源温度:3 5 0℃,汇总得出结果如表4。
3. 结果与分析
3.1 喹诺酮类标准物质
在浓度为5.0ng/mL、10.0ng/mL、20.0ng/m L、8 0 . 0 n g / m L、1 0 0 . 0 n g / m L得到的线性方程,洛美沙星:Y = 5 2 . 8 6 8 6 5 0 X + 1 6 . 2 9 4 1 1 5;恩诺沙星:Y = 7 7 . 5 7 3 1 3 1 X + 3 9 . 5 9 3 3 1 0;诺氟沙星:Y = 3 5 . 5 5 7 6 7 1 X- 0 . 9 2 2 8 2 0;环丙沙星:Y = 2 6 . 1 1 8 1 6 3 X + 1 9 . 6 6 1 1 3 6;氧氟沙星: Y = 8 9 . 4 3 5 7 1 7 X + 1 7 . 0 1 1 2 8 9;培氟沙星:Y = 4 1 . 0 9 7 3 6 0 X + 1 3 0 . 3 8 7 5 4 6。相关系数R2均为0 . 9 9,峰面积与被测物质浓度呈现出的线性关系良好。
3.2 试剂空白
样品空白如表6所示,在3 . 0 2 1 ~ 3 . 2 0 1 m i n之间没有出现峰,所以诺氟沙星未检出;在3 . 1 8 1 ~ 3 . 6 2 1 m i n之间没有出现峰,所以氧氟沙星未检出;在2 . 9 0 1 ~ 3 . 3 4 1 m i n之间没有出现峰,所以培氟沙星未检出;在3 . 1 4 1 ~ 3 . 3 2 1 m i n之间没有出现峰,所以环丙沙星未检出;在2 . 6 5 1 ~ 2 . 5 2 1 m i n之间没有出现峰,所以洛美沙星未检出;在3 . 1 6 1 ~ 3 . 6 0 2 m i n之间没有出现峰,所以恩诺沙星未检出。
如表7所示,本次实验检测方法为,建立6个加入浓度为100ng /mL混合中间标准溶液50μL的空白试验与空白试剂对照,将检测到的各个噪音参数的结果记下来,当S / N =3时得到的最低浓度结果为检出限。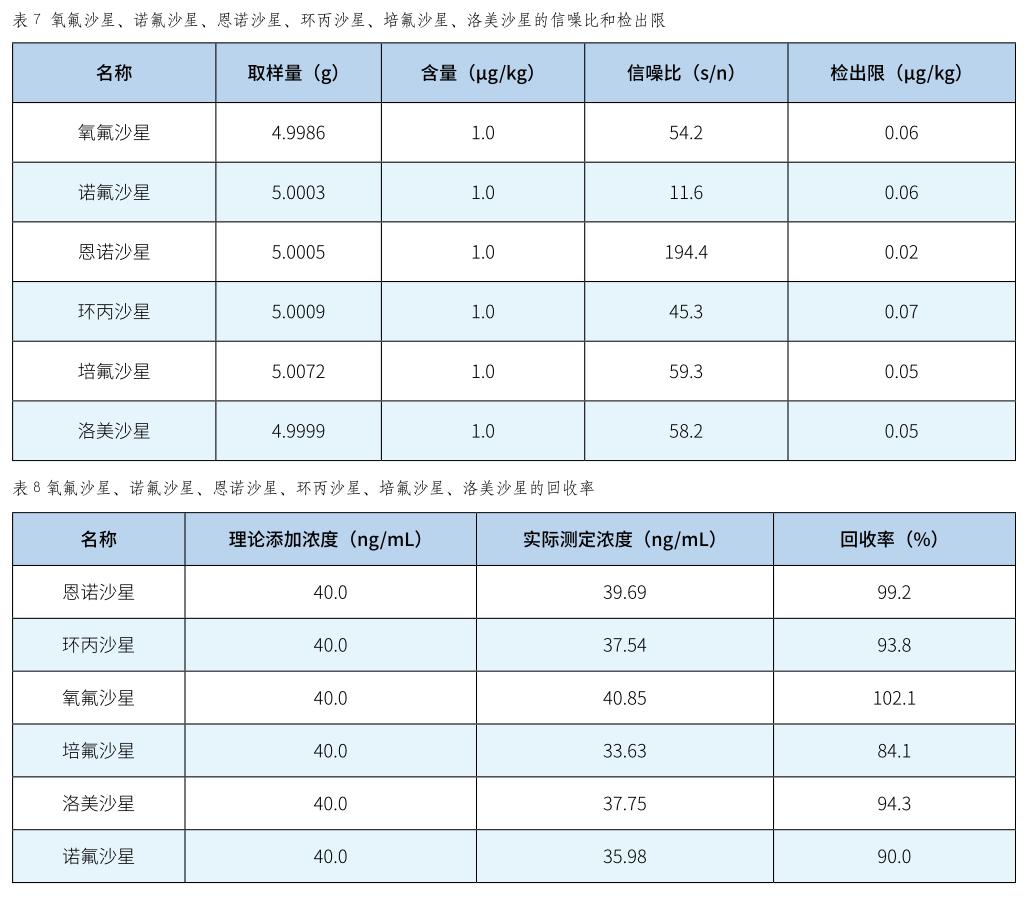
3.4 回收率
如表8所示,因為在实验过程中所有加入的物质都会有一定损失,故可能导致最终结果有所误差。为防止这一现象的发生,在羊肉中加入已知浓度的标准样液,经过涡旋震荡后按实验步骤作其检测值与羊肉样品检测值比较计算,从而知晓试剂是否有配对,羊肉样品的检测结果是否无误。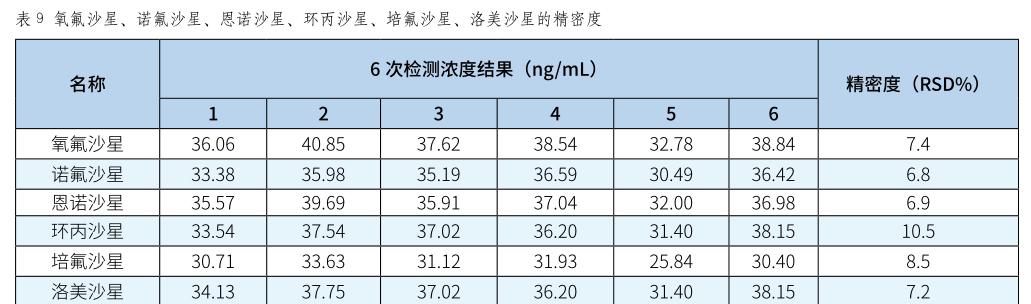
3.5 精密度
精密称取6个空白样品,加入1μg / m L的混合标准中间溶液40μL,按样品处理同法操作。经计算得出,氧氟沙星精密度为7 . 4 %、诺氟沙星精密度为6 . 8 %、恩诺沙星精密度为6 . 9 %、环丙沙星精密度为1 0 . 5%、培氟沙星精密度为8 . 5%、洛美沙星精密度为7 . 2 %。
3.6样品检测
本次试验共检测苏尼特羊、呼伦贝尔羊、大尾羊、山羊、绵羊、小尾寒羊、羊肝、羊毛肚、羊前腿、羊后腿、羊蹄筋、羊心1 2种羊肉样品,每种样品检测2个,以减小随机误差,提高检验的准确性。
根据农业部标准的要求,氧氟沙星、诺氟沙星、培氟沙星和洛美沙星均不得检出,环丙沙星和恩诺沙星之和小于等于1 0 0μg / kg才为合格品,反之则为喹诺酮类药物残留,不合格。
检测结果如表1 0所示,1 2种羊肉样品中均未检测出6种喹诺酮药物,所取羊肉样品均符合农业部标准,为合格品,消费者可放心购买。
4 结论
本实验确定了环丙沙星、氧氟沙星、培氟沙星、诺氟沙星、恩诺沙星、洛美沙星试剂空白值全部为0,检出限分别为0.06μg/kg、0.02μg/kg、0.07μg/kg、0.05μg /kg、0.06μg /kg、0.05μg /kg,回收率为84.1%~102.1%,各物质的精密度依次是10.5%、7.4%、8.5%、6.8%、6.9%、7.2%。实验中所用苏尼特羊、呼伦贝尔羊、大尾羊、山羊、绵羊、小尾寒羊、羊肝、羊毛肚、羊前腿、羊后腿、羊蹄筋、羊心1 2种羊肉样品均未检出6种喹诺酮类药物,本次实验所采羊肉样品符合农业部标准,均为合格品。
参考文献:
[1] 强慧勤,庞晓宇,杨维维等.幼犬使用喹诺酮类药物应谨慎[J].动物保健.2006(12).
[2] 马建民,夏曦,李晓薇.阴离子交换固相萃取-超高效液相色谱-串联质谱法检测猪肌肉中13种喹诺酮类药物[J].中国食品卫生杂志,2015,25(3):249-253.
[3] Thomas H. Tracking persistent pharmaceutical residues from municipal sewage to drinking water[J]. Journal of Hydronautics. 2002.
[4] 胡梁及,朱盛山,彭亮等.水产养殖中药物滥用的危害及问题分析[J].水产学杂志.2015(02).
[5] 刘刚.喹诺酮类药物的特点、应用及使用注意事项[J].养殖技术顾问.2011(02).
[6] 易检祥.浅谈兽药的残留危害及其监管措施[J].湖南畜牧兽医.2004(03).
[7] Kwang-soo Lee, Kisung Kwon, San-cheong Bae, Hyung Soo Kim. Simultaneous determination of thirteen quinolones in livestock and fishery products using ultra performance LC with electrospray ionization tandem mass spectrometry[J], Food Science and Biotechnology. 2013, 10(22): 1-9.
[8] 钱卓真.动物性食品中喹诺酮类药物残留检测技术研究进展[J].福建水产.2007(04).
[9] 乔坤云,孙涛,刘圣红等.高效液相色谱荧光法检测鸡肉中4种氟喹诺酮药物残留[J].分析仪器.2015(06).
[10] 杨卫军,李曼,曹秀梅等.超高效液相色谱法检测鸡肉中氟喹诺酮类药物残留[J].现代畜牧兽医.2016(04).
基金项目:内蒙古自治区科技重大专项(2016年度);内蒙古自治区科技引领项目(2017年度、2018年度)。
