大鼠骨髓间充质干细胞和脂肪干细胞体外成骨能力的比较
2018-12-12卓丽丹冯顶丽芦笛郭红延李红
卓丽丹 冯顶丽 芦笛 郭红延 李红
1976 年,首次通过贴壁培养的方法分离,发现兔骨髓中存在能贴附于塑料培养皿,呈长菱形样成纤维样的细胞,成为骨髓间充质干细胞(bone marrow mesenchymal stem cells,BMSCs)[3],单个细胞呈纺锤状或者梭形,整体呈菊花状或同心圆状排列。Zuk等[4]首次从脂肪组织中分离出一种成纤维样细胞,其形态与BMSCs形态相似, 具有自我更新和多向分化的能力,称之为脂肪干细胞(adipose stem cells,ADSCs)。
BMSCs和ADSCs来源广、取材方便、易培养且有稳定传代增殖能力,是骨组织工程常用的种子细胞[4-5],为了研究两者之间的具体差异,通过增殖能力、流式检测、成骨诱导以及相关基因检测方面进行查看两者之间的差别。
1 资料与方法
1.1 材料
α-MEM(Gibico,USA);血清(天市灏羊生物科技有限公司);青霉素、链霉素(北京吉诺恩泰生物科技有限公司);抗坏血酸、地塞米松、左旋β-甘油磷酸钠、胰蛋白酶、Ⅳ型胶原酶、dispase酶、RNA提取试剂盒、碱性磷酸酶(ALP)试剂盒(Sigma,USA)。
1.2 主要试剂及仪器
CO2细胞培养孵箱(Thermo,USA);流式细胞仪 (BD,USA);离心机(Heraens Cryofuge 8000,德国);I型超净工作台(苏州净化设备厂);RT-PCR检测仪(AXYGEN,USA)。
1.3 方法
1.3.1 细胞培养 取健康3~4 周SD大鼠,脂肪组织分离及鉴定按照我室已建立的方法[6]。在腹部剪梭形切口,暴露腹股沟脂肪垫,取腹股沟处脂肪,无菌PBS清洗3 次,去除脂肪外面所黏连的包膜、肉眼可见的小血管以及较明显的结缔组织。将脂肪组织剪碎大约形成1 mm3并加入1 ml Ⅳ型胶原酶、1 ml dispase酶、4 ml 0.25%胰酶、4 ml H-DMEM。37 ℃、5%CO2消化15 min,100目、200目过滤网过滤,1 000 rpm/min离心5 min,重悬计数,按照2×106接种于中皿,第2天首次进行换液去未贴细胞,随后观察细胞长到90%时进行1∶3进行传代。
参考俞婉璐等[7]提取骨髓间充质干细胞的方法,提取上述大鼠髂骨,并剔除附着肌肉,无菌PBS冲洗3 次,两端剪除少许骨垢端,暴露骨髓腔。用1 ml注射器吸取完全培养基,插入骨髓腔,轻柔冲洗骨髓腔,冲洗骨髓腔至透明,收集骨髓冲洗液,于37 ℃、5%CO2孵箱内培养。接种后第48小时进行1 次半换液,间隔72 h 第1次全换液。此后每隔2 d给细胞全换液1 次,逐渐纯化,倒置显微镜下观察细胞生长情况。
1.3.2 大鼠BMSCs和ADSCs生长能力绘制 P2代大鼠BMSCs和ADSCs增殖达到90%时,用胰酶消化,用新培养基制成细胞悬液后计数,根据细胞计数结果按 2×104/ml 接种于12 孔细胞培养板,2 ml/孔,共27 孔,进行细胞计数。24 h消化细胞显微镜下计数。每隔24 h计数1 次,每次消化3 孔,进行计数,计算平均值,连续计数9 d。
1.3.3 细胞表面标志物的检测 取P3、P10代BMSCs和ADSCs细胞,0.25%的胰酶消化,离心后重悬细胞,分装5 支EP管(分别标记A、B、C、D、E)细胞数约3×105/EP。在1 200 r/min离心8 min用PBS离心洗涤两次。加入100 μl PBS重悬细胞分别加入抗体,抗大鼠CD45(B),CD29(C),CD90(D)、抗大鼠CD34(E)及空白对照(A)仅加PBS,放置4 ℃摇床30 min。在1 200 r/min离心8 min用PBS离心洗涤2 次,E管经洗涤后加入FITC二抗放置4 ℃摇床30 min,E管在1 200 r/min离心8 min用PBS再次离心洗涤2 次。使用400 μl PBS重悬细胞,然后使用流式细胞检测仪检测细胞表面标记情况。
156****5491:喜欢一个姑娘 WJY近 12年了,不知道应不应该对她表白。如果能够上墙我就去表白!
1.3.4 大鼠BMSCs和ADSCs进行成骨诱导 P2代细胞生长达90%时消化计数,1×106接种于6 孔板,第2日成骨诱导,成骨诱导液(含10%FBS、10 mmol/L β-甘油磷酸钠、10-7mol/L 地塞米松、50 mg/L左旋抗坏血酸),另外设置一对照组只添加完全培养基,每间隔1 d更换诱导液。分别在7、14、21 d进行ALP染色,28 d茜素红染色,在倒置显微镜下拍照对比。
1.3.5 ALP染色 按照ALP试剂盒说明书染色,诱导特定时间的BMSCs、ADSCs弃去上清,PBS清洗2 次;加入固定液(1.96 ml蒸馏水、0.04 ml柠檬酸、7.5 ml丙酮)30 s,蒸馏水洗涤2 次;加入染色液(0.05 ml FVB、2.35 ml蒸馏水、0.1 ml AS-MX),6 孔板/ml、12 孔板/500 μl,室温静置30 min后,蒸馏水清洗2 次,留少量的液体拍照,对于拍照结果利用IMAGE J软件进行半定量分析。
1.3.6 茜素红染色 ①1%茜素红配制:0.1 mol/L的 tris-Hcl 100 ml(pH 8.3)加入0.1 g茜素红S,4 ℃保存;②诱导完成的BMSCs和ADSCs用PBS冲洗3 次;4%多聚甲醛固定30 min;茜素红染色5 min;蒸馏水冲洗,留少量液体进行拍照。同时对于拍照结果利用IMAGE J软件进行半定量分析。
1.3.7 大鼠BMSCs和ADSCs成骨诱导后成脂相关基因的RT-PCR 比较 成骨诱导7、14、21 d,使用Trizol提取总RNA,测量RNA 浓度,定量反转录形成cDNA,然后进行PCR检测。成骨相关基因引物为SATB2,核心蛋白(RUNX2),骨涎蛋白(BSP),骨钙素(OCN)相关引物序列参考表 1。PCR的反应体系为:2 ×T5 Fast Qpcr Mix 10 μl,上下引物分别为0.5 μl,cDNA 1 μl,DEPC水8 μl,反应体系为20 μl体系,扩增条件为 95 ℃ 5 s、60 ℃ 34 s,共40 个循环。IQ5 Optical System Software 计算出最终各组相对表达值。

表 1 RT-PCR引物序列
1.4 统计学处理
整理实验数据,采用GraphPad Prism 7,两样本均数采用组间t检验,P<0.05,具有统计学意义。
2 结 果
2.1 大鼠BMSCs和ADSCs形态学观察
原代BMSCs,3 d后换液发现克隆团块,5~7 d细胞增殖速度较快,细胞成长梭形,涡旋状分布,纯度较高。原代ADSCs,贴壁较快,5 h左右贴壁完成,3 d常满皿底,细胞成短梭状,其中有些细胞呈三角形等不规则形态,经传代纯化细胞。P3代BMSCs和ADSCs纯度较高,细胞呈长梭状分布,类似成纤维细胞,呈涡旋状分布,通过此方法可以稳定遗传至10 代(图 1)。
2.2 大鼠BMSCS和ADSCS生长曲线
P3代BMSCs和ADSCs连测9 d,BMSCs前两天生长速度快于ADSCs,随后ADSCs的生长速度明显高于BMSCs,说明ADSCs有较大的生长潜力(图 2)。
2.3 流式结果分析
P3、P10 BMSCs流式结果显示:CD34和CD45表达率较低,CD29和CD90表达率分别为90%和95%以上,强阳性。P3、P10 ADSCs也表现出CD34、CD45表达率低和CD29、CD90的强阳性表达(图 3)。

图 1 BMSCs和ADSCs细胞的形态特征 (×200)
Fig 1 Morphological characteristics of BMSCs and ADSCs (×200)
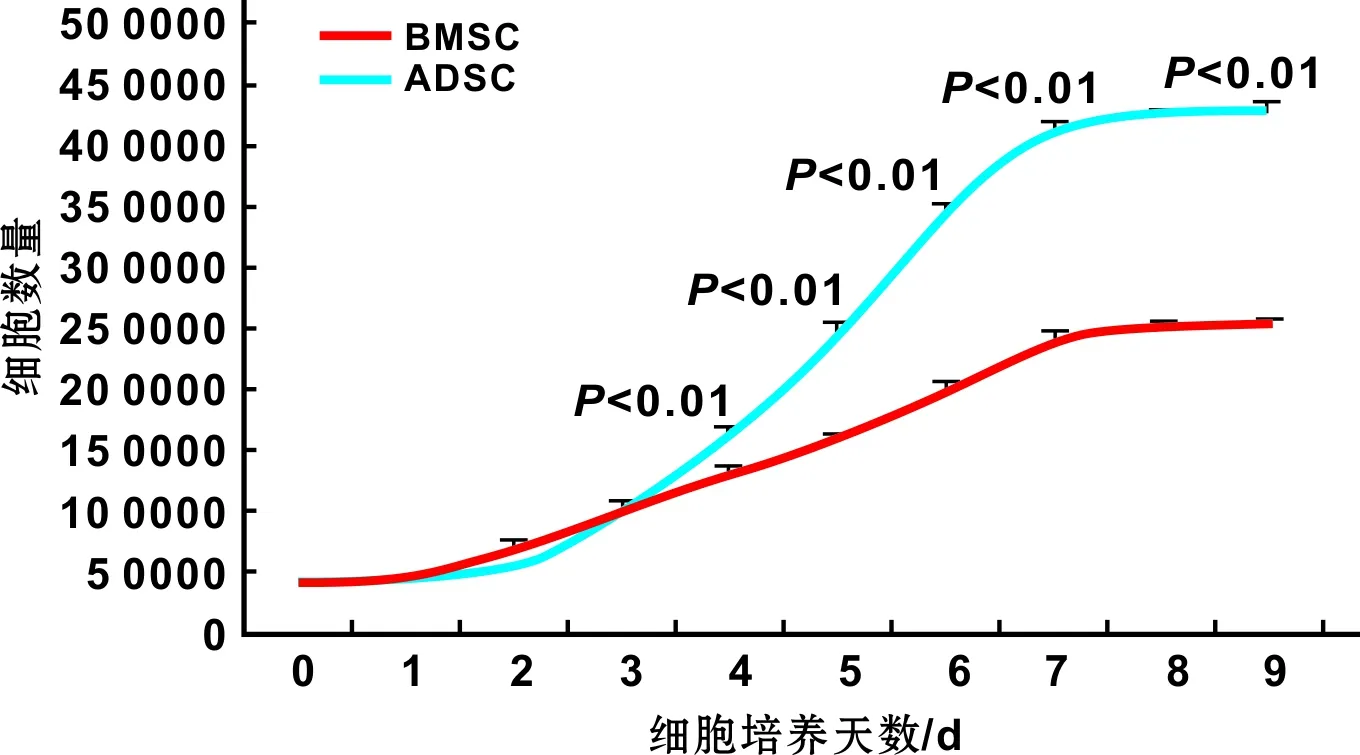
图 2 P3代 BMSCs和ADSCs增殖曲线
2.4 大鼠BMSCs和ADSCs进行成骨诱导和相关基因检测
诱导7 d ALP染色,BMSCs (图 4A)着色范围较广,且蓝紫色较深,ADSCs(图 4D)细胞形态未发生变化,少部分着色;至诱导21 d ALP染色,BMSCs(图 4C)和ADSCs(图 4F) 发现BMSCs染色强于ADSCs,由长梭形逐渐变为立方形,呈复层结构,形成细胞膜片,随后形成多角形的成骨样细胞,细胞质颜色变深,细胞外基质分泌增加。4 周后发现,不透光团状矿物质结节,茜素红染色,显微镜下观察到细胞外基质有橘红色或者红色矿物质结节,BMSCs明显多于ADSCs,IMAGE J分析结果表明,ALP染色7、14 d(P<0.01)21 d(P>0.05);茜素红染色(P<0.01),BMSCs成骨
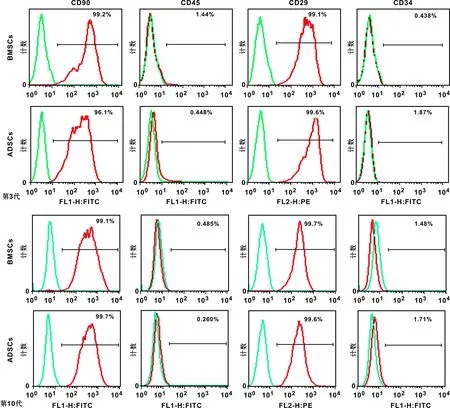
图 3 BMSCs和ADSCs表面抗原标记物的表达
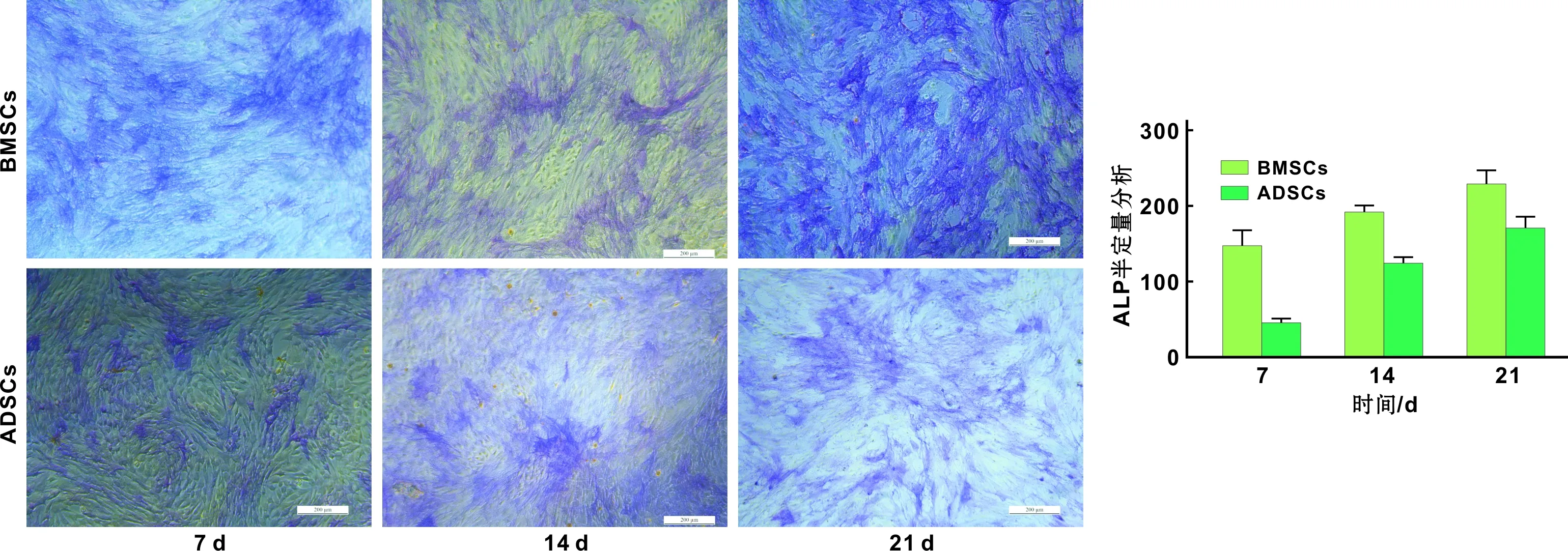
图 4 成骨诱导后ALP染色以及半定量分析结果 (×200)

图 5 成骨诱导后茜素红染色以及半定量分析 (×200)
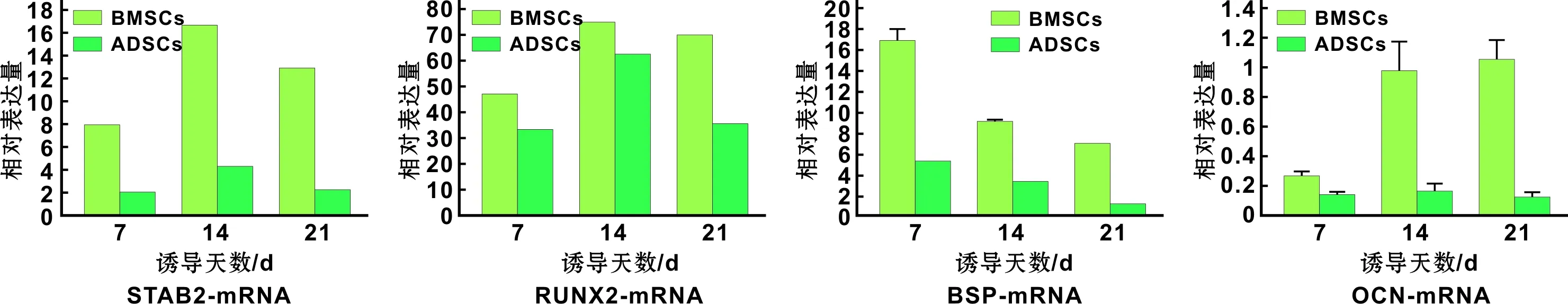
图 6 qPCR定量检测BMSCs和ADSCs成骨相关基因的表达
能力强于ADSCs(图 5)。qPCR检测结果表明,BSP、SATB2(P<0.01)OCN、RUNX2在BMSCs中表达均高于ADSCs(P<0.05)(图 6)。
3 讨 论
干细胞研究正在向医学、生命科学等各个领域交叉渗透,其与生物材料复合进行骨组织工程构建将具有强大影响和应用前景的生命科学研究领域[8-10]。
本实验主要研究关于种子细胞BMSCs和ADSCs之间在体外基础生物学特性方面的差异[11]。将来自相同物种,年龄和性别(3~4 周龄雄性Sprague-Dawley大鼠)的BMSCs和ADSCs进行对比。通过贴壁培养提取原代BMSCs、ADSCs,两者之间没有显着的形态学差异,但BMSCs比ADSCs花费的时间更长,可能是低接触抑制这与Lotfy等[12]和Zhu等[13]的研究结果一致。经过3 代的纯化,细胞生长较好,增殖旺盛,形态均一稳定。流式细胞检测CD29、CD90阳性率高达99%以上,细胞表面抗原CD45以及造血干细胞的表面标志CD34表达率较低与文献[14]一致。通过此方法获得的干细胞可稳定遗传达10代,P10代流式结果显示CD29、CD90阳性率高达98%以上,细胞表面抗原CD45以及造血干细胞的表面标志CD34为表达率低,说明BMSCs、ADSCs仍保持着稳定的增殖能力。
同时实验证明BMSCs、ADSCs体外均有成骨分化的能力,成骨诱导液(10%FBS、10 mmol/L β-甘油磷酸钠、10-7mol/L 地塞米松、50 mg/L左旋抗坏血酸),诱导BMSCs、ADSCs 7、14、21 d后,ALP染色可见:BMSCs颜色深度以及着色范围均强于ADSCs,着色强度及范围随着时间的增加而加强,细胞为多角形的成骨样细胞。诱导28 d茜素红染色观察到细胞外基质有橘红色或者红色矿物质结节,BMSCs明显多于ADSCs,与文献[15]一致。
早期表达蛋白BSP、晚期表达蛋白OCN、核机制蛋白SATB2、核心蛋白RUNX2是骨分化过程中重要的调控因子,其表达量可反映细胞的成骨能力。BSP是骨标志性蛋白,是一种硫酸化的磷蛋白和高度糖基化,能激活成骨细胞,促进骨矿化[16]。OCN一般仅由成骨细胞表达的基质蛋白,具有调节基质钙化的作用,其浓度可以作为成骨细胞活动的标志[17]。SATB2是新近发现的特殊富含序列结合蛋白家族的成员,它可结合到核基质结合区并以依赖的方式激活基因转录过程,可正向调节多种成骨细胞的特异性基因如BSP和OCN的表达[18]。RUNX2 是成骨分化过程中关键的调控因子,能够调控众多基因的转录,RUNX2缺失的鼠中,成骨细胞的分化完全被抑制,均不发生骨膜内成骨和软骨内成骨[19]。通过RT-qPCR检测诱导后BMSCs和ADSCs成骨相关基因 BSP、OCN、SATB2、RUNX2可发现:在成骨分化过程中BSP随着时间的延长而较少;OCN随着时间的延长而增多,但BMSCs表达量仍高于ADSCs;SATB2在14 d时达到较高水平,随后逐渐降低;RUNX2在诱导期间一直处于高表达水平,说明在成骨分化过程中起着至关重要的作用[20],且文献中提到RUNX2具有促进BMP、OCN、STAB2、ALP和Ⅰ型胶原等成骨基因的表达[21-22],这些因子可通过作用于转录过程或相互作用促进干细胞向成骨细胞分化。
研究结果表明,贴壁培养的BMSCs、ADSCs具有稳定的自我复制增殖能力。此外,发现ADSCs比BMSCs增殖能力更强,体外研究中预测,在临床前和临床应用中,ADSCs比BMSCs更容易生长,但与BMSCs相比,其成骨分化能力较低。这表明BMSCs在治疗骨疾病方面可能比ADSCs更有效。该研究结果为临床应用中种子细胞和处理方式的选择奠定理论基础。
