替格瑞洛对急诊PCI术后氯吡格雷抵抗患者血小板聚集功能的影响
2018-12-11杨增芯郑若龙徐卓文陈新军
杨增芯,郑若龙,徐卓文,陈新军
(东南大学医学院附属江阴医院/江阴市人民医院心内科,江苏江阴 214400)
急性ST段抬高型心肌梗死(ST elevated myocardial infarction,STEMI)的病理生理基础是冠状动脉内不稳定斑块的急性破裂,继发血栓形成,从而导致冠状动脉的急性闭塞。循证医学证据表明,尽早施行有效的再灌注治疗,尤其是急诊行经皮冠脉介入术(percutaneous coronary intervention,PCI)治疗,是STEMI患者最有效的治疗方案[1]。阿司匹林联合氯吡格雷的双联抗血小板方案是急诊PCI术后的基础药物治疗。肝脏P450酶的活性在氯吡格雷药物代谢中具有举足轻重的地位,CYP2C19基因多态性导致的P450酶活性的个体差异是致使氯吡格雷不能充分发挥抗血小板作用的关键因素[2]。替格瑞洛是新一代ADP受体拮抗剂,其抗血小板的药理作用不受CYP2C19基因多态性的影响[3]。为探讨氯吡格雷抵抗患者急诊PCI术后抗凝治疗的方法,本研究分析了替格瑞洛对急诊PCI术后氯吡格雷抵抗患者血小板聚集功能的影响,报告如下。
1 资料与方法
1.1 研究对象 入选2016年4月至2018年4月于江阴市人民医院收治且诊断为STEMI的氯吡格雷抵抗患者95例,所有患者在入院后即刻及PCI术后第一天抽血检测血小板聚集率以判定是否为氯吡格雷抵抗。入选标准:①符合2015年急性ST段抬高型心肌梗死诊断和治疗指南中STEMI诊断标准[1];②心肌梗死发病至入院在12小时内;③所有患者入院后均立即接受急诊PCI治疗,且在介入治疗前均接受300mg阿司匹林和300mg氯吡格雷负荷治疗;④氯吡格雷抵抗判定标准[4]:PCI术后第一天测定的血小板聚集率较术前降低<30%。排除标准:①年龄超过75岁;②造影剂或氯吡格雷过敏;③曾经服用替格瑞洛、氯吡格雷或替罗非班等抗血小板药物;④严重的肝肾功能损害;⑤依从性较差。
入选患者随机分为氯吡格雷组(n=47)和替格瑞洛组(n=48),两组患者临床基本情况比较差异无统计学意义(P>0.05),具有可比性。见表1:
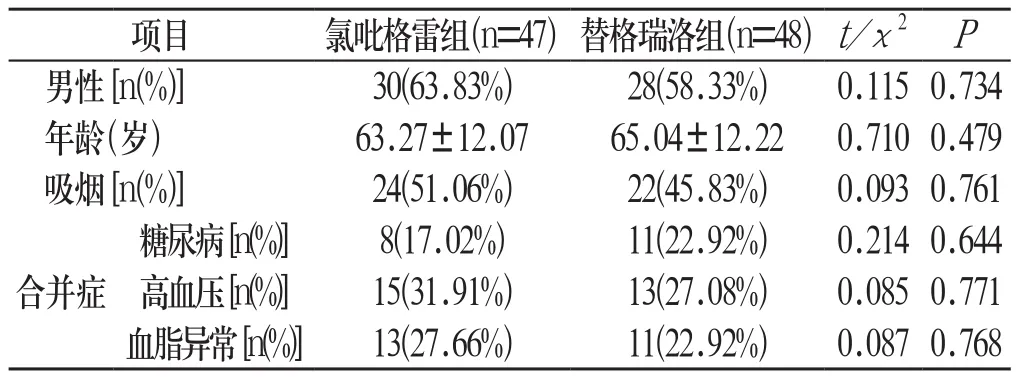
表1 两组患者临床基本情况比较
1.2 干预措施 两组患者均给予阿司匹林抗血小板、他汀类药物稳定斑块、低分子肝素抗凝等常规治疗。此外,氯吡格雷组患者在术后第一天使用高维持剂量氯吡格雷(赛诺菲制药有限公司,75mg/片,国药准字J20130083)150mg每日一次口服;替格瑞洛组患者术后第一天使用替格瑞洛(阿斯利康制药有限公司,90mg/片,国药准字J20130020)90mg每日两次口服,替代氯吡格雷。
1.3 观察指标 分别于术前,术后1周、1个月、3个月抽血测定所有患者的血小板聚集率、P选择素表达情况和血栓素A2水平。
1.3.1 血小板聚集率:应用LBY-NJ4四通道血小板聚集仪(北京普利生仪器有限公司),采用二磷酸腺苷(ADP)诱导的血小板聚集率测定方法检测。检测过程中所有操作流程严格按照使用说明书进行,通过富含血小板血浆透光强度变化,由计算机软件计算获得血小板聚集率。
1.3.2 P选择素:采用流式细胞仪检测血小板P选择素表达水平的变化,PE-P选择素抗体由美国Santa Cruz公司提供,所有操作流程严格按照流式细胞检测仪操作说明进行。
1.3.3 血栓塞A2:采用酶联免疫吸附法(ELISA)测定,试剂盒由上海江莱生物科技有限公司提供。所有的实验操作严格按照相关ELISA试剂盒说明进行,在波长450mm处测定OD值,依据OD值计算血栓素A2的水平。
1.4 统计分析 所有数据采用SPSS 24.0软件进行统计学分析。计量资料用均数±标准差表示,计数资料用百分比表示。计量资料随时间变化的比较采用重复测量的方差分析,同一时间点两组比较采用t检验;计数资料的比较采用卡方检验或Fisher确切概率法。P<0.05认为有统计学差异。
2 结果
两组患者术前血小板聚集率、P选择素和血栓素A2水平比较,差异均无统计学意义(P>0.05)。与术前比较,氯吡格雷组患者术后1周、1个月、3个月的血小板聚集率均明显低于术前(P<0.05),但术后3个月轻度升高;与术前比较,替格瑞洛组患者术后1周、1个月、3个月血小板聚集率均明显低于术前(P<0.05),且明显低于相同时间点氯吡格雷组患者(P<0.05)。与术前比较,氯吡格雷组患者术后1周、1个月、3个月P选择素均明显降低(P<0.05);与术前比较,替格瑞洛组患者术后1周、1个月、3个月P选择素明显降低(P<0.05),且明显低于相同时间点氯吡格雷组患者(P<0.05)。两组患者术后1周、术后1月、术后3月血栓素A2水平比较,差异均无统计学意义(P>0.05)。见表2:
表2 两组患者血小板聚集率、P选择素和血栓素A2水平比较(±s)

表2 两组患者血小板聚集率、P选择素和血栓素A2水平比较(±s)
与本组术前比较:*P<0.05。
检测指标 氯吡格雷组(n=47)替格瑞洛组(n=48) t P血小板聚集率(%)术前 71.57±16.24 72.60±14.35 0.328 0.744术后 1周 48.15±14.43* 39.51±13.66* 2.998 0.004术后1个月 42.90±14.80* 34.97±13.52* 2.728 0.008术后3个月 45.16±13.69* 34.18±12.09* 4.146 0.001 P选择素术前 39.53±5.62 38.24±5.80 1.101 0.274术后 1周 29.97±3.62* 23.16±3.08* 11.897 0.001术后1个月 28.75±3.55* 21.53±2.80* 8.086 0.001术后3个月 26.72±2.60* 20.18±2.74* 6.061 0.001血栓素A2(ng/ml)术前 58.64±10.02 57.60±11.31 0.474 0.637术后 1周 54.72±9.57 52.39±9.37 1.199 0.234术后1个月 53.83±10.76 50.29±9.95 1.742 0.085术后3个月 51.50±9.85 49.89±9.40 0.815 0.417
3 讨论
氯吡格雷抵抗也被称为“氯吡格雷低反应性”,是指患者服用常规剂量的氯吡格雷,血小板聚集率不能达到要求的低水平状态。氯吡格雷抵抗的根本原因是肝脏CYP2C19基因的多态性,CYP2C19基因多态性可直接导致急诊PCI术后血栓事件[5]。目前,我国冠心病患者CYP2C19等位基因缺失比例高达60%,该类患者心血管事件的发生率明显高于普通患者,因此针对氯吡格雷抵抗患者的筛查和治疗工作显得尤为重要[6]。新型抗血小板药物替格瑞洛是否能有效抑制氯吡格雷抵抗患者血小板的聚集作用,一直是临床医师关注的焦点。本研究将传统抗血小板药物氯吡格雷加倍使用,并与新型抗血小板药物替格瑞洛的作用进行对比,结果发现虽然两组患者术后各时间点的血小板聚集率均明显低于术前,但替格瑞洛组氯吡格雷抵抗患者在3个月的随访过程中各时间点血小板聚集率均明显低于氯吡格雷组患者,说明不受CYP2C19基因多态性影响的替格瑞洛在抗血小板聚集方面具有明显优势。
P选择素主要表达于血管内皮细胞和血小板α颗粒膜上,通过与P选择素糖蛋白配体相互作用参与血小板的粘附和聚集过程[7]。急性心肌梗死由冠状动脉内不稳定斑块破裂导致,不稳定斑块破裂后的炎症反应可引起大量血小板聚集,此时P选择素不仅介导血小板粘附在血管内皮,还参与血小板活化和聚集的过程[8]。本研究发现,氯吡格雷组、替格瑞洛组患者PCI术后各时间的P选择表达水平均明显低于本组术前;并且与氯吡格雷组比较,替格瑞洛组患者术后各时间点P选择素的表达水平亦明显降低。已有的研究也表明,替格瑞洛能够通过有效抑制ADP受体降低血小板聚集率,并能抑制血小板的活化,从而有效改善氯吡格雷抵抗现象[9]。血栓素A2是花生四烯酸的主要代谢产物,主要参与环氧合酶-1途径诱导的血小板聚集过程。本研究发现无论是氯吡格雷还是替格瑞洛都对血栓素A2水平没有明显影响,说明ADP受体抑制剂对血栓素A2途径没有作用,可能与环氧合酶-1途径相对独立于ADP受体途径有关[10]。
综上所诉,对于急诊行PCI且存在氯吡格雷抵抗的患者,使用替格瑞洛代替高维持剂量的氯吡格雷,不仅能改善氯吡格雷抵抗现象,还能进一步抑制血小板活化。但替格瑞洛的临床使用也有其局限性,替格瑞洛价格相对昂贵,较氯吡格雷更容易引起呼吸困难、出血等副作用[10]。有关替格瑞洛的临床合理使用,氯吡格雷抵抗患者的优化解决方案,PCI术后长期服用替格瑞洛的不良反应和预后等诸多问题,仍有待更深入的临床研究。
