马疱疹病毒1型XJ2015株全基因组测序及分析
2018-12-05刘建华鲍子磊王世民贾庆瑞王雪竹王思云冉多良
胡 月,刘建华,鲍子磊,王世民,范 斌,贾庆瑞,王雪竹,王思云,冉多良
(新疆农业大学动物医学学院,新疆乌鲁木齐 830052)
马疱疹病毒1型(Equine herpesvirus-1,EHV-1)是一种可导致马属动物多种疾病的重要病原体,具有潜伏期较长(1~4个月),建立终身感染[1]。无论是原发性感染还是潜伏期再激活,均可引起不同程度的呼吸系统疾病、神经系统疾病、孕马流产和新生马驹死亡[2-3]。在全球马产业中造成严重的经济损失[4]。
EHV-1属于疱疹病毒目,疱疹病毒科,α疱疹病毒亚科,水痘病毒属。该亚科以单纯疱疹病毒1型(Herpes simplex virus-1,HSV-1)为典型,还包括马疱疹病毒2型(Equine herpesvirus-2,EHV-2)、马疱疹病毒4型(Equine herpesvirus-4,EHV-4)、伪狂犬病病毒(Pseudorabies virus,PRV)、水痘-带状疱疹病毒(Varicella zoster virus,VZV)[5]。EHV-1虽在疱疹病毒中遗传稳定性较高,但其基因组内仍存在多个单一核苷酸的变异[6-7]。目前,已经有美国、日本、英国、澳大利亚的研究者测得流行毒株全基因组序列,为分子流行病学调查提供了依据[6],而我国尚未报道测得EHV-1病毒的全基因序列。
本研究对2015年新疆伊犁地区马流产胎儿中分离到的EHV-1 XJ2015株[8]进行全基因序列测定,分析其基因组结构,各基因位置、结构及功能,并参考GenBank中31株EHV-1全基因组序列(表1),进行基因组特征及核苷酸同源性分析。旨在进一步认识EHV-1的分子特征及基因背景,填补我国EHV-1全基因组序列测定及分析的空白,为深入了解我国流行毒株的遗传进化关系提供理论依据,为基因缺失疫苗的研发奠定基础。
1 材料与方法
1.1 材料
1.1.1 毒株与细胞 毒株于2015年分离自新疆伊犁地区,命名为EHV-1 XJ2015,BHK-21细胞由本实验室保存。
1.1.2 主要试剂 PrimeSTAR®Max DNA Polymerase 和DM 5000 DNA Marker均购自宝生物工程(大连)有限公司;Viral DNA Kit、Gel Extraction Kit 和Cycle Pure Kit购自OMEGA广州飞扬生物工程有限公司;pEASY-Blunt3 Cloning Kit购自北京全式金生物技术有限公司。
1.2 方法
1.2.1 病毒培养与核酸提取 将EHV-1 XJ2015株接种于BHK-21细胞,待病变率达到80%时收获病毒。按照Viral DNA Kit说明书提取病毒基因组DNA,测定基因组的浓度及纯度,置-20℃保存备用。
1.2.2 引物设计合成、病毒基因组分段克隆及测序 参照GenBank中登录的31株EHV-1全基因组序列(表1),比对后挑选保守区域设计80对特异性引物,以XJ2015株基因组DNA为模板进行PCR扩增,相邻引物扩增区域保证至少重叠200 bp,引物由生工生物工程(上海)股份有限公司合成。PCR产物经10 g/L琼脂糖凝胶电泳验证后使用Gel Extraction Kit 和Cycle Pure Kit回收纯化,克隆至pEASY-Blunt3 Cloning中,构建重组质粒,经转化、克隆、筛选后送生工生物工程(上海)股份有限公司测序。
1.2.3 测序结果拼接及DNA相似性检索 用DNA Man软件对测序结果进行拼接,使用美国国家生物技术信息中心(NCBI)的BLAST进行序列同源性检索。
1.2.4 开放阅读框预测及基因注释 使用ORF finder对XJ2015株全基因组核苷酸序列进行开放阅读框预测及全基因组结构分析,通过Smart BLAST进行基因位置、结构及功能的注释。
1.2.5 基因组特征及同源性分析 使用DAN Man和MEGA7.0进行XJ2015株与GenBank中31株EHV-1基因组特征及核苷酸序列同源性分析。
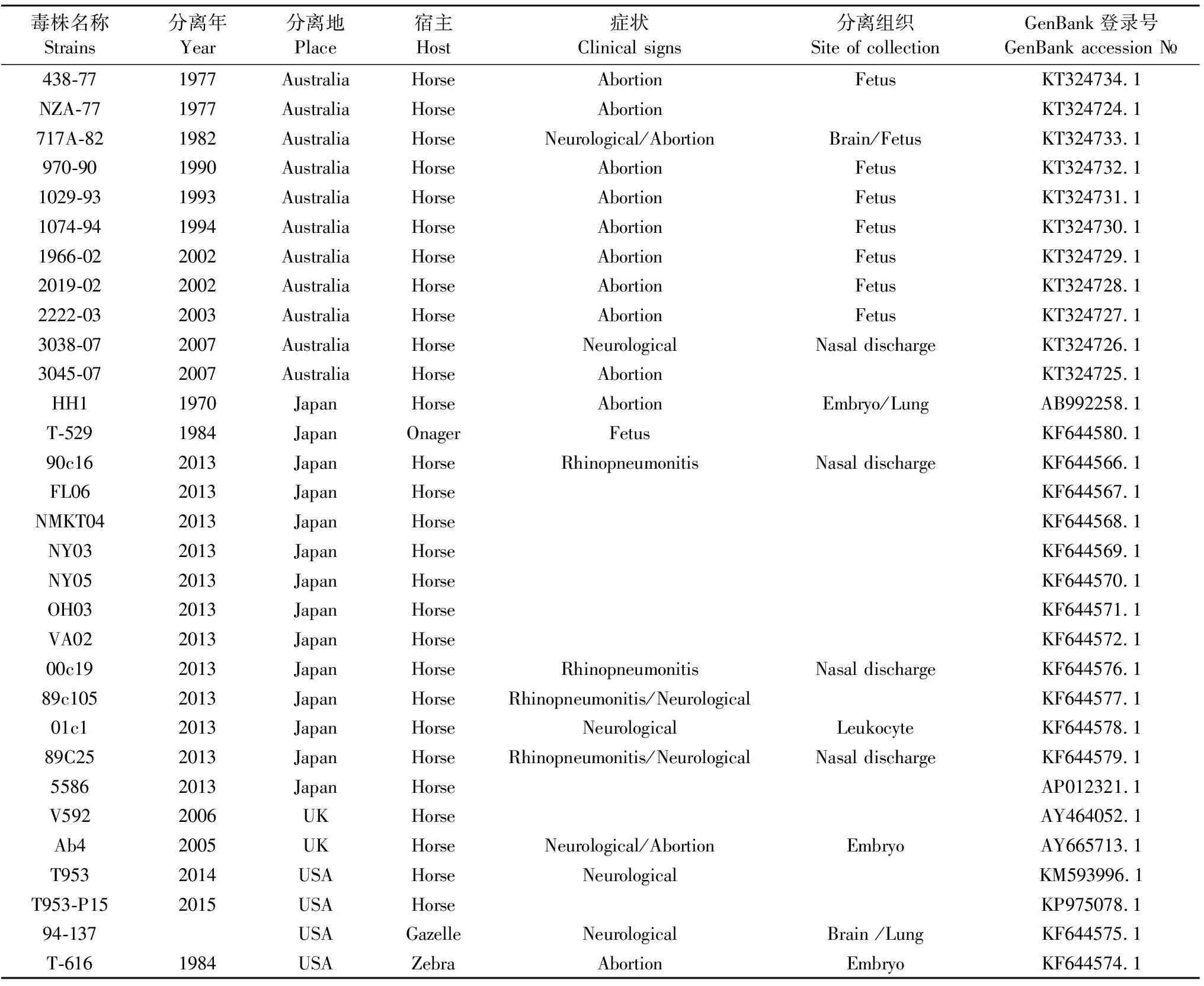
表1 EHV-1参考毒株信息
2 结果
2.1 EHV-1 XJ2015株全基因组结构分析
由图1所示,疱疹病毒基因组结构可以分为5种类型,经测序、拼接及分析得出XJ2015株基因组结构属于D型,分为6部分,即长独特区(Long unique region,UL)、短独特区(Short unique region,US)、长独特区末端/内部重复序列(Terminal repeat /Internal inverted repeat of long unique area,TRL/IRL)、短独特区末端/内部重复序列(Terminal repeat /Internal inverted repeat of short unique region,TRS/IRS),结构简式为TRL-UL-IRL-IRS-US-TRS。基因组全长150 267 bp,G+C含量为56.7%。TRL长32 bp(1-32位)、UL长112 887 bp(33-112 919位)、IRL长32 bp(112 920-112 951位)、IRS长12 659 bp(112 952-125 610位)、US长11 998(125 611-137 608)、TRS长12 659 bp(137 609-150 267位),与PRV和VZV的基因组结构相似。
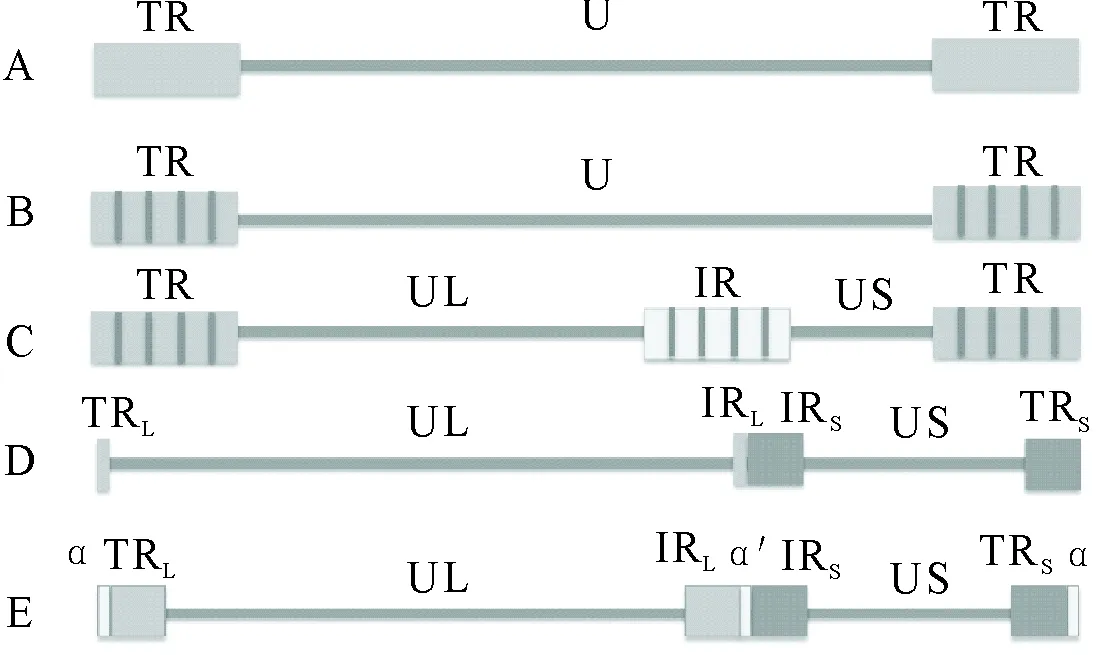
U.独特区;TR.末端重复序列;IR.内部重复序列;α/α′.E型特有反向重复序列;A.EHV-2;B.卡波济肉瘤相关疱疹病毒;C.EB病毒;D.EHV-1;E.HSV-1
U.Unique region; TR.Terminal repeat; IR:Internal inverted repeat; α/α′.E-type unique reverse repeat;A.EHV-2; B.KsHV; C.EBV; D.EHV-1; E.HSV-1
图1疱疹病毒基因组结构类型
Fig.1 Overview of the types of herpesvirus genomes
2.2 EHV-1 XJ2015株基因注释及功能分析
由图2可知,XJ2015株全基因组共80个开放阅读框(Open reading frame,ORF),UL区63个,US区9个,IRL区4个,TRS区4个。包含76个基因,其中64、65、66、67号基因位于TRS/IRS区中,为双拷贝基因。各基因功能分析表明,76个基因分为1个极早期基因(Immediate early gene,IE)、55个早期基因(Early gene,E)和20个晚期基因(Late gene,L)。基因35与64分别编码2种蛋白,因此,全基因组共编码78种蛋白,6种调控蛋白,即IEP(IR1)、EICP0(UL63)、EICP22(IR4)、EICPO27(UL5)、IR2P(IR2)和ETIF(UL12)。30种蛋白参与病毒粒子成熟,其中6种与衣壳相关(UL22、UL25、UL35、UL42、UL43、UL56),12种为内层囊膜蛋白(UL3、UL8、UL11、UL24、UL45、UL46、UL48、UL55、US9),12种膜糖蛋白分别是gK(UL6)、gN(UL10)、gC(UL16)、gB(UL33)、gH(UL39)、gM(UL52)、gL(UL62)、gG(US3)、g300(US4)gD(US5)、gI(US6)和gE(US7)。其余42种蛋白主要涉及病毒粒子复制(表2)。
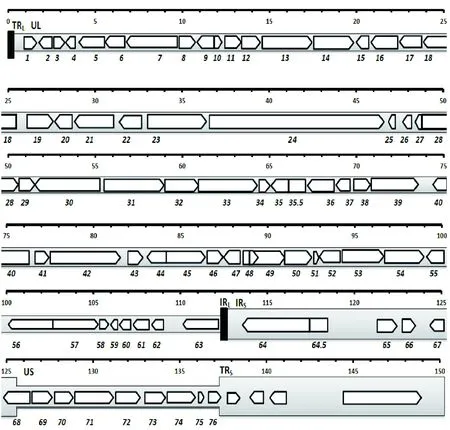
图2 全基因组ORF及各基因位置、结构示意图
表2 EHV-1 XJ2015株基因汇总
Table 2 Total genes of EHV-1 XJ2015 strain

基因Gene起始位点Start locus结束位点Stop locus方向Direction氨基酸大小Condon基因位置Gene location产物特性FunctionHSV相关基因HSV related gene 11 1721 780+202UL1MHC-1 downregulationUL5622 4361 819-205UL2MembraneNone32 7153 488+257UL3Tegument/conserved in DIPNone44 1233 521-200UL4Nuclear proteinUL5555 7484 336-470UL5EICP27UL5466 9165 885-343UL6gKUL53710 1756 930-1 081UL7DNA helicase-primaseUL52810 17410 911+245UL8Tegument proteinUL51911 98911 009-326UL9dUTPaseUL501011 95812 260+100UL10gNUL49a1112 42313 337+304UL11VP22 tegumentUL491213 47114 820+449UL12ETIFUL481315 19317 808+871UL13VP13/14 tegumentUL471417 95920 202+747UL14Tegument proteinUL461521 04620 363-227UL15Virus egress/MembraneUL451622 72721 321-468UL16gCUL441724 11022 905-401UL17MembraneUL431825 57224 355-405UL18DNA polvmeraseUL421926 13827 631+497UL19VHSUL412028 73527 770-321UL20RR2UL402131 15228 780-790UL21RR1UL392232 79231 395-465UL22ICP35 capsid assemblyUL382333 16836 230+1 020UL23ICP32UL372436 46446 870+3 468UL24ICP1/2 tegumentUL362547 32846 969-119UL25Small capsid proteinUL352648 24747 420-275UL26MembraneUL342748 87448 386-162UL27DNA packaging proteinUL332848 78050 642+620UL28DNA packaging proteinUL322950 63551 615+326UL29Req.for envelopmentUL313055 20151 539-1 220UL30DNA polymerase catalyticUL303155 47059 099+1 209UL31ICP8 ssDNA-binding proteinUL293259 26061 587+775UL32Cleavage/Packaging proteinUL283361 44964 391+980UL33gBUL273464 59565 077+160UL34V32 proteinNone3567 11065 170-646UL35Capsid maturation proteaseUL2635.566 15965 170-329UL35.5ICP35 capsid assemblyUL26.53668 99267 229-587UL36CapsidUL253769 91469 096-272UL37Nuclear proteinUL243869 92770 985+352UL38Thymidine kinaseUL233971 20973 755+848UL39gHUL224076 24174 649-530UL40Tegument proteinUL214176 81077 529+239UL41Envelope protein/VirionUL204277 72081 850+1 376UL42Capsid protein/VP5UL194382 10083 044+314UL43Capsid triplex subunit 2(VP23)UL184484 52983 165-454UL44DNA packaging proteinNone4584 49786 617+706UL45DNA packaging /tegumentUL174686 63787 749+370UL46Tegument proteinUL164788 93487 831-367UL47DNA packaging proteinUL154888 96489 917+317UL48Tegument proteinUL144989 38691 170+594UL49Tyr kinaseUL135091 15292 849+565UL50Alkaline DNaseUL125192 80193 025+74UL51Virion/envelopmentUL115294 48993 137-450UL52gMUL105394 40797 070+887UL53Origin-binding helicaseUL9
续表2

基因Gene起始位点Start locus结束位点Stop locus方向Direction氨基酸大小Condon基因位置Gene location产物特性FunctionHSV相关基因HSV related gene 5497 08699 341+751UL54DNA helicase-primaseUL855100 34999 438-303UL55Tegument proteinUL756102 408100 147-753UL56Capsid protein/Potal proteinUL657102 392105 037+881UL57DNA helicase-primaseUL558105 087105 764+225UL58Nuclear protein/VirionUL459106 433105 894-179UL59Protein V57None60107 133106 495-212UL60ICP22UL361108 161107 223-312UL61Uracil-DNA glycosylaseUL262108 820108 164-218UL62gLUL163112 002110 404-532UL63EICP0IE 11064118 526114 063-1 487IR1IEPICP4144 612149 075+1 48764.5118 526115 0291 165IR2IR2PNone145 578149 0751 16565121 160122 209+349IR4EICP22US1141 980140 931-34966122 823123 533+236IR5VirionUS10140 317139 607-23667125 155124 337-272IR6Virion/froms filamentsV67137 986138 804+27268126 236124 980-418US1VirionUS269126 372127 520+382US2Serine-threonine protein kinasseUS370127 642128 877+411US3gGUS471129 058131 511+817US4gp300None72131 454132 812+452US5gDUS673132 920134 194+424US6gIUS774134 427136 079+550US7gEUS875136 076136 468+130US8MembraneNone76136 804137 463+219US9Tegument proteinUS9
2.3 EHV-1病毒基因组特征及同源性分析
如表3所示,EHV-1全基因组大小为147 kb~150 kb,G+C含量为56.4%~56.7%。32株病毒基因组核苷酸序列同源性为86.74%。通过对各毒株基因组6个结构区序列长度及同源性分析得出,TRL/IRL相对较保守,均为32 bp,同源性为99.49%;UL约为112.7 kb,同源性为95.91%;US约为12.1 kb,同源性为94.5%;TRS/IRS约12.0 kb,但变异较大,同源性仅为65.99%。
病毒基因组核苷酸同源性分析显示,XJ2015株与英国毒株Ab同源性最高,达到93.58%,基因组G+C含量相同,均为56.7%;与美国毒株T-616的同源性最低,虽G+C含量相同,但同源性仅为76.72%。由表1可知,T-616是在流产斑马的胚胎器官中分离到的,T529株是在野驴胎儿中分离得到的,94-137是在瞪羚的脑组织和肺中分离得到的,同源性均低于80%。
3 讨论
EHV-1全基因组序列自1991年7月首次发布以来[6],迄今已有33株提交到GenBank中,其中2株为基因缺失株,31株野生毒株。我国虽于1980年由刘景华等[9]首次分离到该病毒,但未测定其基因组序列。本研究为我国首次获得EHV-1流行毒株基因组序列,并经分析表明该毒株与国外多数以马为宿主的EHV-1亲缘关系密切,基因组核苷酸同源性为82.63%~93.58%,但与在斑马、瞪羚、野驴中的分离毒株的同源性只有76.72%~79.79%。与XJ2015株同源性最高的为英国毒株Ab4,该株可引起马严重的临床疾病,包括高频率的流产症状和神经系统疾病,并被视为神经基因型参考毒株[10-12]。
尽管普遍认为EHV-1的宿主范围受到马属动物的限制,但已有报道从非马属动物如牛、骆驼、鹿、北极熊、羊驼中分离到该病毒,其宿主差异导致核苷酸同源性降低[13-15]。Souichi Y等[3]认为EHV-1基因组中的突变使其可在马属动物和反刍动物种间传播,并通过全病毒限制性片段长度多态性(RFLP)分析得出是TRS/IRS和US的变异所致。本文通过对EHV-1基因组结构特性分析表明各毒株TRS/IRS变异最大,同源性仅为65.99%。
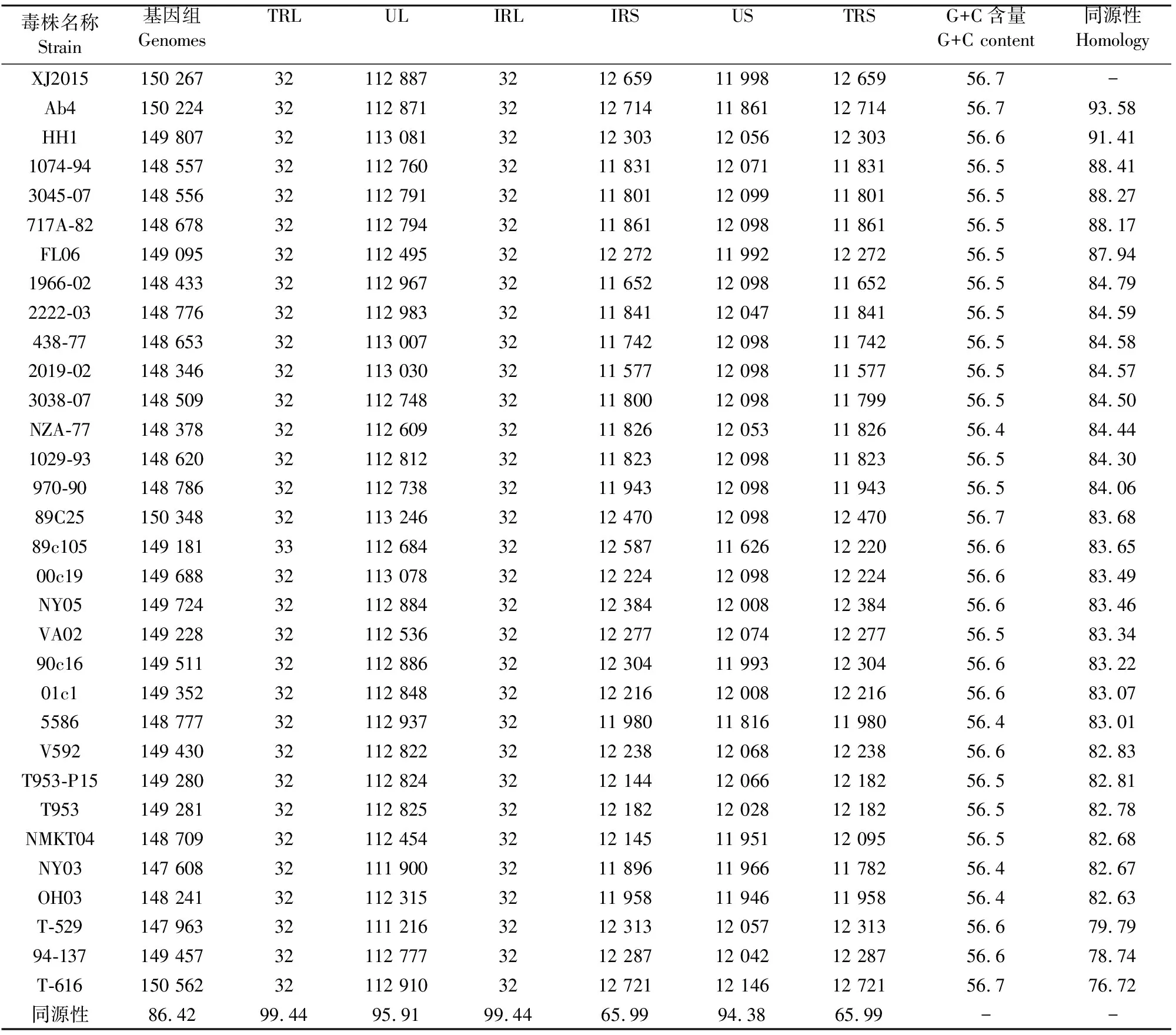
表3 EHV-1基因组结构特性及同源性
注: 基因组、TRL、UL、IRL、IRS、US、TRS单位为bp;G+C含量、同源性单位为%。
Note:Genomes,TRL,UL,IRL,IRS,US,TRSunits:bp; G+C content,Homology units:%.
而根据Seong K等[16]报道位于TRS/IRS的基因ORF64编码的IEP在α疱疹病毒间具有广泛的同源性。EHV-1 IE部分区域与HSV-1的 ICP4和VZV ORF62编码蛋白部分区域有约60%的氨基酸同源性[17]。Ochir P等[18]通过长距离聚合酶链反应(LA-PCR)和RFLP分析比较EHV-1 P和EHV-1B,发现限制性位点差异集中在IEP基因下游且被EHV-4的相应区域替换,表明EHV-1B是EHV-1P和EHV-4之间的自然重组病毒。
本研究获得我国EHV-1流行株毒株XJ2015全基因组序列,掌握其分子特征、基因功能及亲缘关系,得到78个编码蛋白的氨基酸序列。今后将继续探索我国EHV-1流行毒株遗传衍化规律,深入分析TRS/IRS同源重组特性及毒力相关基因特征,为建立反向遗传操作平台及研制基因缺失疫苗提供研究基础与科学依据。
