中华麦饭石对重金属离子的吸附作用
2018-12-04刘玖伟
任 娟,刘玖伟,冯 雷
(优高雅健康科技〈深圳〉有限公司,广东深圳 518000)
麦饭石[1]是我国古代医药学家根据其外观颇似大麦米煮出的饭团而命名的一种传统天然矿物药石,是一种具有良好的矿物质溶出、杂质吸附和生物活性等性能[2]的环境友好型材料。 目前,麦饭石主要应用于水处理、食品、日化品、医疗保健、养殖等领域。
近年来,随着社会的高速发展,工业废水、生活污水排放量急剧增长,且水中的污染物浓度,特别是重金属离子浓度也随之增大。水体中的重金属离子是国际公认的具有致癌、致突、致畸效应[3]和遗传毒性的物质,直接影响人们的身体健康,去除水体中重金属离子的研究已得到越来越多关注。
吸附法在去除水中重金属离子方面已得到应用,常用的吸附剂有活性炭、沸石、膨润土、高分子吸附剂、纳米材料等[4]。麦饭石作为一种储量丰富的天然矿产,其良好的吸附性能已有报道[5]。采用麦饭石作为吸附剂去除饮用水、养殖水体中的重金属离子,在净化水质的同时,又可以调节水质,增加水的元素和生物活性。产于中国内蒙古通辽市奈曼旗的中华麦饭石,被日本地球研究所评为世界上稀有的、质量最佳的麦饭石[6]。目前,中华麦饭石对重金属离子的吸附作用缺乏基础研究,理论数据不全面,尚待深入研究。
因此,本文为了明确产于中国内蒙古通辽市奈曼旗的中华麦饭石对重金属离子的吸附性能,研究不同添加量、浸泡时间及浸泡温度对其吸附性能的影响,探讨吸附机理、解吸作用,研究吸附动力学与吸附等温线,为中华麦饭石用于净化水中Pb2+、Cd2+、Hg2+、As3+、Cr3+等重金属离子提供技术参数和理论依据。
1 方法与材料
1.1 试验材料
中华麦饭石(Chinese medical stone,CMS),产于中国内蒙古通辽市奈曼旗。木质活性炭(万源净水材料贸易有限公司);标准溶液(国家有色金属及电子材料分析测试中心);试验用水为去离子水,其他试剂均为分析纯。
场发射扫描电子显微镜(Nanosem430,美国FEI);X射线衍射仪(D/max 2500,日本Rigaku);全方位行星式球磨机(PMQ2L,卓的仪器);激光粒度分析仪(BT-9300S,丹东百特);精密电子天平(Y20002,上海宇舜恒平);电子天平(FCD-A1000,华志科学仪器);电动搅拌器(JJ-1H 300 W,常州荣华);恒温水浴锅(HH-4,常州荣华);电感耦合等离子体发射光谱仪(Optima8000,美国PerkinElmer)。
1.2 试验方法
1.2.1 CMS扫描电镜及X射线衍射仪衍射检测
CMS粉与木质活性炭粉分别干法球磨2 h,使用激光粒度分析仪测试其粒径D90均为45 μm。对球磨后的CMS进行SEM、XRD测试。
1.2.2 CMS吸附重金属离子试验
使用标准溶液配制质量浓度为0.5 mg/L的重金属离子溶液(浓度值为饮用水国家标准[7]限量值的10倍以上)。取500 mL重金属离子溶液于烧杯中,烧杯置于水浴锅中预热到试验温度后,打开搅拌器,控制转速为700 r/min,加入CMS粉或木质活性炭粉,作用一定时间后,将溶液迅速用滤纸过滤,使用ICP-OES测试滤液中元素含量[8],计算吸附率及吸附量。吸附率吸附量计算方式如式(1)和式(2)。
Y=(C0-Ct)/C0×100%
(1)
qt=V(C0-Ct)/m
(2)
其中:Y—吸附率;
C0—溶液重金属离子初始浓度,mg/L;
Ct—吸附后溶液中重金属离子浓度,mg/L;
qt—任意吸附时间t时刻的吸附量,mg/g;
V—重金属离子溶液体积,L;
m—吸附剂质量,g。
1.2.3 CMS吸附重金属离子的解吸
重金属离子溶液初始浓度为0.5 mg/L,CMS在吸附条件(1∶50、25 ℃、700 r/min、1 h)下吸附重金属离子后,烘干。分别加纯水及2%硝酸在同等解吸条件(1∶20、25 ℃、700 r/min、1 h)下解吸,解吸后的麦饭石100 ℃烘干,在吸附条件(1∶50,25 ℃,700 r/min,1 h)下再吸附,计算CMS吸附量与解吸量。
1.2.4 CMS吸附重金属离子动力学研究
重金属离子溶液初始浓度为0.5 mg/L,同等条件(1∶200、25 ℃、700 r/min)下,吸附时间分别为10、20、30、40、50、60、80、100 min,测试CMS对重金属离子的吸附量。分别采用准一级和准二级速率方程对动力学试验数据进行拟合,求出相关系数R2、平衡吸附量qe及吸附速率常数k1、k2。吸附动力学准一级速率方程和准二级速率方程如式(3)和式(4)。
ln(qe-qt)=lnqe-k1t
(3)
t/qt=1/(k2×qe2)+t/qe
(4)
其中:qe—平衡吸附量,mg/g;
k1—准一级吸附速率常数,min-1;
k2—准二级吸附速率常数,g/(mg·min)。
1.2.5 CMS吸附重金属离子的吸附等温线分析
重金属离子溶液初始浓度分别为0.5、1.5、3.0、4.5、6.0 mg/L,在同等吸附条件(1∶200、25 ℃、700 r/min、2 h)下反应,测试CMS对重金属离子的吸附量。采用Langmuir吸附等温曲线方程对试验数据进行拟合,求出相关系数R2、吸附容量Q、吸附平衡常数b。Langmuir吸附等温曲线如式(5),以Ce、Ce/qe为横纵坐标作图,直线方程如式(6)。
qe=Q×b×Ce/(1+b×Ce)
(5)
Ce/qe=Ce/Q+1/(b×Q)
(6)
其中:Ce—平衡浓度,mg/L;
qe—平衡吸附量,mg/g;
Q—吸附容量,mg/g;
b—吸附平衡常数,L/mg。
2 结果与讨论
2.1 CMS的形貌、结构及成分
图1为CMS样品的微观形貌。由图1可知,经机械破碎后的麦饭石颗粒无规则形状,大小不一,大颗粒表面呈阶梯状结构,且颗粒间孔隙较大。图2为CMS粉体的XRD图谱。由图2可知CMS的主要晶相为SiO2相以及(Na,Ca)Al(Si,Al)3O8相,且该图谱中存在着多个衍射峰,与对应晶相衍射峰一致,衍射峰尖锐,说明CMS晶面生长有序度高,结晶度好,晶体结构完整。而正是由于CMS较大的微观孔隙率和比表面积以及特有的晶相组织结构,使其具有良好的的吸附性能和离子交换能力。

图1 中华麦饭石SEM图Fig.1 SEM Image of Chinese Medical Stone
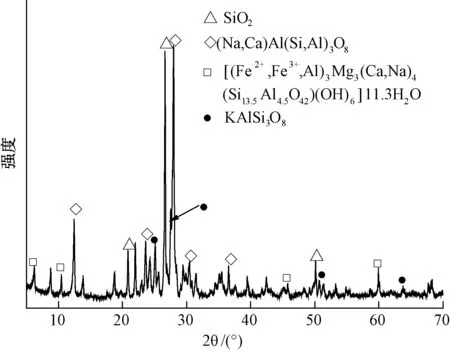
图2 中华麦饭石XRD图谱Fig.2 XRD of Chinese Medical Stone
2.2 CMS与木质活性炭的吸附性能对比
在重金属离子溶液初始浓度0.5 mg/L、添加量为1/5、反应温度为40 ℃时、转速700 r/min、反应时间分别为1 h和4 h的条件下,CMS与木质活性炭对5种重金属离子的吸附率如表1所示。由表1可知,在该条件下,CMS对5种重金属离子吸附效果远大于木质活性炭。在1 h时,CMS对Cd2+、As3+、Cr3+的吸附率就达到了100%,而木质活性炭对Cd2+、As3+、Cr3+的吸附率仅为30%~50%。
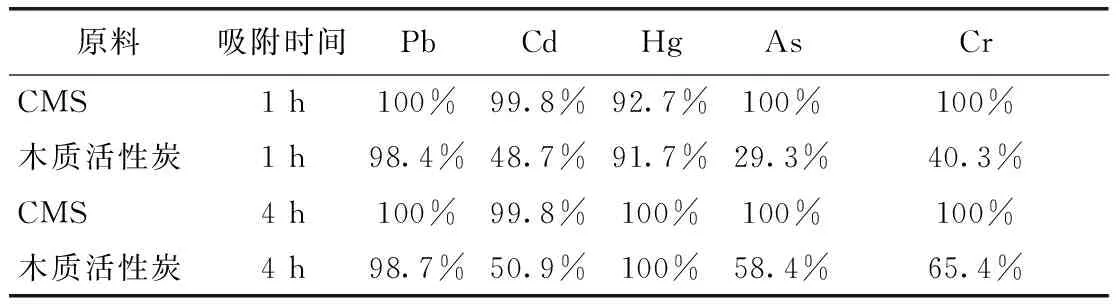
表1 CMS与木质活性炭对重金属离子的吸附率Tab.1 Adsorption Rate of Heavy Metal Ions byCMS and Woody Activated Carbon
2.3 添加量对CMS吸附重金属离子的影响
根据前期试验结果可知,CMS对不同重金属离子的吸附能力应有一定的区别,因此对不同重金属离子分别进行了不同CMS添加量的吸附试验验证这一趋势。重金属离子溶液初始浓度为0.5 mg/L,同等条件(40 ℃、700 r/min、10 min)下,CMS不同添加量对5种重金属离子的吸附率分别如图3、图4、图5所示。
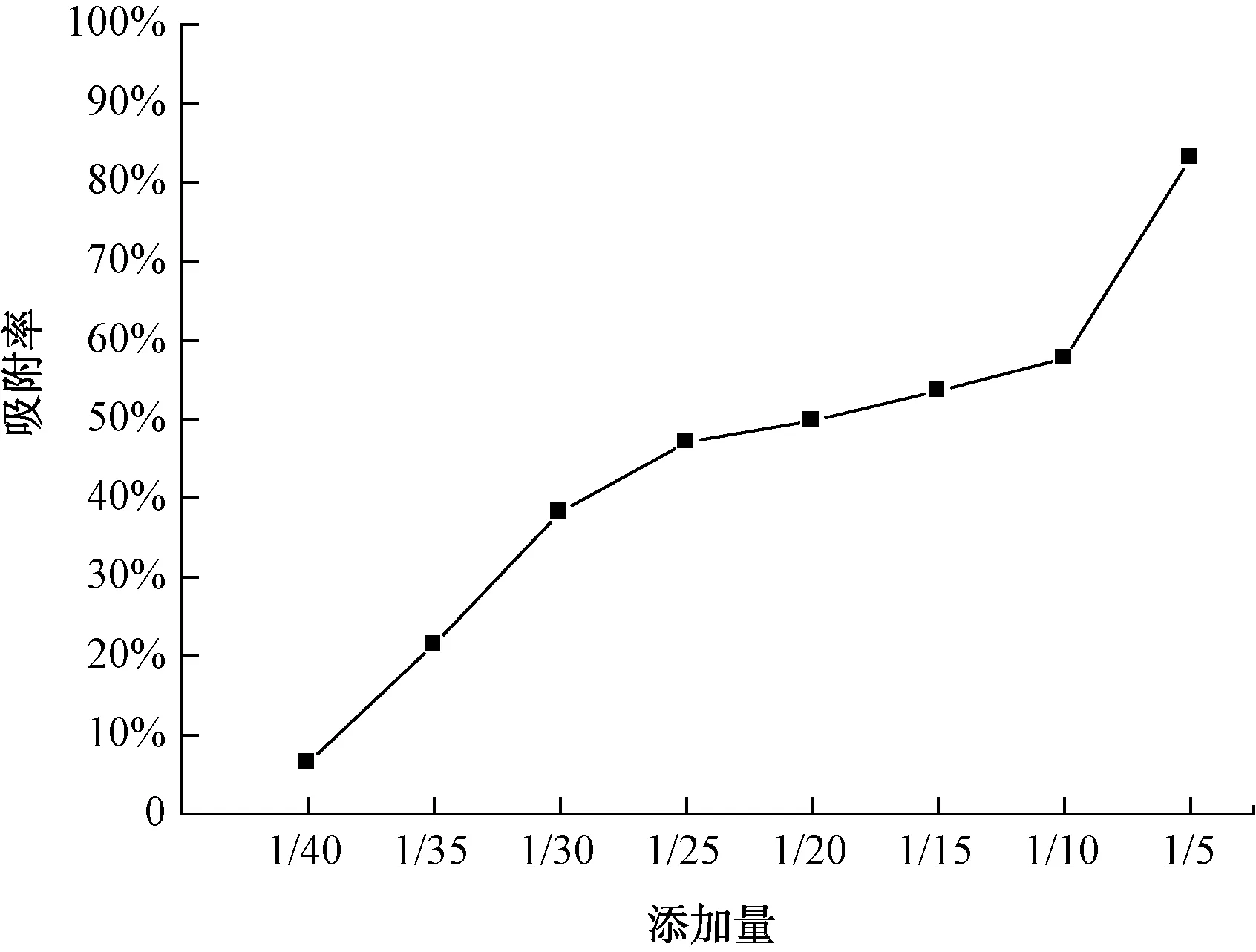
图3 不同添加量的CMS对Hg2+的吸附Fig.3 Adsorption of Hg2+ by CMS with Different Additions

图4 不同添加量的CMS对Cd2+的吸附Fig.4 Adsorption of Cd2+ by CMS with Different Additions
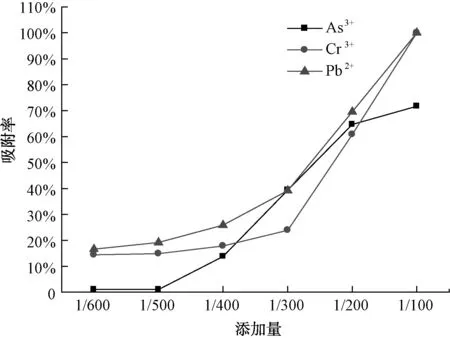
图5 不同添加量的CMS对As3+、Pb2+、Cr3+的吸附Fig.5 Adsorption of As3+,Pb2+ and Cr3+ by CMS with Different Additions
由图5可知,同等条件下,CMS对5种重金属离子的吸附能力强弱为:Pb2+、As3+、Cr3+>Cd2+>Hg2+。随着CMS添加量的增大,其对重金属离子的吸附率均呈现上升的趋势,但是吸附曲线差别较大,这是由于CMS对不同重金属离子发生吸附的主要作用各不相同所致。
2.4 时间对CMS吸附重金属离子的影响
重金属离子溶液初始浓度为0.5 mg/L,同等条件(40 ℃、700 r/min)下,时间对CMS吸附5种重金属离子的影响如图6、图7所示。随着吸附时间的增加,CMS对Hg2+、Cd2+、As3+的吸附率明显增加,而对Pb2+、Cr3+的影响不大。综合考虑吸附效果和工作效率,针对Hg2+、Cd2+、As3+的净化设计处理工艺时,应适当考虑延长作用时间。

图6 时间对CMS吸附Hg2+、Cd2+的影响Fig.6 Effect of Time on Adsorption of Hg2+ and Cd2+ by CMS
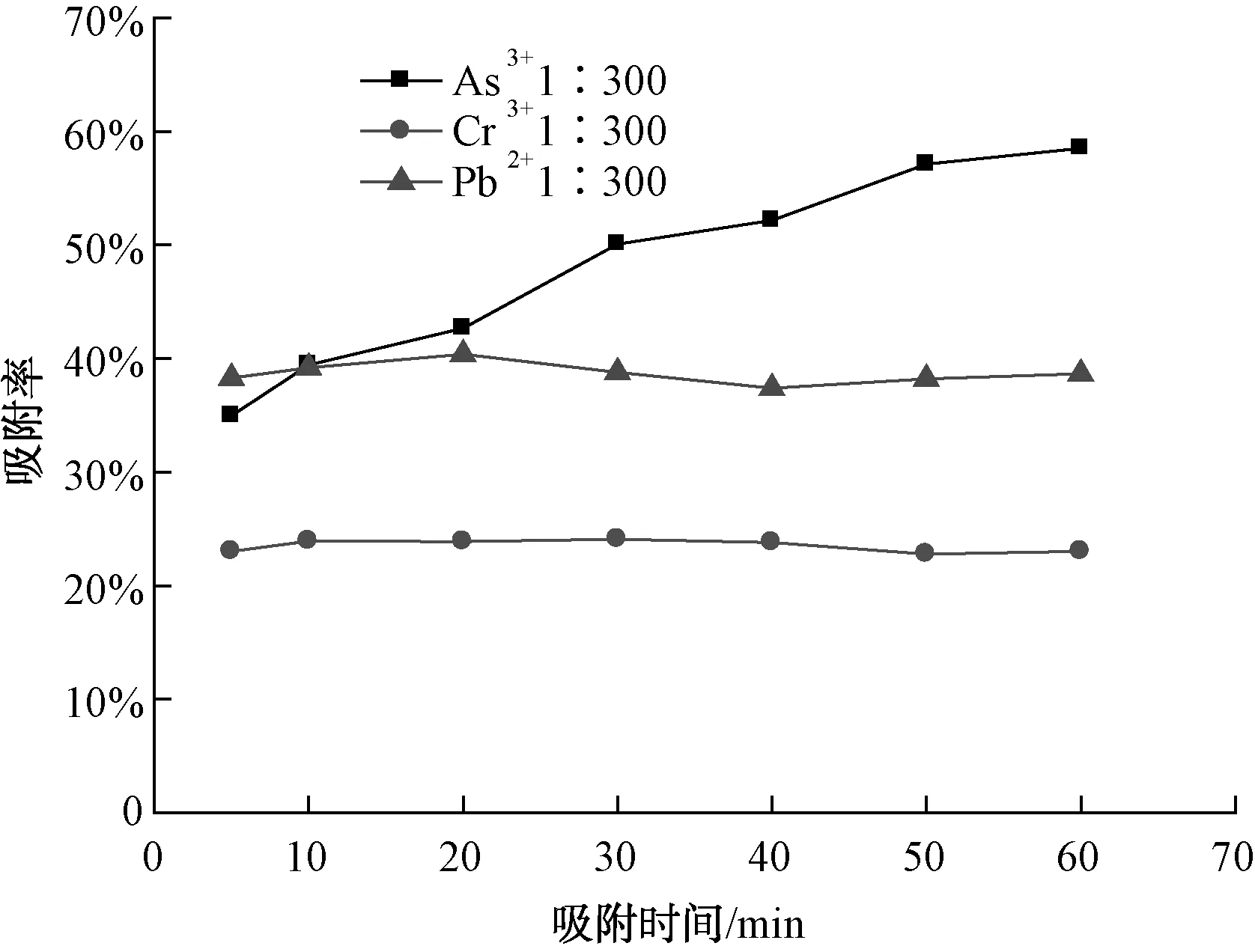
图7 时间对CMS吸附As3+、Pb2+、Cr3+的影响Fig.7 Effect of Time on Adsorption of As3+,Pb2+ and Cr3+ by CMS
2.5 温度对CMS吸附重金属离子的影响

图8 温度对CMS吸附Hg2+、Cd2+影响Fig.8 Effect of Temperature on Adsorption of Hg2+ and Cd2+ by CMS
重金属离子溶液初始浓度为0.5 mg/L,同等条件下(700 r/min,10 min),由图8、图9可知,随着温度的升高,CMS对重金属离子的吸附率同步增加,但对每种重金属离子的影响程度不同。温度对CMS吸附As3+、Cr3+、Hg2+、Cd2+的影响较大,推断是因为离子交换反应随温度升高而加快;温度对CMS吸附Pb2+的吸附则无明显影响。因此针对不同应用场合,需要根据实际情况来选择合适的温度。

图9 温度对CMS吸附As3+、Pb2+、Cr3+的影响Fig.9 Effect of Temperature on Adsorption of As3+,Pb2+ and Cr3+ by CMS
2.6 CMS吸附重金属离子作用机理探讨
麦饭石对重金属离子的吸附性来源于以下3个方面:多孔海绵状结构、离子交换以及表面络合反应[9]。同等条件(1∶10、40 ℃、700 r/min、30 min)下,CMS加纯水为空白组,CMS加混合重金属离子溶液(Pb2+、As3+、Cr3+、Cd2+、Hg2+)为试验组,测试吸附前后溶液中元素的含量,试验结果如表2所示。
由表2可知,与空白组比较,试验组溶液中的重金属离子被CMS吸附的同时,溶液中Ca2+、K+、Mg2+、Na+明显增多,增加量为:Ca2+>Na+>K+>Mg2+。其中,Ca2+明显增多说明重金属离子主要与麦饭石中Ca2+发生离子交换反应。由图1可知,大的孔隙和比表面积使其具有良好的吸附性能,这种吸附属于物理吸附。由此可知,离子交换和物理吸附是中华麦饭石吸附重金属离子的主要形式。
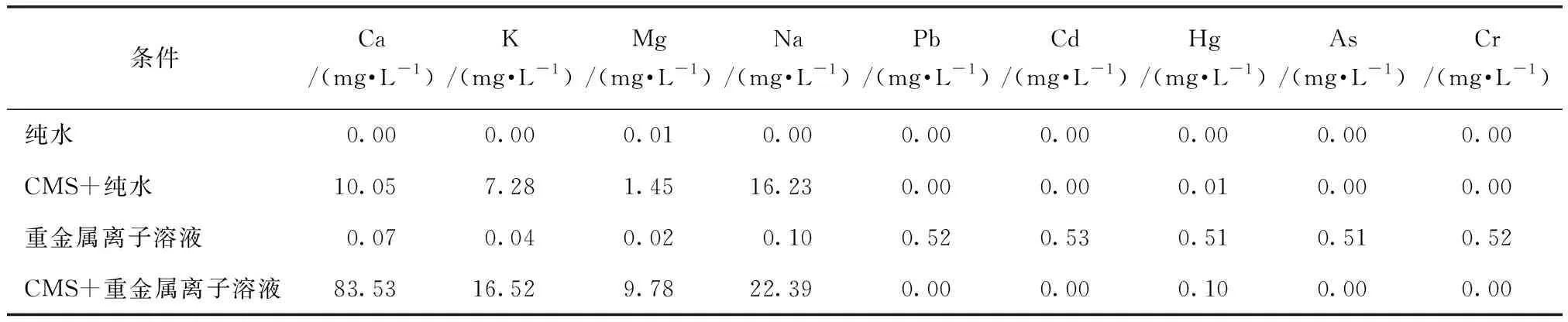
表2 CMS吸附重金属离子试验结果Tab.2 CMS Adsorption of Heavy Metal Ions
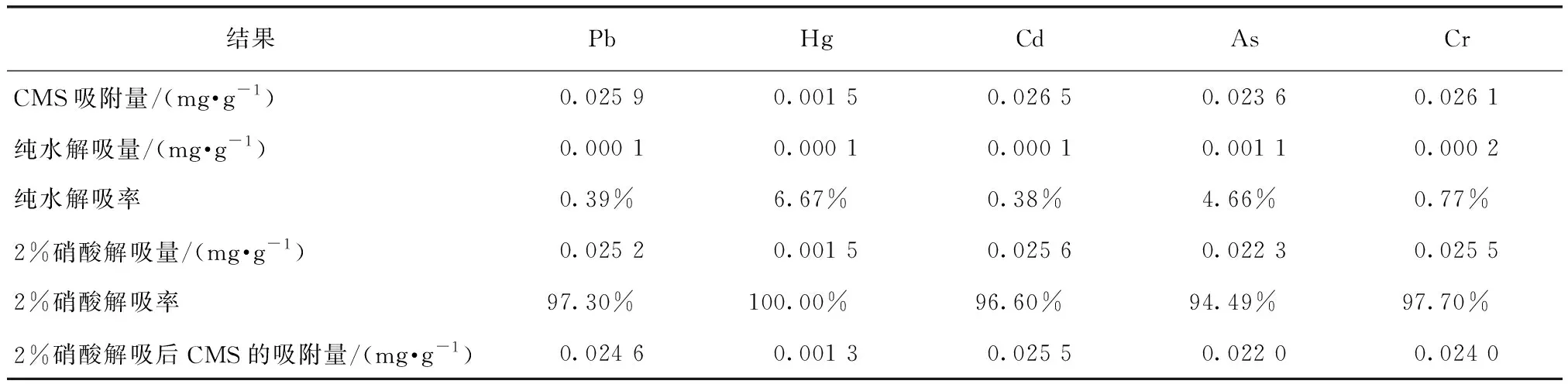
表3 CMS吸附重金属离子解吸结果Tab.3 CMS Desorption of Heavy Metal Ions
2.7 CMS吸附重金属离子的解吸
同等解吸条件下(1∶20、25 ℃、700 r/min、1 h),CMS吸附量与解吸量如表3所示。由表3可知,纯水对CMS吸附的重金属离子没有解吸作用;2%硝酸对CMS吸附的重金属离子的解吸率达94%~100%,说明2%硝酸解吸重金属离子效果很好。2%硝酸解吸后的CMS,吸附重金属离子的量略低于CMS原石粉。
2.8 CMS吸附重金属离子的动力学研究
同等条件(1∶200、25 ℃、700 r/min)下,测试CMS在不同时间对重金属离子的吸附量,结果如表4所示。采用一、二级速率方程对表4的数据进行拟合,如图10~图12所示,相关拟合参数如表5所示。拟合出的一级速率方程相关系数R2为0.751 1~0.909 6,相关性较好,但随着时间的增加,试验数据逐渐偏离拟合曲线,说明一级速率方程只能够描述CMS吸附初始阶段;二级速率方程相关系数R2为0.972 6~0.998 4,且二级速率方程得到的平衡吸附量qe与试验所得数值很接近,说明二级动力学方程能够很好地描述CMS对重金属离子的吸附过程。

表4 CMS吸附动力学试验结果Tab.4 CMS Adsorption Kinetic Test Results

表5 CMS吸附动力学方程参数Tab.5 CMS Adsorption Kinetic Equation Parameters
注:qe为试验测得的平衡吸附量

图10 CMS吸附重金属离子的一级速率方程拟合曲线Fig.10 Fitting Curve of First-Order Rate Equation for CMS Adsorption of Heavy Metal Ions
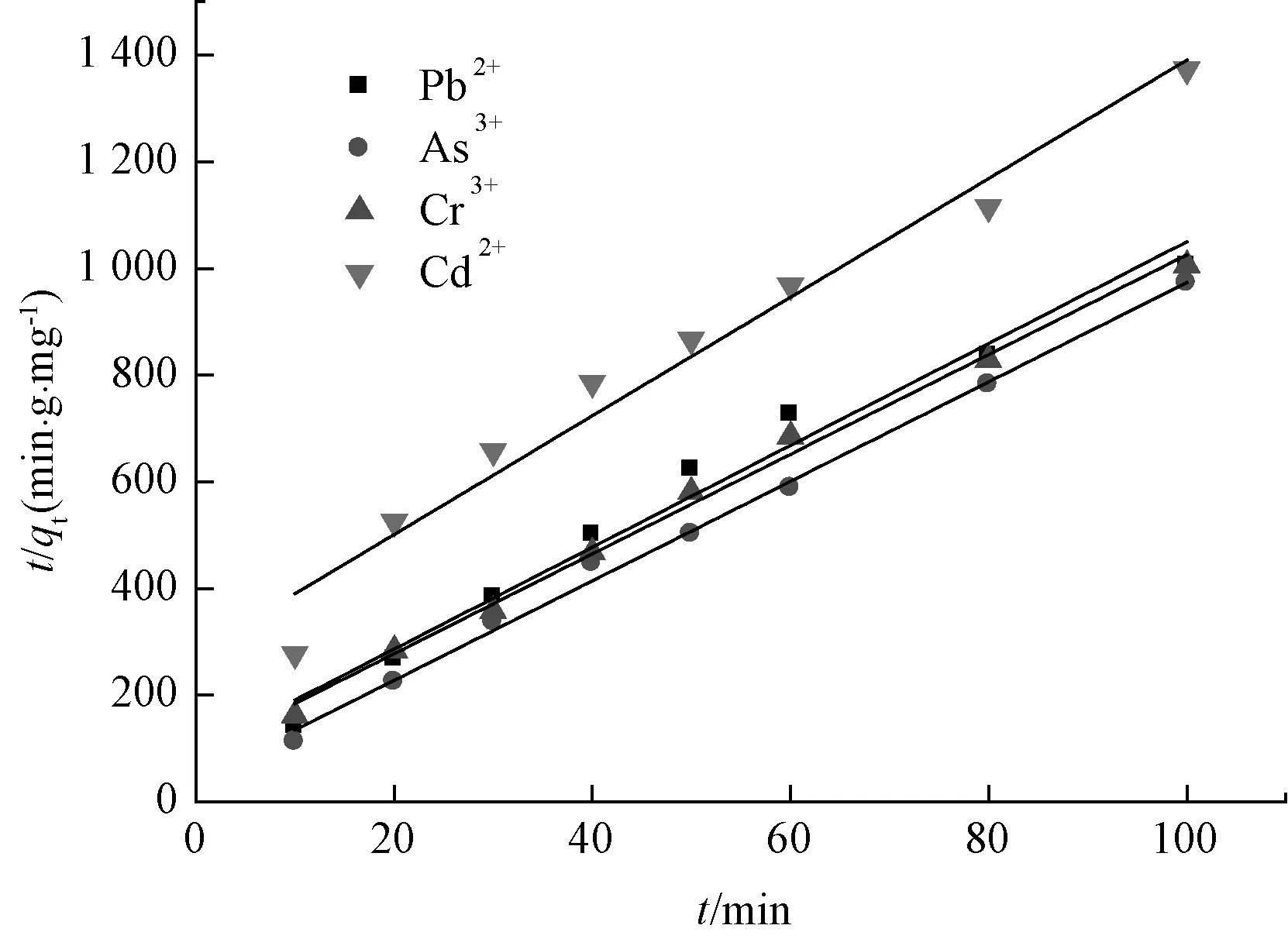
图11 CMS吸附重金属离子的二级速率方程拟合曲线Fig.11 Fitting Curve of Second-Order Rate Equation for CMS Adsorption of Heavy Metal Ions

图12 CMS吸附Hg2+的二级速率方程拟合曲线Fig.12 Fitting Curve of Second-Order Rate Equation for Hg2+ Adsorption by CMS
2.9 CMS吸附重金属离子的等温线分析
试验数据以Ce、Ce/qe为横纵坐标作图,Langmuir吸附等温曲线如图13所示,拟合参数如表6所示。Langmuir吸附等温曲线的相关系数R2都大于0.9,说明CMS对重金属离子的吸附符合Langmuir吸附等温曲线,属于单分子层吸附。CMS对重金属离子Pb2+、As3+、Cr3+、Cd2+、Hg2+的吸附容量Q分别为0.119 8、0.133 1、0.105 4、0.069 8、0.057 5 mg/g。
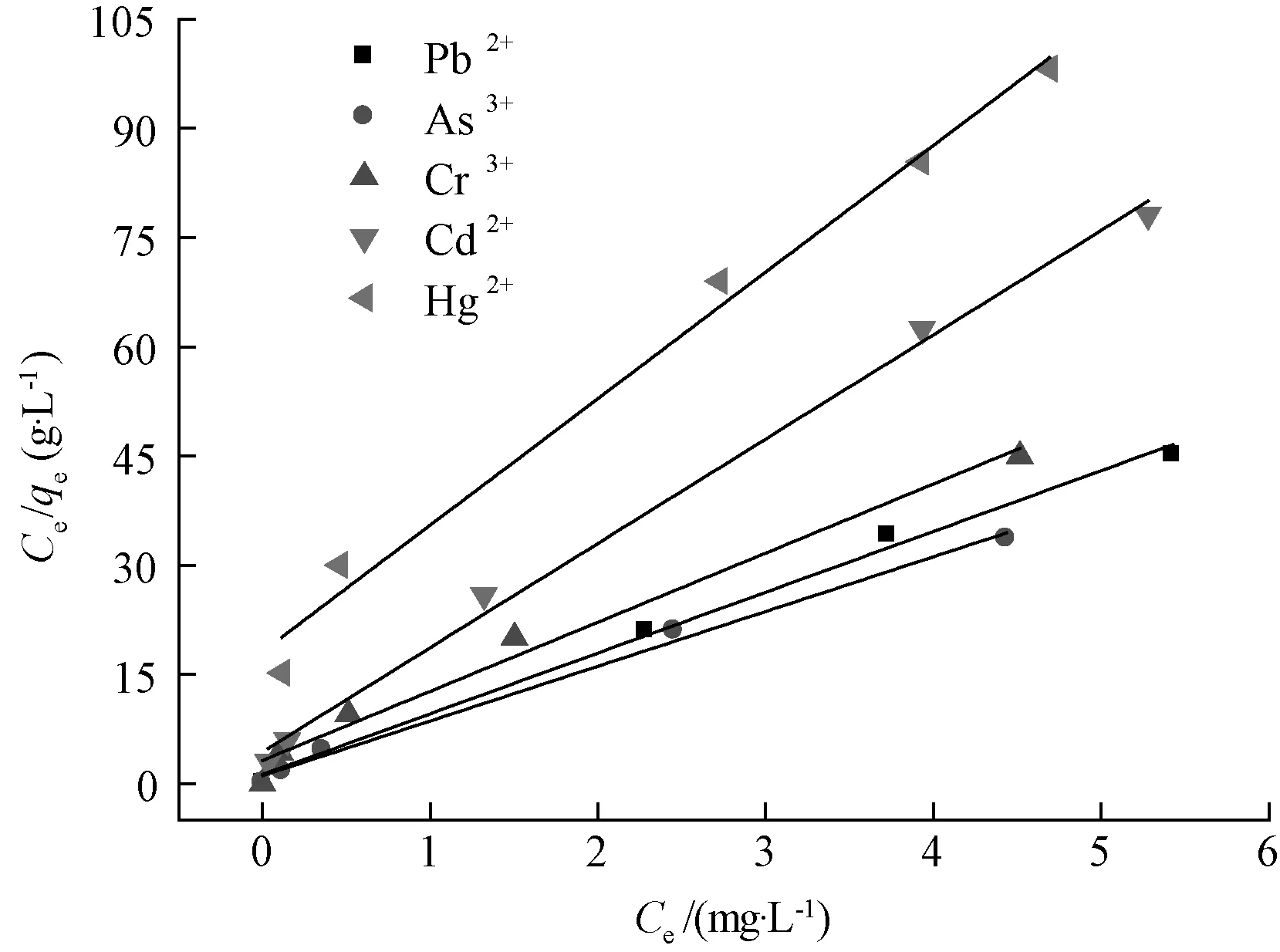
图13 CMS吸附重金属离子的Langmuir吸附等温线Fig.13 Langmuir Adsorption Isotherms of CMS Adsorption of Heavy Metal Ions
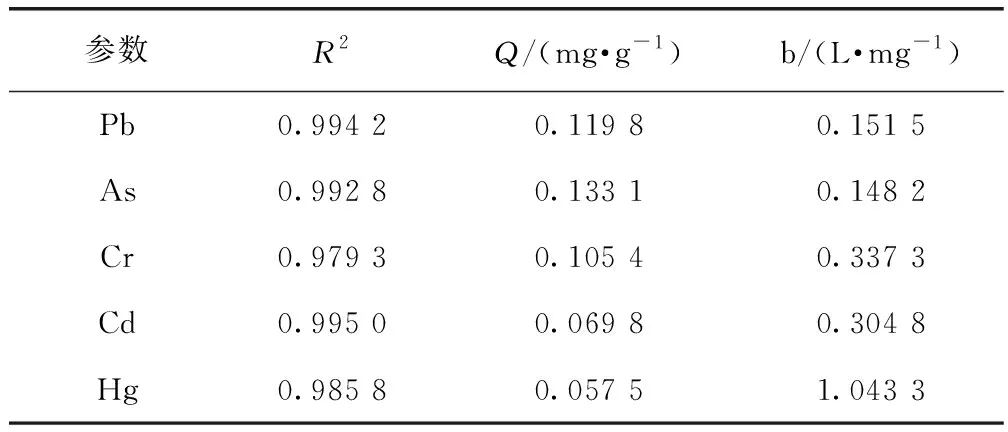
表6 Langmuir吸附等温曲线参数Tab.6 Langmuir Adsorption Isotherm Parameter
3 结论
(1)CMS对重金属离子有很强的吸附作用,尤其对Cd2+、As3+、Cr3+的吸附能力远远大于木质活性炭。
(2)CMS对5种重金属的吸附能力从大至小的排序为:Pb2+、As3+、Cr3+>Cd2+>Hg2+。其中,CMS对Pb2+、As3+、Cr3+的吸附能力在不同吸附条件下会有变化。
(3)时间和温度对CMS吸附重金属离子的影响也不相同。时间对CMS吸附Hg2+、Cd2+、As3+影响较大,随着时间的增加,吸附率升高;但对吸附Pb2+、Cr3+则无明显影响。温度对CMS吸附As3+、Cr3+、Hg2+、Cd2+影响较大,对Pb2+无明显影响。
(4)离子交换和物理吸附是CMS吸附重金属的主要形式,重金属离子主要与Ca2+、K+、Mg2+、Na+发生交换。离子交换与物理吸附及表面络合反应对CMS吸附重金属的协同作用还有待进一步的研究。
(5)2%硝酸对CMS吸附的重金属离子解吸效果良好,解吸液中的重金属可回收利用,无二次污染。解吸后的CMS活化处理后吸附重金属离子效果没有明显下降,说明CMS可以解吸重复利用,重复利用次数需要进一步研究。
(6)从吸附动力学角度分析,CMS吸附重金属离子可以用准二级动力学速率方程很好的描述。
(7)从吸附等温线分析,CMS对重金属离子的吸附符合Langmuir吸附等温曲线,属于单分子层吸附。CMS对重金属离子Pb2+、As3+、Cr3+、Cd2+、Hg2+的吸附容量分别为0.119 8、0.133 1、0.105 4、0.069 8、0.057 5 mg/g。
综上可知,中华麦饭石对重金属离子有良好的吸附作用,且储量丰富,可以做为滤料用于饮用水水质净化及工业废水的净化处理。
