自动乳腺全容积扫描成像系统对乳腺肿块的诊断价值*
2018-11-26申俊玲李婷龚业琼吴晓莉李可基
申俊玲 李婷 龚业琼 吴晓莉 李可基
(攀枝花市中心医院超声科,四川 攀枝花617061)
据中国人口协会于2010年在北京发布的《中国乳腺疾病调查报告》统计,我国城市乳腺癌的死亡率增长了38.91%,其发病率在大城市女性肿瘤中已跃居首位。寻找一种无创、便捷的乳腺癌早期筛查方法的需求日益迫切。乳腺超声检查无创、无辐射、患者易于接受,是当前乳腺疾病的首选方法[1]。但是普通超声采用手动操作,受检查医师的手法及经验等影响较大,具有一定局限性。自动乳腺全容积扫描成像(automated breast volume scanner,ABVS)与普通超声相比,具有自行超声断层扫描、规范化的扫查方法和图像信息储存等优点,尤其是可采集冠状面图像、得到病变部位更多的信息。但在诊断乳腺恶性肿瘤上,ABVS主要是依据“汇聚征”、微钙化等主观性指标,受阅片医师主观影响较大[2-7]。为了减少普通阅片医师主观印象对病变乳腺的影响,本文采用乳腺病变的方位、边缘、毛刺、汇聚征、钙化5个指征作为评价乳腺良、恶性病变的指标,并进行评分,旨在制定一个半定量的方法,以判断乳腺病变的良、恶性,减少阅片医师主观意识的影响,现报告如下。
1 资料与方法
1.1 一般资料 选取2016年4月~2017年6月因乳房疼痛、乳腺包块、乳头溢液等症状在我院就诊并接受手术治疗或超声引导下穿刺活检术的477例患者,均为女性,共检出病灶656个。患者年龄18~76岁,平均(39.3±11.5)岁。排除超声显示为囊性病变的病例。
1.2 检查方法 采用西门子Acuson S2000 ABVS系统,配置14L5BV高频线阵探头,频率为5~14MHz,视野横向范围为15.4cm,径向范围为16.8cm,前后径最大为6.0cm。患者取仰卧位(根据需要也可向一侧稍倾斜),观察患者乳房的大小选择仪器的最佳预设条件。一般采用外侧位、内侧位和前后位3个方位扫查,对情况特殊的患者可加查有价值方位。扫描方向为由下向上自动扫描,每个方位扫查用时约65s,重建图像最小断层间距为0.5mm[8]。自动扫描结束后,定位乳头位置,系统接受后自动将数据传输并进行三维重建,获得3个断面的图像,特别是冠状面图像。检查者可根据需要显示病变与乳腺组织间的关系[9],进行脱机观察分析。
1.3 研究方法 从方位、边缘、毛刺、汇聚征、钙化5个特征进行分析,以术后病理为金标准,统计分析每个特征是否可作为判断良恶性的诊断指标。其后以统计筛选出的诊断指标对每个病变进行评分,每项相加即为该病变的最后得分。
1.4 统计学分析 应用SPSS17.0统计软件对方位、边缘、毛刺、汇聚征、钙化5个特征进行2检验,筛选可用于判断良恶性的诊断指标。根据病变最后得分绘制ROC曲线,计算其曲线下面积及ABVS评分法对乳腺癌的诊断敏感性、特异性、准确性、误诊率及漏诊率,并获得ABVS的最佳临床诊断分界点。
2 结果
2.1 病理结果 本组477例病例656个病变,术后病理结果为良性病变531个,恶性病变125个,见表1。
2.2 5个特征指标的统计学检验 以病理结果为金标准进行2检验,结果显示,方位、边缘、毛刺、汇聚征、钙化均可以作为ABVS判断乳腺良恶性病变的评价指标,见表2。
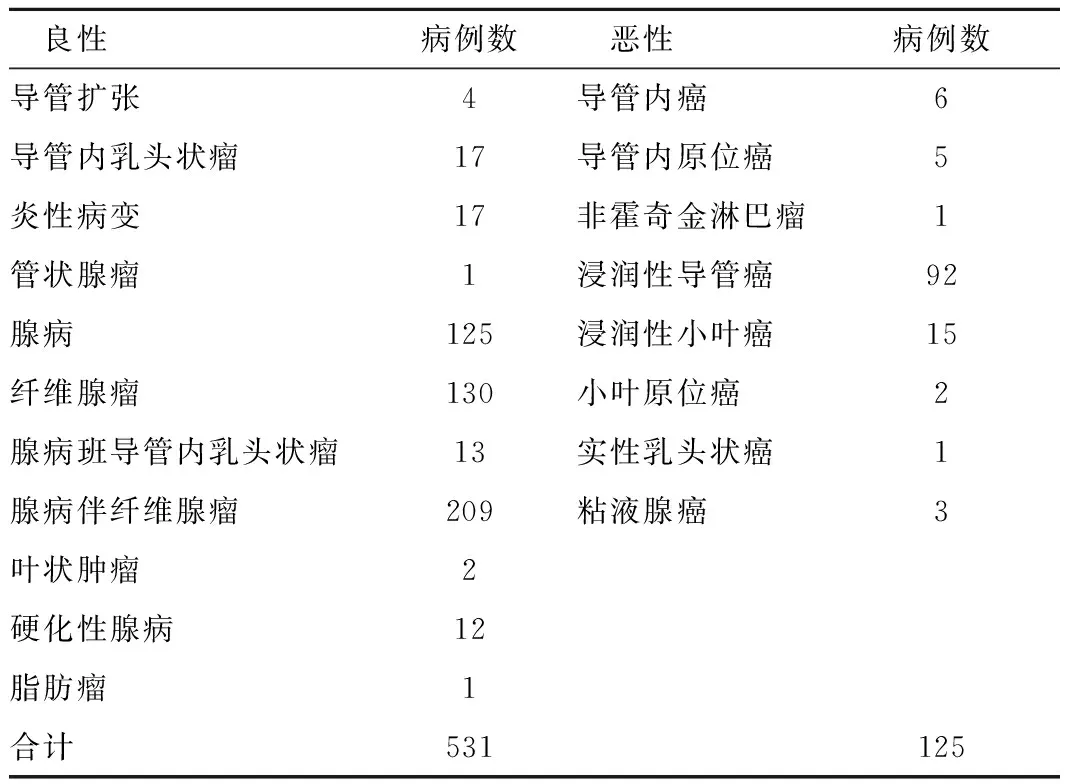
表1 病理结果(n)Table 1 Pathological results
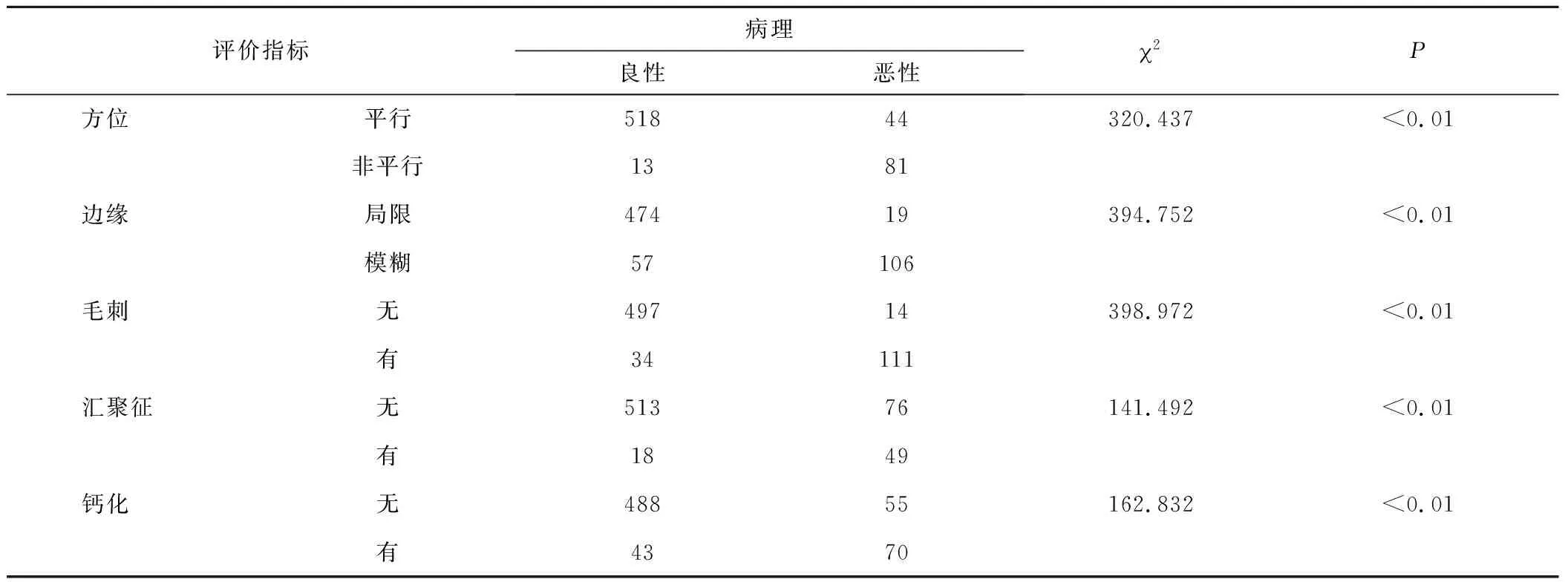
表2 5个特征指标的统计学检验 (n)Table 2 Five characteristic indicators of the test
2.3 乳腺病变的ABVS评分 656个乳腺病变按照5个评价指标进行评分,方位平行为0分,非平行为1分;边缘局限为0分,模糊为1分;无毛刺为0分,有毛刺为1分;无汇聚征为0分,有汇聚征为1分;无钙化为0分,有钙化为1分,5项分值相加为最终得分。具体评分情况见表3。
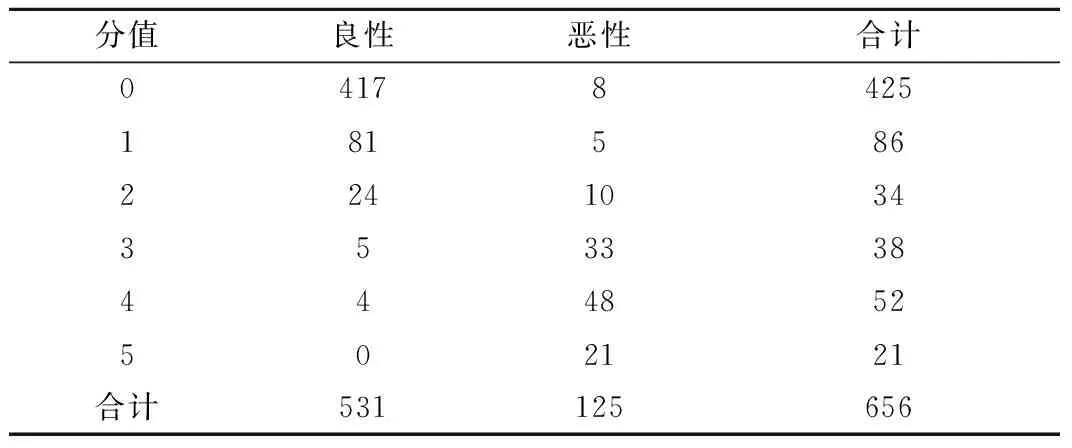
表3 乳腺病变的ABVS评分(n)Table 3 ABVS score for breast lesions
2.4 ABVS评分诊断乳腺癌的ROC曲线与临界点 以分数为参数,以敏感性为纵轴,特异性为横轴,绘制ROC曲线,ROC曲线Az为0.891, Se=0.017,P<0.01。敏感性+特异性最大值所对应的分值为2.5分。以≥2分为超声诊断乳腺癌的临界点,其诊断乳腺癌的敏感性、特异性、准确性、误诊率及漏诊率分别为89.6%、93.8%、93.0%、10.4%和6.2%;以≥3分为超声诊断乳腺癌的临界点,其诊断乳腺癌的敏感性、特异性、准确性、误诊率及漏诊率分别为81.6%、98.3%、95.1%、18.4%和1.7%。因≥2分其敏感性+特异性大于≥3分的敏感性+特异性,故选取≥2分为超声ABVS诊断乳腺癌的临界点,见图1 。
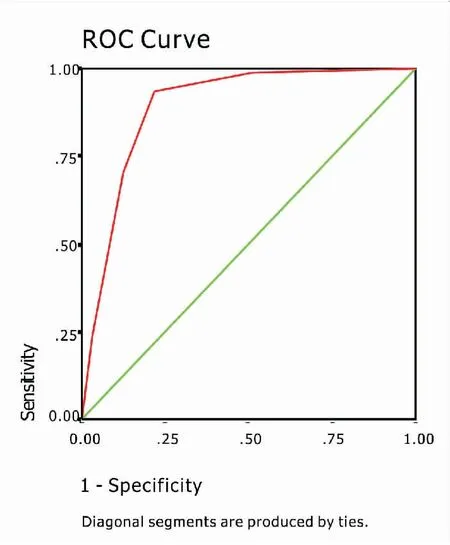
图1ABVS评分诊断乳腺癌的ROC曲线
Figure1ROCcurveofABVSscoreinthediagnosisofbreastcancer
2.5 ABVS图像 用5个指标分析图像可以看出,良性病例出现恶性征象不多于2项,而恶性病例会出现2个以上的恶性征象,见图2、3。
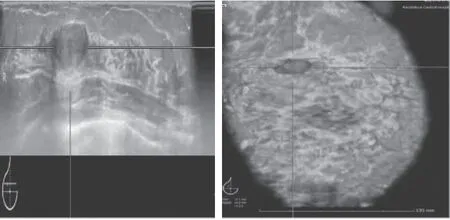
图2 ABVS评分为1分,病理:纤维腺瘤Figure 2 ABVS score of 1 points, pathology: fibroadenoma
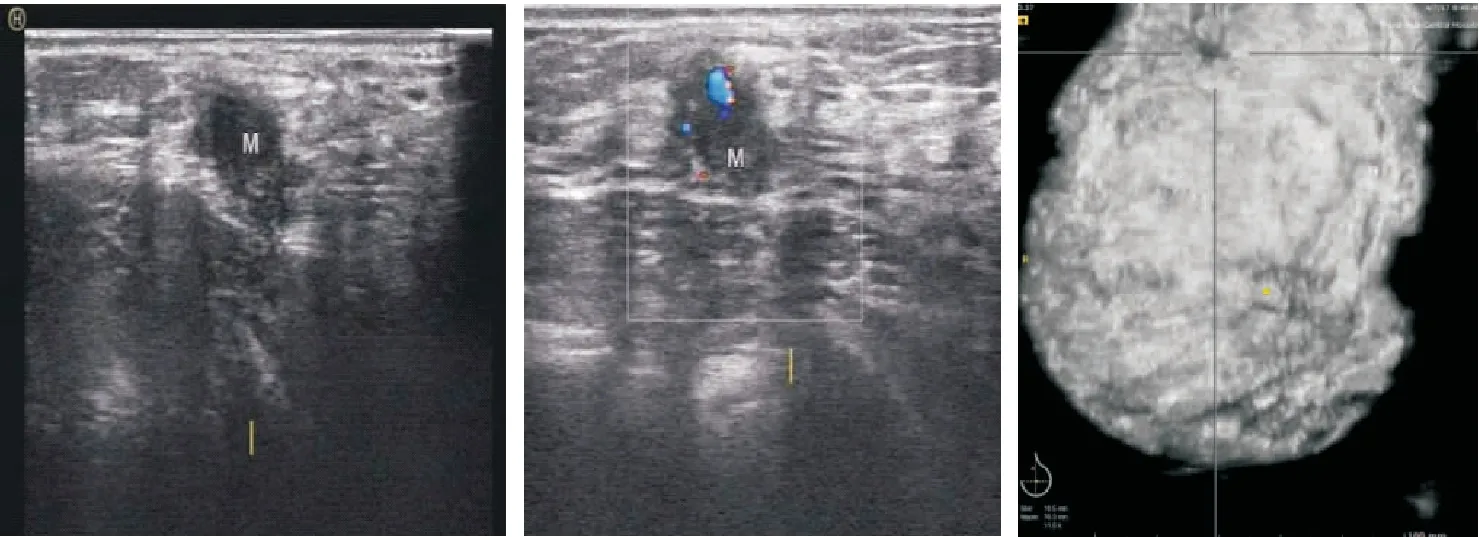
图3 ABVS评分为3分,病理:浸润性导管癌Figure 3 ABVS score of 3 points, pathology: invasive ductal carcinoma
3 讨论
ABVS系统在传统超声技术的基础上,应用自动连续断层扫描技术,是超声技术、操作流程和诊断的一种革新,有以下优点:①3个断面同步显示[10]。②清晰显示病灶内部结构和外部形态,图像分辨率高,能更好地鉴别肿瘤的性质[11]。③显示冠状面图像,弥补二维超声不足,提供更多的信息[12-13]:清晰显示病灶的形态、大小、伪足、纠集腺体及微钙化等特点。④标准化图像存储,可脱机工作,随时读图,有利于系统回顾及分析并可以远程会诊;也可以系统管理病例资料,解决超声质量控制困难的问题[13-14]。⑤ABVS的扫描操作可以由经过培训的技师完成,减轻超声医师工作负担,节约时间[15]。根据以往研究表明[12,16],“汇聚征”对ABVS诊断乳腺癌具有较高的特异性,但不是所有乳腺癌病灶都有“汇聚征”[17-18],单一采用“汇聚征”容易漏诊。另外,在部分纤维腺瘤中也可见到“汇聚征”[19],故以此为诊断标准也可造成误诊。本文从乳腺病灶的ABVS图像特征分析5个诊断指征,并对病灶进行评分,通过一种半定量的方法用于ABVS诊断乳腺癌,以减少阅片医师的主观性。
ABVS有诸多优点,但诊断乳腺疾病的准确性首先取决于标准的图像。因乳腺是一个可活动的器官,诸多因素均可影响图像质量,如乳腺的大小、乳腺的致密程度、探头的滑动、扫查时的体位、探头加压程度、包块的大小、活动度等[20]。现行的ABVS采用流程化操作方式[21]、标准的扫查方法[9],图像采集稳定,使得该技术得到进一步完善,能避免因操作人员扫查手法和经验等原因造成的漏诊。
对656个肿块通过评分法得出ROC曲线, 得出2分为ABVS诊断乳腺恶性肿瘤的理论值,≥2分为恶性,其敏感性、特异性、准确性高,误诊率及漏诊率低,对判断乳腺疾病有较高的临床意义。
以≥2分诊断乳腺癌漏诊13例,分别是导管内癌2例,导管内原位癌4例,非霍奇金淋巴瘤1例,小叶原位癌1例,粘液癌2例,浸润性导管癌1例,浸润性小叶癌2例。从以上病例可以看出漏诊的主要以原位癌、导管内癌居多,可能是由于原位癌的癌细胞未突破基底膜未向周围扩散,恶性征象不典型[22],此时超声诊断较困难。非霍奇金淋巴瘤1例(19岁),图像显示肿块边界清晰,呈多发性,周边未见明显毛刺,患者除乳腺肿块外全身未发现淋巴瘤病灶,故漏诊。粘液癌2例,漏诊原因可能与其镜下组织学特征有关,粘液癌间质及胞浆内含大量粘液,浸润性不强,间质反应轻微,癌栓未形成[23-24]。其病理学特点决定了超声表现出现毛刺、汇聚等特征性指标的可能性不大。浸润性癌3例漏诊,分析原因为病灶小,该研究开展早期阅片医师经验不足所致。
以≥2分诊断乳腺癌误诊33例,分别是腺病15例,炎性病变8例,硬化性腺病6例,纤维腺瘤4例,叶状肿瘤1例。误诊病例中腺病及硬化性腺病共21例,是由其镜下组织学特性所决定的,乳腺腺病是乳腺结构不良症的早期,主要表现为局限性增生、局部组织紊乱造成超声误诊。炎性病变8例可能是因为局部炎性细胞浸润造成超声图像上显示为边界模糊的低回声团块易误诊。纤维腺瘤4例误诊,回顾图像4例均为数枚纤维腺瘤融合而成,使得病灶表现为分叶状、边缘稍模糊、方位非平行等特征,故而误诊。叶状肿瘤1例,主要是病灶呈分叶状、边界不清造成误诊。
ABVS系统的临床应用价值得到了国内外学者的肯定,但其自身也具有一定的局限性[25]:①不适用于所有乳腺疾病患者。如皮肤破溃、乳头内陷、病灶明显突出皮肤等成像效果不佳的患者不宜使用。②探头框架较大,不能进行腋窝的扫查。③对活动度大的病灶检查过程中易出现位移,使冠状面成像不满意。④仅能显示二维图像,缺乏彩色多普勒、血流频谱及弹性成像等对诊断有用的超声信息。⑤设备昂贵。上述局限性大多是普通超声检查所能够弥补的,因此在实际工作中,结合常规超声检查可为临床诊断提供更多的影像学信息。
4 结论与启示
ABVS评分法作为一种新的超声技术,可成为诊断乳腺癌的一项量化指标,与常规超声可互为补充,但两者如何联合尚有待进一步研究。
