对比雷替曲塞与氟尿嘧啶TACE治疗中晚期原发性肝癌疗效及安全性:Meta分析
2018-11-20祖茂衡
周 凡,赵 倩,徐 浩,祖茂衡,许 伟*
(1.徐州医科大学附属医院介入放射科,2.内分泌科,江苏 徐州 221006)
原发性肝癌是常见恶性肿瘤之一,多数患者就诊时已属中晚期,失去手术机会[1]。目前TACE是介入治疗中晚期肝癌的主要方法[2],但在化疗药物选择方面尚无统一标准,临床常用化疗药主要包括氟尿嘧啶类、铂类及阿霉素类等。雷替曲塞为氟尿嘧啶类似物,已广泛用于治疗晚期结肠直肠癌[3],但对其用于TACE治疗中晚期肝癌的临床疗效及安全性仍存在争议。本文对既往有关雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌疗效及安全性的研究报道进行Meta分析。
1 资料与方法
1.1 文献检索 计算机检索PubMed、Cochrane Library、Web of Science、中国生物医学文献数据库、万方数据库、中国知网收录的文献。中文检索词为雷替曲塞、氟尿嘧啶、肝动脉化疗栓塞、肝癌;英文检索词为raltitrexed、fluorouracil、transcatheter arterial chemoembolization、hepatocellular carcinoma。起始检索时间不限,截止2018年04月09日。另人工检索相关文献的参考文献。
1.2 文献纳入及排除标准 纳入标准:①有关雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌的对比研究;②语种为中文或英文;③实验组治疗方式为雷替曲塞TACE,对照组为氟尿嘧啶TACE;④文中可获取患者基线资料、TACE后临床疗效、不良反应等信息。排除标准:①综述、个案报道、会议纪要、专家评论、讲座;②未设立对照组;③研究数据不完整或不能获取全文;④重复发表的文献。
1.3 文献筛选和资料提取 由2名医师独立依据纳入及排除标准筛选文献,并交叉核对结果,有分歧时经讨论达成共识,必要时请第3名医师参与讨论。对检出文献提取资料,包括:①基本特征,包括第一作者、发表年、研究类型、样本量等;②临床疗效,评价指标包括客观有效率(objective response rate, ORR)、疾病控制率(disease control rate,DCR)及患者总生存率(overall survival, OS);③术后不良反应发生情况,包括恶心、呕吐及发热等。
1.4 文献质量评价 采用Cochrane手册标准[4]对纳入文献进行质量评价,分为A(发生偏倚的可能性小)、B(发生偏倚的可能性中等)、C(发生偏倚的可能性大)3级。
1.5 统计学分析 采用STATA 12.0统计分析软件。以Q检验和I2值评价纳入文献的异质性,如异质性可忽略(P>0.1且I2<50%),选用固定效应模型进行Meta分析,否则选用随机效应模型。研究的效应量采用相对危险度(relative risk, RR)及95%CI。绘制森林图合并数据,P<0.05为差异有统计学意义。采用敏感度分析进行结果稳定性检验;以Egger检验评估发表偏倚,P<0.1表明存在发表偏倚。
2 结果
2.1 文献筛选结果 初步检索获得相关文献576篇,阅读文章题目和摘要后排除文献552篇,阅读全文后排除文献16篇,最终纳入8篇[5-12],包括回顾性及前瞻性研究,共635例患者(实验组300例,对照组335例)。文献筛选流程及结果见图1。
2.2 纳入文献基本特征及质量评价 8篇[5-12]中,中文文献6篇[5-8,11-12],英文文献2篇[9-10];质量评价结果为B级7篇[5-11],C级1篇[12];见表1。
2.3 Meta分析结果
2.3.1 ORR、DCR及OS 8篇[5-12]均报道了ORR和DCR,4篇[6-7,9-10]报道了OS,异质性检验显示异质性可忽略(P=0.448、0.103和0.491,I2均=0)。以固定效应模型行Meta分析结果显示,雷替曲塞与氟尿嘧啶TACE治疗的ORR[RR=1.25,95%CI(1.06,1.47),P=0.008,图2]、DCR差异均有统计学意义[RR=1.17,95%CI(1.08,1.26),P<0.001,图3],而TACE后患者OS差异无统计学意义[RR=1.15,95%CI(0.95,1.39),P=0.141,图4]。
2.3.2 术后不良反应 7篇[5-8,10-12]报道了术后恶心、呕吐发生率,异质性检验显示异质性可忽略(P=0.985,I2=0),以固定效应模型行Meta分析结果显示,雷替曲塞与氟尿嘧啶TACE治疗后恶心、呕吐发生率差异无统计学意义[RR=0.90,95%CI(0.73,1.11),P=0.339],见图5。有关术后发热、肝区疼痛、外周血白细胞减少及转氨酶升高的文献分别为7篇[5-6,8-12]、6篇[6,8-12]、7篇[5-8,10-12]和6篇[5-6,8-9,11-12],异质性检验显示异质性均可忽略(P=0.761、0.121、0.589和0.063,I2均=0)。以固定效应模型行Meta分析结果显示,雷替曲塞与氟尿嘧啶TACE治疗后发热[RR=0.90,95%CI(0.77,1.06),P=0.219,图6]、肝区疼痛[RR=0.90,95%CI(0.80,1.01),P=0.219,图7]、外周血白细胞减少[RR=0.89,95%CI(0.65,1.21),P=0.462,图8]及转氨酶升高[RR=0.96,95%CI(0.80,1.16),P=0.663,图9]的发生率差异均无统计学意义。

图1 文献筛选流程
2.4 敏感度分析及发表偏移 通过敏感度分析对纳入文献依次逐一剔除,剔除前后各临床指标合并值未发生明显变化。Egger检验结果显示,ORR(P=0.788)、DCR(P=0.189)、OS(P=0.723)、术后不良反应[恶心、呕吐(P=0.976)、发热(P=0.105)、肝区疼痛(P=0.482)、外周血白细胞减少(P=0.711)、转氨酶升高(P=0.742)]均不存在明显发表偏倚。
3 讨论
TACE将高浓度的化疗药物灌注至靶血管,杀灭瘤细胞并栓塞肿瘤供血动脉,从而达到控制肿瘤进展的目的,已成为中晚期肝癌患者的重要治疗方法[13-14]。TACE常用化疗药物主要为氟尿嘧啶、铂类及阿霉素类等。作为一种抗代谢类叶酸,雷替曲塞在晚期结直肠癌及肝转移中的疗效已得到证实[15],已有研究[9]将其用于代替氟尿嘧啶进行TACE来治疗中晚期肝癌。

表1 纳入文献的基本特征及质量评价
注:*:中位数;—:未获取数据
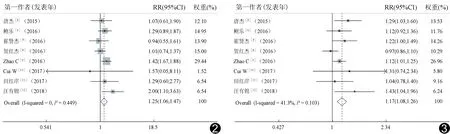
图2 雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌ORR比较森林图 图3 雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌DCR比较森林图

图4 雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌OS比较森林图 图5 雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌术后恶心、呕吐发生率比较森林图

图6 雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌术后发热发生率比较森林图 图7 雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌术后肝区疼痛发生率比较森林图
本研究Meta分析显示,雷替曲塞TACE治疗中晚期肝癌的ORR及DCR均高于氟尿嘧啶。雷替曲塞是一种新型细胞毒性药物,为水溶性胸苷酸合成酶(thymidylate synthetase, TS)特异性选择抑制剂,TS是胸腺嘧啶脱氧核苷三磷酸盐(thymidine three phosphate, TTP)合成过程的关键酶,TTP又是DNA合成的必需核苷酸[16],抑制TS活性可诱发细胞DNA断裂,加速细胞凋亡;通过细胞膜还原型叶酸/氨甲蝶呤载体可被细胞主动摄取,在叶酸多聚谷氨酸合成酶作用下迅速代谢为一系列多聚谷氨酰化合物,作用于TS靶点叶酸结合部位,特异性地抑制TS活性并发挥抗肿瘤作用,且可长时间潴留在细胞内,从而更有效地抑制细胞DNA合成,发挥长期毒性作用[17]。氟尿嘧啶为非特异性TS抑制剂,与雷替曲塞的酶结合位点不同,且其半衰期仅15 min,而雷替曲塞的半衰期长达198 h[18];此外,雷替曲塞具有更高的浓度依赖性,使其在TACE局部动脉灌注给药时能更充分地发挥疗效[19]。本研究中雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌患者OS差异无统计学意义,可能与部分纳入研究的随访时间偏短有关。

图8 雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌术后白细胞减少发生率比较森林图 图9 雷替曲塞与氟尿嘧啶TACE治疗中晚期肝癌术后转氨酶升高发生率比较森林图
TACE将化疗药物直接灌注至肿瘤供血动脉后,药物主要分布于病灶局部,全身其他脏器药物浓度相对较低,可在提高疗效的同时降低化疗药物引起的不良反应[20]。雷替曲塞与氟尿嘧啶TACE治疗后的不良反应主要为恶心、呕吐、发热、肝区疼痛、骨髓抑制等,且多为Ⅰ、Ⅱ级不良反应,经积极对症处理后患者均可耐受。本研究Meta分析显示,2种药物用于TACE在不良反应方面差异无统计学意义,提示雷替曲塞TACE治疗中晚期肝癌并未提高术后不良反应风险,安全性符合临床需要。刘孟兴[21]观察经雷替曲塞或氟尿嘧啶治疗的60例晚期结直肠癌患者的不良反应,发现雷替曲塞的神经毒性低于氟尿嘧啶。Kelly等[22]也认为雷替曲塞无明显心脏毒性,可作为氟尿嘧啶耐药及心功能不全的癌症患者的替代药物。
本研究的不足:①仅纳入中文及英文文献,有潜在语种偏倚;②纳入文献数量较少,且各研究中病例入选标准、药物所用剂量有所不同;③无进展生存期(progress free survival, PFS)也是评价TACE疗效的重要指标,本研究部分纳入文献中未提及患者PFS的风险比(hazard ratio, HR)及其95%CI,无法提取合并相关数据。
