单药白蛋白结合型紫杉醇治疗晚期非小细胞肺癌的疗效及安全性分析△
2018-11-15顾燕兰孙钢浦明之
顾燕兰,孙钢,浦明之
苏州市中医医院呼吸科,江苏 苏州2150090
恶性肿瘤是对人类生存、健康和社会发展影响较大的严重疾病,其中肺癌在目前各种肿瘤疾病中的发病率和病死率均居第1位,而非小细胞肺癌(non-small cell lung cancer,NSCLC)则在肺癌中最为常见,占肺癌总发病率的80%以上,多为60岁以上老年患者,确诊时多已为局部晚期并出现远处转移[1]。全身化疗和分子靶向治疗为晚期NSCLC的主要治疗方案,但靶向治疗费用较高,仅部分患者可以接受,因此化疗仍为晚期NSCLC的重要治疗方案[2]。紫杉醇类药物为恶性肿瘤治疗的常用化疗药物,其中白蛋白结合型紫杉醇(nanoparticle albumin-bound paclitaxel,nab-PC)是半合成紫杉醇类特殊靶向制剂,以人血清白蛋白为辅料,均匀、稳定地分散和运载主体紫杉醇,在一定程度上弥补了以往常用化疗药物的不足,其在肝癌、乳腺癌、卵巢癌等实体肿瘤的治疗中均有较好的疗效和安全性[3-4]。随着中国人口老龄化的加剧和人们对生活质量要求的提高,晚期NSCLC化疗方案的疗效和安全性成为人们关注的重点。本研究对52例NSCLC患者进行nab-PC化疗,分析其临床疗效和安全性,现报道如下。
1 对象与方法
1.1 研究对象
选择2014年2月至2016年2月苏州市中医医院收治的52例NSCLC患者。纳入标准:①均经组织病理学或细胞学检查确诊为NSCLC,并有可测量病灶;②TNM分期为Ⅲb~Ⅳ期,无法进行手术干预治疗;③治疗前卡氏功能状态(Karnofsky performance status,KPS)评分>50分;④既往无其他免疫治疗及化疗禁忌证;⑤血常规、心、肝、肾功能及凝血功能基本正常;⑥预计生存期>6个月。排除标准:①合并颅内转移者;②具有精神疾病病史者;③伴有其他类型肿瘤者;④依从性差、不能配合治疗者,或耐受性差、治疗过程中发生严重不良反应者。52例NSCLC患者中,男36例,女16例;年龄60~81岁,中位年龄71岁,≥70岁18例,<70岁34例;吸烟34例,不吸烟18例;合并症:主要为高血压、糖尿病、冠心病、脑梗死等,单一合并症40例,多种合并症12例,化疗前均已用药将合并症控制在稳定状态;TNM分期:Ⅲb期8例,Ⅳ期44例;病理分型:鳞癌24例,非鳞癌28例;美国东部肿瘤协作组(Eastern Cooperative Oncology Group,ECOG)评分:0分47例,1分5例;化疗线数:3线及以上40例,3线以下12例;既往有紫杉醇类药物化疗史38例,既往无紫杉醇类药物化疗史14例。所有患者均对本研究的治疗方法、治疗过程及可能出现的不良反应知情,且均签署知情同意书。本研究经过苏州市中医医院伦理委员会批准通过。
1.2 治疗方法
治疗第1、8天给予患者130 mg/m2nab-PC,于100 ml生理盐水中稀释后静脉滴注,滴注时间为30 min,21天为1个治疗周期,最少治疗2个周期,计划治疗6个周期。
1.3 观察指标
1.3.1 近期疗效 治疗前和治疗结束后对患者进行CT检查,采用实体瘤疗效评价标准(response evaluation criteria in solid tumours,RECⅠST)1.1版[5]进行疗效评估:完全缓解(complete response,CR),全部靶病灶消失,且无新病灶出现;部分缓解(partial response,PR),靶病灶最长径总和减少≥30%,至少维持4周;疾病稳定(stable disease,SD),介于PR和疾病进展(progressive disease,PD)之间;PD,靶病灶最长径总和增加≥20%,或出现新病灶。客观缓解率(objective response rate,ORR)=(CR+PR)例数/总例数×100%,疾病控制率(disease control rate,DCR)=(CR+PR+SD)例数/总例数×100%。
1.3.2 远期疗效 对患者进行电话随访或门诊随访,随访截至2016年8月1日。观察患者的无进展生存时间(progression-free survival,PFS)和总生存时间(overall survival,OS)。PFS为治疗开始至PD或患者死亡的时间,OS为治疗开始至患者死亡或随访截止时间。
1.3.3 不良反应情况 采用世界卫生组织(World Health Organization,WHO)化疗药物不良反应评价标准[6]将不良反应分为1~4级,等级越高说明不良反应越严重。
1.4 统计学分析
采用SPSS 18.0软件对数据进行统计分析。计数资料以例数和率(%)表示,组间比较采用χ2检验或Fisher确切概率法;计量资料以中位数表示,组间比较采用秩和检验。以P<0.05为差异有统计学意义。
2 结果
2.1 近期疗效与NSCLC患者临床特征的关系
52例NSCLC患者完成2~6个周期的化疗,平均4.3个周期,其中12例PR患者,26例SD患者,14例PD患者,无CR患者,ORR和DCR分别为23.08%(12/52)和 73.08%(38/52)。不同性别、年龄、吸烟情况、合并症情况、临床分期、病理分型、ECOG评分、放疗线数、紫杉醇类药物化疗史的NSCLC患者的ORR和DCR比较,差异均无统计学意义(P>0.05)(表1)。
2.2 不良反应情况
NSCLC患者化疗后的不良反应多为1~2级(表2),出现3级及以上不良反应后暂停或减量用药,应用粒细胞集落刺激因子(granulocyte colony stimulating factor,GCSF)、地塞米松等药物对症治疗后均好转。≥70岁的NSCLC患者3级及以上脱发和中性粒细胞减少的发生率均高于<70岁的患者,差异均有统计学意义(χ2=4.867,P=0.027;χ2=7.251,P=0.007);≥70岁的NSCLC患者3级及以上血红蛋白减少、恶心呕吐、乏力和肝肾功能异常的发生率均高于<70岁的患者,但差异均无统计学意义(P>0.05)。多种合并症的NSCLC患者3级及以上脱发、中性粒细胞减少、血红蛋白减少和恶心呕吐的发生率均高于单一合并症的患者,差异均有统计学意义(χ2=6.861,P=0.010;χ2=7.078,P=0.008;χ2=4.543,P=0.031;χ2=4.543,P=0.031);多种合并症的NSCLC患者3级及以上乏力和肝肾功能异常的发生率比较,差异均无统计学意义(P>0.05)(表3)。
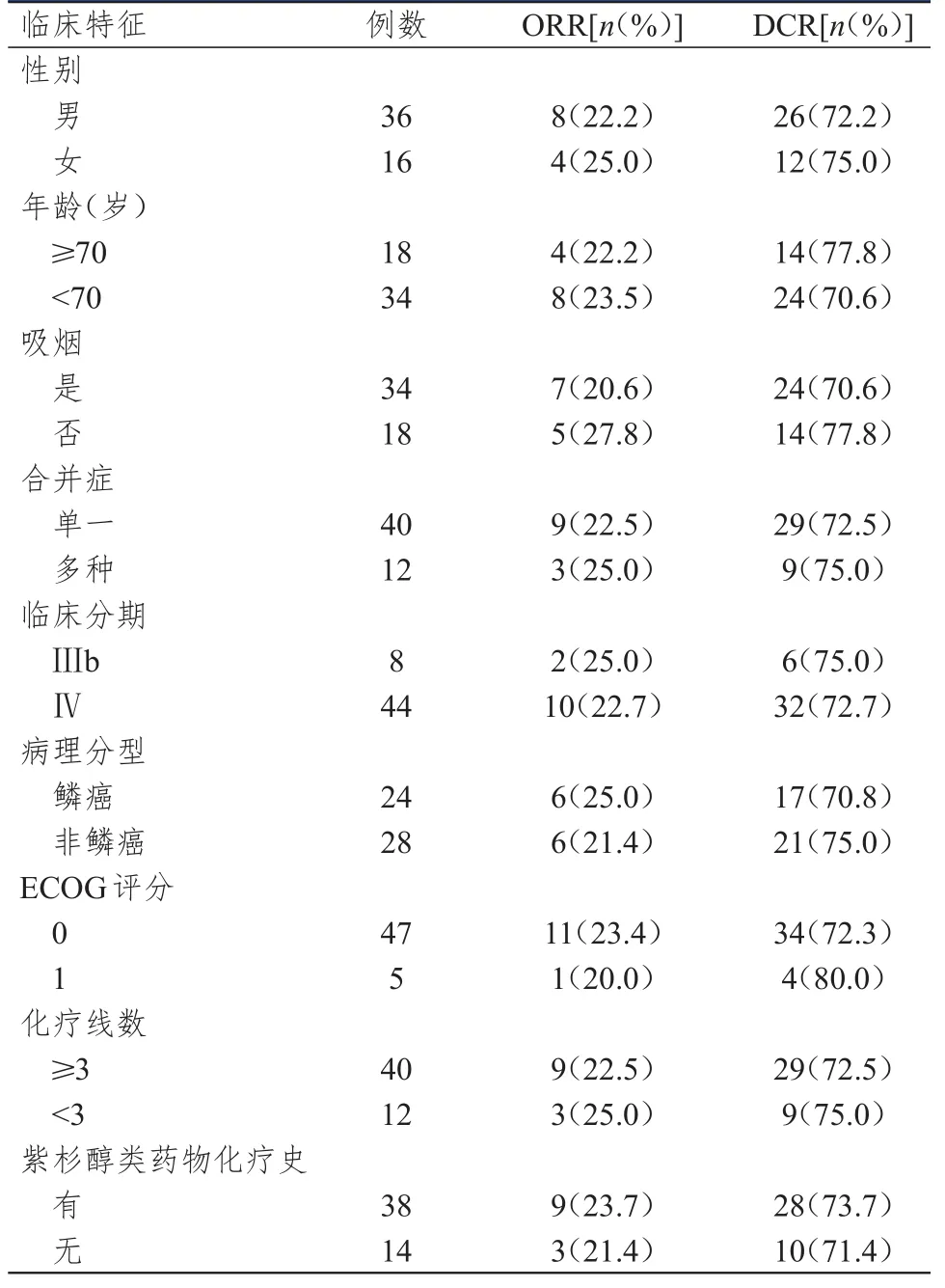
表1 不同临床特征NSCLC患者的近期疗效( n=52)
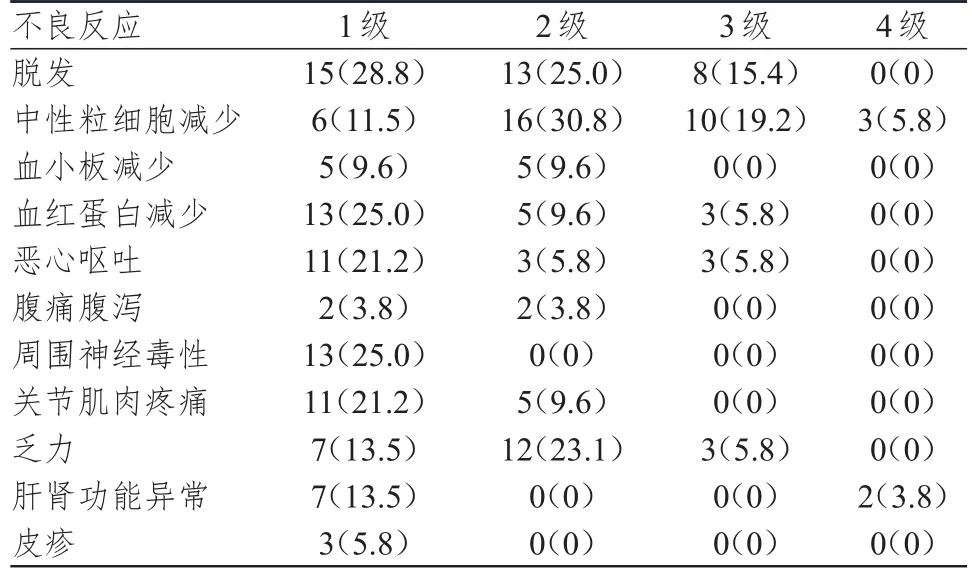
表2 52例NSCLC患者的不良反应发生情况[ n(%)]
2.3 NSCLC患者的远期疗效
52例NSCLC患者随访3.4~22.5个月,中位随访时间为7.2个月,其中22例患者生存,30例患者死亡。患者的中位PFS为4.1个月(95%CⅠ:2.4~5.8个月),中位 OS为 11.3个月(95%CⅠ:5.4~17.2个月)。鳞癌患者的中位PFS和中位OS分别为4.8个月和12.6个月,均长于非鳞癌患者的3.7个月和10.5个月,差异均有统计学意义(P<0.05)。
2.4 典型病例
72岁男性患者,吸烟,合并高血压,2014年5月因胸闷、胸痛入院确诊为非鳞癌,并开始骨转移,接受吉西他滨联合卡铂方案治疗2个周期后病情进展,于同年11月行单药nab-PC治疗,2个周期化疗后行CT复查,目标病灶明显缩小,疗效评价为PR。共化疗4个周期,对患者进行随访,其PFS达到5.8个月,不良反应等级较低,为1~2级中性粒细胞减少和恶心呕吐,整体疗效评价良好。
3 讨论
目前有关NSCLC治疗的研究已经取得了很大的进步,但包括NSCLC在内的肺癌的病死率在全球恶性肿瘤中仍居首位[7]。NSCLC的治疗已进入分子靶向治疗的个体化阶段,但临床应用中只有部分患者可受益,存在一定的局限性,多数NSCLC患者在确诊时已为中晚期,错过了手术治疗的最佳时机,全身化疗仍是其主要治疗方案。NSCLC患者多年龄偏高,常伴有多种合并症,身体状况堪忧,因此尽量延长患者的生存时间、减少化疗不良反应、改善患者的耐受性是晚期NSCLC化疗的目标和关注点[8]。
nab-PC是近些年常用的化疗药物——紫杉醇优化改进的产物,是采用先进的纳米技术以人血清白蛋白为载体结合紫杉醇主体制成的平均粒径为130 nm的微粒系统。其通过减小紫杉醇粒径,解决了原紫杉醇化疗用药需辅用聚氧乙烯蓖麻油助溶的问题,也避免了助溶剂在体内降解引发的一系列不良反应。肿瘤在生长过程中会分泌富含半胱氨酸的酸性分泌蛋白(secreted protein acidic and rich in cysteine,SPARC),其功能与白蛋白受体相似,对白蛋白产生吸引和黏附作用。因此,nab-PC能够迅速到达肿瘤微环境,聚集于肿瘤细胞,提高肿瘤内的药物浓度。近年来,nab-PC在肝癌、乳腺癌等实体瘤的临床研究中均证实其化疗效果较好,美国食品药品监督管理局已于2012年批准nab-PC应用于晚期NSCLC的治疗[9]。鉴于此,本研究将nab-PC纳入晚期NSCLC的多线临床治疗中,旨在进一步证实nab-PC治疗晚期NSCLC的疗效和安全性。
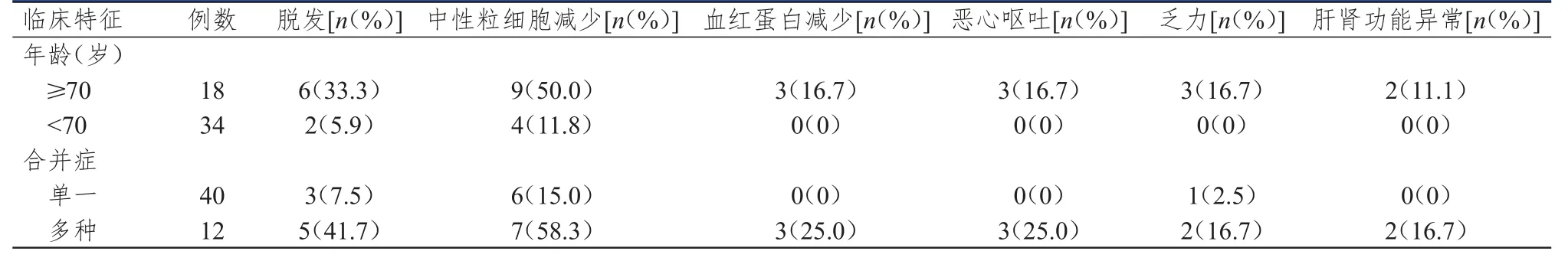
表3 不同年龄、合并症情况的NSCLC患者的 3级及以上不良反应发生情况( n=52)
Socinski等[10]于2012年进行了一项关于1线治疗NSCLC的多中心、随机Ⅲ期临床试验,结果表明,接受nab-PC联合卡铂治疗患者的ORR明显高于接受溶剂型紫杉醇联合卡铂治疗的患者。朱方等[11]对晚期NSCLC患者行2线及以上nab-PC联合铂类方案治疗,结果显示患者的ORR和DCR分别为21.95%和73.17%。本研究中,对晚期NSCLC多线行单药nab-PC治疗,患者的ORR和DCR分别为23.08%和73.08%,与朱方等[11]的研究结果基本一致。本研究结果显示,不同性别、年龄、吸烟情况、合并症情况、临床分期、病理分型、ECOG评分、放疗线数、紫杉醇类药物化疗史的NSCLC患者的ORR和DCR比较,差异均无统计学意义(P>0.05)。说明单药nab-PC治疗晚期NSCLC的适用性广,且近期疗效确切。培美曲塞和多西他赛为晚期NSCLC的2线化疗传统用药,两者联合治疗后患者的中位PFS为2.9个月[12]。二线治疗NSCLC的两项Ⅲ期临床试验结果显示,75 mg/m2多西他赛治疗后患者的中位OS分别是7.2个月和5.7个月[13-14]。本研究中,NSCLC患者多为60岁及以上的高龄患者,且为多线治疗,52例患者的中位PFS为4.1个月,中位OS为11.3个月,优于上述2项研究的结果。本研究结果还显示,鳞癌患者的中位PFS和中位OS均长于非鳞癌患者(P<0.05)。说明单药nab-PC治疗可延长晚期NSCLC患者的生存时间,且对鳞癌更有益,但其具体机制还有待于进一步研究。
本研究对nab-PC化疗的安全性分析主要包括化疗的不良反应和患者耐受性。52例NSCLC患者的不良反应主要为脱发、中性粒细胞减少、乏力、血红蛋白减少、恶心呕吐、关节肌肉疼痛、周围神经毒性、血小板减少和肝肾功能异常,经统计上述不良反应多为1~2级,结果优于以往传统溶剂型紫杉醇应用的不良反应情况[15]。出现3级及以上不良反应后暂停或减量用药,应用GCSF和地塞米松等药物对症治疗后均好转,患者对不良反应均可耐受,未出现放弃治疗或严重不适症状。本研究结果表明,≥70岁的NSCLC患者3级及以上脱发和中性粒细胞减少的发生率均高于<70岁的患者,多种合并症的NSCLC患者3级及以上脱发、中性粒细胞减少、血红蛋白减少和恶心呕吐的发生率均高于单一合并症的患者,差异均有统计学意义(P<0.05)。分析可能原因:①nab-PC有制作工艺上的改进,紫杉醇分布更均匀,单体有效成分增多,在相同用药量的情况下较传统溶剂型紫杉醇可增加疗效,减少不良反应;②nab-PC无须辅用助溶剂,避免了聚氧乙烯蓖麻油在体内降解引发的过敏反应和加重紫杉醇的周围神经毒性;③结合白蛋白,可以快速直达肿瘤微环境,加快紫杉醇离开血液循环,减少血液学不良反应和对正常细胞的损伤;④≥70岁和多种合并症患者可能由于年龄偏高,综合身体素质差,化疗药物易诱发各种合并症的不稳定或加重,因而出现3级及以上不良反应较多。
对于≥70岁和多种合并症的NSCLC患者在化疗中不良反应较重和耐受性较差的情况,笔者结合临床经验认为在化疗前应做好以下预防工作:①静脉滴注采用中心静脉置管,避免长期注射带来的身体痛苦,预防外周静脉炎;②给予患者地塞米松、昂丹司琼、GCSF,预防化疗过程中可能出现的过敏、呕吐、骨髓抑制等不良反应;③严格做好每周的血液检查和周期化疗前的肝肾功能及心电图检查,严密监测患者的身体情况,预防合并症复发或加重及化疗中可能出现的突发事件。
综上所述,单药nab-PC治疗晚期NSCLC的适用性广,疗效确切,不良反应较轻,患者均可耐受,对于≥70岁和多种合并症的NSCLC患者,应做好治疗前的预防工作。
