乳腺癌治疗相关事项
2018-11-14沈雷编辑青鸟
文/沈雷 编辑/青鸟
乳腺癌患者5年生存率目前通过规范化的治疗可达70%一80%。不同的病理检查报告针对乳腺癌患者有不同的治疗方式。除行之有效的手术治疗外,尚需要化疗、放疗、内分泌激素治疗及分子靶向治疗。当然,还需要坚强、乐观的心态。依据不同的情况进行个体化治疗,若化疗需术后尽早实施。
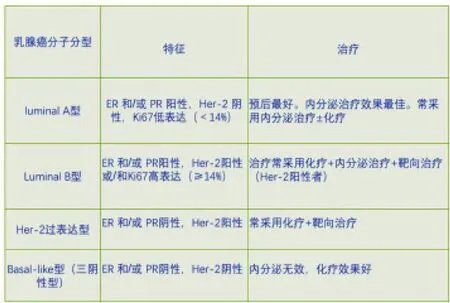
乳腺癌的筛查
乳腺癌在中国一线城市里的发病率早已超过了宫颈癌。乳腺癌通过体检或者自我发现(触及肿块、发现酒窝征)的越来越多,也引起健康人群的警惕。在过去,“君之疾在腠理,不治将恐深,而在骨髓,司命之所属,无奈何也。今在骨髓,臣是以无请也”。目前,即便“疾”在脊髓、在肺腑,通过多学科团队齐抓共管也能大有作为。
超声和钼靶X线检查对于乳腺癌是最常规的检查手段,临床中绝大多数乳腺癌患者都是通过超声和钼靶X线检查发现可疑肿块,从而进行手术治疗。
乳腺隐匿性钙化是乳腺隐匿性病变的一种,即常规钼靶X线检查显示乳腺内成簇钙化灶,而临床症状体征阴性的乳腺隐匿性病变。在临床实践中细小的、颗粒状的成簇的微钙化点是乳腺癌的一个重要的早期表现。部分患者无任何症状,甚至超声检查也未发现乳腺肿块,仅仅乳腺钼靶X线检查发现簇状钙化灶。乳腺钼靶X线检查可提高对于乳腺隐匿癌、早期癌的诊断率,根据微小钙化形态、大小、数量和密集度等表现可反映病变性质和范围。微小钙化点可位于肿块内或周围,一平方厘米内总数目6~15枚以上者高度怀疑,尤其是出现密度不均、大小不等状况。细沙型钙化常是恶性病变的警报;若同时出现周围结构紊乱、双乳腺体不对称、血管影增粗等征象则恶性病变可能性更大。乳腺癌发现的“朝与夕”决定了手术治疗的“毁损程度”,从乳腺切除带来生理和心理上的巨大创伤到保留乳房手术获得的自信完好,都取决于个体化病情。癌症早发现早治疗绝不是一句空话。
有些患者可以在术前或术中注射显影剂或带有放射信号的示踪剂,寻找前哨淋巴结行冰冻病理明确有无转移。前哨淋巴结指的是最先接受癌肿引流的淋巴结,可以是多个。若冰冻病理阴性,则可避免行腋窝淋巴结清扫术,从而避免了诸多不利影响。
乳腺癌的手术治疗
乳腺癌的手术治疗,有乳腺癌扩大根治术、标准根治术、改良根治术、保乳手术。通过对于乳腺癌越来越深入的了解,治疗手段从单一的手术治疗演变为综合治疗。手术范围上从做“加法”到现在尽可能做“减法”,目的只有一个:为乳腺癌患者带来更好的受益。
国内较多的乳腺癌改良根治术常将包括乳头、一部分皮肤、整个乳腺及腋窝淋巴结切除。患者术后需要肩关节制动,保持内收不外展;1周后耸肩活动肩关节、2周后患肢外展行功能锻炼。为防止术后因活动少、皮肤疤痕牵扯所致的上肢抬举受限,患者应尽早活动患侧上肢。术后2一3月肩关节可外展90°,功能基本恢复。上肢功能锻炼不能操之过急,应循序渐,康复训练以患者自主功能锻炼为主。术后一段时间避免用患肢搬动提取重物,注意尽量不在患肢静脉输液。
虽然越来越多的乳腺癌女性可以行保留乳房的手术,但是仍有许多局部晚期的乳腺癌患者治疗时不得不行乳腺癌标准根治术。例如乳腺癌已经侵犯皮肤,表面溃疡糜烂出血,术前辅助化疗后仍然不得不行标准根治术(切除乳腺、胸大肌、胸小肌、腋窝淋巴结甚至到锁骨下淋巴结)。如果胸壁皮肤缺损,无法关闭切口,只能通过取皮刀获取大腿皮肤行刃厚皮片移植。从不能行走、癌肿播散、局部原发灶溃烂到能够行走自如、生活自理,需要依靠患者相当长的一段时间内配合数名医生进行数种不同的治疗方式。虽然最后能转危为安,但还是要向大众提倡早期疾病筛查。
乳腺癌术后的复查
术后应定期到医院复查,根据肿瘤分期、复发转移风险选择术后第1年内每季度复查1次或半年复查1次,术后5年内半年1次,5年以后至少每年1次,应按计划进行术后辅助治疗。术后注意休息,劳逸结合,适当锻炼,保持心情舒畅。
乳腺癌术后化疗与不良反应
乳腺癌是早期便可以血行转移的恶性肿瘤,可以看作是全身性的疾病。用目前的一些诊断方法尚难以检查出来是否体内存在微转移及其体内的循环肿瘤细胞。因此,原发癌虽然彻底切除,而分布于体内的微小转移癌仍将继续生长,最终造成不良后果。须采取局部治疗和全身化疗相结合的综合治疗方法才能全面控制乳腺癌的发展。
化疗是一种以抗癌药物来治疗恶性肿瘤的方法。这些药物在细胞生长增殖的不同环节上起作用,抑制或杀灭癌细胞。目前,在乳腺癌的治疗中,除了0 期和部分Ⅰ期的患者以外,几乎各期患者都需要进行化疗。手术后化疗的目的是为了减少远处播散,从而提高远期疗效。
目前,治疗乳腺癌疗效较好且常用的化疗药物有如下几种:环磷酰胺( CTX )、5-氟尿嘧啶(5-FU)及其衍生物、阿霉素(ADM)、表阿霉素、顺铂(DDP)、卡铂(CBP) 、长春瑞宾(NVB,诺维本、盖诺)、紫杉醇(TAXOL)和多烯紫杉醇等。其中蒽环类(阿霉素,表阿霉素)和紫杉类药物在乳腺癌化疗中更是主打。
乳腺癌患者化疗期间由于药物本身的药理作用、剂量和个人体质差异,都会产生很多不良反应。尤其以骨髓抑制、恶心呕吐、肝功能损害、心脏毒性等为主要不良反应。
1.骨髓抑制是化疗常见的非特异性毒性,也是影响化疗过程及剂量的关键因素。也就是引起白细胞降低、血小板减少甚至贫血,严重者可出现发热性中性粒细胞缺乏症。大多联合化疗在用药后1一2周出现白细胞数下降,3一4周恢复正常。可根据药物的选择和剂量,评估发生的风险分级,预防性使用集落细胞刺激因子。
2.胃肠道的反应、恶心呕吐,这也是让患者难以坚持或者不愿意完成化疗的重要原因。强烈的恶心和呕吐可导致电解质紊乱、代谢性碱中毒,这些反应让患者难受,而且不能进食。化疗期间予以止吐药物,保证化疗的实施。饮食清淡,易消化,忌油腻和刺激类食物。有的患者可以引起腹泻,稀水样便,注意对症支持治疗。
3.口腔黏膜疾病,化疗可以引起一些口腔黏膜的炎症,有些出现溃疡。需要注意饮食避免辛辣,适量补充B族维生素及对症治疗。
4.化疗后脱发使一些年轻女性对化疗产生抵触情绪。这种脱发根据选择的药物不同,发生率也不同。即使脱发了也不是永久性的脱发,在化疗结束以后大多数患者还可以“重头”来过。
5.肝脏和肾脏功能的损害,根据不同的药物,损害程度是不一样的,可以出现转氨酶升高、黄疸,严重的时候还可以产生急性肾功能的衰竭。化疗前应检查肝肾功能,一般轻度的损害不影响后续化疗,化疗结束后一般肝肾功能可逐渐恢复正常。
6.心脏的毒性,主要来源于蒽环类药物。该类药物对心脏的毒性呈现进展性和不可逆性,患者可以出现心慌、胸闷,甚至心率失常、心肌缺血的改变。需要检测化疗期间心功能,严重时需要减量或停药。化疗时可以使用辅助药物预防心肌毒性。
7.过敏反应,这是由药物带来的乳腺癌化疗后的不良反应,分为急速的超过敏反应和慢性的过敏反应。超过敏反应多见于紫杉类药物,应严格按照医生提供的抗过敏预处理方案进行。
8.化疗的时候,如果药物外渗,会引起皮肤、皮下组织的一些坏死。化学药物刺激静脉,会引起静脉炎,甚至静脉血栓。所以目前多推荐建立深静脉通路来进行化疗,如经外周静脉置入中心静脉导管(peripherally inserted central catheter,PICC)、输液港装置、锁骨下插管等。
PICC经上肢贵要静脉、肘正中静脉、头静脉、肱静脉、颈外静脉穿刺置管,尖端位于上腔静脉或下腔静脉的导管。
9.对末梢神经的损害,多见于紫杉类、长春碱类药物。化疗以后患者感觉到手脚发木、发麻,可以通过补充维生素来缓解症状。对于皮肤还可出现皮肤干燥,色素沉着、皮疹、伴有瘙痒,可以对症治疗。
10.免疫功能下降,强烈的化疗可以导致免疫功能下降,对T淋巴细胞功能的影响时间较长,容易导致感染和带状疱疹。注意适当健体,及饮食上各营养要素的补充。
化疗药物的使用目标一定是利大于弊,权衡患者综合情况。除了极早期激素受体阳性的乳腺癌患者和高龄多器官疾病的乳腺癌患者,其他大多数患者还是要考虑要进行化疗。
乳腺癌术后放疗与不良反应
放疗作为乳腺癌综合治疗的主要组成部分,是局部治疗手段之一。放射治疗包括根治术之前、术后作为辅助治疗、晚期乳腺癌的姑息性治疗。乳腺癌术后需要行辅助放疗的情况:单纯乳房切除术后或保乳术后;根治术后病理报告有腋中群或腋上群淋巴结转移者;根治术后病理证实转移性淋巴结占检查的淋巴结总数一半以上或有4个以上淋巴结转移者;病理证实乳内淋巴结转移的病例。根据每位乳腺癌患者的癌肿所在乳腺的具体位置、淋巴结的转移情况需要制定相对个体化的放疗方案,选择术后照射的范围:内乳区、锁骨上下区、腋窝区和胸壁。
放疗的常见不良反应包括皮肤反应和皮下组织纤维化、乳房纤维化、放射性肺炎、放射性血管损伤等。
乳腺癌术后的内分泌治疗
内分泌治疗指通过药物或内分泌腺体的切除去除激素对肿瘤细胞的刺激,起到抗肿瘤作用的治疗方法。
早在一百多年前就有学者提出内分泌系统与乳腺癌之间存在着密切的联系。六十多年前,哈金斯等提出将肾上腺切除术(肾上腺分泌的诸多激素中包括了雌二醇)作为乳腺癌的二线内分泌疗法。虽然当时原理知之甚少,但临床的大量数据告诉我们这个疗法有着很好的疗效。目前,我们通过分子免疫病理检测出的激素受体敏感性的乳腺癌患者,其体内雌、雄激素比例高会刺激乳腺癌细胞的发生和进展。
对于绝经前的乳腺癌患者一线用药是雌激素拮抗剂他莫昔芬。
对于绝经后妇女,卵巢产生的雌激素随年龄增加而减少,循环血液中的低水平雌激素是靠外周组织(包括皮肤、脂肪组织、乳腺组织、肝脏、恶性肿瘤组织)对雄激素进行芳香化作用而产生的。所以对于绝经后妇女,针对雌激素合成最后一步的催化酶,使用芳香化酶抑制剂治疗。目前,临床最常用的是第三代芳香化酶抑制剂,如阿那曲唑、来曲唑和依西美坦。
对于晚期或复发转移风险高的激素受体阳性的乳腺癌患者,另有其他内分泌治疗方式,包括卵巢去势术(手术切除、放射治疗或药物治疗去除卵巢功能),促黄体生成素释放激素激动剂(例如戈舍瑞林,其作用可以停止产生促性腺激素来减少雌激素的释放)、孕激素类药物治疗等。需要结合患者情况选择性使用。
目前,循证医学证据支持乳腺癌术后内分泌治疗的时限是5一10年。内分泌治疗的长期性提示关注其不良反应的重要性。他莫昔芬的主要不良反应包括:闭经,阴道干燥,子宫内膜增厚诱发子宫内膜癌,食欲缺乏,皮肤潮红,肝功能异常等。芳香化酶抑制剂的不良反应包括:骨量丢失致骨质疏松,关节肌肉疼痛,疲劳,偶有呼吸困难,恶心口干,胃肠道症状,阴道干燥流血,头晕失眠,瘙痒皮疹等。
对于绝经前女性服药期间定期复查应注意妇科超声随访,注意子宫内膜增厚变化,必要时可以子宫内膜活检。绝经后女性要常规摄入钙剂和维生素D,增加体育锻炼。骨关节肌肉疼痛症状者,部分患者随着用药时间延长症状会减轻,但要排除骨转移、关节炎等引起的疼痛,轻者补充钙剂和适当体育锻炼,明显疼痛者可服用非甾体类抗炎药,或换一类芳香化酶抑制剂试试。
乳腺癌的靶向治疗
乳腺癌靶向治疗本质上属于一种生物治疗,是指药物进入体内会特异地选择分子水平上的致癌位点结合发生作用,使肿瘤细胞特异性死亡,而不会波及肿瘤周围的正常组织细胞。作为精准的生物导弹一般只对肿瘤有抑制作用,而对正常组织的不良反应较小,其特点是高效、低毒,是一种理想的肿瘤治疗手段。
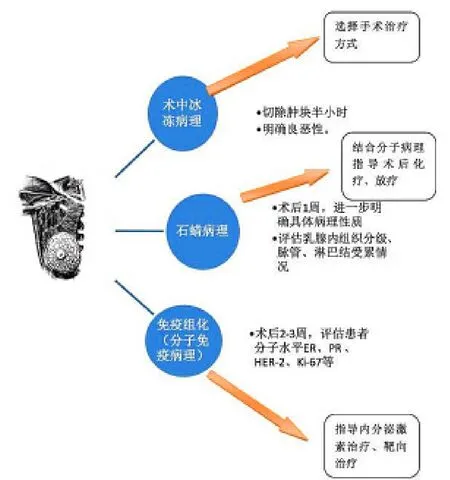
HER-2(也称neu 或者c-erbB-2)是表皮生长因子酪氨酸激酶受体家族的原癌基因,大约20% 的乳腺癌患者中人类表皮生长因子受体2(HER-2)过度表达。乳腺癌患者存在HER-2 扩增和蛋白过度表达,与无HER-2 过度表达比较,伴有HER-2 扩增和蛋白过度表达的患者其肿瘤更易复发和转移,预后更差。乳腺癌靶向治疗药物有两类:一类是单克隆抗体类药物,一类是小分子激酶抑制剂。现在应用较多的是单克隆抗体类药物曲妥珠单抗,商品名叫赫赛汀,以癌细胞表面的HER-2的分子为“靶点”,通过阻断HER-2分子这个环节,抑制并杀死肿瘤细胞。
目前,用于检测HER-2的主要方法有免疫组织化学法(IHC)和荧光免疫杂交法(FISH),两者各有优缺点。IHC用特异的抗体检测HER-2蛋白,而FISH检测的是HER-2基因的扩增。IHC检测简便、普及、价格便宜,但是结果受标本、试剂、技术的影响较大,有时容易出现假性的结果。FISH复杂、昂贵、很多医院无法开展,但是结果更准确、客观。一般情况下,所有乳腺癌的标本均进行IHC检测HER-2,结果分为-、+、++、+++等几种情况:-和+通常定义为HER-2阴性;+++定义为HER-2阳性(过表达);而对于++,HER-2可能为阴性,也可能为阳性,需要用FISH法进一步核实。
多项大型国际研究均证实,HER-2阳性乳腺癌患者应用靶向治疗后,可明显降低复发转移的风险,延长生存时间。目前,临床上针对HER-2的靶向药物有曲妥珠单抗(赫赛汀)、拉帕替尼和帕妥珠单抗。HER-2阳性的早期乳腺癌患者应用曲妥珠单抗辅助治疗一年,相对复发风险下降约50%,死亡风险下降约30%。曲妥珠单抗的不良反应主要是心脏毒性导致心功能不全。
目前,乳腺癌新的靶向药物研发和临床试验也在如火如荼的进行中,以后患者将会有更多的选择方案。
乳腺癌的免疫治疗
另外,乳腺癌免疫治疗作为目前“革命性”的治疗也获得了全世界医学工作者的目光。
人体免疫系统具有识别和排除抗原性异物、维持机体生理平衡和稳定的作用,具有免疫防御、稳定和监视功能。通过正常的免疫监视功能,机体自身可以识别、发现并消灭体内出现的异常增生细胞,防止肿瘤发生。免疫治疗便是通过诱发或加强体内针对肿瘤细胞表面的肿瘤相关抗原的特异性免疫反应,调动宿主的免疫系统来识别并破坏癌细胞。
尽管乳腺癌并不是传统意义上的免疫原性恶性肿瘤,但是多项研究均揭示了瘤内免疫反应与肿瘤进展的密切关系,众多研究者已经清晰地认识到免疫系统在乳腺癌的进展中具有调控作用。
目前研究较多的是CTLA-4 和PD-1及其配体,临床研究结果也会相继公布,时间会给我们答案。
