原位肝移植患者无肝期Narcotrend指数与丙泊酚血药浓度的关系
2018-11-13秦学伟陈宣伶姚兰张斌
秦学伟,陈宣伶,姚兰,张斌
(1北京大学国际医院,北京102206;2解放军第309医院)
肝移植是终末期肝病患者惟一的治疗方法。肝移植的过程分为无肝前期、无肝期和新肝期,无肝前期为手术开始至下腔静脉、门静脉阻断,无肝期为下腔静脉、门静脉阻断至移植肝循环再通,新肝期为移植肝循环再通至手术结束。麻醉药物主要经过肝脏代谢[1],机体在无肝期处于没有肝脏的状态,麻醉药物的代谢会受到不同程度的影响。传统观念认为,无肝期应减少麻醉药物用量,从而防止麻醉药物蓄积。但在无肝期停止麻醉药物的使用是否影响全身麻醉深度,目前尚无定论[2]。Narcotrend(NT)是一种新型的麻醉深度监测仪器[3]。NT能将原始脑电进行自动分级,形成NT脑电分级。临床中常用NT指数(NTI)和麻醉深度级别(NTS)来代表麻醉深度。NTI以量化方式反应麻醉深度,使用0~100无量纲脑电图指数(100为清醒,0为最深麻醉深度)反映从清醒到麻醉深度的全过程。NTI与NTS有着明确的对应关系。NTS为从A~F的6个阶段,15个亚级,临床应用中NTS处于D2~E0水平代表最为理想的麻醉深度[4]。本研究通过观察肝移植患者无肝期NTI的变化,并监测丙泊酚血药浓度,分析NTI与丙泊酚血药浓度的关系,旨在评估肝移植无肝期是否要减少麻醉药物的使用。
1 资料与方法
1.1 临床资料 选择2010年10月~2011年8月在解放军第309医院行原位肝移植的患者31例,男24例、女7例,年龄(45±11)岁,体质量(63±9)kg,美国麻醉医师协会(ASA)分级Ⅰ~Ⅲ级。其中肝癌26例,肝硬化5例。排除标准:肝性脑病、有精神神经疾病、乙醇或麻醉药物依赖者、癫痫病史、脑电图异常。为避免对脑电的影响,患者均不用术前药。患者肝移植手术的无肝期时间为(75±12)min。本研究经医院伦理委员会批准,受试者均签署知情同意书。
1.2 麻醉与NTI、丙泊酚血药浓度检测方法 所有麻醉由同一高年资麻醉主治医师实施。患者入手术室后开放上肢静脉通道,监测心电图、心率、血氧饱和度、有创动脉压。在患者前额部位放置3个NT专用电极,连接NT麻醉深度监测仪,采用单通道,以数据稳定2 min后NTI的数值作为入室基础值。麻醉诱导采用静脉注射咪达唑仑0.1~0.2 mg/kg、丙泊酚1~2 mg/kg、芬太尼3~5 μg/kg、维库溴铵0.1~0.15 mg/kg。麻醉诱导后气管插管并行机械通气,二氧化碳分压(PaCO2)维持在35~45 mmHg。行右颈内静脉穿刺,留置双腔中心静脉导管及鞘管并置入Swan-Ganz导管,连接Vigilance连续心排监护仪,监测心排量(CO)、心脏指数(CI)、血温、混合静脉血氧饱和度(SVO2)等血流动力学指标。术中麻醉深度维持采用丙泊酚2~4 mg/(kg·h)持续中心静脉侧管泵注,每间隔1 h给予芬太尼3 μg/kg和维库溴铵0.1 mg/kg直至无肝期开始。术中NTS维持在D2~E0。下腔静脉、门静脉阻断后,立刻关闭中心静脉给药管路,记录无肝期即刻(T1)、15 min(T2)、30 min(T3)的NTI。30 min后以2~4 mg/(kg·h)丙泊酚静脉持续泵注,记录丙泊酚泵入后15 min(T4)、30 min(T5)的NTI,同时在各个时刻点取中心静脉主管血样,采血3 mL/次,采用高效液相色谱法测量丙泊酚的血药浓度。

2 结果
2.1 无肝期各时点NTI比较 T1~T5时点的NTI分别为39.06±4.18、51.12±3.93、59.48±3.35、49.06±3.95、39.03±2.84。与T1相比,T2、T3时点NTI均上升;与T3相比,T4、T5时点NTI均下降(P均<0.05)。
2.2 无肝期各时点丙泊酚血药浓度比较 T1~T5时点丙泊酚血药浓度分别为(5.08±0.50)、(3.78±0.33)、(2.85±0.27)、(3.95±0.14)、(5.15±0.38)μg/mL。与T1相比,T2、T3时点丙泊酚血药浓度均下降;与T3相比,T4、T5时点丙泊酚血药浓度均上升(P均<0.05)。
2.3 无肝期NTI与丙泊酚血药浓度的相关性 NTI与丙泊酚血药浓度呈负相关(r=-0.847,P<0.01),拟合优度R2=0.581。见图1。
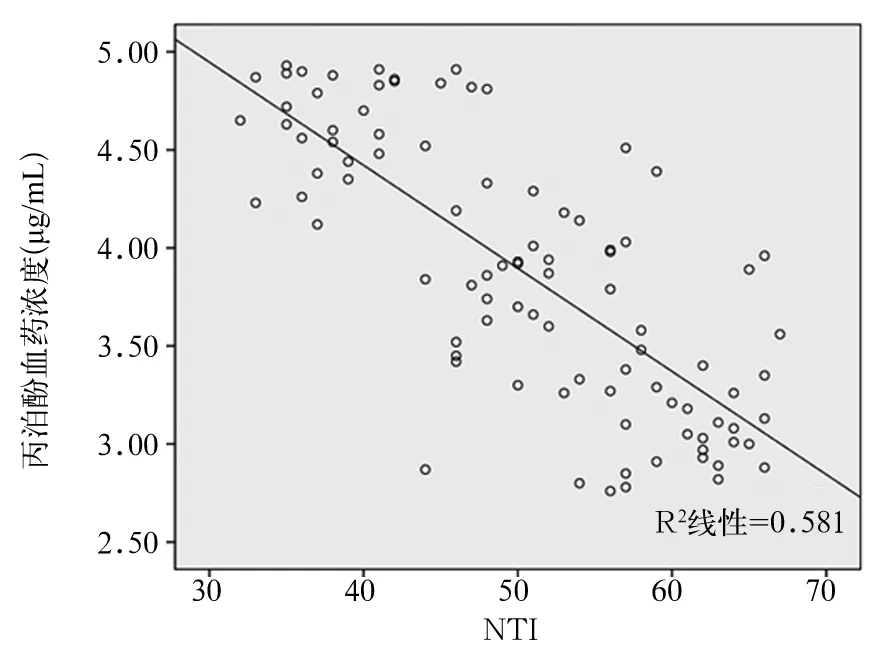
图1 无肝期NTI与丙泊酚血药浓度的相关性
3 讨论
目前临床常用的麻醉深度监测手段为BIS,而NT监测仪是一种新型脑电意识深度监测仪[3,5,6]。BIS和NTI有很强的相关性,均能准确反映麻醉诱导、麻醉维持、麻醉苏醒各阶段的麻醉深度变化,均优于根据体征判断麻醉深度[7~9]。与BIS相比较,NTI较具有波动小、数据处理迅速的特点[10],NT能更加及时地反映大脑生理功能的变化,费用也更低,被认为是目前已有的脑电图监测指标中最可靠的指标。本研究结果显示,NTI与丙泊酚血药浓度呈负相关,提示NTI能准确反映丙泊酚血药浓度的变化。
在肝移植术中,丙泊酚是目前维持麻醉最常用的静脉麻醉药。丙泊酚主要通过肝脏血流代谢。Servin等[11]报道,对肝功能正常与肝硬化患者静脉输注丙泊酚后,比较二者丙泊酚的总清除率,发现与肝功能正常的患者相比,肝硬化患者丙泊酚的总清除率并没有明显减少。表明肝功能障碍并没有改变丙泊酚的最终消除半衰期,因此认为丙泊酚可以在有明显肝病综合征的患者中安全使用。
肝移植术中的无肝期是门、下腔静脉被离断,病肝切除后的时期。此时肝脏对所有药物及其代谢产物的分解功能随之停止。因此在无肝期,维持麻醉深度所需的丙泊酚应停用或减量。本研究结果显示,在原位肝移植无肝期,停止泵入丙泊酚即刻至停止泵注30 min后,NTI由39.06±4.18上升至59.48±3.35;在停止泵入丙泊酚15 min和30 min时,丙泊酚血药浓度由(5.08±0.50)μg/mL下降至(2.85±0.27)μg/mL。表明在无肝期,肝脏停止代谢药物的情况下,丙泊酚血药浓度降低,脑电活动逐步增强,麻醉镇静深度逐渐减浅,说明丙泊酚存在肝外代谢。在开始泵注丙泊酚15 min以及30 min后,NTI由49.06±3.95下降至39.03±2.84,丙泊酚血药浓度由(3.95±0.14)μg/mL上升至(5.15±0.38)μg/mL。表明在肝移植无肝期期间仍需持续泵注丙泊酚维持一定的麻醉深度,以防止出现术中知晓的可能。
既往研究也提出丙泊酚存在肝外代谢。Takizawa等[12~14]指出,丙泊酚存在小肠、肺脏、肾脏代谢。丙泊酚在小肠和肾脏的代谢分别占全身代谢的10%~20%和18%~36%。Dawidowicz等[15]报道,肺组织含有与丙泊酚羟基化相关的P450酶以及葡萄糖醛酸化相关的UGT酶,使丙泊酚转化成2,6-二异丙基-1,4-对苯二酚的形式参与肺脏代谢。Kuipers等[16]报道,肺脏对丙泊酚的首过消除速率达到(1.14±0.23)L/min,约30%被肺脏代谢。朱益贫等[2]纳入5例同种异体原位肝移植患者(年龄9~13岁),分别于麻醉诱导及无肝期开始时静脉注射丙泊酚2 mg/kg,对比两者之间丙泊酚的药代动力学差异;结果显示,在无肝期丙泊酚的药代动力学未受到明显影响,且丙泊酚的清除率大于儿童肝血流量(1~1.3 L/min),也从另一角度说明丙泊酚存在肝外代谢。
综上所述,原位肝移植患者在无肝期脑电活动不断增强,麻醉深度逐步减浅,说明在此期间丙泊酚存在肝外代谢。为了维持适当的麻醉深度,我们建议在无肝期持续泵注丙泊酚。
