基于二氧化碳吸附脱附金属有机框架复合材料的制备
2018-11-12王燕何亮代玉王荣杰贾鑫
王燕,何亮,代玉,王荣杰,贾鑫*
(石河子大学化学化工学院/新疆兵团化工绿色过程重点实验室,新疆 石河子 832003)
据统计全球各种化石燃料(如煤、石油、天然气)燃烧排放到大气中的二氧化碳(CO2)在过去十年中以每年2.7%的速度增长,现在比“京都议定书”的参考年1990年的水平高出60%[1-3],而被利用的CO2不足0.5%,不仅造成了二氧化碳资源的浪费,而且加剧了全球变暖问题[4]。控制二氧化碳排放量,并对排放的二氧化碳回收[5-6]、固定[7-8]、利用及其资源化[9-10],已引起全球各国政府和学界的高度重视。
金属有机框架(MOFs)材料具有超高比表面积和巨大的孔容可实现各种气体的高容量储存,基于其孔径结构上的高度规整性、可调节性和表面基团的可调节性,可实现多种气体的高效分离,以及吸附容量及吸附动力学性能的改善[11],将MOFs材料应用于CO2储存领域具有非常诱人的应用前景。2008年Lillerud[12]小组制备了一个具有超高稳定性的 MOF,标记为 UiO-66,化学式为 Zr6O4(OH)4(CO2)12,骨架坍塌温度高于500℃,且其具有良好的抗水性、抗酸性,但在碱性环境下其结构会发生部分坍塌[13]。在 303 K和 1 bar下,UiO-66的CO2吸附量约为54 cm3g-1,与工业吸附剂(如沸石13X等),其吸附量仍需极大地提高[14]。因此人们在合成MOFs的过程中通过掺杂功能有机材料、引入混合配体或者直接用特定基团修饰MOFs,来制备功能多样化的MOFs材料。2010年Cohen[15]等首次制备了硝基、氨基、溴基、联苯功能化的UiO-66系列MOFs材料,同年,Kandiah等研究发现这些不同配体结构功能化的UiO-66复合材料也同样具有与UiO-66材料相似的高温热稳定性和化学稳定性,Cmarik等也发现了甲氧基和萘基功能基团同样具有稳定性结构。不同的配体制备的复合材料对CO2的吸附能力也不同,如UiO-66-NH2由于氨基的存在,相比UiO-66,CO2吸附量有所提高(在303 K和1 bar下,CO2吸附量约为 65 cm3/g)[15]。
设计MOFs用于在室温条件下吸附脱附CO2依旧充满挑战,这是因为在室温和低压(1 bar)条件下,MOFs材料自身脱附CO2的效率较低,一般需要引入额外大量能量。为了实现在室温条件下吸附脱附CO2,本文研究将PDA@Ag作为功能材料掺杂进金属有机框架(UiO-66)中制备复合材料(PDA@Ag/UiO-66),既减少了CO2脱附时的额外能量要求,又可实现CO2气体的循环利用。
1 材料与方法
1.1 试剂与仪器
1.1.1 试剂
多巴胺盐酸盐:98%,Sigma-Aldrich;硝酸银(AgNO3):分析纯,天津市赢达稀贵化学试剂厂;聚乙 烯 吡 咯 烷 酮 (PVP):99.0% ,Aladdin; 氯 化 锆(ZrCl4):98%,Adamas;1,4- 苯二甲酸(BDC):99%,Adamas;氢氧化钠(NaOH):分析纯,天津永晟精细化工有限公司;甲醇:分析纯,天津市富宇精细化工有限公司;丙酮:≥99.5%,Greagent;N,N- 二甲基甲酰胺(DMF):分析纯,天津市富宇精细化工有限公司;无水乙醇:分析纯,天津致远化学试剂有限公司。用水为超纯水和去离子水。
1.1.2 仪器
日立SU8010型扫描电子显微镜,日本日立公司;Bruker D8 ADVANCE型X射线衍射仪,德国布鲁克公司;麦克ASAP2020型气体吸附仪,美国麦克仪器公司;DZF-6020型真空干燥箱,上海博远医疗设备厂;KH3200B型超声波清洗仪,昆山禾创超声仪器有限公司;101-1AB型电热鼓风干燥箱,天津市泰斯特仪器有限公司;雷磁PHS 25型pH酸度计,上海仪表电气科学仪器有限公司雷磁仪器厂;KH-25 mL型水热釜,郑州英峪领科仪器设备有限公司。
1.2 实验方法
1.2.1 金属有机框架(UiO-66)的制备
UiO-66的合成采用溶剂热法。称取氯化锆(ZrCl4)116 mg于 25 mL反应釜中,加入 15 mL N,N-二甲基甲酰胺(DMF)溶液,再加入30%的乙酸2 mL,超声使其充分溶解;再将83 mg 1,4-苯二甲酸(BDC)加入上述溶液中继续溶解,在120℃烘箱中反应24 h;冷却后离心得到固体产物,用DMF离心洗3次;继续浸在DMF中80℃反应12 h,完全去除没有反应的配体。然后用甲醇溶剂交换3 d,在真空环境下120℃活化24 h。
1.2.2 复合材料(PDA@Ag/UiO-66)的制备
分别称取0.18 g的多巴胺盐酸盐和0.27 g的聚乙烯吡咯烷酮(PVP)于100 mL圆底烧瓶中,然后加入55 mL超纯水,超声溶解,待溶解完全后,用1 mol/L的氢氧化钠溶液和1 mol/L的盐酸溶液调节反应体系的pH值到11;向反应体系中加入一定体积的质量分数为3.5%的AgNO3溶液,使反应体系最终的体积为60 mL,同时以500 rpm转速磁力搅拌30 min;然后离心洗涤至上清液为无色,50℃下真空干燥即得到PDA@Ag。
分别称取 0.348 g的氯化锆,0.249 g的 1,4-苯二甲酸于100 mL的反应釜中,然后加入45 mL的N,N-二甲基甲酰胺(DMF)溶液,超声溶解后加入0.5 mmol前面制备的PDA@Ag,在120℃烘箱中反应24 h,冷却后离心,用DMF洗 3次,再用甲醇洗3次;最后在120℃真空干燥箱中烘24 h,得到白色固体粉末。通过控制加入PDA@Ag的量,如0.5 mmol,1.0 mmol,1.5 mmol和 2.0 mmol,而分别制备了 PDA@Ag/UiO-66-0.5;PDA@Ag/UiO-66-1.0;PDA@Ag/UiO-66-1.5和 PDA@Ag/UiO-66-2.0。
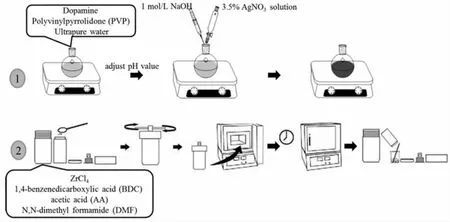
图1 复合材料PDA@Ag/UiO-66的制备Fig.1 Schematic preparation of PDA@Ag/UiO-66 composite material
1.3 材料二氧化碳吸附/脱附性能
微孔吸附仪的工作原理是等温物理吸附的静态容量法,利用气体吸附原理可用于多种气体(如CO2、H2、CH4、N2等) 的等温吸附和脱附分析以及吸附热的计算。
本文研究中CO2气体吸附测试是在美国麦克ASAP2020微孔吸附仪上进行的。二氧化碳(CO2)吸附测试如下:首先,样品在室温条件下抽真空24 h,然后,在150℃下抽真空预处理10 h(以1℃/min的升温速率由室温升到150℃);随后,在200℃或250℃下抽真空热处理16 h(以1℃/min的升温速率由室温升至目标稳定);最后,在298 K下进行二氧化碳吸附,测试压力0-750 mmHg,样品用量50-70 mg。
2 结果与分析
2.1 X射线衍射分析
通过X射线衍射仪测试得到所制备的PDA@Ag/UiO-66复合材料的晶相结构,结果(图2)显示:
(1)PDA@Ag的 XRD谱图和 Ag的标准卡片(JCPDS card no.04-0783)一致,说明Ag被成功还原出。
(2)UiO-66的 XRD 谱图分别在 2θ=7.36°,8.48°,25.68°处出现特征峰,分别与(111)、(002)、(224)晶面相对应,这与文献[16]的研究结果一致。
(3)对于UiO-66与不同含量PDA@Ag制备的复合材料(PDA@Ag/UiO-66)的 XRD谱图中均出现了UiO-66的特征峰,说明它们具有相同的晶体形态,且具有高的对称性以及相同的拓扑结构;同时复合材料中也出现了Ag的特征峰,表明PDA@Ag成功的掺杂入复合材料。
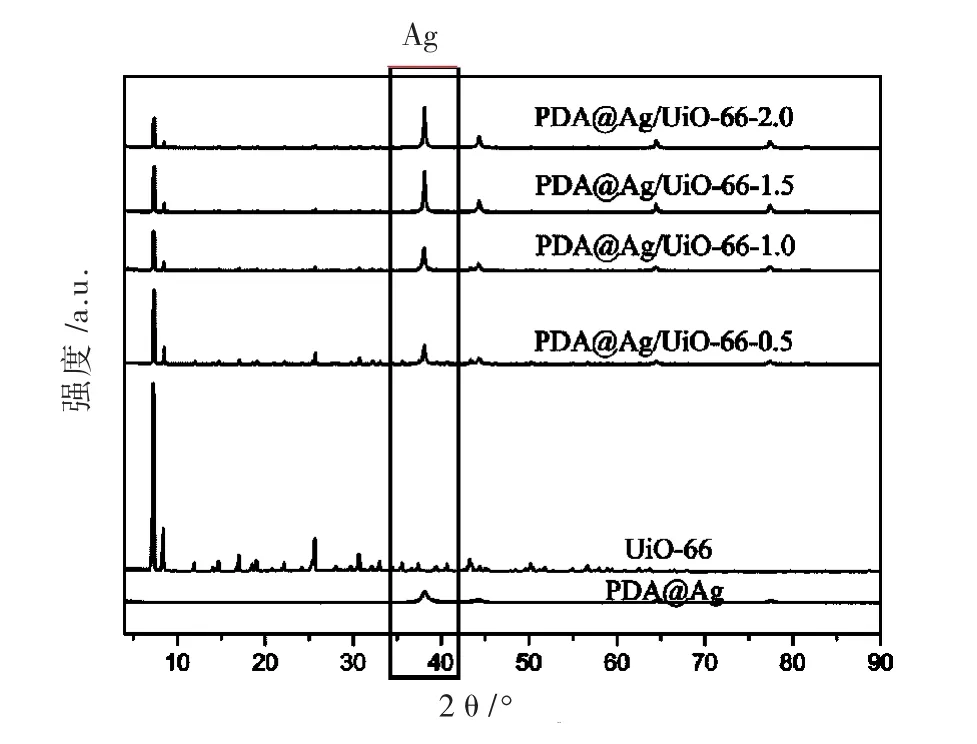
图2 PDA@Ag,原始UiO-66和PDA@Ag/UiO-66复合材料的X射线衍射谱图Fig.2 Powder XRD patterns of PDA@Ag,bare UiO-66,and PDA@Ag/UiO-66 composites
2.2 扫描电镜分析
扫描电镜照片如图3所示。

图3 原始 UiO-66(A)、PDA@Ag/UiO-66-0.5(B)、PDA@Ag/UiO-66-1.0(C)、PDA@Ag/UiO-66-1.5(D)、PDA@Ag/UiO-66-2.0(E)和 PDA@Ag(F)的扫描电镜照片Fig.3 Typical SEM images of bare UiO-66(A),PDA@Ag/UiO-66-0.5(B),PDA@Ag/UiO-66-1.0(C),PDA@Ag/UiO-66-1.5(D),PDA@Ag/UiO-66-2.0(E)and PDA@Ag(F)
由图3可见:原始UiO-66是十四面体,表面非常光滑。复合材料也是十四面体,但相对于原始UiO-66,复合材料的晶型尺寸会小一些,并且能够很明显的看到不光滑的表面,其表面上会有一些“凸起”;大多数都呈立方型,尺寸较均一,平均边长20 nm左右。因此,结合以上XRD谱图得到的结论,判断复合材料表面的“凸起”应该就是PDA@Ag。
进一步对复合材料(PDA@Ag/UiO-66)进行表面化学元素面扫描分析,结果(图4)显示:PDA@Ag/UiO-66-2.0复合材料和PDA@Ag/UiO-66-0.5复合材料中都含有作为UiO-66的中心金属离子锆(Zr),PDA@Ag/UiO-66-2.0复合材料还含有Ag元素,并且均匀的分布在其中,说明PDA@Ag成功的掺杂入UiO-66中。

图4 复合材料(PDA@Ag/UiO-66)表面化学元素面扫描分析Fig.4 EDS elemental mapping analysis of PDA@Ag/UiO-66 composite.
2.3 热重分析
对于复合材料的热稳定性探究,采用TGA考察材料在氮气(N2)中的热稳定性,确定它在N2中的分解温度。从图5可以看出:UiO-66的质量在50-100℃极速减少了15%,这是因为溶剂的去除;随后,TGA曲线出现第一个平台,表明骨架结构在平台温度范围内受热稳定;500℃左右出现了25%的明显质量损失,这可归因于配体与金属的配位键发生了断裂。而PDA@Ag的热稳定性很好,在320℃时仅损失了3%的质量,其可归因于聚多巴胺(PDA)的受热分解。而当UiO-66中掺杂PDA@Ag后,热稳定性明显提高。并且随着PDA@Ag含量的增加,骨架坍塌温度也不断在提高。复合材料在600℃附近都出现了一个较大台阶,这可归因于配体与金属的配位键发生了断裂,并且随着PDA@Ag含量的增加,质量损失越少,如 PDA@Ag/UiO-66-2.0,PDA@Ag/UiO-66-1.5,PDA@Ag/UiO-66-1.0,PDA@Ag/UiO-66-0.5的质量损失分别约为 8、10、15、18%,这进一步说明随着掺杂入功能配体PDA@Ag含量的增加,复合材料的热稳定不断提高。
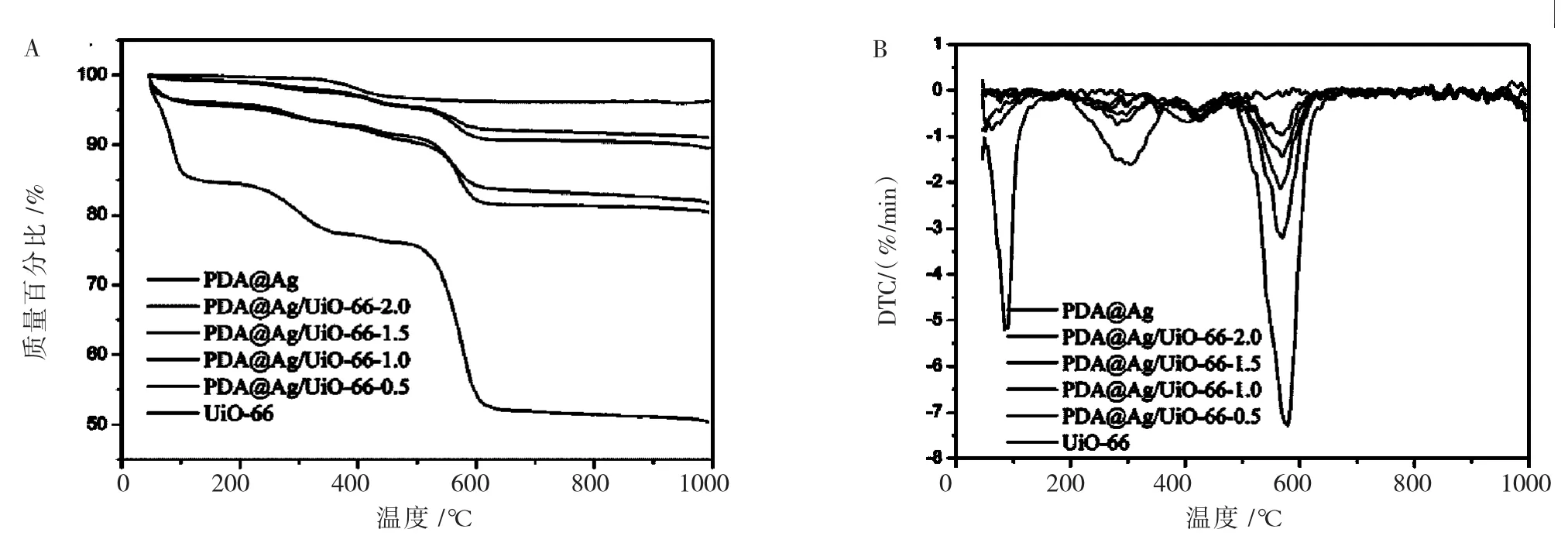
图5 PDA@Ag,原始UiO-66和PDA@Ag/UiO-66复合材料的热重分析曲线TGA曲线(A)和DTG曲线(B)Fig.5 Thermogravimetric analysis curves of PDA@Ag,bare UiO-66,and PDA@Ag/UiO-66 composites TGA(A),DTG(B)
2.4 材料二氧化碳吸附/脱附性能
鉴于UiO-66类MOFs的晶态、微孔骨架结构,本文对 UiO-66及复合材料(PDA@Ag/UiO-66)进行了CO2等温吸附/脱附测试。气体吸附测试之前,所有样品在200-250℃抽真空16 h,以除去溶剂分子及完全脱去无机金属单元中Zr上的羟基。测试温度为298 K,测试压力为0-750 mmHg。

图6 UiO-66,PDA@Ag/UiO-66-0.5和 PDA@Ag/UiO-66-2.0在298 K下的CO2等温吸附/脱附曲线Fig.6 CO2isothermal adsorption/desorption curves of UiO-66,PDA@Ag/UiO-66-0.5 and PDA@Ag/UiO-66-2.0 at 298 K
从常温常压下CO2等温吸附/脱附曲线(图6)可知:
(1)在一个大气压下和298 K的情况下,原始UiO-66的吸附量是47.5 cm3/g(STP)。当UiO-66掺杂入PDA@Ag后制备出复合材料,PDA@Ag/UiO-66-0.5的吸附量是29.8 cm3/g(STP),而PDA@Ag/UiO-66-2.0的吸附量是14.7 cm3/g(STP)。吸附量反而下降说明掺杂入的PDA@Ag能覆盖CO2吸附位点,导致其吸附量下降。
(2)随着掺杂PDA@Ag量越多,覆盖了越多的CO2吸附位点,导致吸附量降低,但脱附量相对而言却增加了。
3 讨论
(1)本文通过多巴胺盐酸盐在碱性环境中可以发生氧化自聚合发生交联而形成聚多巴胺(PDA),而PDA作为还原剂可将硝酸银中的Ag+还原成Ag0,制备出PDA支撑Ag的功能材料,再通过溶剂热法将功能材料(PDA@Ag)掺杂入金属有机框架(UiO-66)中,功能化的 MOFs(PDA@Ag/UiO-66复合材料)既保留MOFs本身的捕碳能力,同时又可用于CO2吸附脱附。
(2)通过扫描电镜和元素面扫描分析证明作为功能材料的PDA@Ag掺杂进了金属有机框架(UiO-66)中。通过X射线衍射分析则发现复合材料(PDA@Ag/UiO-66)的晶型和拓扑结构与UiO-66基本一致。通过热重分析复合材料的热稳定性发现,在UiO-66中掺杂入PDA@Ag后,复合材料的热稳定性明显提高。
(3)对复合材料(PDA@Ag/UiO-66)进行 CO2常温常压下吸附/脱附试验发现,引入PDA@Ag后,复合材料的吸附量反而下降,这可能是因为PDA@Ag部分覆盖了CO2吸附位点,以致复合材料吸附量下降的,其具体CO2吸附脱附性能还有待进一步研究。但这种新型复合材料为将来实现MOFs材料在常温常压下吸附脱附CO2提供了很好的研究方向。
4 结论
(1)通过溶剂热法成功制得了PDA@Ag/UiO-66复合材料。
(2)成功制备出了十四面体纳米晶体材料,该材料能明显提高该复合材料的热稳定性。
(3)掺入 PDA@Ag后,复合材料(PDA@Ag/UiO-66)的吸附量反而下降了,说明PDA@Ag会覆盖住CO2吸附位点,但CO2脱附量相对增加。
