不同增溶剂对鱼金注射液稳定性的影响
2018-11-09何俊婷张芳侠曹爱兰王景峰惠选柱
何俊婷 ,张芳侠 ,曹爱兰 ,王景峰 ,惠选柱
(1.陕西医药控股医药研究院有限公司,陕西 西安 710075; 2.陕西中药研究所,陕西 西安 710075; 3.陕西医药控股山海丹药业有限公司,陕西 西安 710075; 4.陕西省中药提取分离与制剂工艺工程研究中心,陕西 西安 710075)
鱼金注射液是由鱼腥草、金银花经重蒸馏得到的芳香水制成的纯中药制剂,用于急性上呼吸道感染、急性支气管炎[1]。鱼腥草与金银花的芳香水为乳白色混悬液,需加入吐温-80增溶,使其成为澄明溶液。增溶剂的添加是中药注射剂提高有效成分溶解度、保证溶液稳定的常用方法,也是影响中药注射剂质量和安全性的关键技术[2]。吐温-80是一种聚合物,稳定性不佳,含有大量杂质或降解产品,是引发急性过敏症状的主要原因[3-4]。本研究中采用羟丙基-β-环糊精、磺丁基 -β-环糊精、甲基-β-环糊精作为吐温-80的替代品。其中,羟丙基-β-环糊精相对表面活性和溶血活性比较低,且对肌肉无刺激性,是一种理想的注射剂增溶剂[5];磺丁基-β-环糊精是阴离子型高水溶性环糊精衍生物,有较好的增溶作用,能降低肾毒性、缓和药物溶血性等;甲基-β-环糊精能很好地对药物进行分子包合,从而提高药物的稳定性、水溶性、安全性[6-8]。采用3种不同的替代吐温-80的增溶剂制备鱼金注射剂,通过稳定性考察在温度和光线的影响下制剂随时间变化的规律,为产品生产、储存、包装等提供科学依据[9],为辅料及稳定性研究、鱼金注射液再研究、再评价工作的重要切入点。现报道如下。
1 仪器与试药
1.1 仪器
Agilent 7890A型气相色谱仪(美国安捷伦公司);AG-135型电子分析天平(德国,MettlerToledo);WD-A型药物稳定性检查仪(天津药典标准仪器厂)。
1.2 试药
羟丙基-β-环糊精(西安德立生物化工有限公司,批号为 171002);磺丁基-β-环糊精(批号为170301),甲基 -β -环糊精(批号为 170301),均为淄博千汇生物科技有限公司产品;吐温-80(分析纯,上海申宇医药化工有限公司);活性炭(上海活性炭厂有限公司,批号为160305);甲基正壬酮对照品(批号为111640-201005),乙酸龙脑酯对照品(批号为110759-200303),芳樟醇对照品(批号为 1503-200001),均由中国食品药品检定研究院提供;鱼金注射液(批号分别为 20170103,20170104,20170105),鱼腥草、金银花芳香水,均为陕西医药控股集团山海丹药业有限责任公司产品;磷酸盐标准缓冲液(pH=6.86,25℃,上海虹北试剂厂);水为纯化水,其余试剂均为分析纯。
2 方法与结果
2.1 制备方法
取鱼腥草4 kg,金银花2 kg,加水8倍量,水蒸气蒸馏,收集馏液6 000 mL,将蒸馏液进行重蒸馏,收集馏液近1 000 mL,鞣质项检查合格后,用稀释法分次加入增溶剂,混匀,再依次加入焦亚硫酸钠、氯化钠和枸橼酸钠溶液适量调节pH为5.9~6.5,搅匀,配制至1 000 mL,滤过,再用 0.45 μm微孔滤膜,精滤 3次,取滤液,灌装,流通蒸气灭菌30 min,即得。鱼腥草、金银花重蒸馏得到的芳香水为微带乳(黄)色的液体,经试验验证,当加入0.50%羟丙基 -β-环糊精或1.50%磺丁基-β-环糊精或0.45%甲基-β-环糊精增溶后,肉眼可见鱼腥草、金银花重蒸馏溶液变澄清。
2.2 检查
取供试品溶液,照2015年版《中国药典(四部)》不溶性微粒检查法(通则0903)测定,可见异物检查法(通则0904)测定,pH测定法(通则0631)测定。结果显示,3种不同增溶剂配制的鱼金注射液各项检测指标均符合规定。
2.3 含量测定
色谱条件与系统适用性试验:色谱柱为键合交联聚乙二醇为固定液的毛细管柱(DM WAX气相色谱柱,30 m ×0.32 mm,0.25 μm );起始温度 70 ℃ ,维持5 min,再以5℃ /min的速率升温至140℃,维持2 min,再以30℃ /min的速率升温至 250℃,维持 5 min;进样口温度230℃;检测器温度280℃。理论板数按甲基正壬酮峰计应不低于2 000。在此条件下的色谱图见图 1。

图1 气相色谱图
溶液制备:分别取甲基正壬酮、乙酸龙脑酯及芳樟醇对照品适量,精密称定,分别加乙酸乙酯制成每1 mL分别含 100,25,10 μg 的溶液,即得对照品溶液。精密量取鱼金注射液25 mL,置具塞试管中,加入乙酸乙酯5 mL,再加氯化钠5 g,振摇3 min,分取乙酸乙酯层,再加入乙酸乙酯5 mL,振摇3 min,分取2次乙酸乙酯层提取液,定容至10 mL容量瓶中,摇匀,作为供试品溶液。
含量测定:分别精密吸取对照品溶液与供试品溶液各1 μL,注入气相色谱仪,测定,计算,结果见表1。

表1 不同增溶剂配制样品含量测定结果( g/mL)
2.4 影响因素试验
高温试验:取鱼金注射液,60℃条件下放置10 d,于0,5,10 d时取样检测。与0 d比较,供试品性状、含量、pH、可见异物、不溶性微粒均未发生显著变化。
强光照射试验:供试品于照度为(4 500±500)lx条件下放置 10 d,在0,5,10 d时取样检测。供试品性状、含量、pH、可见异物、不溶性微粒均未发生显著变化。
低温冻融试验:低温试验中,分别将鱼金注射液置冰箱中,在4℃条件下观察2 d,然后取出样品置40℃加速条件下考察2 d,反复循环3次。冻融试验中,分别将3批鱼金注射液置低温冰箱中,在-20℃条件下观察2 d,然后取出样品置40℃加速条件下考察2 d,反复循环3次。取样检查外观色泽、可见异物、不溶性微粒、pH及甲基正壬酮、乙酸龙脑酯、芳樟醇含量,结果见表2。
加速稳定性试验:供试品溶液在(40±2)℃条件下放置 6 个月,在 0,1,2,3,6 个月时分别取样,检查供试品性状(无色、澄明)、含量、pH、可见异物(符合规定)、不溶性微粒。结果见表3。显示3种增溶剂样品均未发生显著变化。
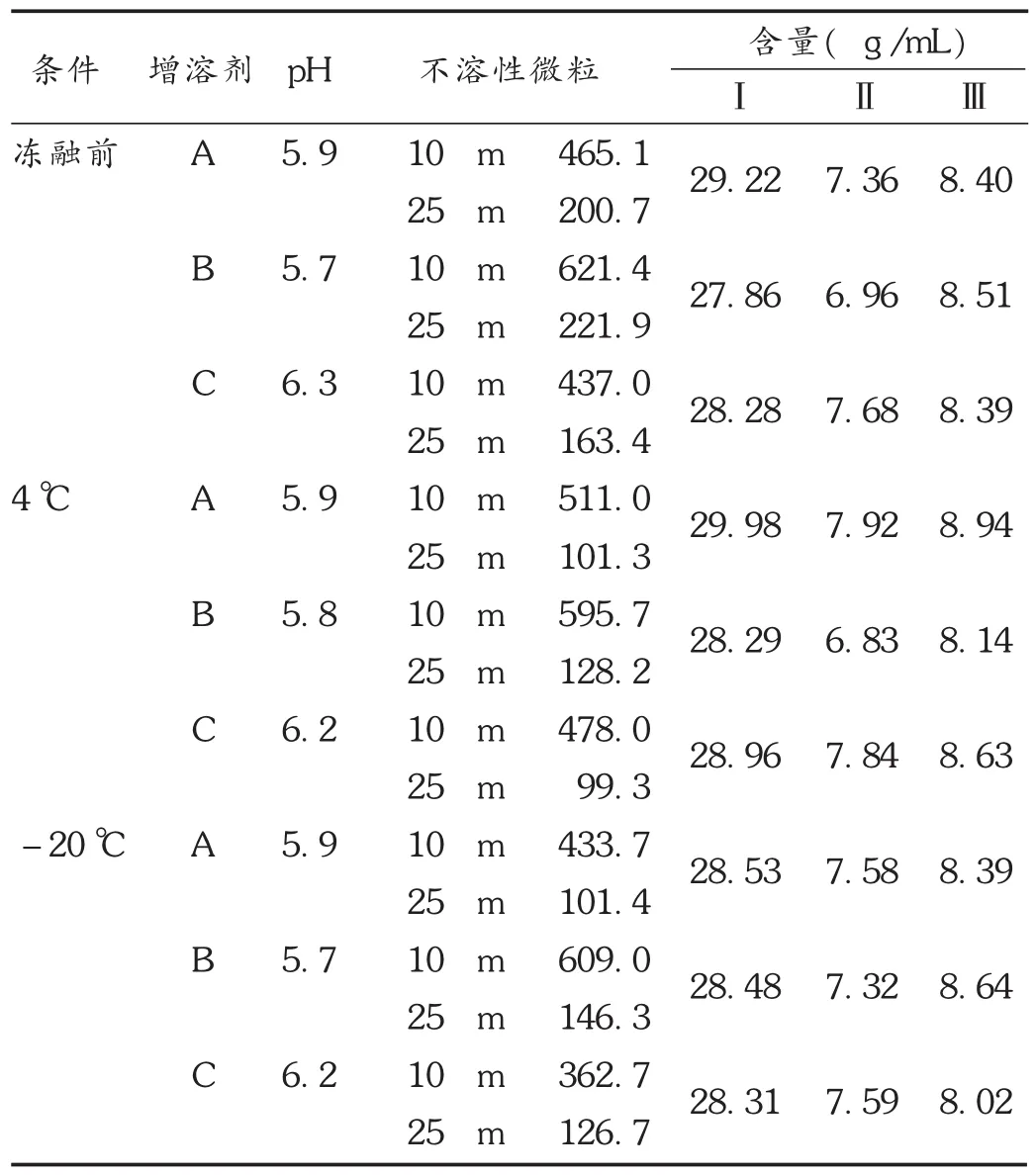
表2 低温冻融稳定性试验结果
3 讨论
3.1 稳定性试验
对鱼金注射液外观形状、不溶性微粒、pH、可见异物及含量测定进行了全面分析。结果表明,影响因素试验对鱼金注射液稳定性无明显影响。低温冻融试验结果表明,试验前后,3组供试品pH、不溶性微粒、有效成分含量变化不大,前后均符合质量标准要求。因此,低温及冷冻对3种增溶剂配制的鱼金注射液稳定性基本无影响。
3.2 加速稳定性试验
羟丙基-β-环糊精、甲基-β-环糊精组供试品外观形状、不溶性微粒、pH、可见异物及含量均未发生明显变化;磺丁基-β-环糊精组供试品溶液在经过6个月加速稳定性试验后,不溶性微粒量增多,供试品外观有轻微的乳光产生。磺丁基-β-环糊精作为增溶剂,添加量为1.5%时才可使鱼金注射液澄清,辅料用量较大,但增溶效果相对较差,制剂稳定性不佳,因此其不适用于鱼金注射液的增溶。
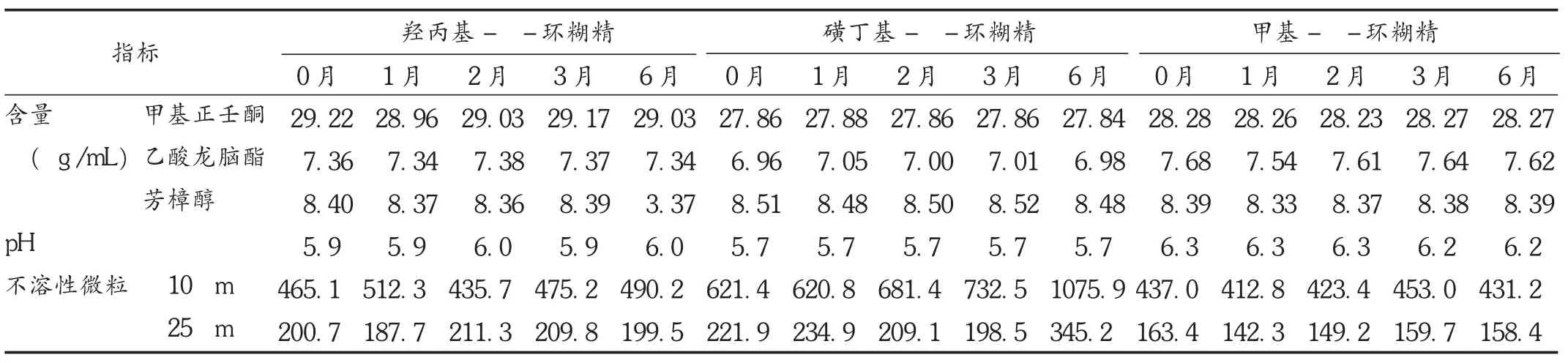
表3 不同增溶剂下供试品溶液加速稳定性试验结果
3.3 后续研究方向
截至目前,已完成6个月长期加速稳定性研究,3种增溶剂制备的鱼金注射液各项指标均符合规定,未来将继续对羟丙基-β-环糊精、甲基-β-环糊精组供试品进行长期稳定性研究。
