50%王铜可湿性粉剂中王铜的测定
2018-11-02黄绍红熊龙云
黄绍红 熊龙云
(江西省化学工业研究所,江西 南昌 330029)
王铜是铜制剂中药害最小的制剂,又称碱式氯化铜,是无机铜保护性杀菌剂,目前测定铜的主要方法有碘还原法[1],(X射线荧光光谱法,双环己酮草酰二腙分光光度法,新式铜灵萃取法)[2],原子吸收光谱法[3],分光光度法[4]。本文介绍一种利用磷酸盐作缓冲溶液控制体系的pH值,用乙二胺四乙酸二钠(EDTA)作显色剂。由于EDTA能与Cu+2在pH值为2.5~10的范围内形成稳定的蓝色络合物。
1 实验部分
1.1 仪器与试剂
UV-6100紫外可见分光光度计;
分析天平;
实验室常用玻璃仪器;
Cu+2标准溶液1.5mg/mL:
移取经105℃烘干脱水的氯化铜3.18g(精确到0.0002g)用去离子水溶解,再加一滴浓盐酸,定容至1升容量瓶中,此溶液Cu+2的含量为1.5mg/mL。
磷酸盐缓冲溶液:
称取39.4克12水磷酸氢二钠与21.1克二水磷酸二氢钠,用纯水溶解,定容至1升容量瓶中,用时过滤,此缓冲溶液的pH值为6.9。
0.25mol/L EDTA溶液:
称取93.1克EDTA,用纯水溶解后,定容至1L容量瓶中,此ETDA溶液浓度为0.25mol/L。
实验所用水为纯净水或二次蒸馏水试样的处理。
1.2 试样的处理
准确称取含Cu+20.375g的王铜试样约1.26克(精确至0.0002g)于烧杯中,加入50mL(1+1)盐酸溶液,加热微沸约15分钟,冷却后转人250ml容量瓶中,用水稀释至刻度,用中速滤纸干过滤,弃去最初的25ml滤液。
1.3 实验方法
在50ml比色管中,分别加入一定量的标准溶液或相应浓度的试样溶液,再依次加入20mL磷酸盐缓冲溶液,20mL 0.25mol/L的EDTA溶液,用水稀释至刻度,摇匀,显色30分钟后,以水空白为参比,用d1比色皿于730nm波长处测其吸光度。
2 结果与讨论
2.1 测定波长的选择
Cu+2与EDTA试液在pH(2.5~10)范围内反应生成蓝色络合物,该络合物的吸收最高峰在波长730nm处。
如图1,因此实验选择730nm作为测定波长。
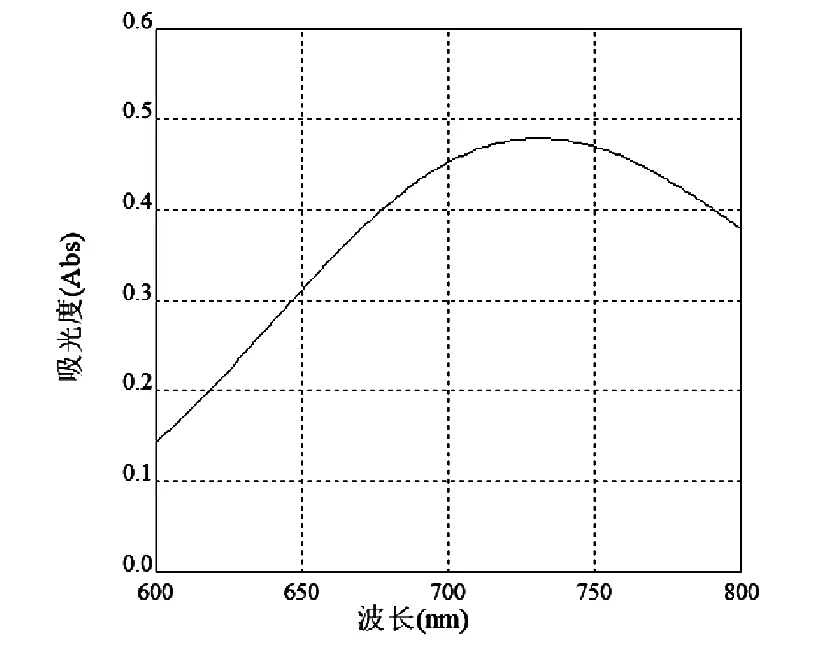
图1 铜络合物在不同波长下的光谱吸收图
2.2 显色酸度,显色剂用量的选择
2.2.1 显色酸度的选择
固定EDTA用量20mL,标液5mL,如表1。

表1 缓冲溶液对吸光度的影响
缓冲溶液的量决定用20mL,大用量的缓冲溶液可以更大地调节体系的酸度,有利于获得更加稳定的吸光度。
2.2.2 显色剂用量的选择
用固定的缓冲溶液20mL,标准溶液5mL,如表2。
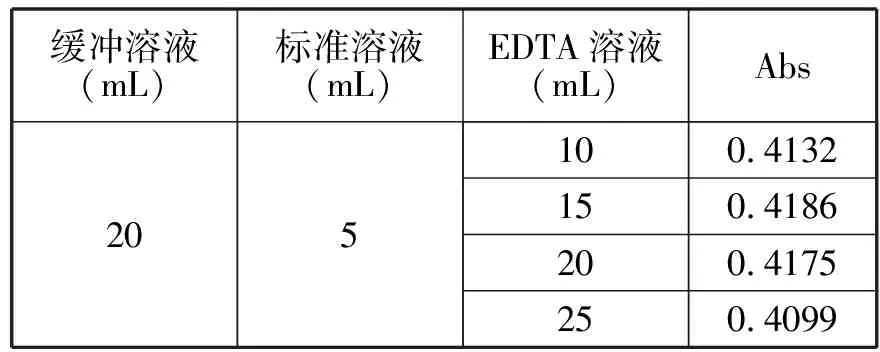
表2 EDTA溶液对吸光度的影响
当EDTA大于20ml时吸光度变小,考虑到EDTA掩蔽其它离子的用量,确定EDTA溶液的用量为20ml。
2.3 标准曲线
分别移取3.0,4.0,5.0,6.0,7.0,8.0ml的标准溶液,按1.3的实验方法测定Abs,得到线性回归方程:
Conc=0.0521+23.8176Abs,r=0.999897,标准曲线的线性图如图2。

图2 铜络合物浓度和吸光度的线性关系图
2.4 样品分析
2.4.1 精密度分析
分别称取5份约1.26g的试样,按照1.2试样处理的方法,各取试样溶液4mL共五份,按照1.3的实验方法检测王铜的含量。结果如表3。

表3 王铜可湿性粉剂的精密度测定结果
2.4.2 回收率分析
依次移取上次五份试样溶液各2mL,分别加入标样溶液2mL。共五份,如表4。

表4 王铜可湿性粉剂的准确度测定结果
3 结论
用上述方法对王铜试样进行了分析方法研究。由结果可以看出,在一定浓度范围内,Cu离子浓度与Abs呈现很好的线性关系。精密度分析变异系数是0.78%,回收率为98.8%。具有较高的精密度和准确度。操作简便,可以作为测定王铜含量的一种方法。
