二次电池废料锂量的测定
——火焰原子吸收光谱法
2018-11-02朱雪琴周家红黄爱红
李 强 胡 玉 朱雪琴 周家红 黄爱红
(江西赣锋锂业股份有限公司,江西 新余 338000)
前言
2017年我国电池总产量约600亿只,其中锂离子电池产量150亿只,同比增长40%,我国电池产量约超过世界电池总产量的一半。2017年新能源乘用车和客车电池搭载量累计分别达120亿瓦时和190亿瓦时,占比为32%和57%。2017年,废电池(铅酸电池除外)回收量约为13万吨,其中废二次电池回收量约为10万吨,未来回收规模将越来越大。
二次电池中含有镍钴锰化合物、碳素材料、隔膜、有机电解液、稀有元素、铜、铁、铝等,如果不对报废后的电池进行回收,不但导致大量的有价金属元素损失,还会对环境带来严重污染。由国家环境保护总局发布的《废电池污染防治技术政策》(环发[2003]163号)要求加快符合环境保护要求的废电池分类收集、贮存、资源再生及处理处置体系和设施建设,推动废电池污染防治工作。发改委发布的《汽车产品回收利用技术政策》(2006年第9号)中规定电动汽车生产企业要负责回收、处理其销售的电动汽车的蓄电池。国务院发布的《节能与新能源汽车产业发展规划(2012—2020年)》[国发〔2012〕22]要求构建动力电池回收利用体系,形成完备的技术标准和管理规范体系。
在市场利好和政策鼓励的条件下,我国形成了大量的电池回收企业,如广东邦普、江西赣锋锂业、四川天齐、格林美、华友钴业等一大批上规模的企业。测算从废旧动力锂电池中回收钴、镍、锰、锂、铜及铁和铝等金属所创造的市场规模会在2018年爆发,达到52亿元;2020年达到136亿元。二次电池废料具有很高的回收价值,带来可观的经济效益。
但是,可利用元素含量不同,回收价值也不同。在二次电池废料贸易的过程中,主要以镍、钴、锰、锂、铁、铜和铝等元素含量来定价。据了解,贵金属和有色金属的价格是每天都在变化,如果笼统的以电池废料的价格来计算,没有按照电池废料中的可利用元素进行计算,有可能回收的废料仅仅是废料,没有可利用价值,这会给回收企业很大的压力,对回收企业来说是不公平的。为了保证回收行业的可持续发展,需要按元素含量来进行计价,就必须对废料中的元素进行分析。故电池废料中的元素分析是回收过程中的重要一环,关系到采购、回收再利用工艺等各个环节,而现在电池的报废量又逐年增加,为减少贸易过程中的摩擦,促进电池回收行业的发展,满足供应商、客户的需求。因此,对于相对欠缺的这些方面,有必要完善电池废料分析的相关方法。
废料中元素含量的不同,采用的处理工艺也会不同,基于此,在电池废料进入回收体系之前,有必要对电池废料在的元素进行分析。研究二次电池化学分析方法,可为新能源的普及起到正向的积极效应,控制电池回收成本,缓解材料危机,还可以减少其他有害化学物质对环境的污染。是推动电池回收行业、环保事业和新能源产业的发展,是重要一环,意义深远。
现在整个二次电池没有形成系统的分析方法,锂的测定方法有重量法[1]、分光光度法[2]、滴定法[3-4]、离子选择性电极法[5]、火焰原子吸收光谱法[6-10]、火焰原子发射光谱法[11-12]、电感耦合等离子体发射光谱法[13-14]、电感耦合等离子体质谱法等[15],其中原子吸收光谱法是目前使用最为广泛的分析方法。
本文重点通过研究原子吸收光谱法对二次回收电池中锂测定的不同条件来探讨采用原子吸收光谱法测定二次回收电池中锂含量的方法。
1 原子吸收光谱仪测定条件的选择
1.1 燃气和助燃气选择
选择燃气助燃气混合比从待测试样的性质、待测元素的灵敏度和稳定性等因素。锂元素在原子吸收上的灵敏度较高,测定锂选择用贫燃性火焰,固定空气压力0.25MPa,乙炔压力0.08MPa,固定单色器通带为0.4nm,灯电流2.0mA,燃烧器高度5mm,改变乙炔流量,考察标准溶液的吸光度值变化,试验结果见表1。

表1 不同乙炔流量测定锂的吸光度
由表1可知,随着乙炔流量的变化,吸光度均值略有增加,乙炔流量在1.4L/min和1.6L/min附近,标准系列溶液的吸光度均较为稳定,本实验选择仪器推荐燃气流量1.4L/min。
1.2 灯电流的选择
使用仪器推荐的固定单色器通带为0.4nm,乙炔流量为1.4L/min,燃烧器高度5mm,改变灯电流,考察标准溶液的吸光度值变化,试验结果见表2。
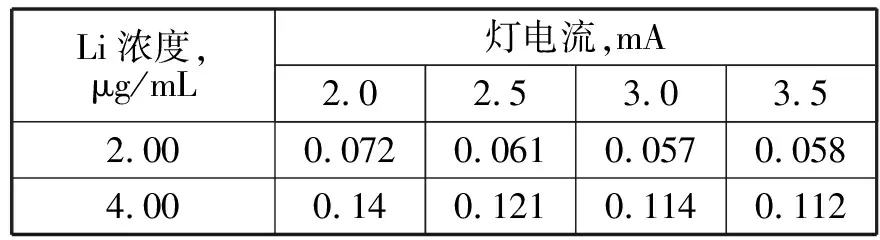
表2 不同灯电流测定锂的吸光度
由表2的实验数据可以看出,灯电流在2.5~3.5mA范围内,随着灯电流的增加,灵敏度略有下降。本试验用仪器的灯电流应用2.0mA的推荐灯电流,仪器性能较好,稳定性强,反而使用3.0mA的灯电流仪器较不稳定且吸光度明显较2.0mA的偏低,进一步补充试验,在2.0mA条件下,对1.00μg/mL的锂标准溶液连续测定11次,相对标准偏差为0,仪器使用灯电流2.0mA。
1.3 光谱仪通带宽度选择
固定灯电流2.0mA,乙炔流量1.4L/min,燃烧器高度5mm,改变单色器通带,考察标准溶液的吸光度值变化,试验结果见表3。
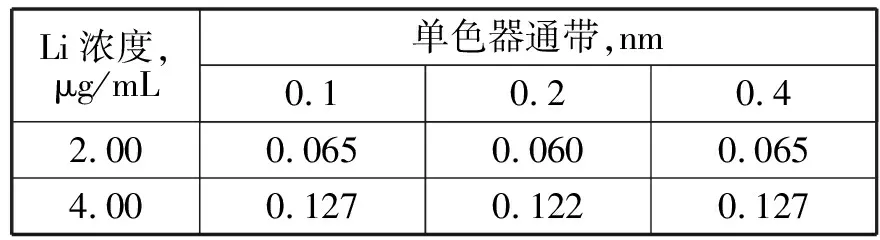
表3 不同单色器通带测定锂的吸光度
由表3的实验数据可以看出,本实验仪器单色器通带的增加,灵敏度变化不大,根据在能分离出待测元素分析线的范围内尽量选择较宽的狭缝,以获得较好的信噪比。锂元素的谱线相对较简单,灵敏度较高,干扰较少,因此可以使用较宽的通带,结合实验通带宽度,选择单色器通带0.4nm。
1.4 燃烧器高度和角度的选择
在火焰区自由原子的空间分布是不均匀的,随火焰条件而改变,通过调节燃烧器高度使光束从基态原子浓度最大的火焰区通过,可获得较高的灵敏度。
固定单色器通带0.4nm,乙炔流量1.4L/min,灯电流为2.0mA,改变燃烧器高度,考察标准溶液的吸光度值变化,试验结果见表4。
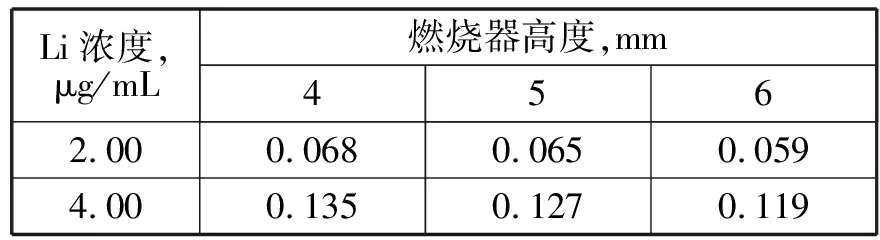
表4 不同燃烧器高度测定锂的吸光度
由表4可知,随着燃烧器高度的增加,仪器吸光度都较为稳定,但是吸光度逐渐降低,故选择燃烧器高度为4mm。燃烧器角度调整角度以将浓度2μg/mL的锂溶液的吸光度于0.055~0.065之间来调节。
1.5 测定条件确认
综合选定最佳测定条件见表5。
2 酸性介质的选择
因考虑硫酸对仪器的影响以及使用安全考虑,只对盐酸与硝酸介质做了验证。将浓度为0、1.00μg/mL、2.00μg/mL、5.00μg/mL的Li溶液配在0%~4%的盐酸、硝酸介质中,在以纯水介质标准曲线下测定其含量,验证不同酸及不同酸度下对测定的影响。结果见表7、表8。
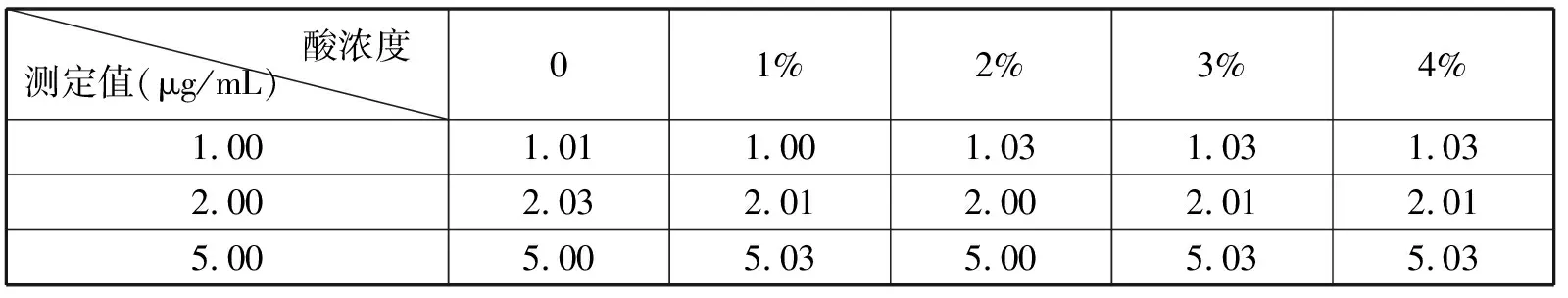
表6 硝酸介质对测试结果的影响
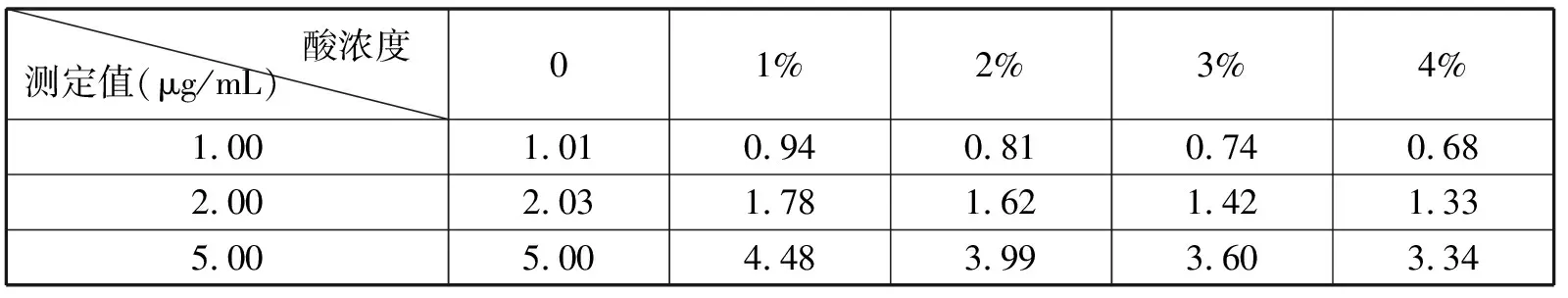
表7 盐酸介质对测试结果的影响
由表6、表7数据可知,在硝酸介质中,在0%~4%范围内,随着酸度的增加,对测定结果无显著影响。在盐酸介质中,测定结果随着酸度的增加急剧减小,酸度影响很大。所以考虑选择硝酸介质,酸度在1%~5%范围内的测定结果接近,本实验同意使用酸度为2%的硝酸作为介质。
此外,我们还验证了分别在2%的硝酸介质和硫酸介质中配制含锂浓度为1.00μg/mL、2.00μg/mL、4.00μg/mL、6.00μg/mL、8.00μg/mL的锂系列标准溶液的工作曲线的对比实验。吸光度见表8。
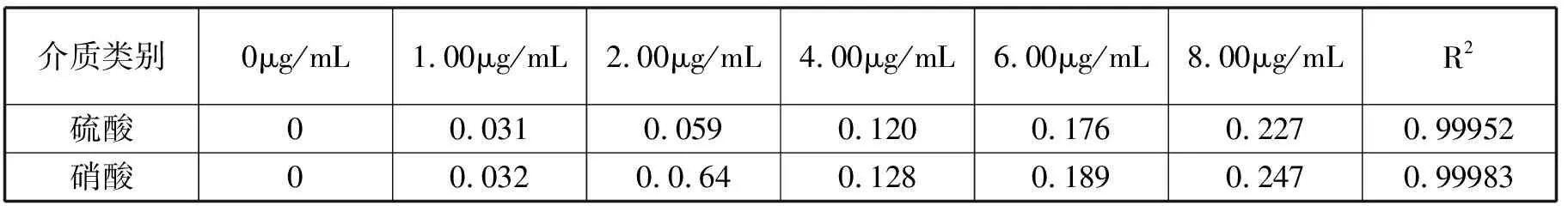
表8 锂在硝酸和硫酸介质标准溶液的吸光度和线性
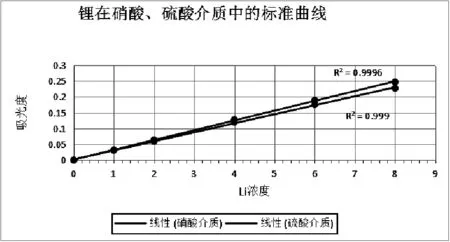
图1 在硫酸和硝酸介质中的浓度-吸光度曲线
由图1可知,在2%的硫酸和硝酸介质中,标准曲线的相关线性都很好,但相同浓度的锂溶液在硝酸介质中吸光度略高于在硫酸介质,说明硝酸介质灵敏度略高于硫酸介质,故同意推荐使用硝酸做为测锂介质。
3 电离干扰消除实验
本实验验证硝酸钾作为消电离剂进行电离干扰消除实验。
取4组100mL容量瓶,第1组容量瓶分别移入0mL、1.00mL、2.00mL、4.00mL、6.00mL、8.00mL浓度为100μg/mL的锂标准溶液(2.5),各加入4mL硝酸(2.2)后定容做无消电离剂试样。后面各组分别按表10加入硝酸钾(2.12,以钾计),加入4mL硝酸(1.6)维持酸度为2%的硝酸体系。用原子吸收光谱仪测定锂的吸光度并与标准工作曲线上查出锂含量,试验结果见表9。
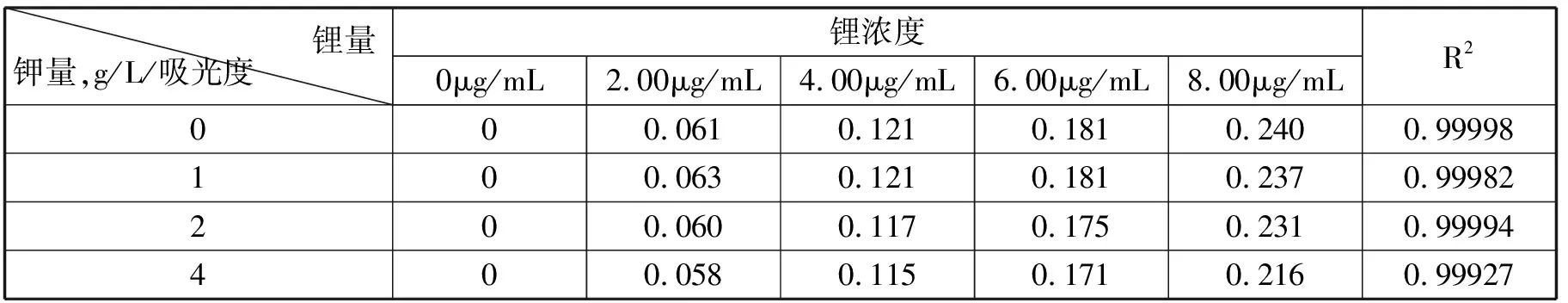
表9 加入消电离剂加入实验
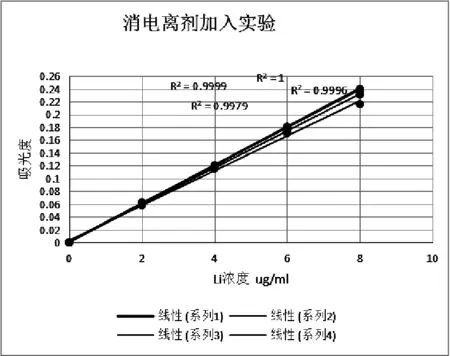
图2 消电离剂加入实验
由表9及图2加入消电离剂与未加消电离剂线性关系都很好,但加入硝酸钾后相同浓度锂溶液吸光度确实降低了,所以同意测锂时不需要加消电离剂的实验结论。
4 标准工作曲线线性和特征浓度
4.1 标准工作曲线线性
配制硝酸浓度为2%,锂浓度为0、1.00μg/mL、2.00μg/mL、4.00μg/mL、6.00μg/mL、8.00μg/mL、10.00μg/mL的系列标准溶液,在原子吸收光谱仪仪器最佳工作条件下,偏转燃烧头,将浓度为2.00μg/mL标准溶液吸光度调于0.055~0.065之间。按浓度由高到低依次测定吸光度,测三次取其平均值,绘制标准工作曲线。数据见表11。
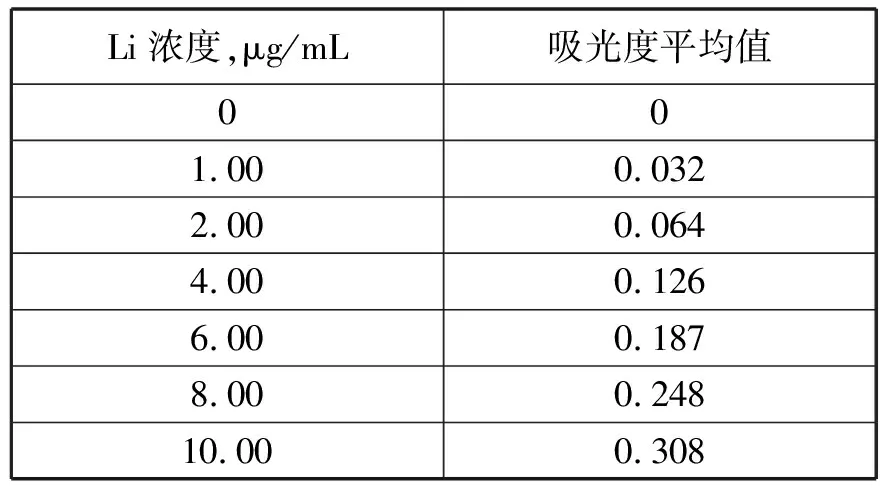
表10 系列标准溶液测定吸光度值
根据表10数据绘制工作曲线如图3。
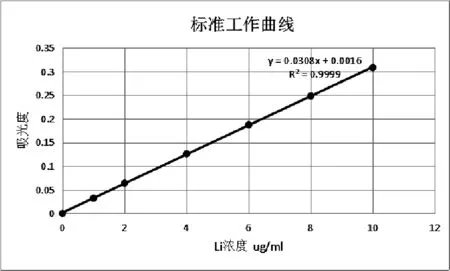
图3 Li标准工作曲线图
4.2 锂的特征浓度
在相同条件下,对1.00μg/mL的溶液连续测定11次吸光度,根据公式:
y=0.0308x+0.0016带入数据,结果见表11。
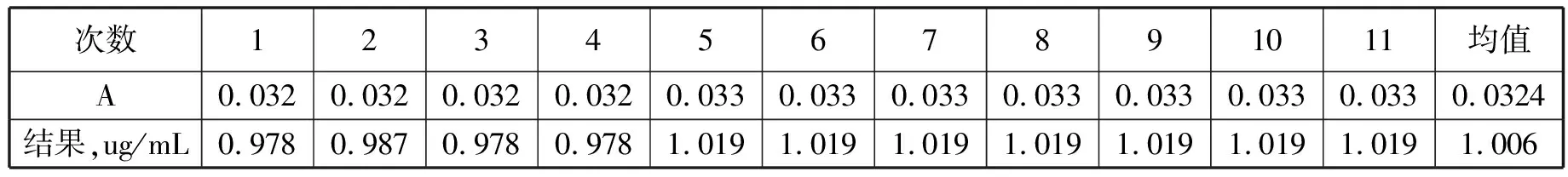
表11 连续测定11次吸光度值及对应浓度
根表11结果,求得吸光度值的相对标准偏差:SA=0.01547(A),
故检出限:DL=3SA=0.04641μg/mL,
特征浓度:SC=0.0044C/A=0.0044×1.006/0.0324=0.1366μg/mL
5 精密度实验
按前述试验条件对1#、2#、3#、4#、5#样品进行Li含量的测定。
称取0.20g试样,精确值0.0001g,于100mL玻璃烧杯中,加少许水润湿试料,加入5mL HNO3(1.2),振荡均匀,缓慢加入1mL过氧化氢(1.3),盖上表面皿,微热使酸可溶物溶解完全,冷却至室温,转移至100mL容量瓶中,定容,摇匀,干过滤,得待测试液。
分取5.00mL待测试液于100mL容量瓶中,加入4mL HNO3(2.5),于原子吸收波长760.78nm处测吸光度,于标准工作曲线(实验部分3.5.3)上查出并计算物料中的锂含量。结果见表12。
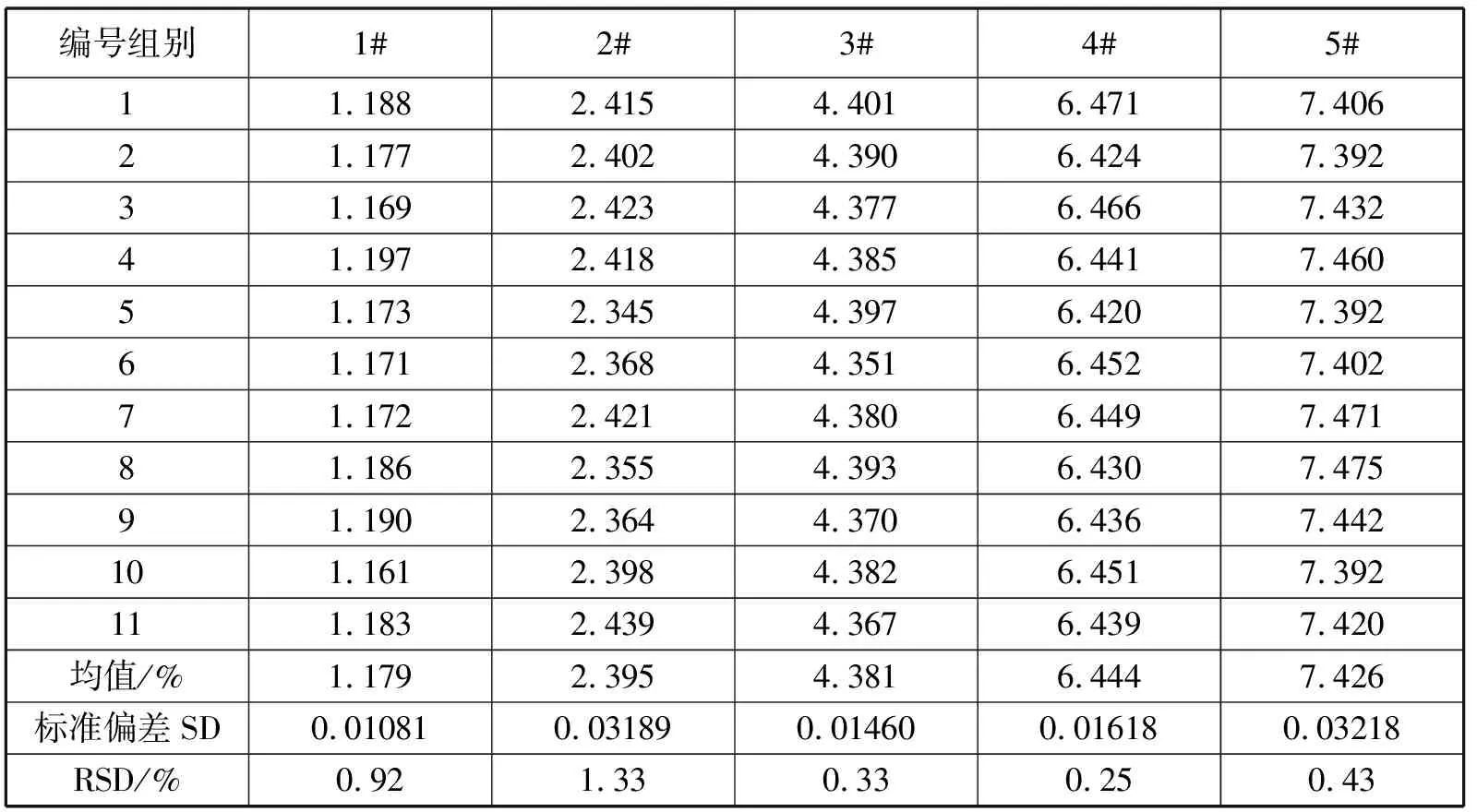
表12 物料中的锂含量
数据结论:独立测量多次所得数据相对标准偏差约在1%左右,精密度较好。
6 实验室间精密度数据
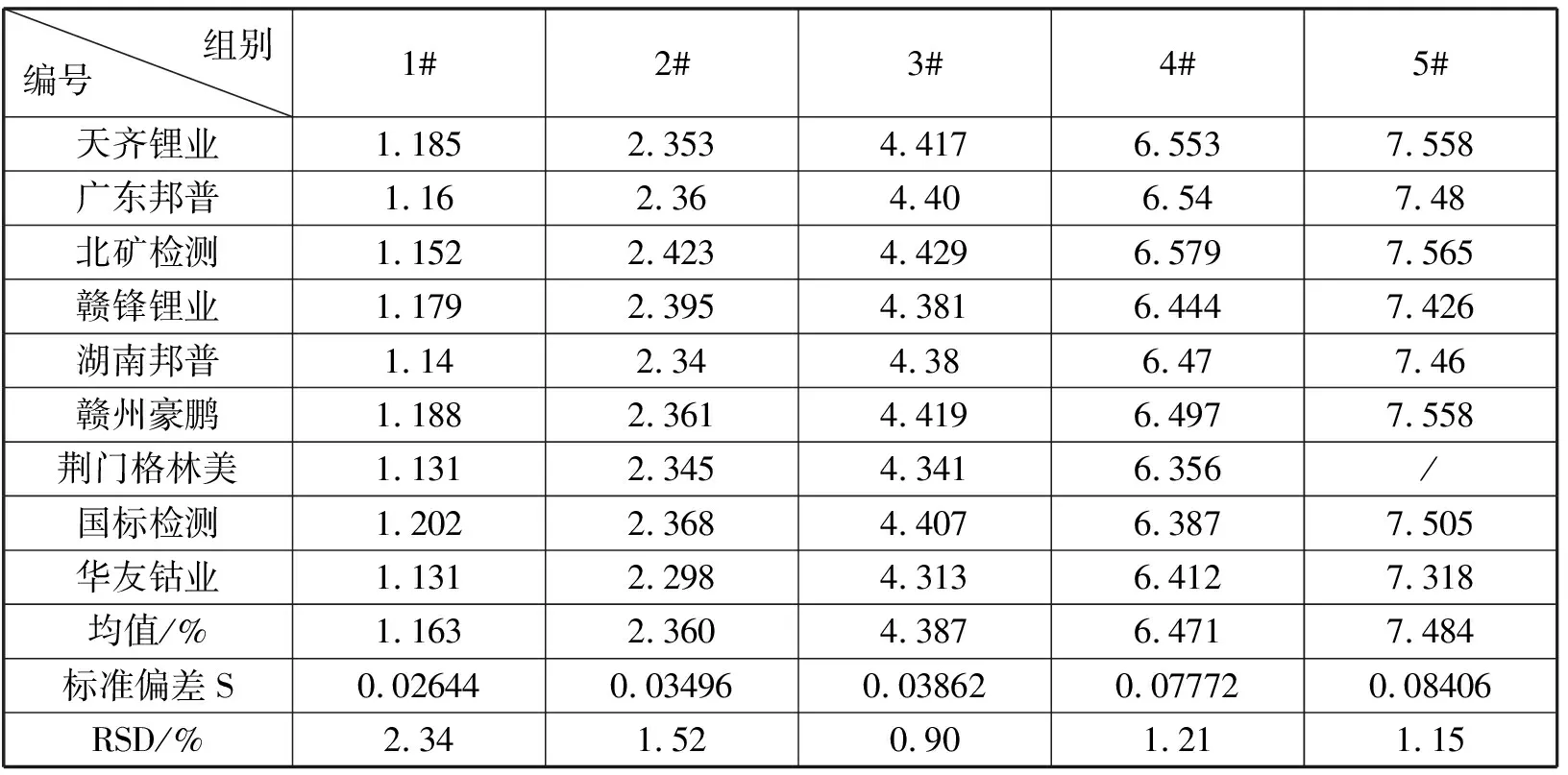
表13 实验室间精密度数据
数据结论:由各实验室的数据可知,除了1#、2#样品因为含量较低而得到的相对标准偏差略高外,其余值均在1%左右,实验室之间的精密度很好。
7 加标回收率实验
按分析步骤对3#样品进行测定锂含量的加标回收率,结果见表14。

表14 加标回收率实验
由表14数据可知,方法的回收率在98%附近。
8 结论
原子吸收法测定二次回收电池中锂含量在1%~10%时,方法操作简便,相对标准偏差小于1%,回收率在98%~102%之间,测定结果可靠,可以作为二次电池废料中锂含量测定的标准方法。
