尼可地尔联合曲美他嗪治疗对经皮冠状动脉介入治疗术后对比剂肾病的预防作用
2018-10-31程伟黄美娥罗助荣
程伟,黄美娥,罗助荣
近年来,随着临床应用的不断普及,经皮冠状动脉介入治疗(PCI)已成为降低冠心病发病率及死亡率的重要方法之一。然而,PCI术中应用碘对比剂带来的对比剂肾病(CIN)不容忽视。相关报道显示,CIN发病率为0.3%~14.5%,高危人群中高达50% 以上[1],已引起医疗界越来越多的关注,但其发生机制尚不明确,目前认为与肾脏缺血、肾小管上皮细胞直接损伤、一氧化氮生成减少以及氧化应激作用密切相关[2]。针对的不同发病机制,许多关于预防CIN的药物研究不断涌现。尼可地尔作为三磷酸腺苷(ATP)敏感性钾离子(KATP)通道开放剂,具有扩张血管、减轻胞内线粒体钙超载、减少氧自由基等作用[3-5],在肾脏缺血再灌注损伤中也能起到增加肾脏血流及减轻炎症的效果[6]。此外,曲美他嗪也被认为在CIN中能起到改善细胞能量代谢、减轻炎症反应等作用[7]。目前单独静脉用尼可地尔[8-10]或口服曲美他嗪[11-12]预防PCI术后CIN均有国外文献报道,但暂未见两药对CIN预防作用的对照或联合用药的研究报道。本文通过观察静脉用尼可地尔和(或)口服曲美他嗪对CIN及血肌酐的影响,评价两药对预防PCI术后CIN是否有协同作用。
1 资料与方法
研究对象:采取前瞻性、随机对照研究设计,连续入选2015-01-02至2017-08-29在中国人民解放军南京军区福州总医院心内科行择期PCI的患者。纳入标准:(1)Mehran危险积分[13]≥6分;(2)18~90岁。排除标准:(1)严重肝、肾功能不全;(2)急性心肌梗死需急诊PCI者;(3)术前2周内曾接受曲美他嗪或尼可地尔治疗;(4)心原性休克或左心室射血分数(LVEF)<30%;(5)有透析史或试验相关药物禁忌证;(6)近7天内使用过碘对比剂或多巴胺、利尿剂、非诺多泮、茶碱、甘露醇等药物;(7)目前使用除阿司匹林外的非甾体类抗炎药物或其他肾毒性药物;(8)手术未成功、无法完成水化、相关材料不全或失访者。研究样本采集过程中,定期进行阶段性统计效力检验,当样本量为521例时,四组间CIN的发病率统计效力出现显著意义(P<0.05),因此,521例患者最终纳入本研究,其中男性383例,女性138例,平均年龄(67.54±12.01)岁。研究方案经中国人民解放军南京军区福州总医院伦理委员会批准通过,所有研究对象均签署知情同意书。
研究方法:采用析因设计,研究对象于入院时利用随机数字表法随机分为四组,即对照组(n=208)、尼可地尔组(n=105)、曲美他嗪组(n=104)、尼可地尔+曲美他嗪组(n=104)。对照组:术前6 h至术后12 h静脉泵入生理盐水1.1 ml/(kg·h);尼可地尔组:将84 mg尼可地尔(12 mg/支)溶于100 ml生理盐水中,于术前6 h开始以0.1 ml/(kg·h)速度静脉泵入,同时静脉泵入生理盐水1.0 ml/(kg·h),均维持至术后12 h;曲美他嗪组:在对照组基础上,术前2 d至术后3 d口服曲美他嗪(20 mg,3次/d);尼可地尔+曲美他嗪组:在尼可地尔组用药基础上,在术前2 d至术后3 d口服曲美他嗪(20 mg,3次/d);各组中严重心力衰竭[LVEF<40%或纽约心脏协会(NYHA)心功能分级≥Ⅲ级]患者水化剂量均减半。
围手术期其他用药:患者术前常规口服氯吡格雷300 mg或替格瑞洛180 mg,术后给予双联抗血小板治疗维持1年以上;无特殊情况下,研究过程中患者常规予以降脂类药物、β受体阻滞剂及血管紧张素转换酶抑制剂等治疗冠心病相关药物,术中使用的对比剂均选用碘普罗胺注射液(优维显,碘浓度 370 mg/ml)。
资料收集及检测:记录患者一般情况,包括性别、年龄、红细胞压积、血压、LVEF、NYHA心功能分级、糖尿病史、吸烟史及PCI手术相关情况(对比剂用量、冠状动脉病变数及冠状动脉置入支架数)。各组于PCI术前清晨及术后(72±3)h各采集肘部静脉血5 ml,监测血肌酐、尿素氮、C反应蛋白及血小板平均体积(MPV)等指标。根据各组术后血肌酐峰值,统计CIN和住院期间主要不良事件(包括死亡、肾脏替代治疗、急性心力衰竭、脑卒中、再发心肌梗死)发生情况。
Mehran评分标准:糖尿病及贫血[红细胞压积<36%(女)或<39%(男)]计3分,年龄>75岁计4分,血肌酐>1.5 mg/dl计4分或估算肾小球滤过率(eGFR) 40~60 ml/(min·1.73 m2)计 2 分、20~40 ml/(min·1.73 m2)计 4 分、0~20 ml/(min·1.73 m2)计6分,心力衰竭(NYHA Ⅲ/Ⅳ级)、低血压(收缩压<80 mmHg且1天内需要至少使用1 h升压药支持或术前24 h内需要使用主动脉内球囊反搏,1 mmHg=0.133 kPa)计5分,每使用100 ml对比剂计1分[13]。基础eGFR通过简化MDRD方程计算[14]。
CIN诊断标准:按照2011年欧洲泌尿生殖放射委员会制定的标准[15]:患者接触碘对比剂后72 h内血清肌酐值较基线绝对值升高≥0.5 mg/dl(44.2 μmol/L)或相对值上升≥25%,并排除其他原因所致的肾功能损害。
统计学方法:应用SPSS 22.0软件对数据进行统计。正态分布计量资料用均数±标准差()表示,组间比较采用方差分析;计数资料以例(%)表示,组间比较采用卡方检验,若任意理论数T<5,则采用Fisher精确检验;非正态分布的计量资料用M(Q1,Q3)形式记录,组间对比应用非参数检验;各组不同时间点的对比应用重复测量的方差分析,并应用q检验进行两两比较;治疗前后比较采用配对t检验,分析药物的主效应及药物间的交互作用采用析因设计方差分析;CIN影响因素分析采用多因素Logistic回归分析;P<0.05为差异有统计学意义。
2 结果
四组患者基础临床特征和Mehran风险评分相关因子比较(表1、2):四组患者性别、收缩压、LVEF、高密度脂蛋白胆固醇、红细胞压积、吸烟史、围手术期用药、冠状动脉病变数及支架置入枚数、Mehran评分各相关因子等一般临床情况比较,差异均无统计学意义(P均>0.05)。
四组PCI术前及术后第3天相关指标水平及药物间交互作用分析:四组患者PCI术前血肌酐、尿素氮、C反应蛋白、eGFR、MPV等基线值差异均无统计学意义(P均>0.05)。四组PCI术后第3天血肌酐、尿素氮、C反应蛋白、MPV较PCI术前均增高,eGFR较PCI术前均降低,且四组间PCI术后与术前血肌酐、尿素氮、C反应蛋白、MPV和eGFR差值上的差异均有统计学意义(P均<0.05);尼可地尔+曲美他嗪组PCI术前及术后第3天血肌酐、尿素氮、C反应蛋白、eGFR、MPV的差值较对照组显著减小(P均<0.05),见表3。此外,主效应和药物交互效应分析发现,尼可地尔和曲美他嗪均能有效降低PCI术后第3天与术前肌酐差值(P值分别为0.010和0.001),且两药之间存在交互作用(P=0.036),两药联用较单一用药效果更好。
表1 四组患者基础临床特征比较()

表1 四组患者基础临床特征比较()
注:HDL-C:高密度脂蛋白胆固醇;ACEI/ARB:血管紧张素转换酶抑制剂/血管紧张素Ⅱ受体拮抗剂。1 mmHg=0.133 kPa。*:非正态分布数据以M(Q1,Q3)表示
项目 对照组 (n=208) 尼可地尔组 (n=105) 曲美他嗪组 (n=104) 尼可地尔+曲美他嗪组 (n=104) P值男性[例 (%)] 154 (74.0) 78 (74.3) 75 (72.1) 76 (73.1) 0.981收缩压 (mmHg)* 133 (130,136) 130 (127,134) 136 (132,139) 135 (131,139) 0.223左心室射血分数 (%)* 60.5 (59.4,61.5) 59 (57.7,60.4) 60.2 (59.6,60.8) 60.7 (59.4,61.9) 0.183 HDL-C (mmol/L) 1.15±1.08 1.10±0.36 1.12±0.31 1.05±0.28 0.740红细胞压积 (%) 37.67±4.17 37.49±3.80 37.15±3.83 37.14±3.82 0.599吸烟史[例 (%)] 85 (40.9) 54 (51.4) 39 (37.5) 47 (45.2) 0.179 β受体阻滞剂[例 (%)] 159 (76.4) 86 (81.9) 88 (84.6) 88 (84.6) 0.101钙拮抗剂[例 (%)] 69 (33.2) 30 (28.6) 32 (30.8) 35 (33.7) 0.826 ACEI/ARB[例 (%)] 161 (77.4) 89 (84.8) 88 (84.6) 89 (85.6) 0.180他汀类药物[例 (%)] 203 (97.6) 103 (98.1) 103 (99.0) 103 (99.0) 0.729利尿剂[例 (%)] 37 (17.8) 28 (26.7) 24 (23.1) 26 (25.0) 0.252冠状动脉病变数 (支) 2.03±0.82 2.11±0.79 2.00±0.88 2.13±0.83 0.586冠状动脉置入支架数 (枚) 1.44±0.70 1.50±0.70 1.40±0.70 1.57±0.77 0.338
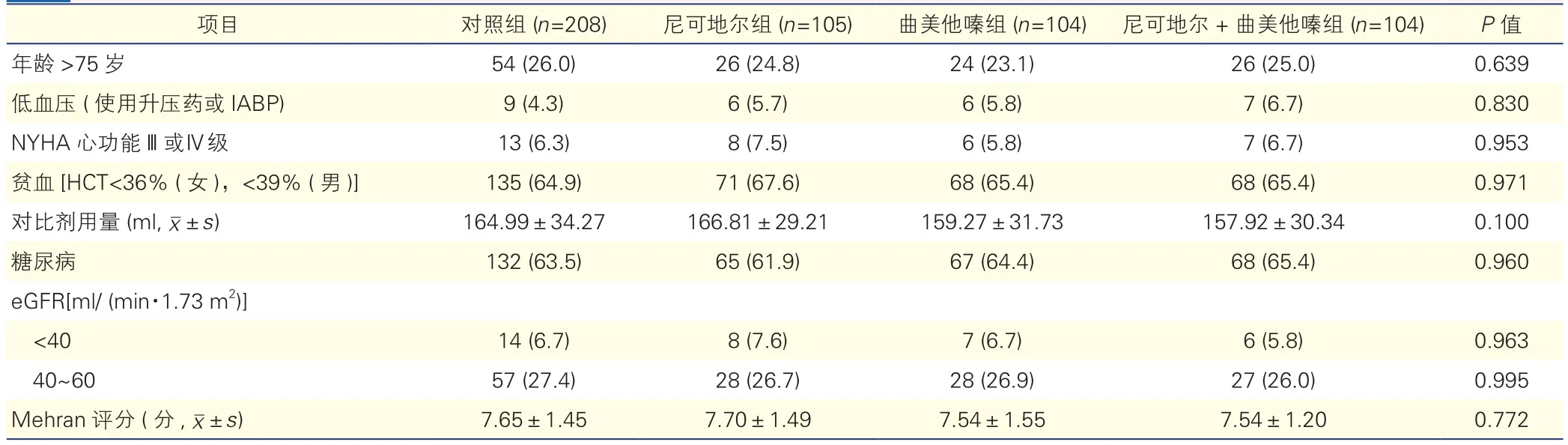
表2 四组Mehran风险评分相关因子分布情况比较[例(%)]
表3 四组经皮冠状动脉介入治疗术前及术后第3天相关指标变化比较()

表3 四组经皮冠状动脉介入治疗术前及术后第3天相关指标变化比较()
注:eGFR:估算肾小球滤过率。*:术后第3天-术前
血小板平均体积(fl)对照组 208术前96.4±25.9 6.5±1.5 65.2±13.1 0.8±0.4 10.2±2.0术后第3天 106.8±27.2 7.4±1.6 59.2±14.2 1.5±0.9 10.7±1.6差值* 10.4±20.2 0.9±1.5 -6.0±12.2 0.7±0.6 0.5±1.1尼可地尔组 105术前97.7±28.4 6.6±1.1 64.6±15.2 0.7±0.4 9.8±1.4术后第3天 101.3±24.3 7.0±1.6 62.7±12.5 1.0±0.8 9.9±0.9差值* 3.6±14.2 0.4±1.5 -1.9±9.2 0.3±0.6 0.1±1.3曲美他嗪组 104术前97.9±30.1 6.7±1.7 65.1±16.3 0.6±0.4 9.5±2.5术后第3天 102.4±30.6 7.1±1.2 62.0±14.8 1.0±0.8 9.7±2.7差值* 4.5±15.9 0.4±1.6 -3.1±11.2 0.4±0.6 0.2±2.0尼可地尔+曲美他嗪组 104术前93.5±22.9 6.3±1.1 67.6±11.5 0.7±0.4 9.6±2.7术后第3天 94.8±27.2 6.4±1.5 67.2±14.5 0.9±0.6 9.7±2.2差值* 1.3±12.9 0.1±1.5 -0.4±12.2 0.2±0.5 0.1±2.3组别 例数 血肌酐(μ mol/L)尿素氮(mmol/L)eGFR[ml/(min·1.73 m2)]C反应蛋白(mmol/L)
四组CIN及院内主要不良事件发生率比较(表4):术后3天内,对照组、尼可地尔组、曲美他嗪组、尼可地尔+曲美他嗪组依次有 17例(8.2%)、3例(2.8%)、4例(3.8%)、1例(1.0%)患者诊断CIN,四组间CIN发生率差异有统计学意义(P=0.021),对照组与尼可地尔+曲美他嗪组之间差异显著(P=0.009);25例CIN患者中,仅对照组有1例患者住院期间行血液透析治疗,其余患者于术后2周内复查血肌酐均恢复至术前基线水平,无需血液透析治疗。四组在全因死亡、需行肾脏替代治疗、急性心力衰竭、再发心肌梗死及脑卒中等事件发生率上的差异均无统计学意义(P均>0.05)。研究过程中,尼可地尔组和尼可地尔+曲美他嗪组共11例患者注射尼可地尔后出现轻度头痛症状,休息后明显好转,未出现恶心、呕吐、心悸、皮疹、皮肤和黏膜溃疡等症状。

表4 四组对比剂肾病和院内临床主要不良事件发生率比较[例(%)]
CIN影响因素的多因素Logistic 回归分析(表5):校正年龄、性别、收缩压、红细胞压积、基础血肌酐水平、糖尿病、对比剂用量及Mehran评分后,多因素 Logistic回归分析结果显示:与单纯水化治疗比较,尼可地尔联合曲美他嗪治疗是 CIN 的独立保护因素(OR=0.114,95%CI:0.015~0.880,P=0.037),而单用尼可地尔或曲美他嗪对CIN发生率均无明显影响。
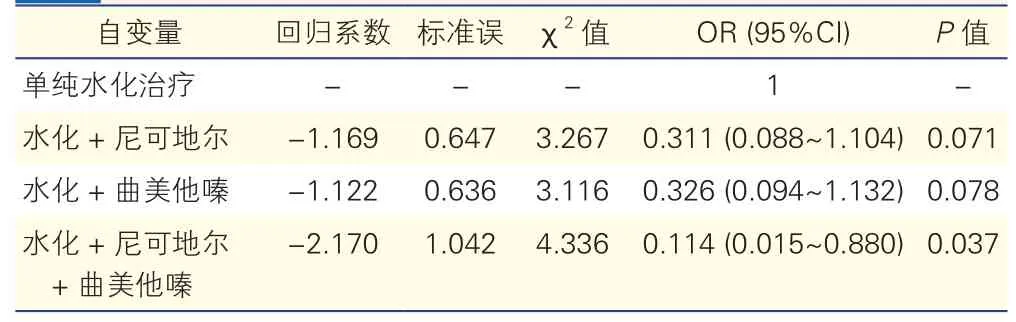
表5 对比剂肾病影响因素的多因素Logistic回归分析
3 讨论
本研究结果表明,对于接受择期PCI的中高危(Mehran危险积分≥6分)急性冠状动脉综合征患者,术前服用常规剂量曲美他嗪或静脉用尼可地尔均可降低CIN发生率,且两药联用可进一步增益,但尼可地尔与曲美他嗪对于CIN的预防作用并无明显差异。
据统计,CIN是目前院内获得性肾损伤的三大病因之一,也是PCI术后继支架内再狭窄、支架内血栓形成后的第三大并发症[16],与患者心血管不良事件及生存预后密切相关[17]。Mehran等[13]报道,在Mehran危险积分>6分的患者中CIN发生率高达14.0%。2012年含碘对比剂在心血管疾病中临床应用的中国专家共识[18]也推荐使用Mehran评分识别中高危人群。因此,对于Mehran危险积分>6分的患者,CIN的预防显得尤为重要。
目前CIN的发病机制仍不明确。近年大量研究认为,CIN是由多因素共同作用的结局,包括肾髓质缺血、直接细胞毒性损伤以及氧化应激等[1]。炎症可能参与了CIN的发病过程,临床上他汀类药物能够通过抗炎作用减少CIN发生的报道亦屡见不鲜[19];C反应蛋白及MPV是检测机体炎症反应的重要指标,近几年研究发现这两种指标也可很好地预测急性肾损伤的发生[20,21]。
临床上,目前除围手术期水化治疗外,暂无其他方案被国内、外指南推荐用来降低PCI术后CIN的发生率[15,18]。
尼可地尔是具备类硝酸酯作用的KATP通道开放剂,胞内KATP通道开放可以起到促进线粒体膜电位超极化、并抑制T型钙离子通道的开放,从而舒张微血管、抑制氧自由基生成的作用[4,5]。临床上,尼可地尔被发现可通过抑制炎症因子、改善血管内皮功能机制来显著改善微血管性心绞痛症状及运动耐量[22,23]。人体心、脑、肾、胰腺等组织均分布有KATP通道。研究表明,尼可地尔在肾脏缺血再灌注损伤中也可促进血管内一氧化氮的产生,降低胞内氧自由基生成,从而达到增加肾内血流以及减少炎症反应的作用[6]。Nawa等[8]对203例接受PCI的肾功能不全患者进行前瞻性、随机研究发现,单纯水化治疗与静脉内注射尼可地尔时CIN发生率分别为10.7%和2.0%(P<0.02),提示尼可地尔对预防CIN有显著作用。
Onbasili等[11]在慢性肾功能不全患者中通过研究发现,单纯水化组与曲美他嗪组的CIN发生率分别 为 16.6% 和 2.5%(P<0.05);Shehata等[12]也 发现,慢性肾功能不全合并糖尿病的患者PCI围手术期口服曲美他嗪与单纯水化治疗相比,不仅可减少术后心肌损伤,也有助于降低CIN发生率(P<0.05)。曲美他嗪的这一效应可能与其独特的药理学特性有关:该药属于哌嗪类衍生物,基础研究显示其具有增强心肌细胞线粒体能量利用,并且降低胞内氧中毒及钙超载产生的氧自由基,减轻细胞溶解及凋亡及血管内膜损伤等作用[24-28]。
单独口服曲美他嗪或静脉用尼可地尔对CIN的保护作用均已有国、内外研究报道,但尚未见尼可地尔与曲美他嗪预防CIN的对照或联合用药的相关研究。理论上,尼可地尔联合曲美他嗪在减少线粒体膜通透性转换孔开放以及减少氧自由基的产生等方面具有协同作用,可以进一步增强肾小管上皮细胞的能量代谢、对急性肾损伤及炎症的抵抗能力。本研究中单独用药的尼可地尔组、曲美他嗪组与对照组相比CIN发生率有所降低,且尼可地尔组术后72 h血肌酐值较术前有下降趋势,但差异均无统计学意义,可能与本研究各组纳入病例太少有关。值得注意的是,单用两药均能有效降低PCI术后第3天与术前血肌酐差值,且两药之间存在交互作用,但尼可地尔+曲美他嗪组血肌酐差值较其他三组上升最少(P<0.05),效果最好;其次,尼可地尔+曲美他嗪组CIN发生率与对照组相比也明显降低(P=0.009);多因素Logistic回归分析提示:与常规水化治疗相比,联合应用曲美他嗪及尼可地尔是CIN的独立保护因素。综上所述,两药联合较单独用药能够进一步提高对PCI术后CIN的预防作用。
MPV是常用于反映血小板活性的参数,最初用于判断出血倾向及骨髓造血功能的变化,近年来发现作为炎症细胞的血小板,甚至能直接引起炎症反应。此外,C反应蛋白也是炎症反应的敏感性标志物。因此,上述两种标志物水平升高表明机体处于促炎症状态。近年研究发现,体内上述两种标志物水平升高与急性肾损伤的发生有明显相关性[20,21]。本研究结果显示,四组患者PCI术后第3天的C反应蛋白、MPV均较PCI前升高,提示应用对比剂可产生炎症反应;尼可地尔+曲美他嗪组PCI术后第3天C反应蛋白和MPV与术前差值较对照组均减少(P均<0.05),可推测联用尼可地尔及曲美他嗪有较好的抗炎作用,其保护肾功能、预防CIN 发生的作用可能与此相关。
总之,曲美他嗪与尼可地尔不仅在心血管疾病治疗中占有越来越重要的地位,而且对中高危患者PCI术后预防CIN也具有重要意义。但由于尼可地尔及曲美他嗪用来预防CIN的给药途径及剂量仍不明确,且本研究未设置不同用药途径及不同剂量亚组,因此,无法确定PCI围手术期应用尼可地尔或曲美他嗪的最佳给药方案;此外,本研究中两种药物预防CIN均尚未得到国内、外指南或专家共识的推荐,故其对CIN的预防效果有待多中心、更大样本的随机对照研究进一步验证。
