红细胞分布宽度变化与缺血性心脏病导致急性左心室收缩功能不全的相关性研究
2018-10-30师树田孙晓东魏璐佳曹晓菁祖晓麟聂绍平
张 倩 师树田 孙晓东 魏璐佳 曹晓菁 叶 明 王 旭 祖晓麟 艾 辉 聂绍平
缺血性心脏病是冠状动脉血流与心肌需求不平衡而导致的心肌缺血性损伤为主要特征的心脏病,是诱发心力衰竭(heart failure,HF)的主要原因之一[1]。随着人口老龄化以及缺血性心脏病治疗效果的改善,使得患者的生存时间延长,发生心力衰竭的机会增加。有报道称心力衰竭患者的5年全因病死率>40%,此数据完胜很多种癌症[2]。而且即便是在药物治疗的情况下,仍然有约25%的患者存在中到重度心力衰竭的症状[3]。所以心内科医师需要一个简单,易行的临床指标对HF患者的病情及预后做出判断。
红细胞分布宽度(red cell distribution width, RDW)是红细胞体积异质性的参数,用红细胞体积分布宽度变异系数(coefficient of variation of red cell distribution width,RDW-CV),或者用红细胞分布宽度标准差(red cell distribution width standard deviation,RDW-SD)来表示[4]。红细胞生成的减少或者破坏的增加都会使其增大[5]。目前现代化的全自动血细胞计数仪能在几十秒钟内对10万个红细胞进行体积的测量,迅速得出RDW结果。
近些年来,人们发现红细胞分布宽度的增加直接与急慢性心力衰竭的严重程度相关,并进一步提出RDW是预测冠心病合并急慢性心力衰竭患者病死率的危险因素[6-11]。还有一些人认为RDW也可以预测由于心力衰竭症状加重导致的再住院率增加[7,10]。
但目前我国对此指标与心力衰竭关系的临床研究较少,我们开展此项研究,为RDW在缺血性心肌病合并急性左心室收缩功能不全中的应用提供理论支持。
资料与方法
1.一般资料 连续入选2016年1月至2016年6月,在我院急诊住院的缺血性心脏病导致急性左心室收缩功能不全的患者657例。平均年龄(74.5±12.7)岁,男性475例,女性182例。缺血性心脏病以欧洲心脏病协会2013年的诊断标准为参照[1]。
(1)入选标准:①有心力衰竭的症状和体征;②有缺血性心脏病的病史,或者客观检查有缺血性心脏病的证据;③超声心动图提示,左心室射血分数(LVEF)≤45%。
(2) 排除标准:①血液性疾病患者;②急性心肌梗死患者;③伴有肥厚性心肌病,心包炎,严重瓣膜病的患者;④严重肝、肾功能不全。肌酐清除率<30mL/min的患者。谷丙转氨酶升高3倍以上的患者;⑤肿瘤患者;⑥3个月内严重外伤,手术的患者;⑦急性感染的患者;⑧甲状腺功能异常者。
2.研究方法 入选患者记录年龄,性别,吸烟史,高血压史,糖尿病史,高脂血症史,冠状动脉旁路移植术(coronary artery bypass graft,CABG)史,经皮冠状动脉介入治疗(percutaneous coronary intervention,PCI)史等,入院即刻检查血压,心率。入院72h内检测HGB,RDW,超声心动图。
目前RDW的正常值为一定区间,一般以区间的中位数分为升高和降低。所以首先按RDW 的大小进行分组,比较两组的EF和病死率。 如果两组的EF差异有统计学意义,再将所有患者按EF值进行重新分组,以期寻找危险因素。
由于在前期计算的基础上发现以EF 35% 进行分组,两组的RDW差异有统计学意义。并且35%可以大致区分心力衰竭的严重程度,故得到结果1后,将所有病例进行重新分组。
3.统计方法 采用SPSS19.0软件包进行分析。计量资料以均数±标准差表示,组间比较采用t检验。计数资料采用例数(率)表示,应用χ2检验。将P<0.1的自变量代入回归模型,采用Logistics多因素分析缺血性心脏病导致急性左心室收缩功能不全的危险因素。应用受试者工作曲线(ROC)用于判断RDW预测急性左心室收缩功能不全的敏感性和特异性。以P<0.05为差异有统计学意义。
结 果
1.将所有患者按RDW大小分为RDW>14.5组(n=168)和RDW≤14.5组(n=489),两组进行比较。RDW>14.5组的病死率明显升高,左心室射血分数明显减低(P<0.05,表1)。
2.重新将所有患者分为EF≤35%组(n=333)和EF>35%组(n=324),两组进行比较,发现年龄,高血压病史比例,PCI史比例,脑血管病史比例,RDW值,血肌酐值,EF≤35%组明显高于EF>35%组(P<0.05)。血红蛋白水平EF≤35%组低于EF>35%组(P<0.05)。
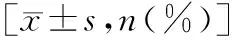
表1 两组患者病死率和左心室射血分数比较
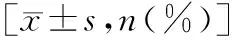
表2 两组心力衰竭患者的基线资料比较
3.将表2进行多因素Logistic回归分析后发现: 年龄,RDW,HGB,高血压史,是预测严重心力衰竭(EF≤35%)的危险因素。

表3 严重心力衰竭患者多因素Logistic回归分析结果
4. RDW诊断缺血性心脏病导致严重急性左心室收缩功能不全的界值是13.8%,其准确性是67.3%,95%CI:62.2~72.3。敏感性是57.2%,特异性是69.5%,见图1。
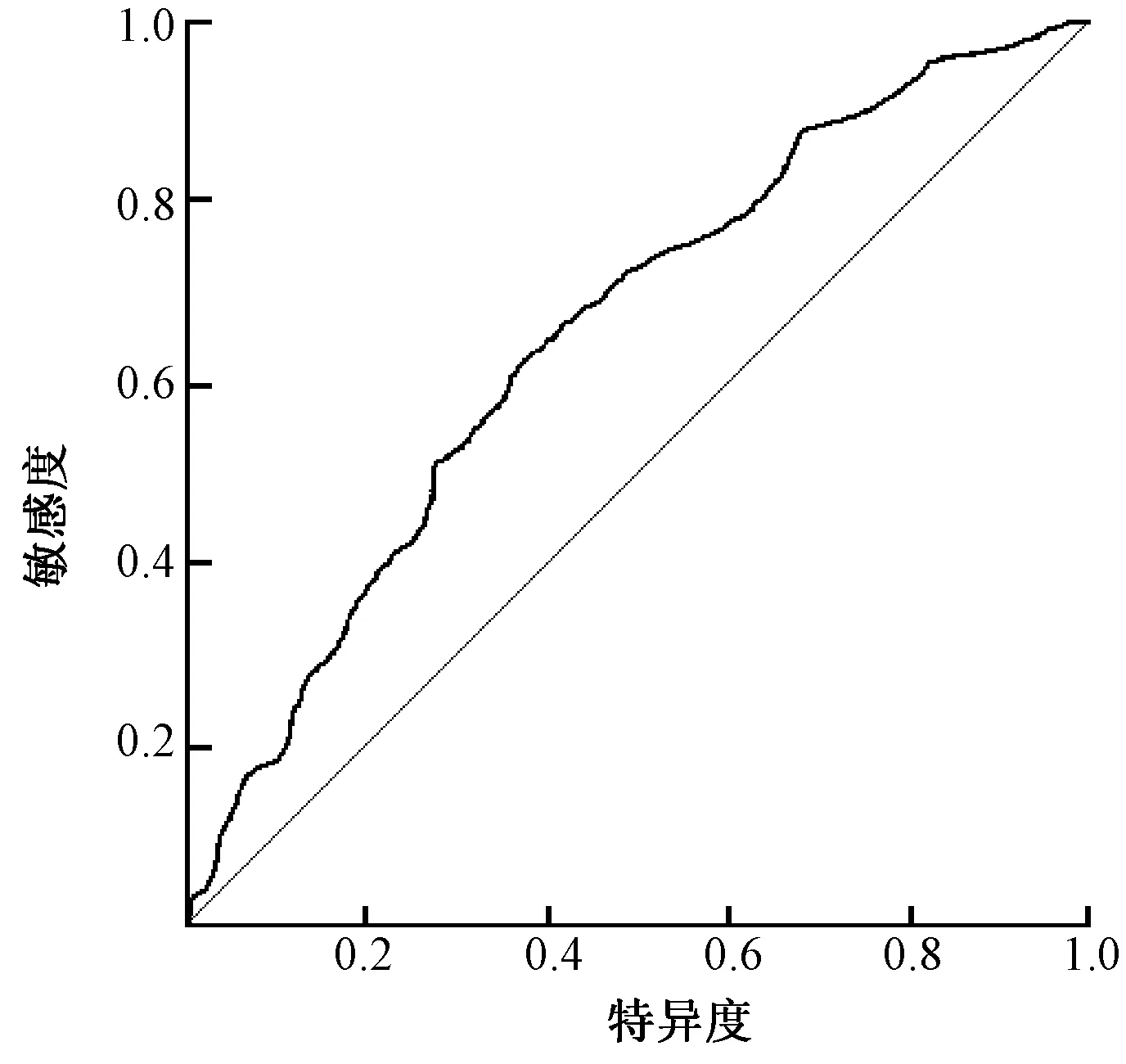
图1 RDW诊断缺血性心脏病ROC曲线图
讨 论
RDW反映红细胞体积的离散程度,临床中最常见的是维生素B12,叶酸和铁缺乏时RDW增加[12]。RDW也与其他血液疾病,肝脏疾病,肿瘤,营养不良等密切相关。
本研究结果认为红细胞分布宽度与缺血性心脏病导致急性左心室收缩功能不全的严重程度相关。这与国内外的很多研究结果是相一致的。早在2007年,Felker等就公布了著名的CHARM研究。此研究纳入了2 600多例患者,随着心功能分级(NYHA)的增加,RDW随之增加。发现RDW是慢性心力衰竭患者发病率和病死率的预测因子。RDW与患者远期病死率的紧密联系甚至超过了LVEF[6]。
此后RDW与急慢性心力衰竭相关性的研究不断涌现,Van等研究了205例急性心力衰竭患者的临床资料,发现RDW指标在这部分患者是明显升高的,而且是急性心力衰竭患者1年病死率的预测因子(HR=1.03 95%CI:1.00~1.06P=0.04)[9]。Makhoul等研究认为,在急性失代偿性心力衰竭患者中,高RDW组患者比低RDW组患者左心室射血分数明显减低,1年死亡率和再住院率均明显升高[13]。RDW与急慢性心力衰竭的严重性,以及与短期和长期死亡率相关已经得到很多证实[8,14-15]。
但是以上心力衰竭研究大都入选患者的左心室射血分数在30%~40%,严重心力衰竭(EF<30%)患者的研究较少。本研究纳入了EF<30%的患者,并且结果认为RDW是预测严重急性左心室收缩功能不全(EF≤35%)的危险因素。这在已经发布的RDW与超声指标的研究中有类似结论。OH等对100例急性心力衰竭患者RDW与超声心动图指标进行研究发现,RDW高值组(RDW>14.5%)与RDW低值组(RDW<13.2%)比较,二尖瓣早期峰值流速/二尖瓣舒张早期峰值流速(E/E’)差异明显。表明RDW可以评估急性左心力衰竭患者的左心室充盈压[16]。Mawlana等[17]也有相似研究结论。
但心力衰竭患者RDW增高的机制是什么呢?现在并不完全清楚。一般认为,①心力衰竭症状出现时,组织的缺氧和脏器的淤血导致炎症因子明显增高,炎症因子会使红细胞膜发生变形,促进红细胞的凋亡[18]。②炎症因子影响骨髓内造血细胞的功能,也会抑制肾脏促红细胞生成素(EPO)的分泌。③促使巨噬细胞对红细胞的吞噬,导致外周血幼稚红细胞的增多[19]。④炎症过程导致血液中铁蛋白功能下降,总铁结合力下降。利用铁的能力下降[20]。
在这一点上,很多人认为RDW是反映机体炎症情况的指标。比如美国第三次健康调查的数据分析显示,RDW的升高与白细胞、C反应蛋白以及纤维蛋白原有紧密联系[21]。Lippi等对数千例门诊患者的血常规指标进行分析后发现,在清除混杂因素后,RDW与高敏C反应蛋白,红细胞沉降率有正相关性。作为心血管疾病中重要炎症因子的IL-6,肿瘤坏死因子(TNF),也证明与RDW有正相关性[18,20],总之,目前研究大多认为炎症因子可能通过影响红细胞的生成,发育,寿命而影响RDW的变化。RDW也是预测炎症的可靠指标。
RDW检测成本低廉,容易取得。RDW值越高,心力衰竭患者的病情越重,远期预后越差。RDW可以协助对心力衰竭患者进行危险分层,有利于医师的早期干预,降低患者病死率。但不足之处是如同很多炎症指标一样,RDW值的变化是由多种因素引起的,不能作为心力衰竭患者的特异性指标[22]。本研究样本例数较少,随访时间短,需要进一步扩大样本量,以求为临床工作提供可靠依据。
