葛根中葛根素与大豆苷元超声提取工艺研究
2018-10-25刘馨湄
崔 颖 ,刘馨湄 ,才 凤
(1.辽宁省中医药研究院,辽宁 沈阳 110034; 2.辽宁省食品检验检测院,辽宁 沈阳 110015)
葛根为豆科野葛Pueraeia lobata(Willd.)Ohwi或甘葛藤Pueraeia thomsoniiBenth.的干燥根,为临床常用中药,《本草纲目》载其性凉、气平、味甘,具清热、降火、排毒功效。民间用葛根退热生津。葛根含12%的黄酮类化合物,如葛根素、大豆黄酮苷、花生素等营养成分,还含有蛋白质、氨基酸、糖和人体必需的铁、钙、铜、硒等矿物质,是老少皆宜的名贵滋补品,有“千年人参”之美誉[1-2]。传统的提取方法有冷浸法、加热回流法、水煎煮法、渗漉法等[3-10],但其提取速度慢、耗能,无法充分利用葛根活性物质,造成资源浪费。本试验中采用低温超声裂解法破碎细胞,加速有效成分进入溶剂,缩短提取时间,减少高温对提出成分的影响,并将有效物质释放出来,以最大限度地提高利用率。现报道如下。
1 仪器与试药
1.1 仪器
LGJ-12型冷冻干燥机(北京松源华兴科技有限公司);RE-2000E型旋转蒸发仪(河南巩义市予华仪器有限公司);BS224S型分析天平(德国赛多利斯仪器公司);JY98-ⅢDN型超声波细胞粉碎机(宁波新芝生物科技股份有限公司);LC-10P型高效液相色谱仪(日本岛津公司)。
1.2 试药
葛根药材(亳州春雷药材有限公司);葛根素对照品(中国食品药品检定研究院,批号为752-200508);大豆苷元对照品(中国食品药品检定研究院,批号为110752-200511)。所用试剂均为分析纯,供试液均按2010年版《中国药典》附录配制。
2 方法与结果
2.1 药材鉴定
葛根为豆科野葛Pueraeia lobata(Willd.)Ohwi或甘葛藤Pueraeia thomsoniiBenth.的干燥根,经辽宁省中医药研究院主任药师刘景文鉴定,符合2010年《中国药典(一部)》[11]葛根项下有关规定。
2.2 葛根素及大豆苷元含量测定
2.2.1 色谱条件与系统适用性试验
色谱柱:Spherigel C18柱(250 mm ×4.6 mm,5 μm);流动相:甲醇-水,梯度洗脱(梯度洗脱条件见表1);检测波长:250 nm;流速:1.0 mL /min;进样量:10 mL;柱温:30℃。理论板数按葛根素峰计不低于4000。色谱图见图1。
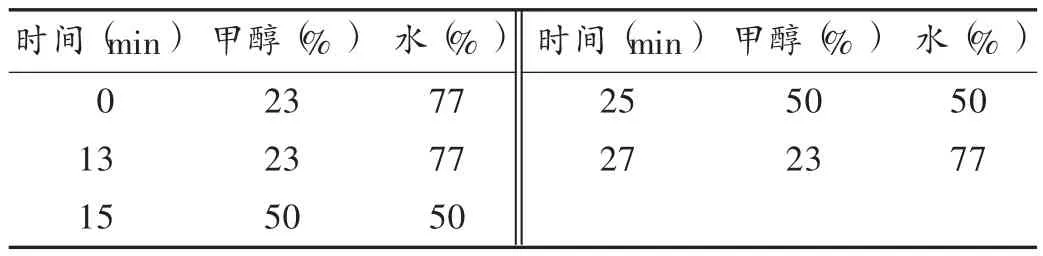
表1 梯度洗脱条件
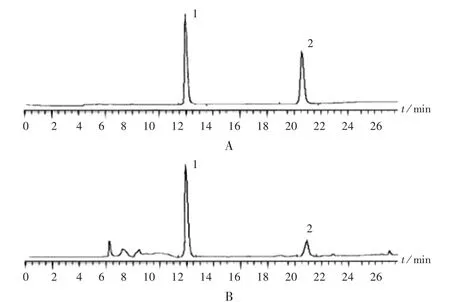
图1 高效液相色谱图
2.2.2 溶液制备
精密称取葛根素对照品和大豆苷元对照品适量,加甲醇溶解并定容至刻度,制得每1 mL含葛根素8 μg和大豆苷元10 μg的混合溶液,作为对照品溶液。
取本品粉末(过 3号筛)0.1 g,精密称定,置锥形瓶中,精密加入50%甲醇50 mL,称定质量,超声处理15 min,放冷,称定质量,用50%甲醇补足减失的质量,摇匀,0.45 μm微孔滤膜滤过,作为供试品溶液。
2.2.3 方法学考察
线性关系考察:分别精密量取对照品溶液3,5,10,15,20 μL 进样,按 2.2.1 项下色谱条件测定峰面积,以峰面积(Y)为纵坐标、进样量(X,μg)为横坐标进行线性回归,得葛根素回归方程Y=37 700 889X+7 451,R=0.9997(n=5),进样量线性范围为0.024~0.160μg;大豆苷元回归方程为Y=674 583X-403.6,R=0.999 7(n=5),进样量线性范围为 0.03 ~0.20 μg。
精密度试验:精密吸取同一对照品溶液20 μL,连续进样 6次。结果的RSD为0.76% (n=6),表明仪器精密度良好。
稳定性试验:精密吸取同一供试品溶液,分别于0,2,4,6,8,12 h 时进样,测定峰面积。结果葛根素和大豆苷元峰的RSD分别为 1.00% 和 1.10% (n=6),表明供试品溶液在12 h内稳定。
重复性试验:精密称取6份样品,依法制得供试品溶液,进样测定。结果葛根素和大豆苷元峰面积的RSD分别为0.80%和0.90%(n=6),表明方法重复性良好。
回收率试验:称取已知含量供试品粉末6份,每份0.05 g,精密称定,加葛根素对照品 0.18 mg,大豆苷元对照品 0.25 mg,按 2.2.1项下色谱条件测定并计算。结果葛根素和大豆苷元的回收率分别为99.87%和100.32%,RSD分别为 0.70%和 1.80% (n=6)。
2.2.4 样品含量测定
精密吸取对照品溶液和供试品溶液各10 μL,注入液相色谱仪,测定,结果葛根素含量为40 mg/g,大豆苷元含量为 1.06 mg /g。
2.3 提取工艺正交试验
取野葛药材300 g,破碎备用。根据野葛中葛根素的理化性质,以水作为溶剂进行超声提取,按L9(34)表进行正交试验,采用高效液相色谱法[12-14],以葛根素、大豆苷元为考察指标,以加水量(因素A)、提取时间(min)(因素B)、提取次数(因素C)为考察因素,优选葛根超声提取最佳工艺。因素水平表见表2,试验结果见表3,方差分析结果见表4。影响水提效果的因素顺序为A>C > B。查表得F0.05(2.2)= 19.00,F0.01(2.2)= 99.00,方差分析结果表明,因素A、因素B、因素C具有显著性意义,表明本试验设计较有意义。结合R水平,得出葛根素、大豆苷元最佳提取工艺为A1B3C3,即加8倍量水,每次提取30 min,提取3次。
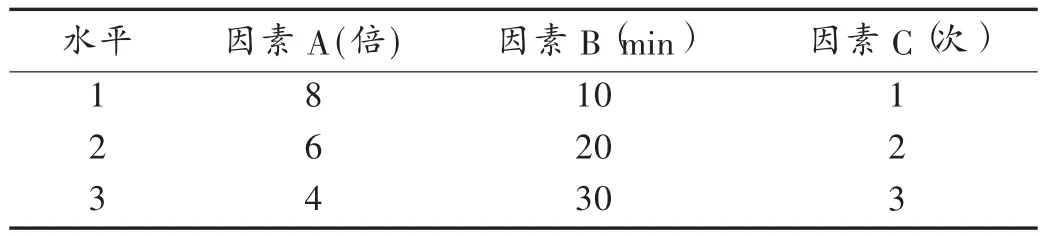
表2 因素水平表
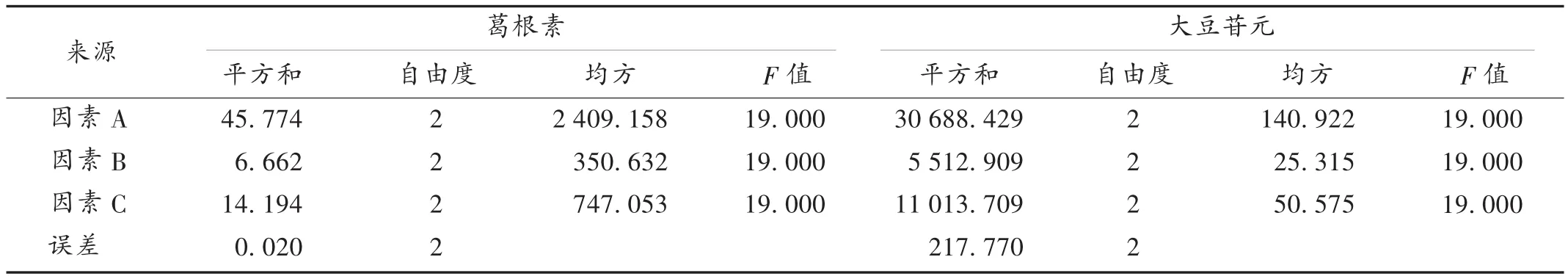
表4 方差分析表
2.4 验证试验
称取药材5份,精密称定,按最佳提取条件进行提取、浓缩,分别测定葛根素、大豆苷元总量。结果见表5。得出的数据与正交试验直观分析得出的结论相吻合,本试验中确定的水提工艺可行、稳定、合理。

表5 最佳工艺验证试验结果
2.5 葛根收率
将2.4项下的5份提取液合并,经旋转蒸发仪适当浓缩,利用冷冻干燥技术[15]进行干燥,温度为-60℃,预冻4 h,然后在程序升温曲线条件下干燥28 h,即得。计算葛根的收率为52.4%,程序升温曲线见图2。
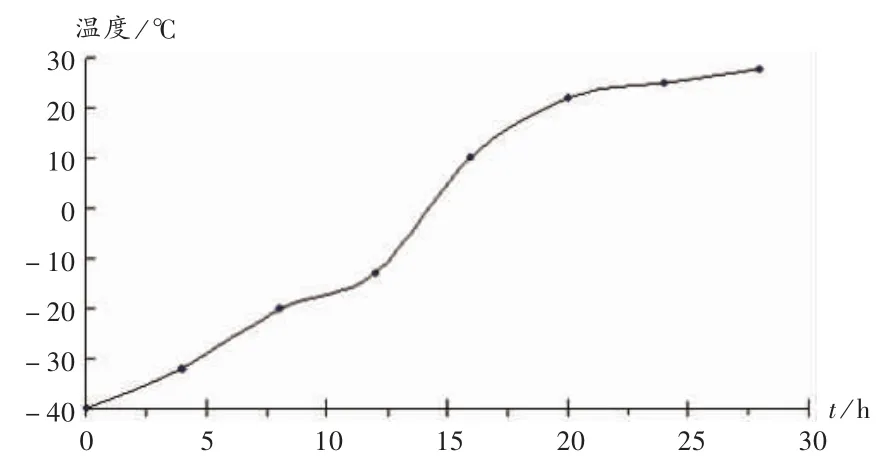
图2 葛根的程序升温曲线
3 讨论
通过单因素和正交试验,优化了超声提取的工艺条件,确定最佳提取工艺为加8倍量水,提取3次,每次提取30 min。该试验以水溶液为提取剂,成本低廉,工艺操作简单,且提取过程中未加入任何有毒物质,因此安全性较高,适于工业化生产。
关于葛根药材成分提取的研究报道很多,提取过程中影响因素很多,优化时所考虑的影响因素不同,各因素水平也不相同,同时各因素间又相互影响,因而在提取过程中要综合考虑各种因素,以保证最佳提取工艺优化的确定性。结合文献研究和预试验,本研究中以水为提取溶剂,并以低温超声的提取方式进行提取,以葛根主要化学成分和活性成分葛根素、大豆苷元的含量作为考察指标,专属性强,并采用正交试验,确定最佳提取工艺。优选的工艺简单、稳定、可行,可控性良好。本研究中采用低温冷冻干燥技术对葛根提取物进行干燥,不但脱水较彻底,且干燥后的多肽成分性质稳定,便于长时间贮存,能更好地控制温度,保护活性成分。
