双管大通道椎板间内镜术式治疗腰椎管狭窄症
2018-10-24张建军崔洪鹏付本升卢正操
丁 宇,张建军,崔洪鹏,朱 凯,付本升,卢正操,李 雯
腰椎管狭窄症(lumbar spinal stenosis,LSS)是最为常见的腰椎疾患之一,已成为老年人腰腿疼痛的重要原因,严重影响日常生活质量[1]。作为一种临床症候群,LSS病理改变复杂,多数脊柱外科医生推荐开放减压椎弓根内固定术,但老年患者常不能耐受或接受该类手术治疗[2]。近年来脊柱内镜技术快速发展,大通道内镜技术日趋成熟,有望以较为简单、微创的手术方式达到充分的硬膜囊、神经根减压,从而获得满意的LSS微创治疗临床疗效[3]。目前,有代表性的大通道内镜技术为DELTA、WOLF经椎板间减压术式,其内镜直径较椎间孔镜管径略粗,可以通过该管道使用相对较粗的手术工具进行神经减压,同时符合和遵循微创内镜手术的基本原则[4]。但大通道内镜系统存在手术视野出血多、术中磨除骨质费时费力等缺点,如何通过简单、安全的微创外科操作达到切实的椎管减压仍是亟待解决的问题。基于此,海军总医院康复医学科及脊柱微创中心提出并开展了双管大通道椎板间内镜技术,具有相对简单、可操作性强、减压彻底等特点,现将临床应用情况报道如下。
1 资料与方法
1.1 临床资料 收集海军总医院康复医学科与脊柱微创中心于2015年3月—2017年3月收治的行双管大通道椎板间内镜微创手术治疗LSS患者资料17例,其中男性9例、女性8例,年龄56~78(66.7±16.9)岁,随访时间6~24(12.5±7.3)月,所有患者均表现为不同程度的慢性腰腿疼痛、麻木等症状,病程6~38(14.7±7.1)月。均为单节段退变,其中L3-4节段2例、L4-5节段10例、L5-S1节段5例。
1.2 临床表现及体征 本组患者均有急、慢性腰肌劳损及腰腿疼痛史,并伴有间歇性跛行。腰痛伴下肢及足趾麻痛者10例、腰痛伴大腿外侧、膝内侧麻痛者2例、单纯下肢麻木者15例,其中合并有腰骶部疼痛不适者5例、下肢无力者8例、患肢发凉怕冷者13例。17例患者均有不同程度的腰背部肌肉僵硬及腰部活动度减小,脊柱侧弯者11例,胸腹部垫枕试验均阳性者9例,屈颈试验阳性者3例,直腿抬高试验阳性者7例,股神经牵拉试验阳性者5例,膝跟腱反射减弱者15例。
1.3 影像学检查 所有患者均常规行腰椎X片、CT及MRI扫描检查,结合临床症状及体征,进一步综合分析、判断引起临床症状的“责任”节段。重点观察椎间盘突出程度、后纵韧带有无钙化、小关节增生内聚情况、黄韧带肥厚及侧隐窝、椎间孔狭窄程度。
1.4 临床诊断、病例纳入与排除标准
1.4.1 LSS临床诊断标准[5]①症状与体征不符,主诉多体征少;②体位改变与症状轻重有直接关系,卧位、坐位症状减轻或消失,站立、行走症状明显;③间歇性跛行;④影像学改变参考椎管或侧隐窝间距标准,即椎管前后径<1.0~1.2 cm,侧隐窝间距<0.3~0.5 cm;⑤经CT或MRI证实有腰椎管狭窄,黄韧带肥厚大于5 mm,且判断责任节段为单节段退变。
1.4.2 病例纳入标准 ①腰椎间盘突出合并侧隐窝神经根管狭窄患者;②椎管、神经根管内明显骨性或软性压迫者;③全身情况评估可以耐受手术者;④自愿签署手术同意书,不接受开放手术治疗。
1.4.3 病例排除标准 ①合并有脊柱结核、肿瘤或节段不稳病例,应考虑开放手术治疗;②期望值过高或抑郁症患者;③全身情况差,不能耐受系统治疗者。
1.5 双管大通道椎板间内镜手术方法 联合应用显微椎间盘镜(microendoscopic discectomy,MED)手术工作通道及操作水介质脊柱内镜微创手术设备。
1.5.1 工作大通道建立 患者取俯卧位,暴露腰背部并适当前屈。在术中X光机透视下确定病变腰椎节段的体表投影,取责任节段椎板间隙旁开1 cm为进针点及切口中心。0.5%利多卡因局部麻醉,由皮肤逐层直至椎板及关节突关节。切开约2 cm纵行切口,深度至深筋膜,使用MED手术用逐级扩张套管达椎板骨面,放置大通道工作套管。
1.5.2 建立椎板间镜工作通道,完成初步椎管减压
于大通道内再次植入椎板间镜通道,管中套管即双管操作,是为双管大通道椎板间内镜术式技术关键。细套管置入方法同椎间孔内口入路(medial foraminal decompression,MFD),单侧入路双侧置管减压。①神经探子定位椎板间隙外侧角,置入导向扩张器并再次确定位置,随之沿导向器置入舌形套管,其斜面紧贴同侧关节突关节内侧缘。应用环踞锯除关节突内侧局部增生骨质及黄韧带附着点,透视监测达椎间孔内口及椎间隙后缘(图1A/C)。②退出导向器及舌形细套管,于棘间韧带及黄韧带间隙向对侧进入,术中透视引导,使得舌形套管斜面紧贴对侧关节突关节内侧面,同样应用环踞锯除对侧关节突内侧局部增生骨质及黄韧带附着点,达对侧椎间孔内口及椎间隙后缘(图1B/D)。整个操作过程中须与患者交流,确定腰骶部及下肢无疼痛麻木等不适主诉。
1.5.3 水介质椎板间镜下减压操作 连接水介质椎板间镜(椎间孔镜)、光源和成像系统,于细套管内操作行对侧及同侧椎管减压(图1E/F/G/H)。镜下清理术野,咬除肥厚增生黄韧带,取出环踞磨除后剩余的骨质,同时磨除神经根腹侧增生的骨质,必要时使用髓核钳摘除突出的间盘,镜下观察到神经及硬膜囊恢复自主搏动,完成二次减压。最后,利用大通道内可以随意摆动放置细套管的优势,针对MFD尚未达到的上位下椎板缘及下位上椎板缘进行镜下咬除减压操作,扩大不同层面的椎管及神经根管,完成最终减压。

图1 双管大通道椎板间内镜术式治疗LSS
1.6 神经功能及临床疗效评定
1.6.1 神经功能评定 包括视觉模拟评分法(Visual Analogue Scale/Score,VAS)、腰椎疾患日本骨科协会评估治疗(Japanese Orthopaedic Association,JOA)评分、Oswestry功能残障量表(Oswestry Disability Index,ODI)及SF-36生活质量量表评定。患者术前、术后即刻、术后6个月及末次随访时段,分别予以评估,计算、记录相应分值。
1.6.2 临床疗效评定标准 结合Nakai标准[6]及JOA评分改善率进行疗效评估,改善率=(末次随访时评分-术前评分)/(29-术前评分)×100%。优:腰痛及下肢放射疼痛、麻木、跛行等症状完全消失,改善率等于或大于75%;良:显效,症状、体征基本消失,长时间活动后疼痛出现,改善率介于50%~75%;可:症状、体征有明显改善,负重或激烈活动后疼痛加重,改善率介于25%~50%;差:症状、体征无改善,改善率低于25%。
1.7 统计学处理 应用SPSS 19.0软件,计算临床治疗优良率所占百分比,VAS、JOA、ODI及SF-36分值以均数±及标准差(±s)表示,神经功能评分比较采用配对设计资料均数t检验,以P<0.05为差异有统计学意义。
2 结果
2.1 微创手术前后各项评分 双管大通道椎板间内镜术后评估神经功能恢复情况,显示VAS、JOA、ODI及SF-36大部分项目分值均能维持在较满意水平,与术前相比差异有统计学意义(P<0.05),术后6个月及末次随访显示临床症状均有较满意改善,腰腿疼痛缓解、生活质量改善、社会活动适应性增加。 见表1、表2。
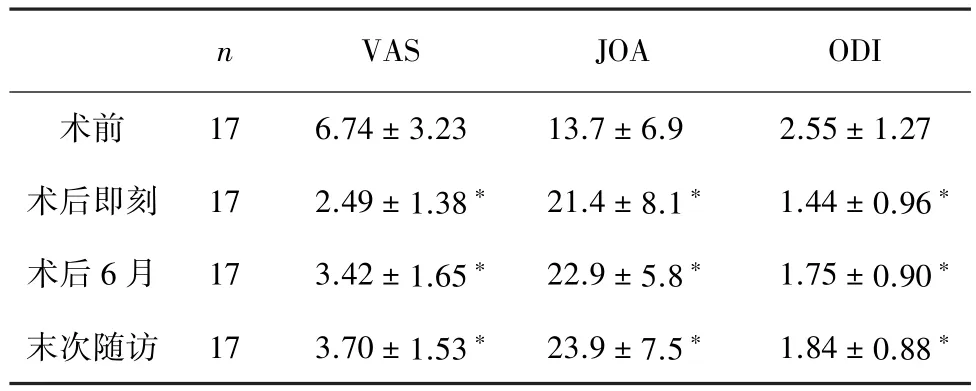
表1 LSS患者双管大通道椎板间内镜术式治疗各项评分(VAS,JOA及ODI分值)
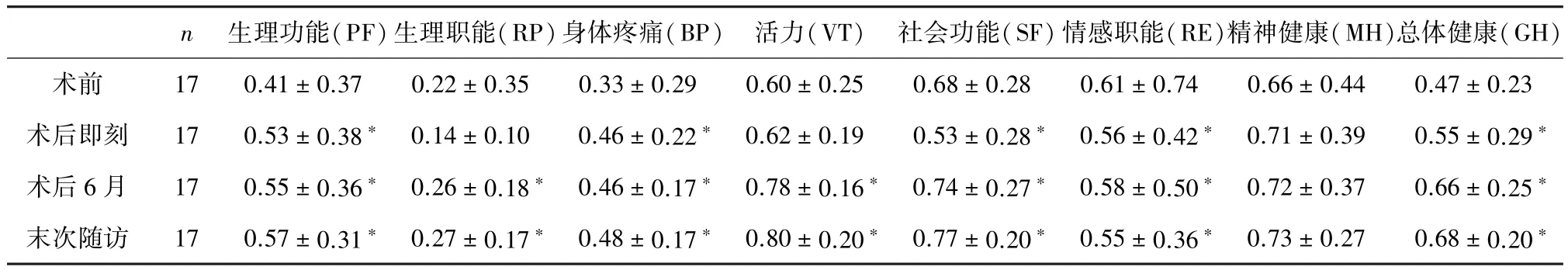
表2 LSS患者双管大通道椎板间内镜术式治疗评分(SF-36分值)
2.2 手术后临床疗效评定 双管大通道椎板间内镜术后半年随访评定:优4例、良8例、可4例、差1例,治疗优良率达70.59%。末次随访评定:优4例、良10例、可3例、差0例,治疗优良达82.35%。
2.3 不良反应及并发症 2例患者术后3 d出现根性症状加重,考虑为术中神经根干扰或炎性刺激,局部封闭后缓解。1例患者术后腰骶部发生酸胀不适伴大便力量减弱,考虑为马尾神经刺激所致,经康复治疗,术后4周缓解。1例高龄严重LSS患者,术中接近完成椎管减压时出现类脊髓高压症,及时结束手术,45 min后缓解。不良反应率为23.53%,未出现硬膜囊撕裂、神经根损伤等严重并发症。
3 讨论
人类年龄超过60岁以上时较易发生腰椎骨质增生、椎间隙狭窄等退变老化现象,椎间三关节复合体解剖结构改变、力平衡失调和髓核突出物理化学的慢性刺激是LSS的基本病理改变[7]。椎管管径变小造成神经受压,椎管内静脉压力增高,继而出现组织炎性水肿、粘连及马尾神经缺血、神经根炎等一系列病理改变,临床症状顽固,一般不为药物或保守治疗所缓解[8]。经后路椎板切除或开窗减压仍是经典的临床术式,可同时解除黄韧带肥厚、小关节增生内聚及椎间盘突出压迫,中远期疗效肯定[9]。腰椎间孔镜微创手术治疗可避免开放手术所致医源性节段不稳、融合内固定节段丧失、相邻节段退变、内置物松动断裂、异物反应、感染等风险[10],但较难达到传统意义上的硬膜囊神经根周围360°彻底减压,只是针对单纯侧隐窝狭窄或伴有椎间盘突出的病例有确切疗效。利用大通道内镜技术,选择传统腰椎后方椎板间隙入路,可有效解除范围较大的中央管狭窄或者双侧侧隐窝狭窄,借助管道打开狭窄椎管,减压同侧神经根后潜行进入到椎管中央和对侧进一步神经根减压。
但作者认为目前应用大通道技术治疗LSS多为理想化的设计,与现实临床操作仍存在一定偏差。MED技术较为成熟,LSS椎管减压彻底,疗效肯定;但操作介质为空气,MED术中视野出血较多,重要结构相对显示不清晰,熟练的小切口单椎板技术和MED陡峭的学习曲线限制了该技术的广泛应用。大通道手术同样符合和遵循微创内镜手术的基本原则,较少切除腰椎骨性结构,不会影响到节段稳定性,水介质内镜技术具有术中视野清晰、减压较为彻底等优点,但事实上仍存在实施减压时间过长、操作较为困难、器械容易折断损坏等不足。
为突破LSS微创治疗瓶颈,双管大通道椎板间内镜术式的形成经过几个阶段:①在团队使用内镜早期,针对重度LSS或巨大脱垂型腰椎间盘突出症,应用后正中入路有限切开联合水介质内镜减压术式(图2)。首先通过3 cm左右开放手术切口,剥离椎旁肌、显露椎板间隙,继而放置内窥镜,行镜下椎板开窗、椎管减压,基于解剖结构放大及水介质冲洗,视野较为清晰,手术安全、可靠。但是,该术式存在创伤相对较大、周围肌肉组织水肿等问题,术后康复时间相对较长。②团队提出MFD减压术式[11],自椎板间隙外侧角向外上方向减压,达椎间孔内口及椎间隙平面,行程过程中可同时部分打开侧隐窝,可有效治疗合并有侧隐窝狭窄的腰椎退变病例。该技术融合了传统椎板开窗及内镜操作的优势,但由于减压范围所限,术后复查发现严重LSS后方上下椎板平面减压不甚理想,因此多平面、大范围减压仍显不足。③MED联合水介质内镜术式,结合水介质内镜手术视野清晰、安全、易操作及MED减压范围广的优点,先行大通道打开手术视野,其次在水介质内镜辅助下进行重要结构辨认及神经根减压,最后应用MED技术进行扩大减压(图3)。该术式较为安全可靠,避免了MED出血多、视野不清晰等缺点,但两种类型内镜交替使用较为繁琐,同时内镜下减压仍较为费时费力。④双管大通道椎板间内镜术式,应用MED大通道打开手术视野,使得接下来细套管辅助内镜操作灵活摆动,可以实现有效、多平面减压,同时大通道有助于防止周围组织水肿,利于术后快速康复。另外,MFD操作较为简单、有效、省时省力,可较快完成椎管内主要部位的减压,同时利用大通道内灵活置管的优势,对于MFD易忽视区域如神经根管内口进行有效减压,解决了MFD置管减压过程中“灯下黑”的问题。
与传统椎板开窗手术相比,双管大通道椎板间内镜术式切口小(<2 cm),且钝性剥离椎旁肌肉损伤更小,较好地保护了腰大肌、多裂肌、半棘肌等椎旁深层稳定肌,减少了椎旁肌肉去神经化及去血管化发生率,有利于术后康复[12-13]。双管大通道椎板间内镜术式应用舌形套管及环锯组合,术中影像实时监护磨除部分椎板及增生关节突关节,结合与局麻状态下患者的良好沟通,可有效避免神经损伤。水介质镜下操作进一步完善椎管减压,避免了常规开放手术中因出血所致视野不清的缺点,同时冲洗作用有利于减少术后感染的风险。
应用双管大通道椎板间内镜技术治疗LSS病例数尚少、临床随访时间亦短,临床经验有待丰富,期望多中心、远期随访提供充分佐证。腰椎微创手术优势在于疗效明显、创伤小、并发症少、不会对后续治疗产生影响,双管大通道椎板间内镜术式仍不失为有意义的临床探索。双管大通道椎板间内镜的技术创新在于证实了大通道双管联合水介质操作的可行性,使得多平面、后中柱椎管减压更为便捷,脊柱外科医生易于理解掌握、学习曲线较为陡峭。但相对于常规脊柱内镜微创技术,双管大通道椎板间内镜术式创伤仍显较大,主要适应症为中老年发育性或重度LSS。对于75岁以上的高龄、超高龄LSS患者,则建议予以“立体微创”治疗或行内镜下神经根腹侧减压,以有效改善患者生活质量、减少合并症为主要目的[14-15]。
总之,应用双管大通道椎板间内镜术式针对LSS实施靶点治疗,可操作性强、减压彻底,具有“精准、精巧、精细”特点,短期随访疗效肯定,一定程度上克服了腰椎退变疾病的微创治疗难点。

图2 小切口联合操作水介质内镜行椎管减压术
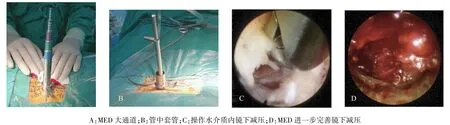
图3 MED联合操作水介质内镜行椎管减压术
