胃食管早期多原发肿瘤12例分析
2018-10-23王沧海刘揆亮
王沧海 吴 静 刘 红 刘揆亮 宿 慧 魏 南
(首都科医科大学附属北京世纪坛医院消化内科 首都医科大学消化病学系,北京 100038)
随着人群保健意识的增强和消化内镜诊治技术的进步,早期肿瘤及癌前病变明显增多,消化道多原发癌也变得更加常见,早期发现第二原发癌并进行根治性治疗,有助于提高患者生存率和生活质量,因此如何认识多原发癌的特征十分重要。本文选取2008年1月至2018年6月于首都科医科大学附属北京世纪坛医院行胃镜检查的患者,发现12例胃食管多原发肿瘤患者,总结如下。
1 对象与方法
1.1 研究对象
2008年1月至2018年6月期间本院消化科完成胃镜诊治55 831例,其中胃恶性肿瘤358例,食管癌201例,胃食管早癌68例,胃食管多原发肿瘤12例(男性10例,女性2例,年龄58~76岁)。
1.2 诊断标准
采用Moertel标准[1]:①各病灶在病理学上证明为恶性或高级别瘤变,且非转移或直接浸润所致;②所有病灶均有正常组织相隔离;③以起病的病灶或最大的病灶为主病灶, 其他病灶全部为副病灶。一般肿瘤发生时间间隔≥6个月称为异时性多原发癌,相隔< 6个月为同时性[2]。
1.3 统计学方法
2 结果
2.1 患者一般资料
12例上消化道多原发肿瘤患者就诊主诉包括上腹胀4例,嗳气2例,反酸1例,纳差2例,上腹痛2例,黑便2例。其中同时性癌9例,异时性癌3例,发病间隔时间分别为19个月、3年、7年。同时期单发胃食管早癌患者68例,其中男性47例,女性21例,年龄42~84岁。
2.2 胃镜下表现
同时性癌9例,共19处癌灶,2个癌灶者8例,3个癌灶患者1例,第一病灶12例中9例为进展期癌。第二病灶12例中10例为早癌及高级别瘤变。第一病灶最大直径5cm,最小0.5 cm,平均(2.35±1.31)cm,第二病灶最大直径3 cm,最小0.3 cm,平均(1.42±0.79)cm。详见表1。

表1 单发胃食管早癌与多原发胃食管癌临床特点比较Tab. 1 Comparison of clinical features between multifocal gastroesophageal neoplasms and single gastroesophageal neoplasms
3例异时性癌患者中,第1例患者肿瘤诊断间隔19个月:第一原发肿瘤为胃底低分化腺癌,异时原发肿瘤为食管中段重度不典型增生。第2例患者肿瘤诊断间隔3年:第一原发肿瘤为贲门低分化腺癌,异时原发肿瘤为胃体溃疡中分化腺癌。第3例患者肿瘤诊断间隔7年:第一原发肿瘤为胃窦低分化腺癌,异时原发肿瘤为贲门高中分化腺癌。
与同时期68例单发胃食管早癌患者相比,多原发癌患者的性别、年龄差异均无统计学意义。病灶位置均以远端胃最多见,单发早癌位于远端胃者30例,多原发癌者,第一病灶和第二病灶位于远端胃均为4例,其次为近端胃和食管。单因素方差分析病灶大小,多原发癌病灶与单发早癌病灶之间差异具有统计学意义(P=0.037),第一病灶(2.35±1.31)cm显著大于单发早癌病灶(1.57±1.15)cm(P=0.036),第二病灶(1.42±0.79)cm与单发早癌病灶大小之间比较,差异无统计学意义(P=0.242)。第一病灶、第二病灶及单发病灶的分化程度分布差异有统计学意义(P=0.011),单发早癌分化程度最高。
2.3 内镜漏诊情况
9例同时性癌的患者,5例正确诊断,其余4例,初次内镜诊断仅发现了进展癌而漏诊早癌2例,其中1例漏诊病变位于食管(图1),1例漏诊病变位于胃底(图2),均于外科术后3个月复查胃镜时发现。初次内镜诊断同时发现了两处病灶者2例,但是副病灶初次病理仅提示低级别瘤变,处理主病灶后每2个月复查胃镜并活检副病灶,1例7个月后、1例19个月后病理提示高级别瘤变(图3)。
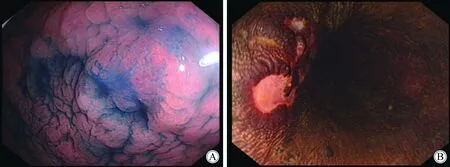
图1 食管与胃窦同时多原发肿瘤Fig.1 Synchronous cancer at esophagus and gastric antrum

图2 胃窦与胃底同时多原发肿瘤Fig.2 Synchronous cancer at gastric antrum and fundus
A:Main tumor at gastric antrum was low differentiated adenocarcinoma;B:Gastric fundus was high differentiated adenocarcinoma.
2.4 治疗及预后
9例同时性多原发肿瘤患者,主病灶外科手术6例,内镜黏膜下剥离术(endoscopic submucosal dissection, ESD)3例;副病灶外科手术2例,ESD 6例,1例外院就诊。
3例异时性癌患者第一原发肿瘤均外科根治手术。 1例异时原发肿瘤接受ESD治疗,1例外科手术,随访时间6个月至6年,仍存活。另1例第一原发肿瘤胃底低分化腺癌,发现异时原发肿瘤(食管高级别瘤变)时已经全身肿瘤多发转移状态,未处理食管病变,2个月后死亡。
3 讨论
随着内镜检查技术及成像清晰度、放大倍数的提高,越来越多上消化道肿瘤得以早期诊断,并通过ESD 等技术得到早期治疗,最大程度保留原有解剖结构,提高患者生活质量,延长患者生存期。文献[3]报道,多原发癌以消化道肿瘤为第一位,其中又以胃癌居多,肿瘤的产生是由于抑癌基因发生突变,原癌基因激活成致癌基因,癌细胞不断增生,最终导致肿瘤的发生。肿瘤患者一旦出现第一肿瘤,发生第二原发癌的风险很高[3],因此医生应该加强对多原发肿瘤的认识,对于已发现一处病灶的患者,更应详细检查,排除其他同时发生的病灶。

图3 胃窦与贲门下方同时多原发肿瘤Fig.3 Synchronous early cancer at gastric antrum and cardia
日本Ribeiro等[4]的研究显示,在553例胃癌患者中发现了19例同时多原发癌,第二病灶多为早期肿瘤,本研究结果与此相似,第二病灶12例中10例为早癌及高级别瘤变,与单发早癌的形态大小无差异,易于漏诊。孙洁等[5]统计食管外原发肿瘤,其中以胃癌最常见(55.2%)。Urabe 等[6]发现36%的异时性多原发食管鳞癌第二病灶出现在首次病灶的同一节段,食管病灶集中出现于中段,胃部以贲门部及上1 /3 胃体常见[7]。首都科医科大学附属北京世纪坛医院近10年诊断的胃肿瘤患者358例,食管癌患者201例,多原发癌12例,第二病灶位于胃上部1/3及食管的达5例,而且漏诊的2例患者第二病灶均位于胃底。张培趁等[8]曾报道漏诊率可高达30%。本研究显示多原发肿瘤第一病灶大小大于单发早癌(P=0.036),而第二病灶大小与单发早癌差异无统计学意义(P=0.242)。分析可能是因为多原发性胃食管癌第二病灶多为早癌, 病灶小, 浸润表浅,容易漏诊。若主癌灶与副癌灶相距较近,则即使漏诊,手术仍有可能切除干净, 若相隔较远, 则可能因手术切除范围不足而残留,造成患者二次手术的痛苦。
日本学者[9]随访175 例多原发胃癌患者,发现第一肿瘤术后6个月内随访胃镜,可帮助检出19%的漏诊癌。合理的内镜随访方案是异时多原发癌的最佳预防及治疗方法,严格的内镜随访使得96.6%的第二肿瘤可早期发现,得以内镜下切除,从而其生存期较独立肿瘤发生患者差异无统计学意义。朱一苗等[10]报道了1例8年间先后胃食管发现5处腺癌、鳞癌及不典型增生的患者。此外,李小毅等[11]的统计显示,同时或异时发生胃癌以外恶性肿瘤也不少见,以结直肠癌最多,占 27.43%(31/113),肺癌其次,占 15.04%,因此胃癌治疗时需注意同时合并其他器官原发癌的可能。必要时结合磁共振等其他影像学检查手段[12-13]。
卢戈液食管染色及卢戈液联合内镜窄带成像术(narrow band imaging,NBI)进行观察比单独应用白光及NBI 更易检测出食管病变,尤其是食管早癌[14]。配合化学染色(如靛胭脂)、放大内镜、NBI[15]等手段可显著提高早期胃肠肿瘤检出率。因此内镜医师要有发现早癌的强烈欲望,结合现在先进的内镜技术及必要的化学染色方法,提高同时多原发癌的发现率。
