杜氏盐藻LYCB基因克隆及在盐胁迫下的表达分析
2018-10-22安茜周雅莉宋亚楠岳敏赵熙宁王计平李润植
安茜,周雅莉,宋亚楠,岳敏,赵熙宁,王计平,李润植
(山西农业大学 分子农业与生物能源研究所,山西 太谷 030801)
杜氏盐藻(DunaliellaSalina) 是一种无细胞壁,可以在高盐、高温条件下生存的光合自养的单细胞真核绿藻,是迄今为止发现的最耐盐的生物之一[1]。它能高水平富集类胡萝卜素,糖类及油脂等,可作为天然的优质保健品,具有较高的营养价值和商业价值。尽管对杜氏盐藻耐盐机制和类胡萝卜素等天然产物的代谢机理进行了诸多研究,但类胡萝卜素生物合成及其调控网络还有待深入解析[2,3]。
类胡萝卜素是一种天然色素,广泛分布于微生物和植物光合组织中[4]。它是一种含8个异戊二烯单位的四萜类化合物, 由2个二萜缩合而成[5]。植物类胡萝卜素生物合成的前体物质为异戊烯二磷酸(isopenteny diphosphate, IPP)[6~8]。IPP可在内质网上由乙酰CoA经羟甲基戊二酰-CoA途径(mevalonate, MVA)合成, 更多的是在质体内由磷酸甘油醛与丙酮酸经2-C-甲基-D-赤藓糖醇-4-磷酸途径(2-C-methyl-D-erythritol-4-phosphate, MEP)合成[6~8]。形成的IPP经多次缩合生成第一个类胡萝卜素即八氢番茄红素(phytoene),再经脱氢、环化、羟基化、环氧化等生物化学反应转变为其它类胡萝卜素。
番茄红素(lycopene)环化是植物体内类胡萝卜素生物合成途径中的一个重要部分,它是由番茄红素 β-环化酶(lycopene β-cyclase, LYCB)和番茄红素 ε-环化酶(lycopene ε-cyclase,LYCE)共同催化[9]。在合成β-胡萝卜素时,LYCB经过2次催化反应将番茄红素先转化为γ-胡萝卜素,然后再生成β-胡萝卜素(β-carotene)。在合成α-胡萝卜素时,番茄红素先在LYCE催化下,生成δ-胡萝卜素,然后再在LYCB催化下,生成α-胡萝卜素(α-carotene)。但是,在莴苣中有一种特殊的LYCE,可以将番茄红素催化生成ε-胡萝卜素[10]。Stickforth等在蓝细菌中分离并鉴定了一种新的环化酶,可催化形成β-环和ε-环,将番茄红素催化生成α-胡萝卜素[11]。
番茄红素β-环化酶(LYCB)是β-胡萝卜素合成途过程的关键酶之一,其在基因转录活性水平上影响着上游番茄红素和下游β-胡萝卜素等产物的积累。Moreno等发现超量表达DcLCYb1胡萝卜中β-胡萝卜素显著提高,而沉默DcLCYb1时会降低β-胡萝卜素的含量[12];柑橘中LCYB表达量下调会导致番茄红素的积累[13~15]。因此,本研究选用从运城盐湖中分离获得的一株生长较好,β-胡萝卜素含量较高的杜氏盐藻株系Ds-YC011为试验材料,通过高保真PCR扩增,获得DsLYCB基因的cDNA克隆,并应用生物信息学手段分析该酶蛋白理化性质。同时,采用实时荧光定量PCR技术分析在高盐(3 mol·L-1NaCl)胁迫下,DsLYCB的表达模式,进一步测试了藻细胞中β-胡萝卜素含量的变化。本文为进一步研究DsLYCB的功能及作用机制奠定了基础。
1 材料与方法
1.1 试验材料
1.1.1 藻种及培养
杜氏盐藻(Dunaliellasalina)株系Ds-YC011由山西农业大学分子农业与生物能源所从山西运城盐湖分离和保存。盐藻培养基为DM培养基,25 ℃,1 250 lx光强,光暗比1∶1,每天摇瓶2~3次。RNA 提取试剂Trizol 购自 Invitrogen 公司,AMV 第一链 cDNA 合成试剂盒为abm试剂盒,凝胶回收试剂盒和质粒DNA提取试剂盒购自北京天根生物公司。
1.2 试验方法
1.2.1 杜氏盐藻总RNA的提取
取生长至对数期的本地盐藻,收集藻细胞,按照Trizol法提取盐藻总RNA。-80 ℃保存,备用。
1.2.2 杜氏盐藻LYCB基因的扩增
参考abm试剂盒使用方法进行操作。用经过浓度和纯度测定后的总RNA作为模板,反转录的反应体系参照说明书,反应条件:25 ℃,10 min;42 ℃,15 min;85 ℃,5min,得到的cDNA用于后续实验。依据 GeneBank 中杜氏盐藻(D.salina)DsLYCB基因转录本序列 (EU327 876.1)设计扩增全长的引物LYCB-F:5’-CGCGGATCCATGCAGGCCCTGCAGCAA-3’和LYCB-R:5’-CCCAAGCTTTCAACTTTTTTGTCCTTGCG-3’。高保真RT-PCR 反应采用Pfu DNA Polymerase 酶,反应体系参照说明书,反应条件为:95 ℃预变性5 min,58 ℃退火30 s, 68 ℃延伸2 min 30 s,30 次循环,68 ℃ 保温 15 min,16 ℃ 15 min。将所有扩增片断纯化回收后连接到PMD18-T 载体上,转入感受态大肠杆菌DH5-α中,筛选出阳性克隆,提取质粒DNA送通用生物公司(安徽) 测序。
1.2.3DsLYCB的生物信息学分析
将上述获得的序列在NCBI-ORF(Open Reading Frame,ORF)中查找其开放阅读框并将核酸、氨基酸进行比对[16]。通 过 ExPASy-ProParam 工具(http://www.expasy.ch/tools/protparam.htmL)对该蛋白质进行基本的理化性质分析。利用ProtScale对该蛋白序列进行亲水性/疏水性分析。利用SOPMA软件(https://npsa-prabi.ibcp.fr/cgi-bin/np)预测并分析蛋白质的二级结构,采用SWISS-MODEL(https://swissmodel.expasy.org/repository/)同源建模数据库对该蛋白进行三级结构预测[17]。应用 CBS预测信号肽、转运肽及其跨膜结构域[18,19]。利用MEGA 7.0 软件采用NJ 法构建系统进化树[20]。
1.2.4 荧光定量RT-PCR(qRT-PCR)分析
向正常条件(1.5 mol·L-1NaCl)培养至对数生长期的盐藻培养液中添加固体NaCl,使其终浓度达到3 mol·L-1,在25 ℃下进行培养。分别提取高盐胁迫0 h(对照)、1、4、12、24 h 的盐藻的总RNA。3个生物学重复提取藻细胞总RNA。用核酸浓度仪测定提取的总RNA 的纯度和浓度。取各RNA 样品2 μL用于反转录。DsLYCB基因荧光定量引物为:LYCB-F:5’-TGCAAATGCTCTTTGTCCTG-3’和LYCB-R:5’-CCCTGTCTGCGTAGTCATCA-3’,18 S内参引物为:
N-1∶5’-TTGGGTAGTCGGGCTGGTC-3’,N-2∶5’-CGCTGCGTTCTTCATCGTT-3’[21]。荧光定量PCR反应体系为:Eva Green 2X qPCR 反应液5 μL,上下游引物各0.3 μL,cDNA 模板0.5 μL,ddH2O 3.9 μL。反应条件为:95 ℃预变性10 min;95 ℃变性15 s,57 ℃退火1 min,40个循环。反应结束后确认扩增曲线和融解曲线。采用2-ΔΔCt法计算DsLYCB基因的相对表达量含量[22]。通过SPSS 软件对所得数据进行统计分析。
1.2.5 杜氏盐藻类胡萝卜素的提取及其含量的测定
经高盐处理后的杜氏盐藻,分别取胁迫0 h(对照)、1、4、12、24 h的藻液20 mL,采用周静等人[23]的方法提取类胡萝卜素并测定其含量。
2 结果
2.1 杜氏盐藻LYCB基因克隆
对源于盐藻藻株Ds-YC011藻细胞cDNA进行高保真RT-PCR扩增目标cDNA, 扩增产物电泳分离结果(图1)显示,RT-PCR反应扩增出一条长度约为1 970 bp的目标条带。经测序获得1 910 bp的核苷酸序列。编码区序列与NCBI GeneBank 中杜氏盐藻LYCB基因(EU327 876.1)序列比对结果表明,从Ds-YC011盐藻株系扩增的DsLYCBcDNA克隆与GeneBank中录入的杜氏盐藻LYCB基因核酸序列有4%的差异,但推测的氨基酸序列无差异。这表明分离获得了正确的DsLYCBcDNA克隆。
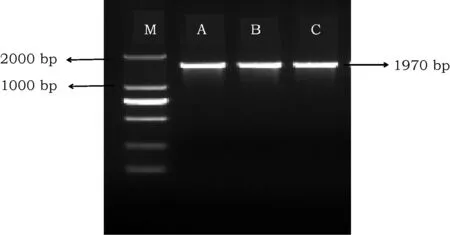
图1 杜氏盐藻DsLCYB基因的 cDNA克隆Fig.1 cDNA clone of DsLCYB gene in D. salina注:M为Marker;A、B、C为DsLYCB全长Note: M is Marker; A, B, C are full length of DsLYCB
2.2 杜氏盐藻DsLCYB酶蛋白特性的生物信息学分析
上述扩增到的杜氏盐藻DsLCYB基因cDNA全长为1 910 bp,其中 5’非翻译为 83 bp,3’非翻译为72 bp,开放阅读框(ORF)1 755 bp(核苷酸序列位置84~1 838),编码 584 个(核苷酸序列位置84~1 838),编码 584 个氨基酸的蛋白质(图2)。
推导的该蛋白质理论等电点(pI) 为 7.66,相对分子质量64 541.99Da。负电荷残基(Asp+Glu)数为57,正电荷残基(Arg+Lys)数为58,不稳定系数为35.32,因此将该蛋白归为稳定蛋白,其疏水性平均值为-0.183,表现为亲水性,无明显的疏水区域。DsLCYB基因编码氨基酸序列通过 ProtScale 软件进行亲水性/疏水性分析,结果表明,杜氏盐藻DsLCYB蛋白第152 位 Arg疏水性最强,分值达到-2.530,第104 位Ile亲水性最强,分值达到1.380,预测该蛋白为疏水性蛋白(图3)。在CBS 软件上对杜氏盐藻DsLCYB 蛋白进行的亚细胞定位预测,其结果表明,杜氏盐藻DsLCYB 蛋白没有信号肽和跨膜区域,为非分泌蛋白,该蛋白定位在叶绿体。二级结构预测显示,无规则卷曲占39.73%,α-螺旋占39.9%。使用SWISS-Model 在线预测分析 DsLCYB 蛋白3D结构(图4)显示,结果表明与二级结构预测一致。

图2 杜氏盐藻DsLCYB 基因cDNA全长及其推导氨基酸序列Fig.2 DsLCYB gene cDNA sequence and its deduced amino acid sequence
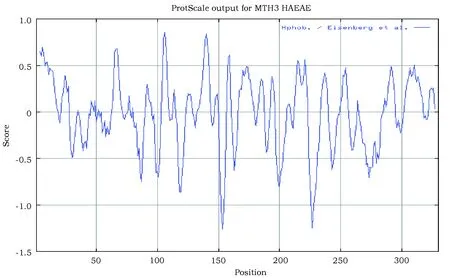
图3 杜氏盐藻DsLCYB蛋白疏水性预测Fig.3 Prediction of DsLCYB protein hydrophobicity
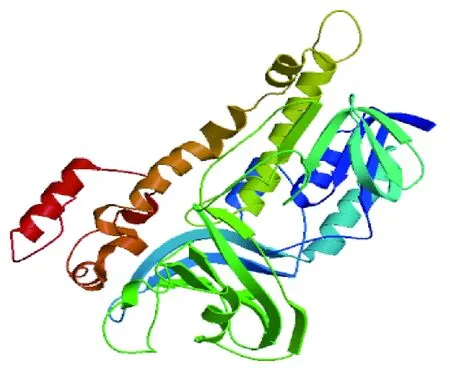
图4 杜氏盐藻DsLCYB蛋白三级结构模拟Fig.4 3 D structure of DsLCYB protein from Dunaliella salina
2.3 杜氏盐藻DsLYCB与其他植物LYCB蛋白系统进化分析
以DsLYCB 蛋白序列为搜索序列。对NCBI 数据库进行 Blast分析。从BLAST获得序列中选取与DsLYCB同源性较高的 12 个物种的LYCB蛋白序列构建系统进化树。 这12个LYCB蛋白分别来自雨生红球藻(Haematococcuslacustris)、佐夫色绿藻(Chromochloriszofingiensis)、莱茵衣(Chlamydomonaseustigma)、团藻(Volvoxcarterif.nagariensis)、单针藻(Monoraphidiumneglectum)、胶球藻(CoccomyxasubellipsoideaC-169)、微茫藻(Micractiniumconductrix)、原壳小球(Auxenochlorellaprotothecoides)、克莱门柚(Citrusclementina)、山嵛菜(Eutremasalsugineum)、江南卷柏(Selaginellamoellendorffii)和风疹荠菜(Capsellarubella)。结果(图5)显示:这12个LYCB蛋白系统进化树共分为两大支,即8个藻类LYCB聚为一枝,4个高等植物的LYCB聚为另一枝。杜氏盐藻DsLYCB与雨生红球藻LYCB蛋白亲缘关系最近, 与莱茵衣藻LYCB蛋白亲缘关系次之。
2.4 杜氏盐藻DsLYCB在高盐胁迫下的表达分析及其对类胡萝卜素积累的影响
提取的各样品藻细胞总RNA,经核酸浓度仪测定OD260/280均在1.8~2.2,可以用作随后cDNA合成和荧光定量PCR检测DsLYCB基因的表达谱。定量表达分析结果(图6)表明,高盐胁迫下,DsLYCB基因表达量明显上升,在胁迫4 h时表达量达到峰值,为正常生长条件(1.5 mol·L-1)下的2倍,差异达到著水平(P<0.05)。在胁迫后期,DsLYCB表达量逐渐下降,但仍显著高于对照正常条件下表达量。说明DsLYCB基因为盐胁迫上调表达基因。对高盐胁迫处理条件下杜氏盐藻藻细胞中类胡萝卜素含量测试(图7)显示,随着高盐胁迫时间增加,杜氏盐藻类胡萝卜素含量呈现上升趋势,在胁迫1~4 h期间增加最快,12 h后类胡萝卜素含量趋于稳定。显然,在高盐胁迫条件下,DsLYCB基因表达谱变化模式与藻细胞富集类胡萝卜素动态过程呈正相关性。

图5 杜氏盐藻DsLYCB与其他12种植物LYCB蛋白系统进化树Fig.5 Phylogenetic tree of the LYCB proteins from Dunaliella salina and other 12 organisms

图6 杜氏盐藻DsLYCB基因在3 mol·L-1盐胁迫下表达量变化Fig.6 Expression of DsLYCB gene in Dunaliella salina at 3 mol·L-1 salt stress
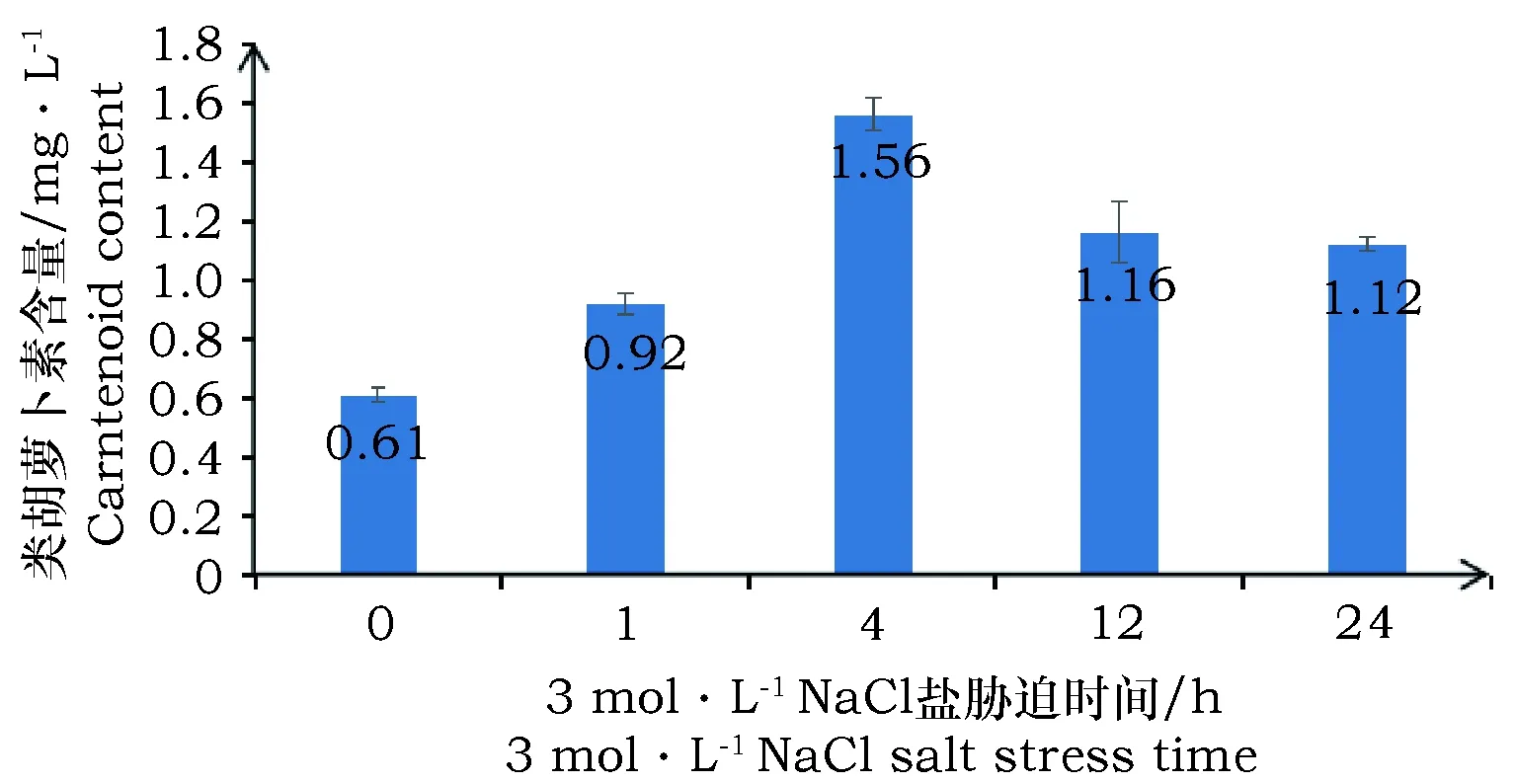
图7 高盐胁迫对杜氏盐藻类胡萝卜素积累的变化Fig.7 Effect of high salt stress on carotenoid acculmulation in Dunaliella salina
3 讨论
藻类类胡萝卜素合成途径与植物相似,在类胡萝卜素合成过程中,番茄红素 β- 环化酶(LYCB)在类胡萝卜素次生代谢途径中可直接将番茄红素催化生成β-胡萝卜素。2006年,陶俊等从枇杷中分离并获得番茄红素β-环化酶基因的片段[24];张建成等从红肉脐橙中克隆到β-环化酶基因片段[25];同时LYCB基因也应用于转基因工程技术中,梁燕等从胡萝卜获得番茄红素β-环化酶的反义RNA并将该基因转入烟草细胞中,结果发现,转化胡萝卜株组织中的胡萝卜素含量相对较高[26]。晏露等从杜氏盐藻中克隆到番茄红素β-环化(LYCB)基因[27]。杜氏盐藻在极端条件下可以大量积累类胡萝卜素,但是,在这些研究中,分离得到的大多为cDNA序列,但是对其作用机理研究较少。
本研究从运城盐湖分离的一株盐藻(Ds-YC011)中扩增获得DsLYCB基因的cDNA全长序列,利用生物信息学对该基因氨基酸的特性及其空间结构进行分析和预测,并且研究了在高盐胁迫下不同时期的表达量的变化及类胡萝卜素含量的变化。杜氏盐藻LYCB全长1 910 bp,开放阅读框(ORF)长1 769 bp,编码584个氨基酸。LYCB为不稳定亲水性蛋白,无跨膜结构。二级结构预测显示该蛋白分子中α-螺旋结构最多,占39.9%。同源比对结果表明,杜氏藻DsLYCB蛋白与雨生红球藻亲缘关系最近。经过高盐胁迫,DsLYCB基因的表达量随着胁迫时间的增加呈先升高后缓慢降低的趋势,但总体表达量显著高于对照。类胡卜素含量随着胁迫时间的增加,表现为先上升后基本稳定的趋势,但类胡萝卜素含量总体高于对照。高盐胁迫上调杜氏盐藻DsLYCB基因的表达量,且DsLYCB基因表达谱与类胡萝卜素富集模式相吻合。
本研究通过克隆获得了杜氏盐藻DsLYCB基因 cDNA 全长序列,对其进行了生物信息学分析,并对其进行盐胁迫表达分析,为在杜氏盐藻中DsLCYB调节β-胡萝卜素生物合成的分子机制奠定了分子基础。
