肺肉瘤样癌的CT表现
2018-10-17梁拥辉刘尼军董卫红
梁拥辉,刘尼军,董卫红
(1.河南省中医院放射科,河南 郑州 450000;2.陕西省核工业215医院放射科,陕西 咸阳 712000;3.河南省濮阳市安阳地区医院病理科,河南 安阳 455000)
肺肉瘤样癌(pulmonary sarcomatoid carcinoma,PSC)是一组含有肉瘤形态细胞或肉瘤样[梭形细胞和(或)巨细胞)]分化的非小细胞肺癌。PSC占肺部恶性肿瘤的0.3%~4.7%[1],虽发病率较低,但其侵袭性强,预后差,临床应给予足够重视。现收集2007—2017年河南省中医院收治的13例经病理证实的PSC的临床、病理及CT资料,探讨其CT表现特点,以提高对该病的认识。
1 资料与方法
1.1 一般资料 13例中,男11例,女2例;年龄40~88岁,平均 64.5岁,60岁以上 11例(84.62%)。病程20 d~3个月。9例有长期吸烟史。主要症状有咳嗽、咳痰、胸痛,2例伴咯血,1例声音嘶哑,3例体检发现。
1.2 仪器与方法 13例均行胸部CT平扫及增强扫描。采用Siemens Somatom 16排螺旋CT机,自肺尖至肺底螺旋扫描。扫描参数:120 kV,150 mAs,矩阵512×512,重建层厚、层距均为5 mm。增强扫描采用高压注射器经肘静脉团注非离子型碘对比剂碘海醇(300 mgI/mL),流率 3.5 mL/s,延迟时间为 35 s。
1.3 图像分析 由2名主治医师以上胸部放射科医师独立评价图像。观察内容:病灶部位、大小(直径<3 cm为结节,≥3 cm为肿块)、边缘、分叶、毛刺、胸膜凹陷征,病灶密度、强化方式,有无胸膜增厚、胸水、淋巴结肿大及远处转移。
1.4 病理及诊断标准 采用2004年WHO肺肿瘤分类法,将PSC定义为含有肉瘤成分或肉瘤样分化[梭形细胞和(或)巨细胞]的低分化非小细胞肺癌,包括多形性癌、梭形细胞癌、巨细胞癌、癌肉瘤和肺母细胞瘤5个亚型[2]。免疫组化检测主要包括:上皮细胞角蛋白(CK)、上皮细胞膜抗原(EMA)、波形蛋白、Ki67等。
2 结果
2.1 CT表现 本组均为单发。中央型1例,表现为右肺门旁不规则肿块,病灶内大片状坏死,不均匀明显强化,坏死区无强化,右肺上叶支气管阻塞,同侧可见癌性淋巴管炎及胸腔积液,右侧肺门及纵隔淋巴结肿大伴坏死。周围型12例(92.31%),右肺上叶6例(图1a),左肺上叶2例,左肺下叶3例,右肺下叶1例;9例病灶与胸膜接触(图1b),且接触面较宽;12例周围型PSC中,1例为结节,11例为肿块,直径2.4~12.3 cm,7例 >5 cm,4例 <5 cm,平均 7.0 cm,仅1例直径<3 cm,1例病灶于46 d后复查病灶增大3 cm,并侵犯胸膜,发生纵膈淋巴结转移及左心房癌栓。病灶呈浅分叶6例,无分叶6例。11例肿瘤边界光整,1例边界毛糙,8例周围可见少许条索影,2例咯血者可见晕征。CT平扫5例病灶密度均匀,8例密度不均匀,可见大片状低密度区,1例见点状钙化。所有病灶均未见典型毛刺征、胸膜牵拉征及空洞。CT增强扫描8例可见不均匀强化或边缘厚环形强化,CT值升高30~40 HU,坏死区无强化(图1c);5例为均匀轻度强化。6例纵隔淋巴结肿大,1例左心房栓子,3例同侧胸腔积液。9例病灶与胸膜广泛接触,其中7例(53.85%)经病理证实为胸膜受侵。
2.2 病理及免疫组化 穿刺活检2例、手术病理学及免疫组化检测11例均证实为肉瘤样癌。免疫组化:13例 CK(+),8例波形蛋白(+),Ki67+(5%~80%)。
3 讨论
3.1 病理及临床表现 2004年WHO肺肿瘤分类中,将PSC定义为含有肉瘤形态细胞或肉瘤样分化的非小细胞性肺癌[2]。PSC起源于共同的原始上皮干细胞,经稳定的上皮-间叶转化(epithelial-mesenchymal transition,EMT)直到完全性间叶表型关闭,是以 EMT 为特征的转化性癌[3],大量证据[4]表明,PSC是由EMT所致、伴不同程度异向分化的癌,而非癌肉瘤。PSC包括5种亚型:多形性癌、癌肉瘤、梭形细胞癌、巨细胞癌和肺母细胞瘤:①多形性癌是PSC最常见病理亚型,肿瘤组织中含肉瘤样成分和上皮癌成分,其中肉瘤样成分主要为梭形细胞癌或巨细胞癌(至少占10%以上),上皮癌成分可以是鳞癌、腺癌或大细胞癌。②癌肉瘤含恶性上皮成分和真性肉瘤成分[5],是光镜下有双相分化特征的肿瘤,癌成分以鳞癌最常见,肉瘤成分主要是软骨肉瘤、横纹肌肉瘤或骨肉瘤,或几种肉瘤共存。③肿瘤组织中仅包含梭形细胞或巨细胞,则为梭形细胞癌或巨细胞癌,这类肿瘤非常罕见。④肺母细胞瘤是一种双相分化的恶性肿瘤,上皮部分为单一性的高分化胎儿性腺癌,而肉瘤可以是分化型或间变性的骨肉瘤、软骨肉瘤或横纹肌肉瘤等。免疫组化发现,在PSC中,肉瘤样成分常表达CK、EMA等上皮性标志物,而癌成分也同时表达波形蛋白等间叶性标志物,其中CK阳性是最有力的诊断证据[6]。电镜技术也在肉瘤样成分中发现存在角素母细胞颗粒、张力原纤维、桥粒和前黑色素颗粒等,证实PSC中肉瘤样成分实际上是具有肉瘤样形态的癌,本质上仍是上皮性肿瘤。
PSC发病率仅占肺部恶性肿瘤的0.3%~4.7%[1],占非小细胞癌(non-smallcell lung cancers,NSCLCs)的2.35%[7],但其侵袭性及复发率高,5年生存率仅为24.5%,明显比其他NSCLCs预后差。肺母细胞瘤好发于儿童,PSC平均发病年龄在60岁左右,临床多见于有重度吸烟史的中老年男性,男女性别比4∶1。临床表现多以咳嗽、咳痰、咯血为主,病变侵及胸膜、胸壁时可引起胸痛。本组13例中,60岁以上11例,占84.62%,均为男性,且9例有长期吸烟史,符合本病临床特点。本组患者病较短,20 d~3个月,临床表现无特异性,3例为体检发现。
3.2 CT表现 胸部具有良好的自然对比,CT技术具有良好的密度和空间分辨力,能够行多种图像后处理,是目前胸部疾病的主要影像学检查方法。CT检查可详细观察病变部位、形态、大小、密度、强化方式、与周围结构的关系,以及有无肺门、纵隔淋巴结、远处转移等。结合相关文献及本组病例,总结其CT表现如下。
3.2.1 部位 PSC分为中央型和周围型。中央型位于肺门区,段及叶支气管以上,此类型在PSC中少见,大多为周围型。 Fishback等[8]报道 PSC 60%为周围型,而Kim等[9]报道周围型占70.7%。本组周围型占92.31%,与文献报道一致。本组发生于上叶9例,占69.23%,其中右肺上叶6例,明显多于左肺上叶及两肺下叶,具体原因不明。12例周围型中,9例与邻近胸膜接触,病灶越大与胸膜接触面越大。结合文献发现,PSC发病部位具有以下特征性,即以周围型为主,右肺上叶多见,病灶多接触邻近胸膜。
3.2.2 大小 PSC恶性程度高,生长速度快,发现时肿块一般较大。徐晓莉等[10]报道20例PSC,所有病灶均>3.0 cm,50%的肿块>5 cm。本组除1例中央型病灶形态不规则无法测量,12例周围型病变直径平均7.0 cm,最大12.3 cm,仅1例病变<3 cm。另1例间隔46 d后复查病灶增大3 cm,并侵犯胸膜,发生纵隔淋巴结转移及左心房癌栓,说明本病生长迅速,恶性程度高。
3.2.3 形态及边缘 PSC多表现为结节及肿块,以类圆形肿块多见,边缘较光整。多数报道[11-12]认为PSC分叶征相对较多见,而毛刺征、棘突征、空泡征、胸膜凹陷征、血管集束征等征象相对少见。本组12例周围型PSC,仅1例为结节,其余为肿块,均为类圆形,无分叶或浅分叶,肿块边缘光整,均未见毛刺征、胸膜牵拉征等典型肺癌征象,但病灶周围多伴少许条索影,可能为周围肺组织受压迫或炎症所致。本组2例咯血者,病变边缘出现晕征,考虑为病灶出血所致,不具有特征性。
3.2.4 密度 PSC病灶生长迅速,病灶内因血供不足出现坏死,常表现为病灶内片状低密度影。文献[13]报道直径>5 cm者坏死空洞多见,且与肿瘤的亚型无明显关联。本组7例>5 cm病灶平扫可见片状低密度区,边界模糊;5例<5 cm者未见明显坏死;1例中央型PSC病灶也可见片状低密度区,以上特点与文献报道一致。但本组均未出现空洞,与文献报道存在差异,可能与例数较少有关。本组仅1例病灶内见点状钙化,提示本病较少发生钙化。
3.2.5 增强扫描 PSC与肉瘤的CT强化方式类似,表现为肿瘤周围不规则片状强化或厚环形强化,中央区域强化不明显或无强化,为黏液样变性或坏死、出血所致,多见于最大径>5 cm的肿瘤中。本组5例<5 cm的病灶均表现为较均匀轻度强化,而7例>5 cm的周围型病灶和1例中央型病灶,均见大片状无强化坏死区,且坏死边界较清楚,肿瘤未坏死部分表现为环形或不规则斑片状强化,为持续性,较平扫CT值平均上升30~40 HU。
3.2.6 转移及侵犯 PSC可发生远处转移或周围侵犯。本组6例CT上可见纵隔淋巴结肿大,经手术病理证实为转移。1例中央型病灶伴同侧癌性淋巴管炎及胸腔积液。9例周围型病灶与胸膜广泛接触,3例伴同侧胸腔积液,提示胸膜侵犯可能,其中7例(53.85%)经病理证实。徐晓莉等[10]报道的20例PSC中68%累及胸膜,提示胸膜侵犯是PSC的一个重要特点。本组1例发生左心房内瘤栓。所有患者均未见骨、脑、肺、肝脏或肾上腺等远处转移。
综上所述,60岁以上、长期吸烟的男性患者,在肺部周围特别是右肺上叶邻近胸膜区域出现较大肿块且边缘光整、密度不均及大片状坏死,周边斑片状或环形强化,伴肺门或纵隔淋巴结肿大,周围未见毛刺、空泡征、支气管充气征等特征时,应考虑PSC可能。
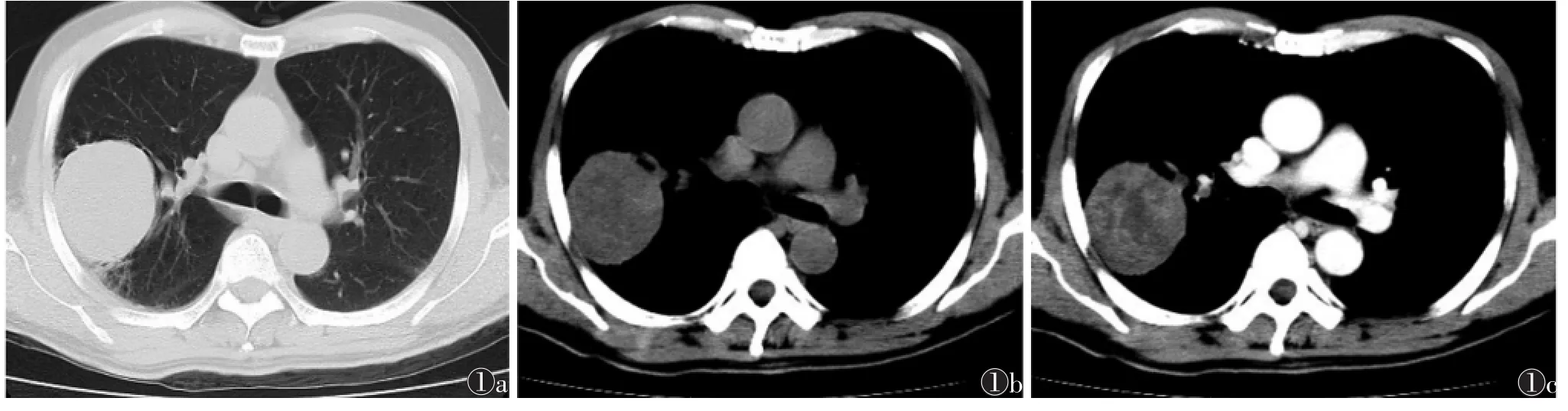
图1 男,64岁,右肺上叶肉瘤样癌 图1a CT平扫肺窗示右肺上叶类圆形病灶,边缘光整,位于胸膜下,未见毛刺、分叶 图1b 平扫纵隔窗示病灶大小6.5 cm×7.0 cm,密度不均匀,CT值32 HU 图1c CT增强扫描示病灶不均匀强化,CT值65 HU,低密度坏死区无强化
