UPLC-LTQ-Orbitrap-MS法 快速分析鬼箭羽中的化学成分
2018-10-11姬瑞芳全庆华郭晓宇张伽妹王政霖宋勇丽田婧鋆孙倩倩刘永刚
姬瑞芳,全庆华,郭晓宇,张伽妹,王政霖,宋勇丽,田婧鋆, 孙倩倩,谭 鹏,韩 静,刘永刚
(北京中医药大学中药学院,北京 100102)
鬼箭羽(Euonymusalatus)[1-2]为卫矛科Celatraceae卫矛属植物卫矛,为具翅状物的枝条或翅状附属物,史载于《神农本草经》,其性寒、味苦、辛,归肝、脾经。药理研究表明[3],鬼箭羽具有降血糖、调血脂及延缓动脉粥样硬化等作用,可治疗糖尿病[4]、高脂血症、慢性肾病等多种内科病症,单用或组方应用均有很好的疗效。通过提取、分离技术得到鬼箭羽中含有的化合物类型包括[5-8]:糖、强心苷、有机酸、五环三萜、黄酮、黄酮苷、三萜、酚酸、脂肪族、生物碱等。据文献[9]报道,黄酮类成分具有很强的活性氧自由基清除功能,是鬼箭羽药材的主要活性成分之一。
中药材的化学成分复杂,应用传统的提取、分离、纯化技术从中药材中获得单体化学成分的方法繁琐、费时、费力,且很难分离得到含量较低或结构相似的化学成分。液相色谱-质谱(LC-MS)联用技术[10-11]与传统方法相比,具有分离快速、鉴定准确、适用于检测未知化合物等优点。目前,对鬼箭羽中化学成分的研究仅限于传统的分离手段和半制备色谱法等,未见LC-MS法检测鬼箭羽化学成分的报道。
本研究拟利用UPLC-LTQ-Orbitrap-MS技术对鬼箭羽中多种组分进行快速识别,通过查阅文献,总结各类化合物的裂解规律,建立各类化合物的识别方法,为鬼箭羽化学成分的研究提供参考。
1 实验部分
1.1 主要仪器与装置
Accele 600 Pump高效液相色谱仪和LTQ-Orbitrap XL线性离子阱-串联静电轨道场质谱仪:配有电喷雾离子源和Xcalibur 2.1工作站,美国Thermo Fisher公司产品;KQ5200DE型数控超声波清洗器:昆山市超声仪器有限公司产品;BT125D十万分之一型电子天平:德国Satorious公司产品。
1.2 主要材料与试剂
鬼箭羽药材:北京三和药业有限公司产品,鬼箭羽具翅状物的枝条,产自河北,经北京中医药大学刘勇教授鉴定为鬼箭羽。
甲醇:分析纯,北京化工厂产品;乙腈、甲酸:质谱纯,美国Thermo Fisher公司产品;实验用水:娃哈哈纯净水。
1.3 实验条件
1.3.1色谱条件 色谱柱:Waters Acquity UPLC BEH C18柱(2.1 mm×50 mm×1.7 μm);流速1.0 mL/min;进样量10 μL;检测波长254 nm;干燥气(N2)流速10 L/min;柱温25 ℃;流动相:A为乙腈,B为0.1%甲酸水溶液;梯度洗脱程序:0~18 min(5%~21%A), 18~35 min(21%~34%A),35~42 min(34%~38%A),42~52 min(38%~65%A),52~70 min(65%~95%A)。
1.3.2质谱条件 ESI离子源;负离子检测模式;质量扫描范围m/z50~2 000;离子源温度350 ℃;电离源电压4 kV;管透镜电压110 V;雾化压力275.86 kPa;毛细管电压3 000 V;鞘气和辅助气均为高纯氮气(纯度>99.99%),鞘气流速40 L/h,辅助气流速20 L/h。
1.4 供试样品的制备
精密称取约1 g鬼箭羽药材粉末于50 mL锥形瓶中,用25 mL甲醇溶液溶解,超声1 h,过滤,共提取3次,将得到的滤液减压浓缩至25 mL,取上清液过0.45 μm微孔滤膜,即得供试品。
2 结果与讨论
2.1 鬼箭羽甲醇提取物的UPLC-LTQ-Orbitrap-MS分析
在负离子模式下,供试品的总离子流图示于图1。由图可得化合物的精确分子质量以及二级质谱碎片离子信息,结合相关文献报道,共鉴定得到65种成分,包括36种黄酮类、4种酚酸类、7种三萜类、12种脂肪族和6种其他类成分,其中,有28种化合物为首次在鬼箭羽中发现。65种化合物的详情列于表1。
2.2 鬼箭羽中酚酸及其酯类成分的UPLC-LTQ-Orbitrap-MS分析
从鬼箭羽中共鉴定得到4种酚酸类成分、1种酚酸酯类成分。酚酸类成分极性较大,保留时间较短,容易丢失羧基;酚酸酯类成分容易失去酯基。以化合物8为例,在负离子模式下,准分子离子峰为m/z167.03[M-H]-,其二级质谱图示于图2。碎片离子m/z122.94、151.89和107.7分别为其母离子丢失羧基、甲基和同时丢失羧基与甲基所得,结合文献[12],可推断化合物8为香草酸,其可能的裂解途径示于图3。
化合物11和12具有相同的准分子离子峰m/z192.99 [M-H]-,其分子式均为C10H10O4,可能互为同分异构体。化合物11的碎片离子中存在m/z148.95 [M-H-COOH]-,表明取代基中存在羧基,据此判断为阿魏酸。化合物12的碎片离子不存在m/z148.95[M-H-COOH]-,但存在m/z133.92[M-H-CO2-CH3]-,推断其为咖啡酸甲酯。
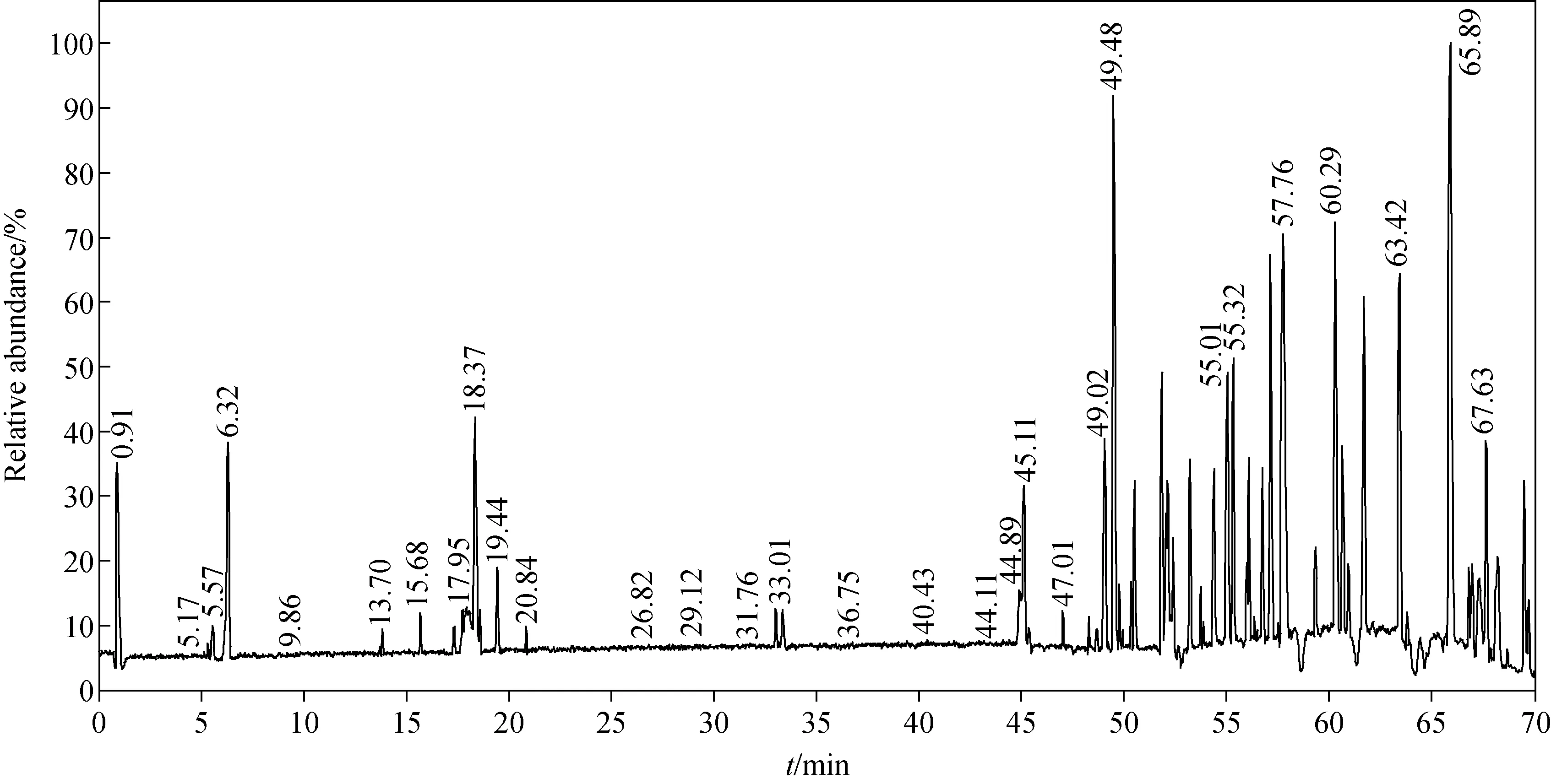
图1 鬼箭羽的总离子流图Fig.1 Total ion chromatogram of Euonymus alatus

序号No.保留时间tR/min 准分子离子Molecularions (m/z)碎片离子Fragment ions (m/z)分子式Molecularformulas 鉴定结果Results1* 1.26503.16431.11[M-H-C2O3]-,C23H20O13异牡荆素草酸酯341.14[M-H-C5H6O6]-21.31 341.03 179.02[M-H-C6H10O6]- C12H22O12蔗糖[12]3 1.68 169.01 125.01[M-H-CO2]-C7H6O5 没食子酸[12]4*3.83577.12559.15[M-H-H2O]-C30H26O12原矢车菊素B5* 6.17 137.02 108.94[M-H-CO]-C7H6O3原儿茶醛[12]66.19179.00135.01[M-H-CO2]-C9H8O4咖啡酸[12]76.20137.0292.86[M-H-CO2]-C7H6O3对羟基苯甲酸8 6.55167.03 151.86[M-H-CH3]- ,C8H8O4香草酸[12]122.74[M-H-CO2]-97.13289.07245.10[M-H-CO2]-C15H14O6儿茶素10*7.14561.14543.20[M-H-H2O]-C30H25O11原矢车菊素B衍生物11 8.06192.99148.95[M-H-CO2]-C10H10O4阿魏酸[12]12 8.43192.99133.92[M-H-CO2-CH3]-C10H10O4 咖啡酸甲酯13*9.24289.07245.08[M-H-CO2]-C15H14O6表儿茶素1410.79 609.41301.38[M-H-C12H20O9]-,C27H30O16芦丁[13]273.12[M-H-C12H20O9-CO]-15*11.13 609.14463.09[M-H-C6H10O4]-,C28H34O15槲皮素-3-O-β-D-葡萄糖301.23[M-H-C6H11O4-C6H11O5]-(1,2)-α-L-鼠李素苷 1611.15 609.14301.00[M-H-C6H11O4-C6H11O5]-C28H34O15橙皮苷1711.68 579.13433.10[M-H-C6H10O4]-C27H32O14柚皮苷1812.34575.12557.45[M-H-H2O]-,C30H24O12氢双儿茶精A449.12[M-H-C6H6O3]-1912.66595.13301.07[M-H-C6H10H5-C5H8H4]-C26H28O16槲皮素-3-半乳糖-木糖苷2012.72593.13285[M-H-C12H20O9]-C27H30O15山奈酚-3-O-β-D-芸香糖苷21* 13.16593.13447.20[M-H-C6H10O4]-,C27H30O15山奈酚-3-O-β-D-葡萄糖基285.13[M-H-C6H10O4-C6H10O5]-(1,2)-α-L-鼠李糖22*13.57593.13447.21[M-H-C9H5O2]-,C30H26O13银锻苷285.11[M-H-C9H5O2-C6H10O5]-23*13.66623.16477.18[M-H-C6H10O4]-,C28H32O16异鼠李素-3-O-β-D-葡萄315.09[M-H-C6H10O4-C6H10O5]- (1,2)-α-L-鼠李糖苷 24*13.92 463.09301.08[M-H-C6H10O5]-C21H20O12槲皮素-3-O-β-D-葡萄糖苷25*14.31623.16315.08[M-H-C12H20O9]-C28H32O16异鼠李素-3-O-β-D-芸香糖2614.25463.09301.00[M-H-C6H10O5]-C15H9O7金丝桃苷[12]27*14.65463.09300.04[M-H-C6H11O5]-,C21H20O12异槲皮苷[12]301.00[M-H-C6H10O5]-
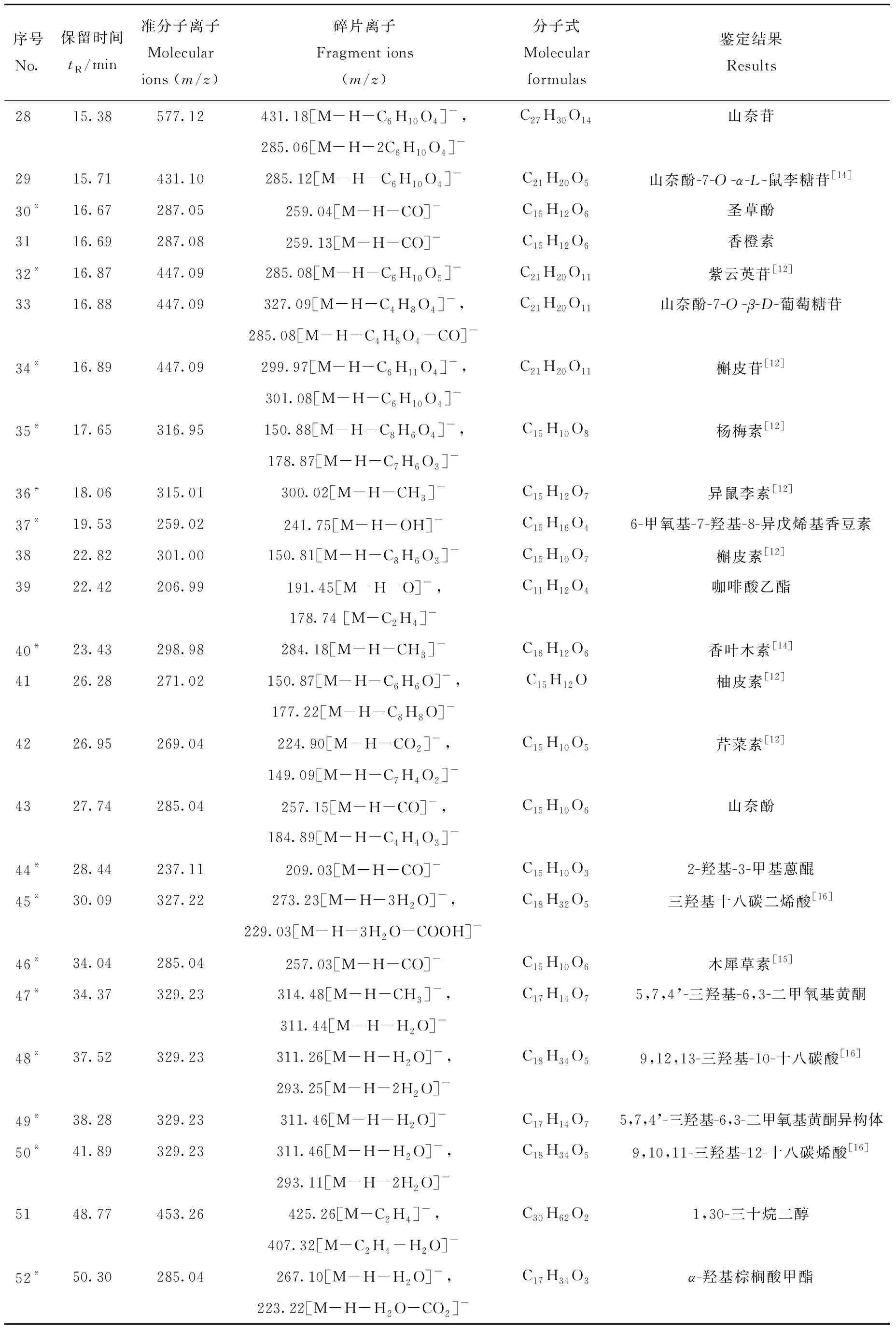
续表1

续表1
注:*为首次在鬼箭羽中发现的化合物
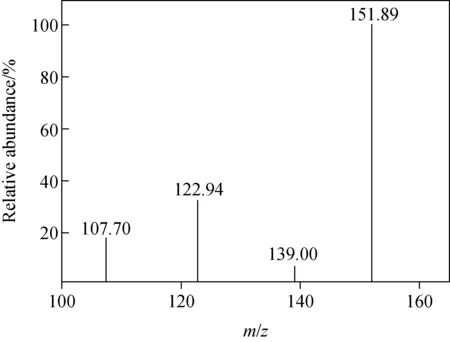
图2 负离子模式下,化合物8的二级质谱图Fig.2 MS2 spectrum of compound 8 at negative ion mode
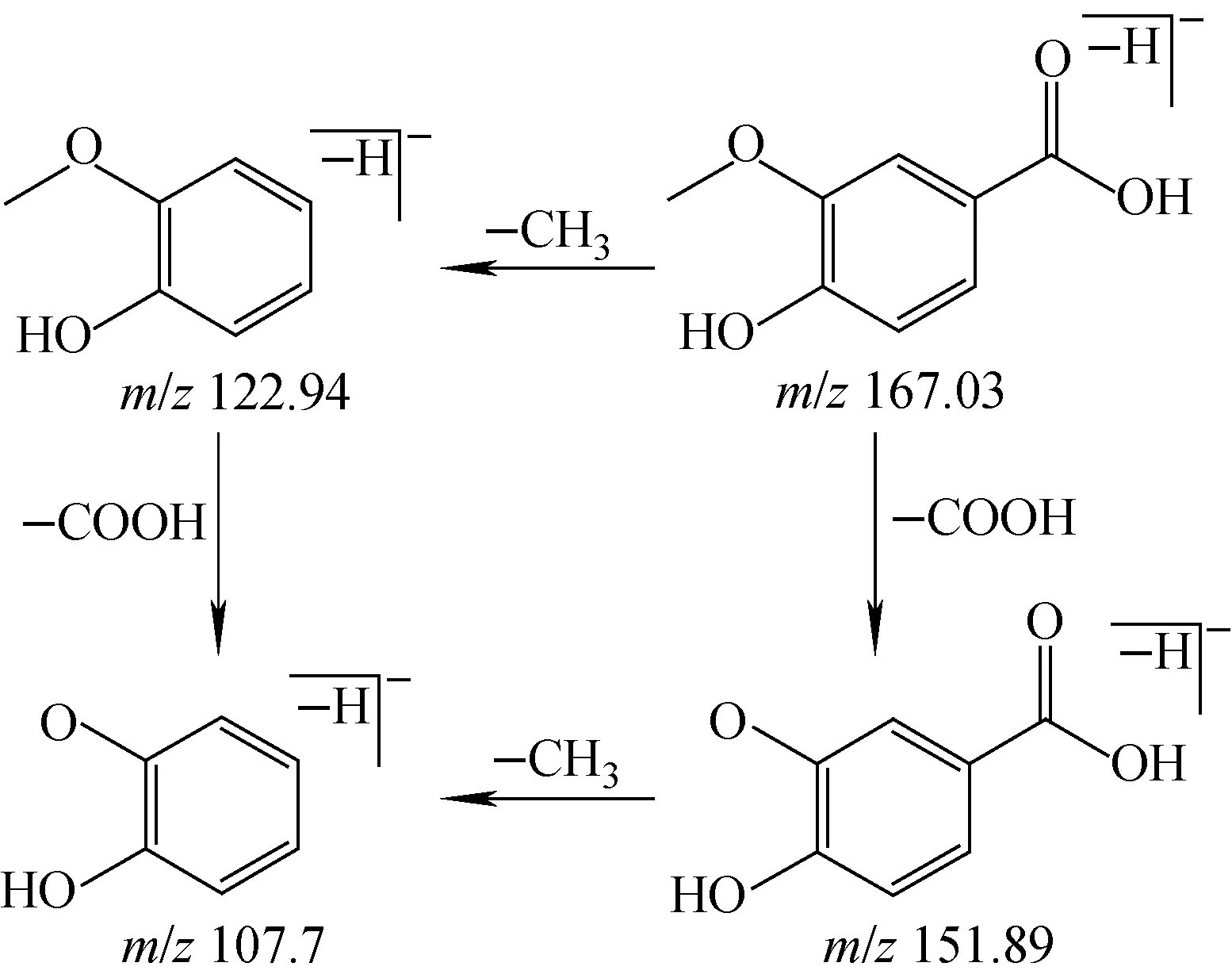
图3 负离子模式下,香草酸可能的质谱裂解途径Fig.3 Fragmentation pathway of vanillic acid at negative ion mode
2.3 鬼箭羽中黄酮类成分的UPLC-LTQ-Orbitrap-MS分析
黄酮类化合物容易丢失C环中的羰基和氧原子等,还容易发生不同部位的反迪尔斯-阿德尔(RDA)裂解,生成碎片离子m/z151。黄酮苷类化合物则先丢失糖基,形成相应的苷元后再进一步裂解。根据黄酮类化合物的裂解规律以及查阅相关文献[12-15],在鬼箭羽中最终鉴定得到36种黄酮类成分。由于不同类型的黄酮类化合物在C环产生RDA裂解的位置不同,因此分情况讨论。
正黄酮类化合物在C环的1,3键或1,4键断裂产生RDA裂解。在负离子模式下,峰42的准分子离子峰为m/z150.90[M-H]-,其二级质谱图示于图4a,C环发生1,3键断裂,生成碎片离子m/z150.90、116.91,形成[A1,3]和[B1,3]碎片离子。母离子m/z269.04分别失去H2O、C2H2O、CO2产生碎片离子m/z251.07、226.92、225.03。A环丢失C3O2后经氢重排得到的离子结构不稳定,故发生C环开环后,丢失C2H2O形成稳定共轭结构的离子m/z158.76,根据文献[19]推断其为芹菜素,属于正黄酮类化合物,其可能的裂解途径示于图5。

图4 负离子模式下,鬼箭羽中峰42(a),峰38(b),峰41(c)的二级质谱图Fig.4 MS2 spectra of peak 42 (a), peak 38 (b) and peak 41 (c) at negative ion mode

图5 负离子模式下,芹菜素可能的质谱裂解途径Fig.5 Fragmentation pathway of apigenin at negative ion mode
黄酮醇类化合物在C环的1,2键或1,3键断裂产生RDA裂解。在负离子模式下,峰38的准分子离子峰为m/z301.00[M-H]-,其二级质谱图示于图4b,准分子离子失去CO2产生碎片离子m/z257.18;碎片离子m/z178.97、150.90是其C环分别发生1,2和1,3键断裂,形成[A1,2]和[A1,3]的碎片离子。根据文献[12]推断其为槲皮素,属于黄酮醇类化合物,可能的裂解途径示于图6。
二氢黄酮类化合物在C环的1,3键和0,4键断裂产生RDA裂解。在负离子模式下,峰41的准分子离子峰为m/z271.11[M-H]-,二级质谱图示于图4c,其母离子的C环分别发生1,3和0,4键断裂,形成碎片离子[A1,3]、[A0,4]和[B0,4],分别为m/z150.87、107.05和177.22。根据文献[20]推断其为柚皮素,属于二氢黄酮类化合物,可能的裂解途径示于图7。

图6 负离子模式下,槲皮素可能的质谱裂解途径Fig.6 Fragmentation pathway of quercetin at negative ion mode
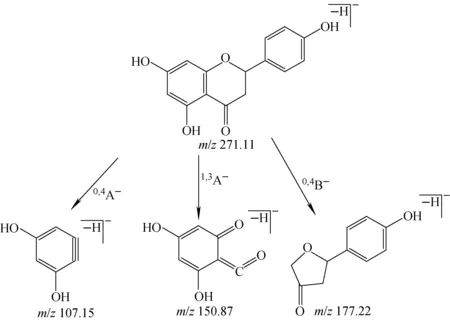
图7 负离子模式下,柚皮素可能的质谱裂解途径Fig.7 Fragmentation pathway of naringenin at negative ion mode
2.4 鬼箭羽中长链脂肪族成分的UPLC-LTQ-Orbitrap-MS分析
从鬼箭羽中共鉴定得到12种长链脂肪族类化合物,其质谱图一般由一系列的峰簇组成,且峰簇之间相差14 u。
以脂肪族化合物长链脂肪酸为例,长链脂肪族一元羧酸类化合物容易丢失羧基、羟基和水分子,具有γ氢的化合物容易发生麦氏重排生成信号较强的特征离子m/z(60+14n),各峰簇之间相差14 u。在负离子模式下,化合物56的准分子离子峰为m/z395.07[M-H]-,二级质谱图示于图8,其发生麦氏重排生成碎片离子m/z340.11;母离子失去羧基生成碎片离子m/z351.02;质谱图中还出现了一系列峰簇组,且峰簇组之间相差14 u,分别为m/z380.10、366.23、352.12。根据文献[16],推断该化合物为2-丁基二十二烷酸,其可能的裂解途径示于图9。
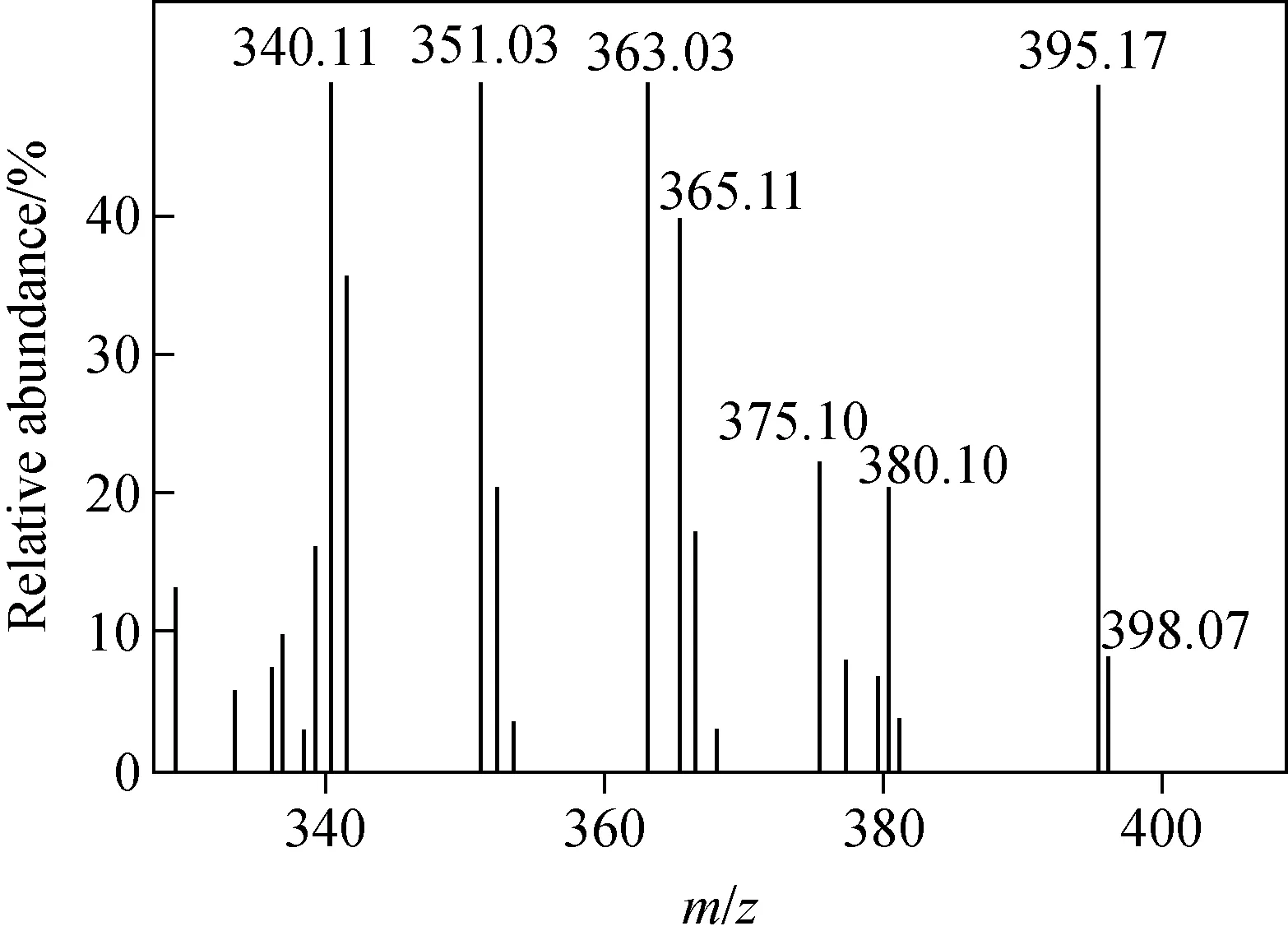
图8 负离子模式下,峰56的二级质谱图Fig.8 MS2 spectrum of peak 56 at negative ion mode
峰59、60具有相同的准分子离子峰m/z409.16 [M-H]-,其分子式可能为C28H38O或C30H50。峰59的碎片离子有m/z365.28 [M-C2H4-OH]-,表明存在羟基取代基,据此判断其为正二十八烷醇。峰60中的碎片离子不存在m/z365.28 [M-C2H4-OH]-,但存在m/z353.04[M-C4H8]-,推断其为角鲨烯。
2.5 鬼箭羽中三萜类成分的UPLC-LTQ-Orbitrap-MS分析
从鬼箭羽中共鉴定得到7种三萜类化合物,不同母核的三萜类化合物有不同的裂解特征。以峰55为例,在负离子模式下,准分子离子峰为m/z469.08 [M-H]-,二级质谱图示于图10。母离子先后失去COOH、H2O生成碎片离子m/z407.47,再重排失去C2H6生成碎片离子m/z377.32;或先失去COOH生成碎片离子m/z425.38,再重排失去C2H6生成碎片离子m/z395.41,根据文献[21],推断该化合物为11-羰基乳香酸,其可能的裂解途径示于图11。

图9 负离子模式下,2-丁基二十二烷酸的质谱裂解途径Fig.9 Fragmentation pathway of 2-butyl behenate at negative ion mode

图10 负离子模式下,峰55的二级质谱图Fig.10 MS2 spectrum of peak 55 at negative ion mode
2.6 鬼箭羽中其他成分的UPLC-LTQ-Orbitrap-MS分析
对于一些含量较低的化合物,采用与相关文献[12,16]比对的方法进行解析。以峰2为例,在负离子模式下,其准分子离子峰为m/z341.03[M-H]-,特征峰为m/z179.02[M-H-C6H10O6]-,将其保留时间、相对分子质量以及特征峰与文献[12]中蔗糖的质谱信息进行对比,可推断峰2为蔗糖。
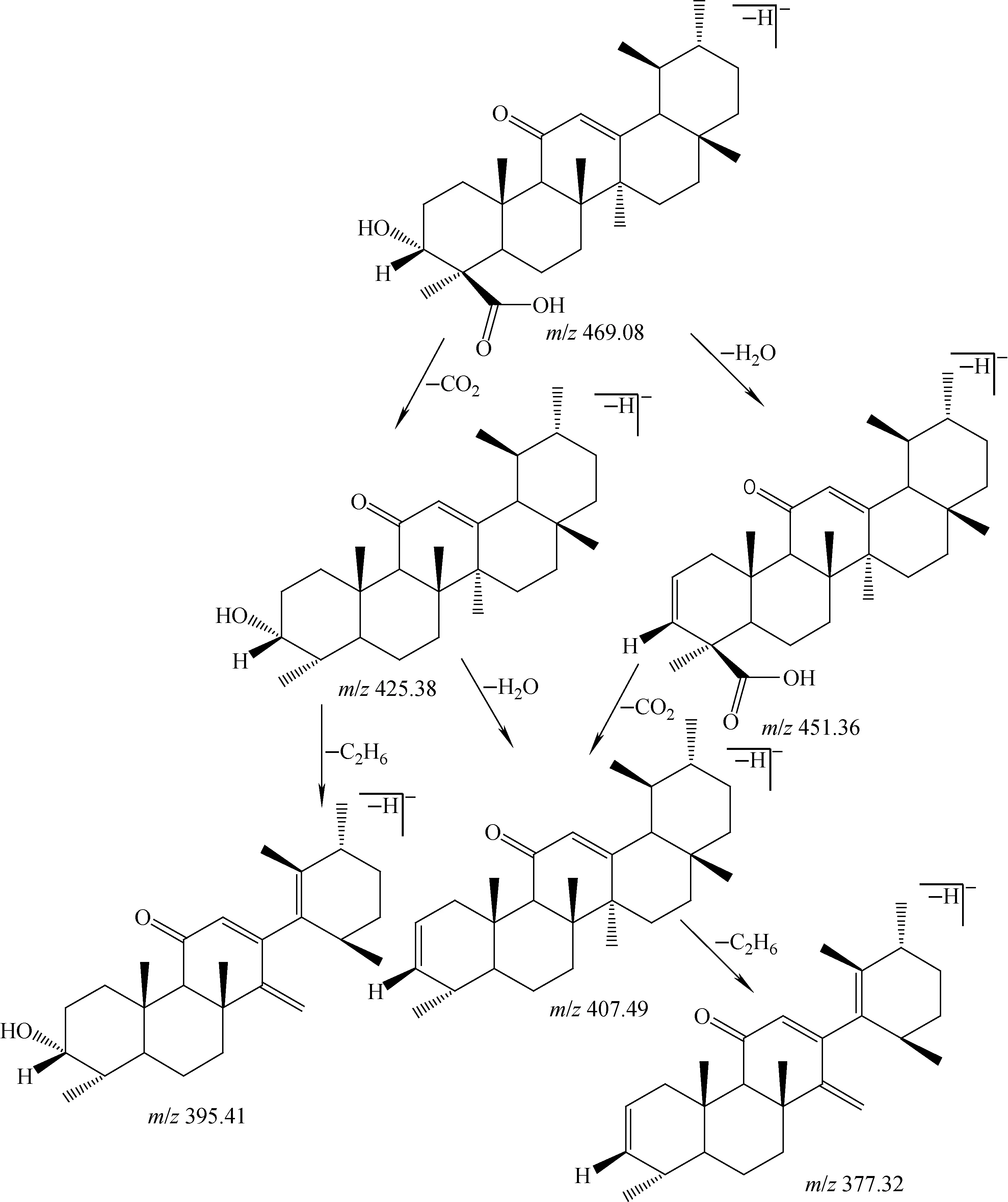
图11 负离子模式下,11-羰基乳香酸可能的质谱裂解途径Fig.11 Fragmentation pathway of 11-carbonyl boswellic acid at negative ion mode
3 结论
本实验采用LC-MS技术分析鬼箭羽的甲醇提取物,利用Xcalibur 2.1软件对质谱信息进行解析,共分析得到65种不同类型的化合物,其中28种为首次在鬼箭羽中发现。通过总结鬼箭羽中不同类型化合物的裂解方式,建立了已知化学成分数据库,可为研究鬼箭羽的化学成分提供基础数据。
