基于LTQ-Orbitrap高分辨质谱技术的 柘木化学成分分析
2018-10-11张伽妹郭晓宇全庆华姬瑞芳孙倩倩田婧鋆刘永刚
张伽妹,郭晓宇,全庆华,姬瑞芳,孙倩倩,田婧鋆,谭 鹏,刘永刚
(北京中医药大学,北京 100102)
柘树广泛分布于我国的华南、华东、西南以及河北以南地区,柘木为桑科柘属植物柘树Cudraniatricuspidata(Carr.)Bur.的干燥根及木材,是我国传统的中药材,用于治疗肝炎、风湿病、跌打损伤、黄疽、疥疮、痛经、体内外出血和慢性胃炎等疾病,具有非常重要的药用价值[1]。柘木糖浆作为消化系统癌症治疗的辅助药物,具有较好的临床疗效[2]。柘木含有丰富的黄酮类化合物,研究表明[3-5],这些化合物表现出显著多样的生物活性,如抗肿瘤、抗炎、抗菌、抗脂质过氧化以及保肝等活性。此外, 柘木中还含有占吨酮类、生物碱、木质素、香豆素等成分,但药理作用尚未明确。
电喷雾离子源质谱具有灵敏度高、操作简便、分子离子峰丰度高等优点[6-8],线性离子阱与Orbitrap傅里叶扫描质谱组成的串联质谱仪能够将离子阱与质谱的高分辨能力结合起来,实现母离子和多级质谱碎裂的高分辨采集。目前,对柘木的研究主要集中在黄酮类成分的分离与活性评价[9-12],尚未见采用液相色谱-质谱(LC/MS)法分析柘木中化学成分的报道。
本研究拟采用高分辨质谱法对柘木中多种组分进行快速识别,以期为柘木的临床应用提供理论基础,为类似化合物的质谱裂解途径研究提供方法参考。
1 实验部分
1.1 主要仪器与设备
Accele 600 Pump高效液相色谱仪,LTQ-Orbitrap线性离子阱-串联静电轨道场高分辨质谱仪:美国Thermo Fisher公司产品,配有电喷雾离子源和Xcalibar 2.0工作站;KQ5200DE型数控超声波清洗器:昆山市超声仪器有限公司产品;BT125D十万分之一型电子天平:德国Satorious公司产品。
1.2 主要材料与试剂
柘木:采自山东沂水,经北京中医药大学刘勇教授鉴定为桑科植物柘树Cudraniatricuspidata(Carr.) Bur.的干燥茎。
甲醇:分析纯,北京化工厂产品;乙腈、甲酸:质谱纯,美国Thermo Fisher公司产品;水:娃哈哈纯净水。
1.3 实验方法
1.3.1色谱条件 色谱柱:Agilent SB C18柱(4.6 mm×150 mm×5 μm);柱温:30 ℃;流速:1.0 mL/min;检测波长:290 nm;流动相:A为水(含0.1%甲酸),B为乙腈;梯度洗脱条件:0~15 min(10%B),15~40 min(10%~15%B),40~65 min(15~35%B),65~90 min(35%~90%B);进样量:10 μL。
1.3.2质谱条件 FT Orbitrap质量检测器;电喷雾离子源(ESI);质量扫描范围m/z100~1 000;喷雾电压4.0 kV;管状透镜电压110 V;毛细管温度350 ℃;鞘气流量30 L/h,辅助气流量10 L/h;采用负离子扫描模式,分辨率设为30 000;二级和三级质谱采用数据依赖性扫描,选取上一级丰度最高的3个峰进行碰撞诱导解离(CID)碎片扫描,以离子阱检测碎片离子。
1.4 供试样品的制备
精密称取约1 g柘木药材于锥形瓶中,加入25 mL甲醇,超声处理1 h,用甲醇补足质量损失,过滤后得到滤液,取上清液过0.45 μm微孔滤膜,即得供试品溶液。
2 结果与讨论
在ESI负离子模式下,柘木供试品溶液的总离子流图示于图1。可以看出,多数化合物有较高的响应,因此本实验选择负离子模式检测样品。在质谱分析中,通过高分辨质谱计算各个主要成分的元素组成,参考相关文献[14-17],并结合二级质谱的裂解碎片信息,对HPLC分离出的柘木的主要色谱峰进行分析和鉴定,共推断出45种化合物,结果列于表1。

图1 负离子模式下,柘木样品的总离子流图Fig.1 TIC of Cudrania tricuspidata (Carr.) Bur at the negative ion mode
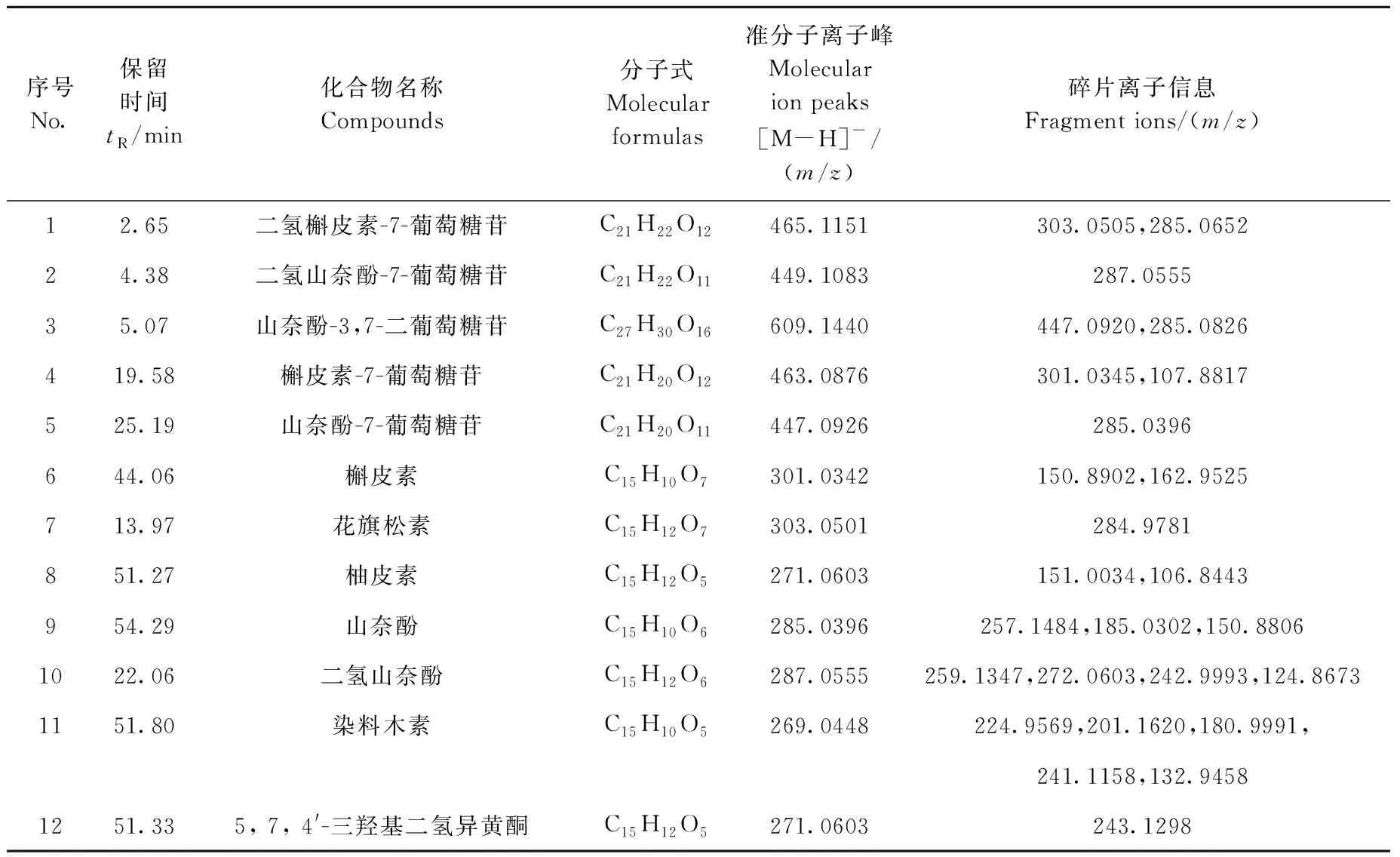
序号No.保留时间tR/min化合物名称Compounds分子式Molecularformulas准分子离子峰Molecularion peaks[M-H]-/(m/z)碎片离子信息Fragment ions/(m/z)12.65二氢槲皮素-7-葡萄糖苷C21H22O12465.1151303.0505,285.065224.38二氢山奈酚-7-葡萄糖苷C21H22O11449.1083287.055535.07山奈酚-3,7-二葡萄糖苷C27H30O16609.1440447.0920,285.0826419.58槲皮素-7-葡萄糖苷C21H20O12463.0876301.0345,107.8817525.19山奈酚-7-葡萄糖苷C21H20O11447.0926285.0396644.06槲皮素C15H10O7301.0342150.8902,162.9525 713.97花旗松素C15H12O7303.0501284.9781851.27柚皮素C15H12O5271.0603151.0034,106.8443954.29山奈酚C15H10O6285.0396257.1484,185.0302,150.88061022.06二氢山奈酚C15H12O6287.0555259.1347,272.0603,242.9993,124.86731151.80染料木素C15H10O5269.0448224.9569,201.1620,180.9991,241.1158,132.94581251.335, 7, 4'-三羟基二氢异黄酮C15H12O5271.0603243.1298

续表1
在已鉴定的45种化合物中,包括28种黄酮类(黄酮醇类、二氢黄酮、异黄酮类及黄酮苷类化合物)、11种占吨酮、6种其他类化合物。由于同类化合物在质谱中具有相似的裂解规律,因此选取有代表性的化合物阐述其详细的裂解规律。
2.1 黄酮醇类化合物
以化合物6为例,其分子离子峰为[M-H]-m/z301.034 2,推断该化合物的分子式为C15H10O7。以m/z301.034 2为母离子进行二级质谱分析,得到的图谱中出现了明显的m/z150.890 2(C7H3O4)和m/z162.952 5(C8H3O4)碎片离子。根据相关文献[18],推测该化合物为槲皮素。m/z150.890 2和m/z162.952 5为C环发生1,3键和0,2键裂解产生的[A1,3]-和[A0,2]-碎片离子,其中[A1,3]-为黄酮醇类的特征碎片离子,其结构和裂解途径示于图2。

图2 槲皮素的裂解途径Fig.2 Fragmentation pathway of quercetin
2.2 异黄酮类化合物
以化合物11为例,其分子离子峰为[M-H]-m/z269.044 8,推断该化合物的分子式为C15H10O5。以m/z269.044 8为母离子进行二级质谱分析,图谱中出现m/z201.162 0(C12H9O3) 和m/z132.945 8(C8H5O2)碎片离子,推测该化合物为染料木素。m/z201.162 0为A环失去C3O2碎片得到,相对丰度达61.25%,m/z132.945 8为C环发生0,3键裂解产生的[B0,3]-碎片离子,其结构及裂解方式示于图3。

图3 染料木素的裂解途径Fig.3 Fragmentation pathway of genistein
化合物18的分子离子峰为[M-H]-m/z299.055 3,推断该化合物的分子式为C16H12O6,二级碎片离子为m/z283.989 7,推测其由[M-H]-丢失CH3所得。根据文献推测[19],该化合物为3′-O-甲基奥洛波尔。
2.3 黄酮类化合物
以化合物24为例,其分子离子峰为[M-H]-m/z337.107 3,推断该化合物的分子式为C20H18O5。以m/z337.107 3为母离子进行二级质谱分析,图谱中出现m/z281.107 6(C16H9O5)、293.092 3(C18H13O4)、321.963 8(C19H14O5) 和m/z219.071 4(C12H11O4)碎片离子,推测该化合物为8-异戊烯基-芹菜素。m/z281.107 6碎片离子为[M-H-56]-(A环失去异丁烯分子),m/z321.963 8由[M-H-CH3]-产生,m/z293.092 3为m/z321.963 8进一步丢失CHO产生,m/z219.071 4为C环发生1,3键裂解产生的[A1,3]-碎片离子。该化合物的二级裂解途径主要为丢失异丁烯分子,其裂解方式示于图4。
化合物13的分子离子峰为[M-H]-m/z351.086 2,推断该化合物的分子式为C20H16O6。以m/z351.086 2为母离子进行二级质谱分析,得到碎片离子m/z333.090 2(C20H13O5)和m/z295.095 8(C16H7O6),推测该化合物为环桂木黄素。m/z333.090 2为该分子离子峰失去1分子H2O所得,m/z295.095 8为[M-H]-失去异丁烯分子所得,相对丰度为16.17%,可见环桂木黄素的二级质谱裂解方式主要为失去1分子H2O。
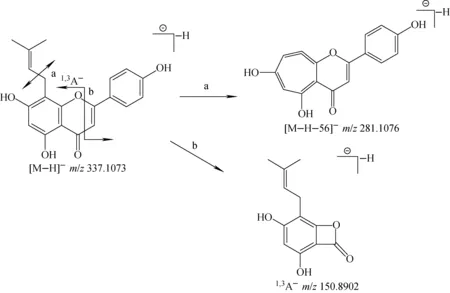
图4 8-异戊烯基-芹菜素的裂解途径Fig.4 Fragmentation pathway of 8-prenylapigenin
2.4 二氢黄酮醇类化合物
化合物19~22分别为Gericudranins A、Gericudranins B、Gericudranins D、Gericudranins E,分子离子峰分别为m/z515.133 7(C29H23O9)、409.164 7(C22H17O8)、499.138 9(C29H23O8) 和393.096 9(C22H17O7)。化合物19、20的二级质谱碎片均为[M-H]-丢失1分子H2O所得,化合物21、22的二级质谱碎片均为[M-H]-丢失1分子CO所得,且化合物19、21的二级裂解均可得到m/z337.035 5(C17H5O8)碎片离子。
2.5 黄酮苷类化合物
根据质谱信息,共推测出5种黄酮苷类化合物,该类化合物的裂解方式主要是脱去糖基产生[M-H-162]-碎片离子,将脱糖后的碎片进行二级裂解,可进一步推测其苷元结构。
化合物1的二级碎片离子为m/z303.050 5(C15H11O7)、m/z285.065 2(C15H9O6),可推测出其苷元为二氢槲皮素;化合物2的二级碎片为m/z287.055 5(C15H11O6),可推测其苷元为二氢山奈酚;化合物3失去1分子葡萄糖的二级碎片离子为m/z447.092 0,再失去1分子葡萄糖得到m/z285.062 6(C15H9O6)碎片,可推测其苷元为山奈酚;化合物4的二级碎片离子为m/z301.034 5(C15H9O7)、m/z107.881 7(C6H4O2),可推测其苷元为槲皮素。根据相关裂解规律,推测化合物1~4分别为二氢槲皮素-7-葡萄糖苷、二氢山奈酚-7-葡萄糖苷、山奈酚-3,7-二葡萄糖、槲皮素-7-葡萄糖苷。
2.6 占吨酮类化合物
化合物31、33、34具有相同的分子离子峰 [M-H]-m/z395.149 0,分子式为C23H24O6,这3种化合物可能为同分异构体。根据极性大小,推测它们分别为柘树占吨酮J、柘树占吨酮L、柘树占吨酮M。柘树占吨酮J和柘树占吨酮M的二级质谱裂解均可得到碎片离子m/z339.270 2[M-H-56]-。3种化合物的二级裂解均可得到m/z351.116 9[M-H-CO2]-碎片离子。柘树占吨酮J、柘树占吨酮M的m/z351.116 9碎片离子的相对丰度分别为40.19%、72.25%,而柘树占吨酮L的m/z351碎片离子为其二级质谱的最高峰,因此三者丢失CO2的难度顺序为柘树占吨酮L>柘树占吨酮M>柘树占吨酮J。这3种化合物的结构式示于图5。
化合物29、32的分子式均为C23H22O6,这两个化合物可能为同分异构体,根据相关文献[20-21]推测,它们分别为柘树占吨酮B、柘树占吨酮K,其二级质谱裂解均可得到m/z378.210 5[M-H-CH3]-碎片离子,进一步丢失CH3、CH2可得到m/z349.172 0碎片离子。

图5 柘树占吨酮J(a), 柘树占吨酮L(b), 柘树占吨酮M(c)的结构式Fig.5 Chemical structures of Cudraxanthone J (a), Cudraxanthone L (b) and Cudraxanthone M (c)
3 结论
本研究采用LTQ-Orbitrap质谱分析柘木中化学成分,共鉴别了柘木中45种化合物,包括28种黄酮类、11种占吨酮类和6种其他类化合物,其中芹菜素和二氢槲皮素-7-葡萄糖苷为柘木中首次发现。本研究鉴定的化合物大多数源于对已知化合物的筛查,对未知化合物进行结构确认仍较为困难,尤其是对结构高度相似的同分异构体,需要结合核磁共振等技术进一步分析,以获得化合物的准确结构。
通过实验总结了不同类型化合物的裂解规律,可为柘木的化学成分研究提供依据,也可为柘木质量控制及药效研究奠定物质基础。
