液相色谱-电感耦合等离子体质谱联用测定富硒酵母中硒形态的不确定度评定
2018-10-08陆奕娜张林田卢金素姚丹仪吕坚羚
陆奕娜 张林田 卢金素 姚丹仪 吕坚羚
汕头出入境检验检疫局 广东汕头 515031
硒(Se)是人和动物所必需的14种微量元素之一[1],常见的硒形态有亚硒酸[Se(Ⅳ)]、硒酸[Se(Ⅵ)]、硒胱氨酸(SeCys2)、甲基硒代半胱氨酸(SeMeCys)、硒蛋氨酸(SeMet)等。硒在机体抗癌、抗氧化等方面发挥着重要作用[2]。人体摄入硒可以增强免疫力、防癌、抗衰老,硒元素摄入不足会使机体免疫力和抗氧化能力下降,导致多种疾病[3]。富硒酵母作为一种含硒保健食品,是国内市场目前消费较多的补硒制剂。有研究表明人体内硒生物活性不仅取决于摄入的总硒量,还与硒的化学形态密切相关[4]。由于动物及人对硒的需要量与中毒量之间的阈值很窄,不同硒形态的毒性亦不同[5],因此准确定性定量分析不同硒形态对硒的安全食用具有重要意义。测量不确定度是表征合理地赋予被测量之值的分散性[6],是评价测量水平准确度的重要指标,是判定测量结果可靠程度的依据[7]。本文建立了液相色谱-电感耦合等离子体质谱联用测定富硒酵母中硒形态的不确定度评定方法,根据试验过程的数学模型,分析不确定度的来源[8],对不确定度分量进行计算,并计算出硒形态的检测结果的合成不确定度及扩展不确定度。
1 检测原理和检测过程
1.1 测试原理
试验样品粉碎后经蛋白酶XIV溶液37℃水解提取7 h后,用液相色谱对富硒大米中的硒形态进行分离,并联用电感耦合等离子体质谱仪测定,与标准系列进行比较定量。
1.2 仪器与试剂
高效液相色谱仪(HPLC,Agilent 1200),电感耦合等离子体质谱仪(ICP-MS,Agilent 7700X),天平:感量为0.1mg,水浴振荡器(昆山一恒 DKZ-3),离心机(Eppendorf 5417R),去离子水净水机(密理博Direct 8),超声萃取仪(CBL C9860A)。 标准储备液(中国计量科学研究院提供),10 mmol/L柠檬酸溶液(pH 5.60),氨水(上海凌峰化学试剂有限公司),蛋白酶XIV(百灵威公司)。
1.3 检测过程
称取1.0000 g富硒酵母于25 mL离心管中,加10 mL水,超声10 min,加入 20 mg蛋白酶 XIV,在37℃的恒温水浴摇床上振荡7 h,10 000 rpm离心,取上清液经0.22 μm水性滤膜过滤后待测(图1)。
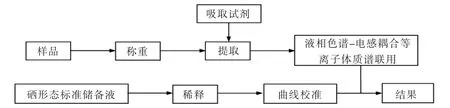
图1 硒形态含量检测流程图
1.4 仪器条件
1.4.1 HPLC条件
Hamilton PRP-X100阴离子分析柱,250 mm×4 mm,10 μm,流动相 10 mmol/L 柠檬酸(pH 5.60),梯度洗脱,柱温30℃,进样量100 μL,洗脱梯度程序如表1所示。
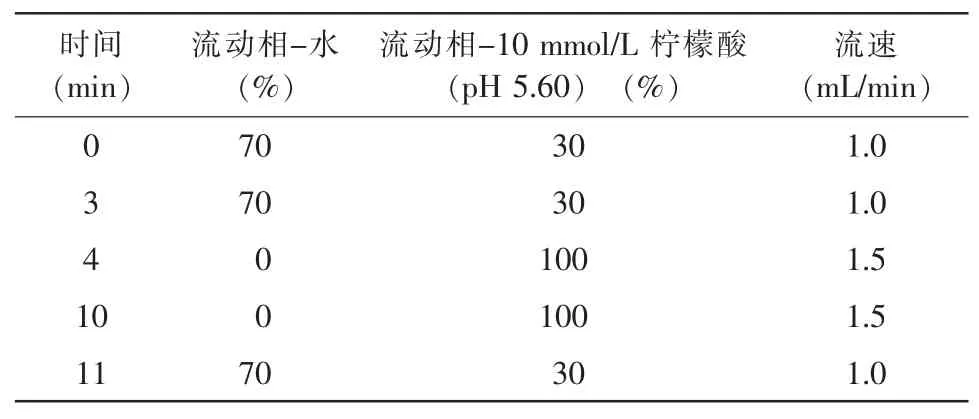
表1 梯度洗脱程序
1.4.2 ICP-MS条件
测质量数 78(Se),m/z 采集模式:TRA,采样周期:0.8 s,采集时间:1 200 s,载气:高纯液氩,雾化器:同心雾化器,载气流速:1.0 L/min,辅助气流速:0 L/min。
2 建立数学模型
样品中硒形态质量分数按公式(1)计算。

式中:w——样品中硒形态质量分数,mg/kg;
C——测定液中扣除试剂空白后硒形态的浓度,μg/mL;
V——样品萃取液体积,mL;m——样品质量,g。
3 不确定度分量的主要来源及其分析
液相色谱-电感耦合等离子体质谱联用法测定富硒酵母中硒形态含量的不确定度评定主要有以下5个来源:
(1)标准物质:包括标准储备液的不确定度和稀释过程引入的不确定度。
(2)样品前处理:包括样品均匀性、天平的最大允许误差(MPE)、移液枪定量误差、温度引起的水膨胀系数、样品回收率等。
(3)最小二乘法拟合标准曲线校准得出Co时所产生的不确定度。
(4)仪器产生的不确定度。
(5)重复性实验:使用因果图(鱼骨图)系统地分析各不确定度来源,如图2所示。
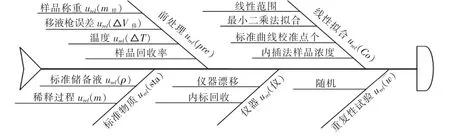
图2 样品硒形态不确定度分量的因果关系图
4 标准不确定度的评定
4.1 标准物质不确定度
4.1.1 标准储备液的不确定度
5种硒形态标准储备液由中国计量科学研究院提供,其信息详见表2所示。

表2 硒形态标准储备液相对不确定度(证书)
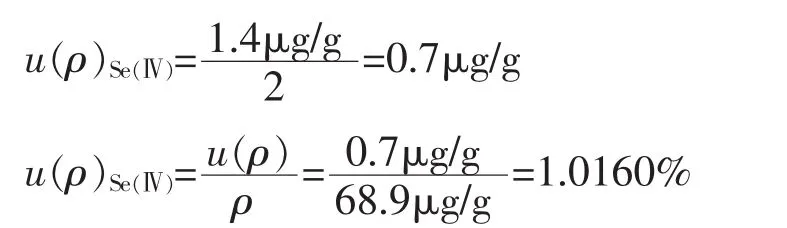
其他硒形态按照以上公式计算,其不确定度及相对不确定度如表2所示。
4.1.2 稀释过程引入的不确定度
分别称取 1.0000 g Se(Ⅳ)、Se(Ⅵ)、SeCys2、SeMeCys及SeMet至标准配备瓶内,用去离子水定量至 6.8900 g、7.5100 g、9.3500 g、9.6600 g、 9.7900 g,制成10 μg/g 5种硒形态标准使用液。使用的天平的最小分度为0.0001 g,根据鉴定证书该准确级的天平在0~50 g的最大允许误差为±0.0005 g,稀释过程各由2次回零称量所得(储备液由空瓶重、标准储备液重称量获得,稀释液由储备液重及稀释液重称量获得),取矩形分布。
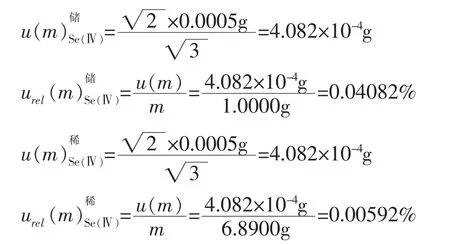
则天平的MPE导致的不确定度由以下两个不确定度合成:

同理,其他4种硒形态的稀释过程引入的相对不确定度分别为 0.04118%、0.04105%、0.04104%、0.04104%。
4.1.3 标准物质引入的不确定度由标准物质引入的不确定度分量:

其他 4 种硒形态 Se(Ⅵ)、SeCys2、SeCys及SeMet由标准物质引入的相对不确定度分别为1.5984%,1.3375%,1.3464%,1.2775%。
4.2 样品前处理过程引入的不确定度
4.2.1 取样均匀性
本实验依照GB/T 5009.1-2003《食品卫生检验方法 理化部分 总则》[9]规定,将样品充分混匀后随机取样,可认为样品是均匀的、代表性充分,由此所致的不确定度忽略不计。
4.2.2 提取过程
4.2.2.1 称重
准确称取1.0000 g样品,使用的天平的最小分度为0.0001 g,根据鉴定证书该准确级的天平在0~50 g的最大允许误差为±0.0005 g,样品质量由2次回零(空瓶mtare和样重msamp)称量所得,取矩形分布,则天平的MPE导致的不确定度。
4.2.2.2 移液枪引入的不确定度
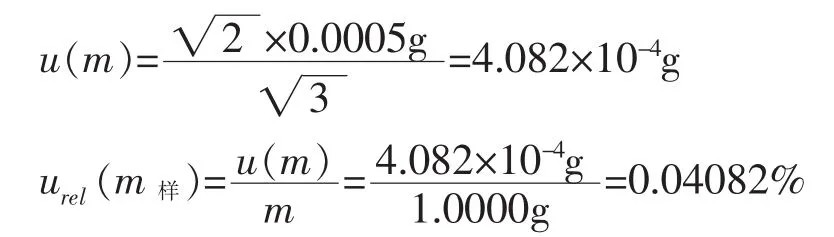
JJG 646-2006《移液器》[10]第 5节规定10 mL可调移液器取10 mL的容量允差(Δ)为±0.6%,取矩形分布,则移液器引入的不确定度:
4.2.2.3 温度引入的不确定度
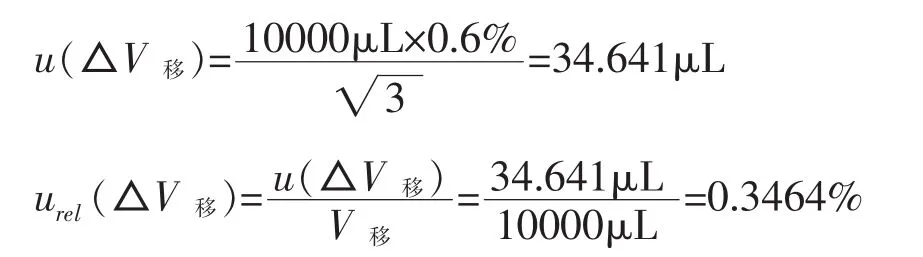
水的膨胀系数为 2.1×10-4℃-1,实验温度为30℃,容量瓶和溶液温度与校准时不同引起的体积变化所引入的不确定度:
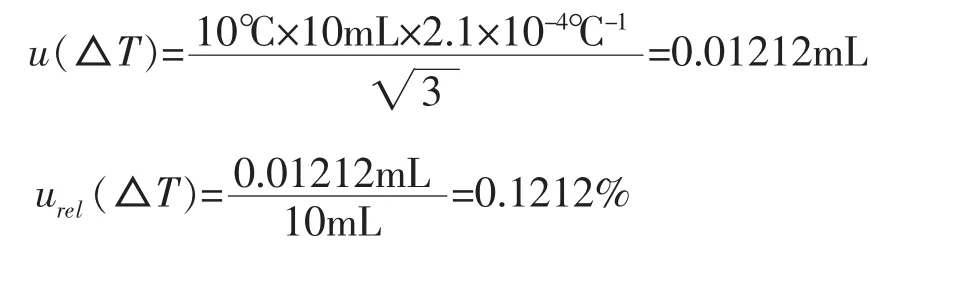
4.2.2.4 回收率引入的不确定度
由于样品提取不完全导致硒形态损失或者操作过程导致硒形态转变污染等,将使样品中的硒形态回收率不能为100%。加标实验结果:5种硒形态的回收率为 a-~a+, Se(Ⅳ): 89.2%~93.4%、 Se(Ⅵ)、SeCys2、SeMeCys及SeMet,样品回收率的不确定度按JJF 1059.1-2012《测量不确定度评定与表示》附录A.1.4节计算。区间半宽度为公式(2)所示。

a+>a-假如在区间分布均匀,取矩形分布:
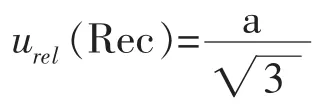
则样品回收率引入的不确定度如表3所示。
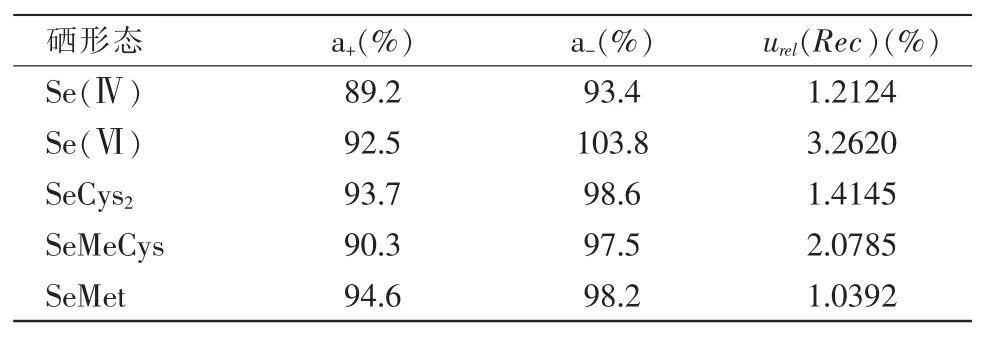
表3 样品回收率引入的不确定度
4.2.3 样品前处理引入的不确定度
30 mg蛋白酶量少由其带入的不确定度忽略不计。因此上述评定可知样品前处理引入的不确定度由 urel(m)、urel(ΔV移)、urel(ΔT)及 urel(Rec)组成,合并前处理不确定度为:
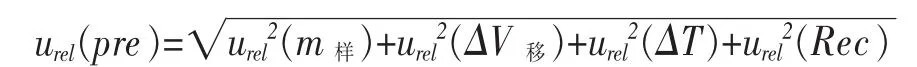
按照此公式计算,5 种硒形态 Se(Ⅳ)、Se(Ⅵ)、SeCys2、SeMeCys及SeMet由样品前处理引入的不确定度分别为:1.2673%、3.2828%、1.4619%、2.1110%、1.1029%。
4.3 最小二乘法拟合标准曲线校准得出Co时所产生的不确定度
通过对质量浓度分别为 0、5、10、20、50、100 μg/L的 Se(Ⅳ)、Se(Ⅵ)、SeCys2、SeMeCys 及 SeMet混合标准工作液进行测定,每个校准点测定2次,其计数值y如表4所示,采用最小二乘法拟合标准溶液的浓度与峰面积曲线,用最小二乘法进行拟合,得到方程y=a+bx(a为截距,b为斜率,x为浓度)和相关系数r,详见表4。

表4 最小二乘法拟合标准溶液浓度-计数值y
应用该曲线,对C20.0浓度上机液进行了2次测量,C1[Se(Ⅳ)]=19.57 μg/L,C2[Se(Ⅳ)]=20.31 μg/L,求得平均浓度 Co[Se(Ⅳ)]=19.94 μg/L,Co[Se(Ⅳ)]的标准不确定度按照公式(3)计算[11]。
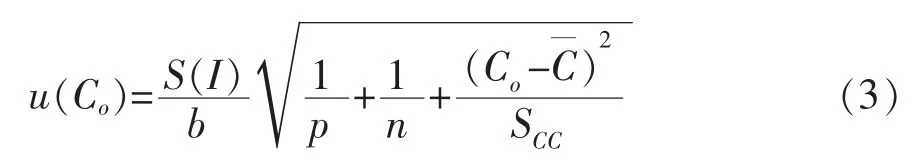
SCC=,标准溶液浓度的残差的平方和;
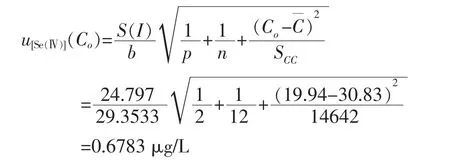
n——标准溶液的测量次数,本例为12;
p——Co的测量次数,本例为2。
根据以上公式推算,其他4种硒形态线性拟合产生的相对不确定度见表5。

表5 线性拟合产生的不确定度
4.4 仪器产生的不确定度
由国家计量所提供的校准证书给出的不确定度范围,按矩形分布计算不确定度。高效液相色谱的不确定度为0.67%,电感耦合等离子体质谱仪的不确定度为9Be为 2.1%、115In为 1.7%、209Bi为 2.8%,取最大不确定度2.8%。

4.5 重复性实验引入的不确定度
3 次测量结果 ωSe(Ⅳ):3.59 mg/kg,3.78 mg/kg,3.96 mg/kg,3 次测量算术平均值=3.78 mg/kg
根据JJF1059.1-2012《测量不确定度评定与表示》[12]4.3.2.3节查得3次测量的极差R为1.69,则

根据以上公式推算,其他4种硒形态重复试验引入的相对不确定度见表6。
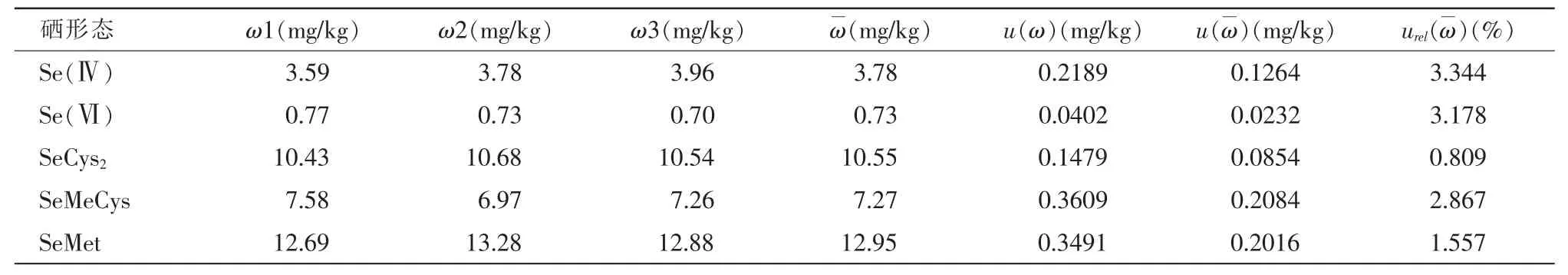
表6 重复性试验引入的不确定度
4.5 试剂空白
本实验所用试剂柠檬酸、氨水、蛋白酶等,均为优级纯,因而扣除空白所致的硒形态的微小变化产生的影响很小,可忽略不计。
5 不确定度分量列表
根据以上评定,将各项相对不确定度用方和根法合成为相对合成不确定度。假设置信概率为0.95时,取包含因子k=2,则扩展相对不确定度按公式Ucrel=k×ucrel计算,扩展不确定度按 U=×Ucrel计算。富硒酵母中5种硒形态不确定度评定结果见表7。

表7 富硒酵母中5种硒形态不确定度评定结果
6 讨论
以亚硒酸Se(Ⅳ)为例,LC-ICP-MS联用测定富硒酵母中亚硒酸的不确定度分量对合成标准不确定度的影响见图3。
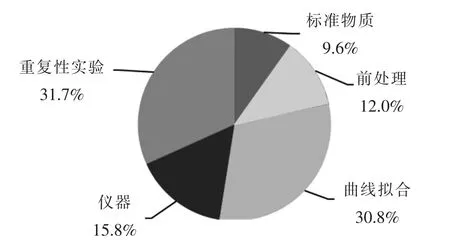
图3 不确定度分量
由图3可见,重复性实验和曲线拟合产生的不确定度最大。在日常工作中,仪器性能的维护和调试非常重要,保证仪器处在最佳工作状态,是保证试验结果准确可靠的基础。标准曲线拟合引入的不确定度也较大,试验过程应当提高标准溶液配制,降低其对结果的影响。样品前处理选择的萃取方式及萃取试剂也对不确定度带来影响,因此实验过程中应当提高样品萃取过程及重复性试验等实验技术水平,使测定结果更加准确,更接近真实值。
